2025年中考化学一轮专题复习 第六单元碳和碳的氧化物复习 课后检测题(含答案)
文档属性
| 名称 | 2025年中考化学一轮专题复习 第六单元碳和碳的氧化物复习 课后检测题(含答案) |  | |
| 格式 | doc | ||
| 文件大小 | 256.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-06 21:05:18 | ||
图片预览


文档简介
第六单元复习 课后检测题
巩固性作业
一、选择题
1.我国提出争取在2030年前实现碳达峰,2060年前实现碳中和。“碳达峰”“碳中和”中的“碳”指的是( )
A.碳元素 B.碳原子 C.碳单质 D.二氧化碳
2.碳单质的性质与用途对应关系错误的是 ( )
A.石墨导电性好可作电池电极 B.活性炭吸附性强可作冰箱除味剂
C.金刚石硬度大可制作铅笔芯 D.炭黑常温化学性质稳定可制墨汁
3.下列有关CO和CO2的说法,正确的是( )
A.CO和CO2都具有可燃性 B.CO和CO2都能使紫色石蕊溶液变红
C.CO和CO2都是空气污染物 D.一定条件下CO和CO2可以相互转化
4.下列有关自然界中碳循环、氧循环的说法,正确的是( )
A.植物呼吸作用放出氧气 B.化石燃料燃烧会大幅降低大气中氧气含量
C.植物光合作用可以将大气中CO2全部吸收 D.碳、氧循环失衡会导致人类生存环境恶化
5.用如图装置验证二氧化碳的性质。一段时间后,观察到纸花变红且短蜡烛熄灭,关闭K,片刻后长蜡烛熄灭。下列结论能由该实验得出的是( )
A.二氧化碳不支持燃烧 B.二氧化碳的密度比空气小
C.二氧化碳能与水发生反应 D.二氧化碳气体显酸性
二、非选择题
6.阅读下面短文,回答问题。
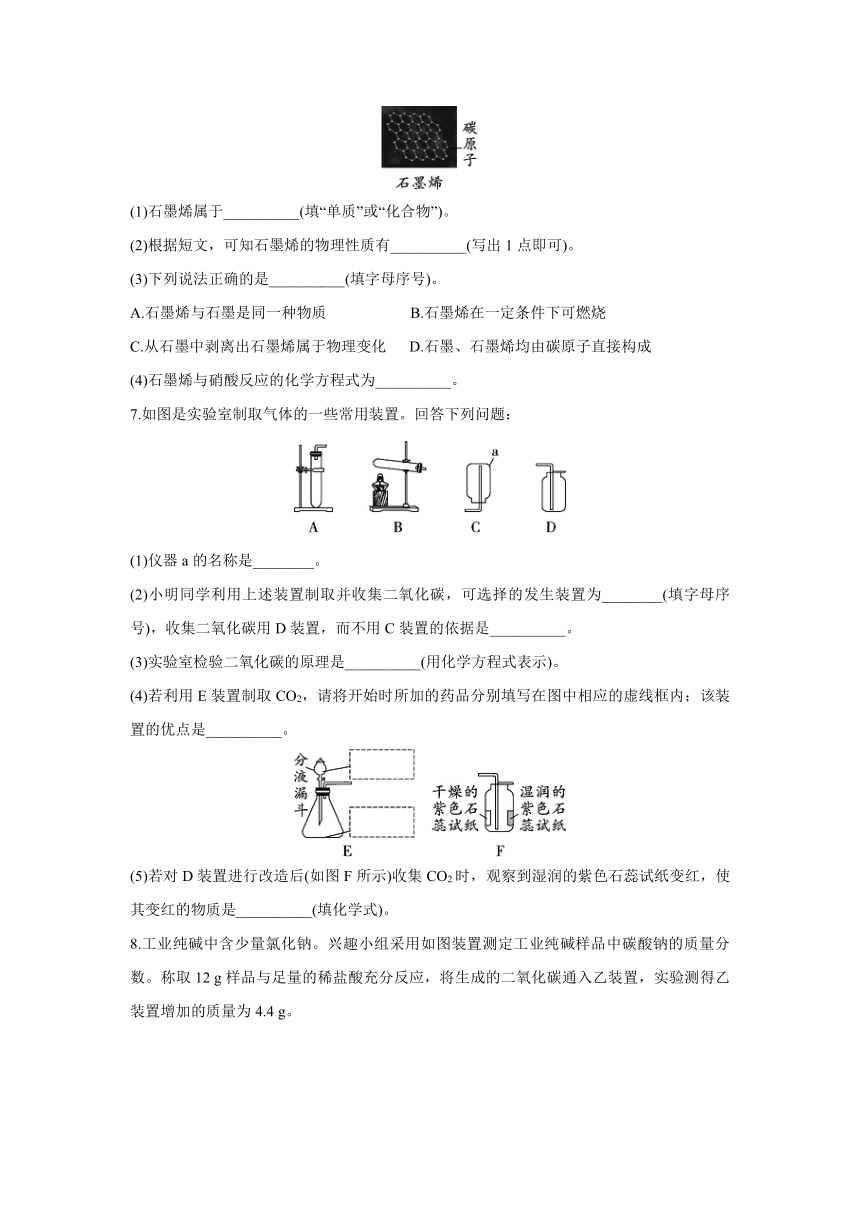
石墨烯是一种新型纳米材料,具有超高强度、超高导热系数,被业界誉为“新材料之王”。石墨烯本来就存在于自然界,只是难以剥离出单层结构(如图),石墨烯一层层叠起来就是石墨。石墨烯可被氧化性酸氧化,如它可以和硝酸在一定条件下反应生成二氧化氮、温室气体和一种最常见的氧化物,随着科技的发展,制备、使用石墨烯的方法也层出不穷。
(1)石墨烯属于__________(填“单质”或“化合物”)。
(2)根据短文,可知石墨烯的物理性质有__________(写出1点即可)。
(3)下列说法正确的是__________(填字母序号)。
A.石墨烯与石墨是同一种物质 B.石墨烯在一定条件下可燃烧
C.从石墨中剥离出石墨烯属于物理变化 D.石墨、石墨烯均由碳原子直接构成
(4)石墨烯与硝酸反应的化学方程式为__________。
7.如图是实验室制取气体的一些常用装置。回答下列问题:
(1)仪器a的名称是________。
(2)小明同学利用上述装置制取并收集二氧化碳,可选择的发生装置为________(填字母序号),收集二氧化碳用D装置,而不用C装置的依据是__________。
(3)实验室检验二氧化碳的原理是__________(用化学方程式表示)。
(4)若利用E装置制取CO2,请将开始时所加的药品分别填写在图中相应的虚线框内;该装置的优点是__________。
(5)若对D装置进行改造后(如图F所示)收集CO2时,观察到湿润的紫色石蕊试纸变红,使其变红的物质是__________(填化学式)。
8.工业纯碱中含少量氯化钠。兴趣小组采用如图装置测定工业纯碱样品中碳酸钠的质量分数。称取12 g样品与足量的稀盐酸充分反应,将生成的二氧化碳通入乙装置,实验测得乙装置增加的质量为4.4 g。
(1)计算样品中碳酸钠的质量。
(2)实验分析:该方法测得的碳酸钠的质量分数误差较大,原因可能是__________。
拓展性作业
一、选择题
9.Y形管为许多化学实验的进行创造了条件,如图为用Y形管完成的实验(加热装置已省略),下列有关说法不正确的是( )
A.左端高温加热,一段时间后右端澄清石灰水变浑浊
B.装置中气球可以收集尾气,防止污染空气
C.若最终没有得到红色固体,可能是装置气密性不好
D.该实验涉及的基本反应类型均为置换反应
10.工业炼铁的部分反应如图所示,则下列说法错误的是( )
A.X可以是木炭 B.反应②为化合反应
C.③反应后的尾气可直接排放 D.Y中铁元素以化合态存在
11.某兴趣小组为探究影响化学反应速率的因素,使用等量的同种钙片和白醋开展四组实验,分别测得产生的二氧化碳浓度随时间的变化曲线如图所示。选取CO2的浓度从0~8%为研究对象,下列实验结果的分析,错误的是( )
①、③为研磨成粉末状钙片②、④为片状钙片
A.对比①③,温度越高,反应速率越快
B.对比②③,反应物接触面积越小,反应速率越慢
C.对比③④,反应物接触面积越大,反应速率越快
D.对比①②③④,④的反应速率最慢
二、非选择题
12.在实际生产中,常采用足量NaOH溶液来“捕捉”(吸收)CO2,部分流程图如下。
(1)捕捉室内反应的化学方程式为__________。
(2)操作①的名称是________,所用到的玻璃仪器有烧杯、玻璃棒和________。
(3)往纯碱溶液中加入X溶液,得到NaOH溶液和CaCO3,X的化学式是________。
(4)整个流程中可以循环使用的物质是__________。
(5)若要确认“捕捉”后的气体中CO2含量已经降得很低,先分别取一瓶“捕捉”前和一瓶“捕捉”后的气体,接下来的实验操作是__________。
13.碳与氧气反应后会生成不同的产物,兴趣小组同学对碳还原氧化铜的气体产物进行如下探究。
【提出问题】碳还原氧化铜生成的气体是什么?
【作出猜想】猜想Ⅰ:CO;猜想Ⅱ:CO2;猜想Ⅲ:CO2和CO。
【实验步骤】小组同学利用如图所示装置进行实验。
【实验1】定性分析气体成分
(1)将块状木炭研细并与氧化铜粉末混合均匀的目的是________。
(2)开始实验时,要先通一段时间N2,目的是________。
(3)小组同学根据观察到的现象,得出猜想Ⅲ正确的结论。生成气体中含有一氧化碳的依据是:装置A中黑色固体开始变红时,观察到________。
【实验2】定量分析确定气体组成
(4)重复上述实验,测得反应前后的数据如下表:
测定对象 反应前的质量/g 反应后的质量/g
A中的玻璃管+固体药品 121.6 120.2
B+C+D中的集气瓶+溶液 1133.5 1134.4
依据上表数据计算:
二氧化碳的质量为_______g,一氧化碳的质量为_______g。
【反思与评价】
(5)装置A中生成CO的化学方程式可能为________(写一个即可)。
(6)小组同学经讨论后一致认为“实验2”可以不用的装置是________(填标号),理由是________。
探究性作业
14.如图是实验室中常见装置,回答下列问题:
查阅资料:常温下,CO2难溶于饱和NaHCO3 溶液。
(1)用装置A制取气体的不足之处是________。
(2)常温下,下列收集 CO2 的方法中不可行的是________(填字母序号)。
a.向上排空气法 b.向下排空气法 c.排饱和 NaHCO3溶液法
(3)若要收集干燥的 CO2,可将含有水蒸气的CO2从装置 D 的________(填“m”或“n”)端导入,试剂X是________。
(4)为制得CO2的水溶液,CO2应从装置D(试剂X为水)的________(填“m”或“n”)端通入。
(5)将CO2的水溶液转移至烧杯,并组装装置如图 E所示,置于阳光下一段时间,观察到有气泡产生,检验该气体的方法是_________。
(6)某同学进行如图F所示的操作时,观察到高的蜡烛先熄灭,其原因可能是________。
(7)某化学兴趣小组设计实验验证二氧化碳温室效应。如图所示,选用体积大小相等的两个塑料瓶,分别盛满同条件下的空气、二氧化碳与空气的混合物(体积比1∶1),并用一个小塑料管连接(在塑料管中间有一滴红墨水),置于阳光下。一段时间后红墨水滴会________(填“向右”“向左”或“不”)移动。
参考答案
1.D2.C3.D4.D5.A
6.(1)单质 (2)超高强度(或超高导热系数) (3)BD (4)C+4HNO3一定条件4NO2↑+CO2↑+ 2H2O
7.(1)集气瓶 (2)A 二氧化碳密度比空气大 (3)CO2+Ca(OH)2=CaCO3↓+H2O (4) 可控制反应速率 (5)H2CO3
8.(1)解:样品中碳酸钠的质量为x
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 44
x 4.4 g
= x=10.6 g
答:样品中碳酸钠的质量为10.6 g。
(2)盐酸具有挥发性,生成的二氧化碳中混有HCl,被氢氧化钠溶液吸收,会导致结果偏大(或实验结束后,装置中残留的二氧化碳没有完全被氢氧化钠溶液吸收,会导致结果偏小,合理即可)
9.D【解析】C和CuO在高温条件下反应生成Cu和CO2,一段时间后右端澄清石灰水变浑浊,A正确;反应过程中可能会有CO产生,装置中气球可以收集尾气,防止CO污染空气,B正确;若最终没有得到红色固体,可能是装置气密性不好,反应生成的Cu又被空气中的O2氧化成CuO,C正确;该实验中CO2与澄清石灰水的反应不属于置换反应,D错误。
10.C【解析】碳与氧气反应生成二氧化碳,木炭的主要成分是碳,X可以是木炭,A正确;反应②为CO2与C在高温条件下反应生成CO,属于化合反应,B正确;③是与氧化铁在高温下反应生成铁和二氧化碳,一氧化碳有毒,直接排放到空气中会污染环境,反应后的尾气不能直接排放,C错误;Y是氧化铁,铁元素以化合态存在,D正确。
11.B【解析】从图象对比①③可看出,①③其他条件相同,只有温度不同,在相同时间内,①生成二氧化碳的浓度大于③生成二氧化碳的浓度,由此说明温度越高,反应速率越快,A正确;从图象对比②③可看出,钙片的形状不同,温度不同,因此无法比较,B错误;从图象对比③④可看出,③④其他条件相同,只有钙片的形状不同,在相同时间内,③生成二氧化碳的浓度大于④生成二氧化碳的浓度,由此说明反应物接触面积越大,反应速率越快,C正确;从整个图象可看出,在相同时间内④生成二氧化碳的浓度最小,D正确。
12.(1)2NaOH+CO2=Na2CO3+H2O (2)过滤 漏斗 (3)Ca(OH)2 (4)氢氧化钠、氧化钙(或NaOH、CaO) (5)加入等量澄清石灰水,观察变浑浊情况
13. (1)增大木炭和氧化铜的接触面积,使反应更充分 (2)排出装置内部残留的空气,避免影响实验 (3)装置E中有连续的气泡产生,水被压进装置F中 (4)0.9 0.5 (5)CuO+CCu+CO↑(或CO2+C2CO) (6)B 不需要检验二氧化碳(或装置C中的氢氧化钠溶液可充分吸收二氧化碳)
14.(1)不能随时控制反应的发生和停止(合理即可) (2)b (3)m 浓硫酸 (4)m (5)将带火星的木条伸入收集到的气体中,观察木条是否复燃 (6)二氧化碳倾倒过快,先使高蜡烛火焰附近氧气浓度减少 (7)向左
巩固性作业
一、选择题
1.我国提出争取在2030年前实现碳达峰,2060年前实现碳中和。“碳达峰”“碳中和”中的“碳”指的是( )
A.碳元素 B.碳原子 C.碳单质 D.二氧化碳
2.碳单质的性质与用途对应关系错误的是 ( )
A.石墨导电性好可作电池电极 B.活性炭吸附性强可作冰箱除味剂
C.金刚石硬度大可制作铅笔芯 D.炭黑常温化学性质稳定可制墨汁
3.下列有关CO和CO2的说法,正确的是( )
A.CO和CO2都具有可燃性 B.CO和CO2都能使紫色石蕊溶液变红
C.CO和CO2都是空气污染物 D.一定条件下CO和CO2可以相互转化
4.下列有关自然界中碳循环、氧循环的说法,正确的是( )
A.植物呼吸作用放出氧气 B.化石燃料燃烧会大幅降低大气中氧气含量
C.植物光合作用可以将大气中CO2全部吸收 D.碳、氧循环失衡会导致人类生存环境恶化
5.用如图装置验证二氧化碳的性质。一段时间后,观察到纸花变红且短蜡烛熄灭,关闭K,片刻后长蜡烛熄灭。下列结论能由该实验得出的是( )
A.二氧化碳不支持燃烧 B.二氧化碳的密度比空气小
C.二氧化碳能与水发生反应 D.二氧化碳气体显酸性
二、非选择题
6.阅读下面短文,回答问题。
石墨烯是一种新型纳米材料,具有超高强度、超高导热系数,被业界誉为“新材料之王”。石墨烯本来就存在于自然界,只是难以剥离出单层结构(如图),石墨烯一层层叠起来就是石墨。石墨烯可被氧化性酸氧化,如它可以和硝酸在一定条件下反应生成二氧化氮、温室气体和一种最常见的氧化物,随着科技的发展,制备、使用石墨烯的方法也层出不穷。
(1)石墨烯属于__________(填“单质”或“化合物”)。
(2)根据短文,可知石墨烯的物理性质有__________(写出1点即可)。
(3)下列说法正确的是__________(填字母序号)。
A.石墨烯与石墨是同一种物质 B.石墨烯在一定条件下可燃烧
C.从石墨中剥离出石墨烯属于物理变化 D.石墨、石墨烯均由碳原子直接构成
(4)石墨烯与硝酸反应的化学方程式为__________。
7.如图是实验室制取气体的一些常用装置。回答下列问题:
(1)仪器a的名称是________。
(2)小明同学利用上述装置制取并收集二氧化碳,可选择的发生装置为________(填字母序号),收集二氧化碳用D装置,而不用C装置的依据是__________。
(3)实验室检验二氧化碳的原理是__________(用化学方程式表示)。
(4)若利用E装置制取CO2,请将开始时所加的药品分别填写在图中相应的虚线框内;该装置的优点是__________。
(5)若对D装置进行改造后(如图F所示)收集CO2时,观察到湿润的紫色石蕊试纸变红,使其变红的物质是__________(填化学式)。
8.工业纯碱中含少量氯化钠。兴趣小组采用如图装置测定工业纯碱样品中碳酸钠的质量分数。称取12 g样品与足量的稀盐酸充分反应,将生成的二氧化碳通入乙装置,实验测得乙装置增加的质量为4.4 g。
(1)计算样品中碳酸钠的质量。
(2)实验分析:该方法测得的碳酸钠的质量分数误差较大,原因可能是__________。
拓展性作业
一、选择题
9.Y形管为许多化学实验的进行创造了条件,如图为用Y形管完成的实验(加热装置已省略),下列有关说法不正确的是( )
A.左端高温加热,一段时间后右端澄清石灰水变浑浊
B.装置中气球可以收集尾气,防止污染空气
C.若最终没有得到红色固体,可能是装置气密性不好
D.该实验涉及的基本反应类型均为置换反应
10.工业炼铁的部分反应如图所示,则下列说法错误的是( )
A.X可以是木炭 B.反应②为化合反应
C.③反应后的尾气可直接排放 D.Y中铁元素以化合态存在
11.某兴趣小组为探究影响化学反应速率的因素,使用等量的同种钙片和白醋开展四组实验,分别测得产生的二氧化碳浓度随时间的变化曲线如图所示。选取CO2的浓度从0~8%为研究对象,下列实验结果的分析,错误的是( )
①、③为研磨成粉末状钙片②、④为片状钙片
A.对比①③,温度越高,反应速率越快
B.对比②③,反应物接触面积越小,反应速率越慢
C.对比③④,反应物接触面积越大,反应速率越快
D.对比①②③④,④的反应速率最慢
二、非选择题
12.在实际生产中,常采用足量NaOH溶液来“捕捉”(吸收)CO2,部分流程图如下。
(1)捕捉室内反应的化学方程式为__________。
(2)操作①的名称是________,所用到的玻璃仪器有烧杯、玻璃棒和________。
(3)往纯碱溶液中加入X溶液,得到NaOH溶液和CaCO3,X的化学式是________。
(4)整个流程中可以循环使用的物质是__________。
(5)若要确认“捕捉”后的气体中CO2含量已经降得很低,先分别取一瓶“捕捉”前和一瓶“捕捉”后的气体,接下来的实验操作是__________。
13.碳与氧气反应后会生成不同的产物,兴趣小组同学对碳还原氧化铜的气体产物进行如下探究。
【提出问题】碳还原氧化铜生成的气体是什么?
【作出猜想】猜想Ⅰ:CO;猜想Ⅱ:CO2;猜想Ⅲ:CO2和CO。
【实验步骤】小组同学利用如图所示装置进行实验。
【实验1】定性分析气体成分
(1)将块状木炭研细并与氧化铜粉末混合均匀的目的是________。
(2)开始实验时,要先通一段时间N2,目的是________。
(3)小组同学根据观察到的现象,得出猜想Ⅲ正确的结论。生成气体中含有一氧化碳的依据是:装置A中黑色固体开始变红时,观察到________。
【实验2】定量分析确定气体组成
(4)重复上述实验,测得反应前后的数据如下表:
测定对象 反应前的质量/g 反应后的质量/g
A中的玻璃管+固体药品 121.6 120.2
B+C+D中的集气瓶+溶液 1133.5 1134.4
依据上表数据计算:
二氧化碳的质量为_______g,一氧化碳的质量为_______g。
【反思与评价】
(5)装置A中生成CO的化学方程式可能为________(写一个即可)。
(6)小组同学经讨论后一致认为“实验2”可以不用的装置是________(填标号),理由是________。
探究性作业
14.如图是实验室中常见装置,回答下列问题:
查阅资料:常温下,CO2难溶于饱和NaHCO3 溶液。
(1)用装置A制取气体的不足之处是________。
(2)常温下,下列收集 CO2 的方法中不可行的是________(填字母序号)。
a.向上排空气法 b.向下排空气法 c.排饱和 NaHCO3溶液法
(3)若要收集干燥的 CO2,可将含有水蒸气的CO2从装置 D 的________(填“m”或“n”)端导入,试剂X是________。
(4)为制得CO2的水溶液,CO2应从装置D(试剂X为水)的________(填“m”或“n”)端通入。
(5)将CO2的水溶液转移至烧杯,并组装装置如图 E所示,置于阳光下一段时间,观察到有气泡产生,检验该气体的方法是_________。
(6)某同学进行如图F所示的操作时,观察到高的蜡烛先熄灭,其原因可能是________。
(7)某化学兴趣小组设计实验验证二氧化碳温室效应。如图所示,选用体积大小相等的两个塑料瓶,分别盛满同条件下的空气、二氧化碳与空气的混合物(体积比1∶1),并用一个小塑料管连接(在塑料管中间有一滴红墨水),置于阳光下。一段时间后红墨水滴会________(填“向右”“向左”或“不”)移动。
参考答案
1.D2.C3.D4.D5.A
6.(1)单质 (2)超高强度(或超高导热系数) (3)BD (4)C+4HNO3一定条件4NO2↑+CO2↑+ 2H2O
7.(1)集气瓶 (2)A 二氧化碳密度比空气大 (3)CO2+Ca(OH)2=CaCO3↓+H2O (4) 可控制反应速率 (5)H2CO3
8.(1)解:样品中碳酸钠的质量为x
Na2CO3+2HCl=2NaCl+H2O+CO2↑
106 44
x 4.4 g
= x=10.6 g
答:样品中碳酸钠的质量为10.6 g。
(2)盐酸具有挥发性,生成的二氧化碳中混有HCl,被氢氧化钠溶液吸收,会导致结果偏大(或实验结束后,装置中残留的二氧化碳没有完全被氢氧化钠溶液吸收,会导致结果偏小,合理即可)
9.D【解析】C和CuO在高温条件下反应生成Cu和CO2,一段时间后右端澄清石灰水变浑浊,A正确;反应过程中可能会有CO产生,装置中气球可以收集尾气,防止CO污染空气,B正确;若最终没有得到红色固体,可能是装置气密性不好,反应生成的Cu又被空气中的O2氧化成CuO,C正确;该实验中CO2与澄清石灰水的反应不属于置换反应,D错误。
10.C【解析】碳与氧气反应生成二氧化碳,木炭的主要成分是碳,X可以是木炭,A正确;反应②为CO2与C在高温条件下反应生成CO,属于化合反应,B正确;③是与氧化铁在高温下反应生成铁和二氧化碳,一氧化碳有毒,直接排放到空气中会污染环境,反应后的尾气不能直接排放,C错误;Y是氧化铁,铁元素以化合态存在,D正确。
11.B【解析】从图象对比①③可看出,①③其他条件相同,只有温度不同,在相同时间内,①生成二氧化碳的浓度大于③生成二氧化碳的浓度,由此说明温度越高,反应速率越快,A正确;从图象对比②③可看出,钙片的形状不同,温度不同,因此无法比较,B错误;从图象对比③④可看出,③④其他条件相同,只有钙片的形状不同,在相同时间内,③生成二氧化碳的浓度大于④生成二氧化碳的浓度,由此说明反应物接触面积越大,反应速率越快,C正确;从整个图象可看出,在相同时间内④生成二氧化碳的浓度最小,D正确。
12.(1)2NaOH+CO2=Na2CO3+H2O (2)过滤 漏斗 (3)Ca(OH)2 (4)氢氧化钠、氧化钙(或NaOH、CaO) (5)加入等量澄清石灰水,观察变浑浊情况
13. (1)增大木炭和氧化铜的接触面积,使反应更充分 (2)排出装置内部残留的空气,避免影响实验 (3)装置E中有连续的气泡产生,水被压进装置F中 (4)0.9 0.5 (5)CuO+CCu+CO↑(或CO2+C2CO) (6)B 不需要检验二氧化碳(或装置C中的氢氧化钠溶液可充分吸收二氧化碳)
14.(1)不能随时控制反应的发生和停止(合理即可) (2)b (3)m 浓硫酸 (4)m (5)将带火星的木条伸入收集到的气体中,观察木条是否复燃 (6)二氧化碳倾倒过快,先使高蜡烛火焰附近氧气浓度减少 (7)向左
同课章节目录
