3.4.2 羧酸衍生物(教学课件)(共31张PPT)_高中化学人教版(2019)人教版选择性必修三
文档属性
| 名称 | 3.4.2 羧酸衍生物(教学课件)(共31张PPT)_高中化学人教版(2019)人教版选择性必修三 |  | |
| 格式 | pptx | ||
| 文件大小 | 58.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-08 08:18:23 | ||
图片预览











文档简介
(共31张PPT)
3.4.2 羧酸衍生物
学习重难点
重点
羧酸衍生物的结构特点与主要性质,如酯的水解、酰胺的形成等。
羧酸衍生物之间的相互转化关系,构建知识网络。
难点
理解羧酸衍生物水解、醇解等反应的机理,尤其是化学键的断裂与形成过程。
运用羧酸衍生物的知识解决实际问题,如有机合成中的应用。
课前导入
同学们,生活里常见的尼龙衣物、背包很实用,大家知道它是怎么来的吗?尼龙是二元胺和二元羧酸缩聚而成,其中含有的酰胺键,就是羧酸衍生物。今天咱们就来探究神奇的羧酸衍生物 。
羧酸衍生物
PART 01
1.羧酸衍生物
定义 羧酸分子中羧基上的羟基被其他原子或原子团取代后的生成物。 构成 必有酰基: 或RCO— 酰基与卤素原子(—X)、烃氧基(RO—)和氨基(—NH2)等相连构成
常见的羧酸衍生物 酰卤(如乙酰氯 )、 酯(如乙酸乙酯 )、 和酰胺(如乙酰胺 )等 R
C
O
CH3
C
O
Cl
CH3
C
O
OC2H5
CH3
C
O
NH2
酯
PART 02
1.酯
概念:酯是羧酸分子羧基中的—OH被—OR‘取代后的产物。
官能团:酯基
C
O
O R‘
(不能与H2发生加成反应)
通式:
①酯的通式一般为RCOOR‘或 ,其中R代表任意的烃基或氢原子,R‘是任意烃基,R和R‘都是烃基时,可以相同也可以不同。
②饱和一元羧酸和饱和一元醇形成的酯的通式是CnH2nO2(n≥2)。
C
O
O R‘
R
命名:根据生成酯的酸和醇的名称称为“某酸某酯”。命名时,酸的名称写在前面,醇的名称写在后面,将其中的“醇”改写为“酯”即可。
1.酯
物理性质:酯的密度一般比水的小,难溶于水,易溶于乙醇、乙醚等有机溶剂。低级酯是具有芳香气味的液体,存在于各种水果和花草中。
丁酸乙酯
乙酸异戊酯
戊酸戊酯
2.酯的化学性质
酯的重要化学性质之一是可以发生水解反应,生成相应的羧酸和醇。
【思考】
①根据酯基的结构,分析酯类物质在化学反应中可能的断键位置?
②乙酸乙酯水解的速率与反应条件有着怎样的关系呢?请你预测一下。
③可以通过哪些实验现象来比较乙酸乙酯水解速率的大小?
温度、浓度、催化剂(无机酸、碱、盐等)
由于O的电负性大于C,酯基中的C-O的极性较大,在化学反应中容易断裂。
R-C-O-R`
=
O
因为羧基为亲水基,乙基为疏水基,所以乙酸易溶于水,乙酸乙酯在水中的
溶解度较小。故酯层消失即表示乙酸乙酯水解完全。
2.酯的化学性质
【实验探究】探究溶液酸碱性对乙酸乙酯水解反应速率的影响
【实验试剂】乙酸乙酯、蒸馏水、稀硫酸、30%NaOH、石蕊溶液
【实验设计—1】
①向盛有2ml稀硫酸、2mlNaOH、2ml蒸馏水的试管中分别加入几滴石蕊溶液,震荡;
②分别向三支试管中加入1ml乙酸乙酯;
③水浴加热(温度不超过76℃);
④观察记录酯层消失的时间。
已知:
(1)乙酸乙酯在常温下水解速率很慢
(2)乙酸乙酯的沸点为76.5—77.5℃
2.酯的化学性质
【实验探究】探究温度对乙酸乙酯水解反应速率的影响。
【实验试剂】乙酸乙酯、蒸馏水、稀硫酸、石蕊溶液
【实验设计—2】
①向两支盛有2ml稀硫酸的试管中分别加入几滴石蕊溶液,震荡;
②分别向两支试管中加入1ml乙酸乙酯;
③一只试管置于常温,另一支水浴加热(温度不超过76℃);
④观察记录酯层消失的时间。
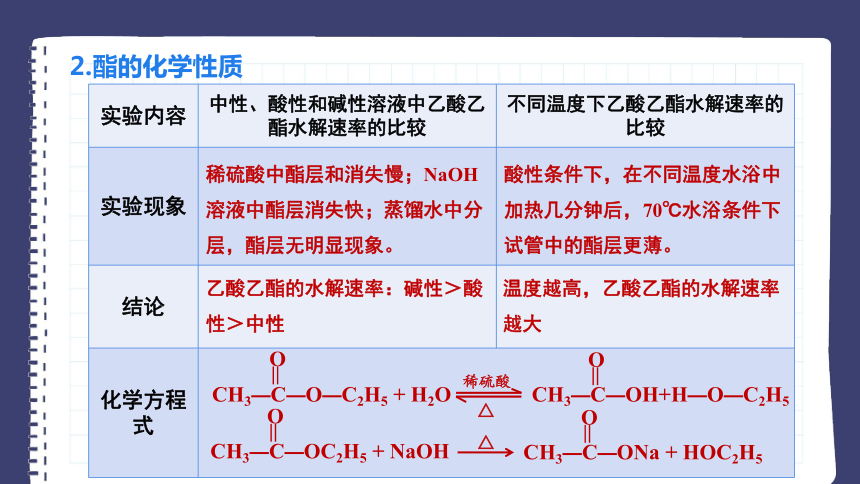
2.酯的化学性质
实验内容 中性、酸性和碱性溶液中乙酸乙酯水解速率的比较 不同温度下乙酸乙酯水解速率的比较
实验现象
结论
化学方程式 稀硫酸中酯层和消失慢;NaOH溶液中酯层消失快;蒸馏水中分层,酯层无明显现象。
酸性条件下,在不同温度水浴中加热几分钟后,70℃水浴条件下试管中的酯层更薄。
乙酸乙酯的水解速率:碱性>酸性>中性
温度越高,乙酸乙酯的水解速率越大
CH3—C—O—C2H5 + H2O
CH3—C—OH+H—O—C2H5
O
O
稀硫酸
△
CH3—C—OC2H5 + NaOH
CH3—C—ONa + HOC2H5
△
O
O
2.酯的化学性质
(1)酸性条件下,酯的水解反应与酯化反应互为可逆反应;碱性条件下,碱能把生成的羧酸中和,水解能进行完全。
(2)酯的水解反应在稀酸催化下即可发生,说明它的逆反应即酯化反应在该条件下也能进行,而酯化反应却使用浓硫酸,目的是催化的同时吸收生成的水,使平衡最大限度地向生成酯的方向移动,提高酯的产率。
(3)在酸或碱存在的条件下,酯都能发生水解反应生成相应的羧酸(盐)和醇。
R—C—OR’+ H2O
R—C—OH+H—O—R’
O
O
稀硫酸
△
R—C—ONa + H—O—R’
△
O
R—C—OR’+ NaOH
O
酸性水解:
碱性水解:
油脂
PART 03
1.油脂的组成和结构
油脂的成分主要是高级脂肪酸与甘油形成的酯,由C、H、O三种元素组成,官能团是酯基,结构表示如下:
R1-C-O-CH2
R2-C-O-CH
R3-C-O-CH2
O
=
O
=
O
=
油脂的结构
①R1、R2、R3代表高级脂肪酸的饱和烃基或不饱和烃基(含碳碳双键);
②如果R1、R2、R3相同,这样的油脂称为简单甘油酯;如果R1、R2、R3不相同,这样的油脂称为混合甘油酯;
③在天然油脂中,R1、R2、R3一般不相同,属于混合甘油酯。
1.油脂的组成和结构
形成油脂的几种重要的高级脂肪酸:
酸名 软脂酸 硬脂酸 油酸 亚油酸
分子式 C15H31COOH C17H35COOH C17H33COOH C17H31COOH
饱和高级脂肪酸甘油酯在常温常压下呈固态或半固态,称为脂肪;
不饱和高级脂肪酸甘油酯在常温常压下呈液态,称为油。
2.油脂的化学性质
请写出硬脂酸、油酸分别与丙三醇反应的化学方程式。
HO—CH2
HO—CH
HO—CH2
3C17H35COOH +
C17H35COOCH2
C17H35COOCH
C17H35COOCH2
+ 3H2O
HO—CH2
HO—CH
HO—CH2
3C17H33COOH +
C17H33COOCH2
C17H33COOCH
C17H33COOCH2
+ 3H2O
催化剂
△
催化剂
△
2.油脂的化学性质
(1)水解反应
油脂是高级脂肪酸的甘油酯,能够发生水解反应;而高级脂肪酸中又有不饱和的,因此许多油脂又兼有烯烃的化学性质,可以发生加成反应。
油脂在酸、碱或酶等催化剂的作用下,均可发生水解反应。1mol油脂完全水解可生成1mol甘油和3mol高级脂肪酸。
a.酸性水解:油脂在酸作催化剂的条件下,发生水解反应,生成甘油和高级脂肪酸。如:
C17H35COOCH2
C17H35COOCH
C17H35COOCH2
+ 3H2O
3C17H35COOH
+
硬脂酸
CH2OH
CH2OH
CHOH
甘油
硬脂酸甘油酯
稀硫酸
△
2.油脂的化学性质
(1)水解反应
b.碱性水解:油脂在碱性溶液中的水解反应又称为皂化反应,如:
C17H35COOCH2
C17H35COOCH
C17H35COOCH2
+ 3NaOH
3C17H35COONa
+
硬脂酸钠
CH2OH
CH2OH
CHOH
甘油
硬脂酸甘油酯
高级脂肪酸钠(或钾)盐是肥皂的有效成分,工业上利用油脂的皂化反应来制造肥皂。
2.油脂的化学性质
(2)油脂的氢化——(加成反应)
CH2OOCC17H33
CHOOCC17H33
CH2OOCC17H33
CH2OOCC17H35
CHOOCC17H35
CH2OOCC17H35
+3H2
催化剂
不饱和程度较高、熔点较低的液态油,通过催化加氢可提高饱和度,转变成半固态的脂肪,这个过程称为油脂的氢化,也称为油脂的硬化。如:
油酸甘油酯
硬脂酸甘油酯(脂肪)
2.油脂的化学性质
3.胺
(1)定义:烃基取代氨分子中的氢原子而形成的化合物;胺也可以看作是烃分子中的氢原子被氨基所替代的化合物。
甲胺:CH3—NH2
苯胺:
—NH2
一般可写作R—NH2
(2)化学性质
①胺类化合物具有碱性
—NH2+HCl
—NH3Cl
甲胺和苯胺都是合成医药、农药和染料等的重要原料。
“氨”“铵”“胺”的区别:氨是指氨气(NH3);铵一般出现在铵盐中;胺是指一类含氨基(—NH2)或取代的氨基(—NRR’)的有机物。
4.酰胺
(1)结构
酰胺是羧酸分子中羟基被氨基所替代得到的化合物。
(2)常见物质
①乙酰胺
②苯甲酰胺
③N,N-二甲基甲酰胺
CH3—C—NH2
O
H—C—N(CH3)2
O
—C—NH2
O
4.酰胺
(3)化学性质
①与盐酸:
②与氢氧化钠溶液:
(4)应用
酰胺常被用作溶剂和化工原料。例如,N,N 二甲基甲酰胺是良好的溶剂,可以溶解很多有机化合物和无机化合物,是生产多种化学纤维的溶剂,也用于合成农药、医药等。
酰胺键,与酯基类似,在酸或碱存在并加热的条件下可以发生水解反应。请写出下列化学方程式。
△
△
RCONH2+H2O+HCl RCOOH+NH4Cl
RCONH2+NaOH RCOONa+NH3↑
随堂训练
1.判断正误
(1)酯类在碱性条件下的水解程度大。 ( )
(2)油脂的相对分子质量较大,故属于有机高分子。( )
(3)汽油、甘油都属于油脂。( )
(4)油脂的水解反应叫做皂化反应。( )
(5)酯化反应与酯的水解反应均为取代反应。( )
(6)乙酸乙酯在碱性条件下也能发生水解反应,也称皂化反应。( )
随堂训练
2.油脂皂化反应后,使肥皂从反应混合液中分离的方法有①分液 ②蒸馏 ③过滤 ④盐析,其中正确的顺序是( )
A.①②③
B.④③②
C.④③
D.③②
C
随堂训练
3.可以判断油脂皂化反应基本完成的现象是( )
A.反应液使红色石蕊试纸变蓝色
B.反应液使蓝色石蕊试纸变红色
C.反应后静置,反应液分为两层
D. 反应后静置,反应液不分层
D
随堂训练
4.在一定条件下,动植物油脂与醇反应可制备生物柴油,化学方程式如下:
下列叙述错误的是( )
A.生物柴油由可再生资源制得 B.生物柴油是不同酯组成的混合物
C.动植物油脂是高分子化合物 D.“地沟油”可用于制备生物柴油
C
随堂训练
5.某中性有机物,在酸性条件下可以发生水解,生成相对分子
质量相同的A和B,A是中性物质,B可以与碳酸钠反应放出气体,
该有机物是( )
A.CH3COOC3H7 B.CH3COOC2H5
C.CH3COONa D.CH3CH2Br
A
随堂训练
6.某有机物的结构简式是
关于它的性质描述正确的是( )
①能发生加成反应 ②能消耗NaOH 3 mol
③能水解生成两种酸 ④不能使溴水褪色
⑤能发生酯化反应 ⑥有酸性
A.①②③ B.②③⑤ C.仅⑥ D.全部正确
D
谢谢观看
3.4.2 羧酸衍生物
学习重难点
重点
羧酸衍生物的结构特点与主要性质,如酯的水解、酰胺的形成等。
羧酸衍生物之间的相互转化关系,构建知识网络。
难点
理解羧酸衍生物水解、醇解等反应的机理,尤其是化学键的断裂与形成过程。
运用羧酸衍生物的知识解决实际问题,如有机合成中的应用。
课前导入
同学们,生活里常见的尼龙衣物、背包很实用,大家知道它是怎么来的吗?尼龙是二元胺和二元羧酸缩聚而成,其中含有的酰胺键,就是羧酸衍生物。今天咱们就来探究神奇的羧酸衍生物 。
羧酸衍生物
PART 01
1.羧酸衍生物
定义 羧酸分子中羧基上的羟基被其他原子或原子团取代后的生成物。 构成 必有酰基: 或RCO— 酰基与卤素原子(—X)、烃氧基(RO—)和氨基(—NH2)等相连构成
常见的羧酸衍生物 酰卤(如乙酰氯 )、 酯(如乙酸乙酯 )、 和酰胺(如乙酰胺 )等 R
C
O
CH3
C
O
Cl
CH3
C
O
OC2H5
CH3
C
O
NH2
酯
PART 02
1.酯
概念:酯是羧酸分子羧基中的—OH被—OR‘取代后的产物。
官能团:酯基
C
O
O R‘
(不能与H2发生加成反应)
通式:
①酯的通式一般为RCOOR‘或 ,其中R代表任意的烃基或氢原子,R‘是任意烃基,R和R‘都是烃基时,可以相同也可以不同。
②饱和一元羧酸和饱和一元醇形成的酯的通式是CnH2nO2(n≥2)。
C
O
O R‘
R
命名:根据生成酯的酸和醇的名称称为“某酸某酯”。命名时,酸的名称写在前面,醇的名称写在后面,将其中的“醇”改写为“酯”即可。
1.酯
物理性质:酯的密度一般比水的小,难溶于水,易溶于乙醇、乙醚等有机溶剂。低级酯是具有芳香气味的液体,存在于各种水果和花草中。
丁酸乙酯
乙酸异戊酯
戊酸戊酯
2.酯的化学性质
酯的重要化学性质之一是可以发生水解反应,生成相应的羧酸和醇。
【思考】
①根据酯基的结构,分析酯类物质在化学反应中可能的断键位置?
②乙酸乙酯水解的速率与反应条件有着怎样的关系呢?请你预测一下。
③可以通过哪些实验现象来比较乙酸乙酯水解速率的大小?
温度、浓度、催化剂(无机酸、碱、盐等)
由于O的电负性大于C,酯基中的C-O的极性较大,在化学反应中容易断裂。
R-C-O-R`
=
O
因为羧基为亲水基,乙基为疏水基,所以乙酸易溶于水,乙酸乙酯在水中的
溶解度较小。故酯层消失即表示乙酸乙酯水解完全。
2.酯的化学性质
【实验探究】探究溶液酸碱性对乙酸乙酯水解反应速率的影响
【实验试剂】乙酸乙酯、蒸馏水、稀硫酸、30%NaOH、石蕊溶液
【实验设计—1】
①向盛有2ml稀硫酸、2mlNaOH、2ml蒸馏水的试管中分别加入几滴石蕊溶液,震荡;
②分别向三支试管中加入1ml乙酸乙酯;
③水浴加热(温度不超过76℃);
④观察记录酯层消失的时间。
已知:
(1)乙酸乙酯在常温下水解速率很慢
(2)乙酸乙酯的沸点为76.5—77.5℃
2.酯的化学性质
【实验探究】探究温度对乙酸乙酯水解反应速率的影响。
【实验试剂】乙酸乙酯、蒸馏水、稀硫酸、石蕊溶液
【实验设计—2】
①向两支盛有2ml稀硫酸的试管中分别加入几滴石蕊溶液,震荡;
②分别向两支试管中加入1ml乙酸乙酯;
③一只试管置于常温,另一支水浴加热(温度不超过76℃);
④观察记录酯层消失的时间。
2.酯的化学性质
实验内容 中性、酸性和碱性溶液中乙酸乙酯水解速率的比较 不同温度下乙酸乙酯水解速率的比较
实验现象
结论
化学方程式 稀硫酸中酯层和消失慢;NaOH溶液中酯层消失快;蒸馏水中分层,酯层无明显现象。
酸性条件下,在不同温度水浴中加热几分钟后,70℃水浴条件下试管中的酯层更薄。
乙酸乙酯的水解速率:碱性>酸性>中性
温度越高,乙酸乙酯的水解速率越大
CH3—C—O—C2H5 + H2O
CH3—C—OH+H—O—C2H5
O
O
稀硫酸
△
CH3—C—OC2H5 + NaOH
CH3—C—ONa + HOC2H5
△
O
O
2.酯的化学性质
(1)酸性条件下,酯的水解反应与酯化反应互为可逆反应;碱性条件下,碱能把生成的羧酸中和,水解能进行完全。
(2)酯的水解反应在稀酸催化下即可发生,说明它的逆反应即酯化反应在该条件下也能进行,而酯化反应却使用浓硫酸,目的是催化的同时吸收生成的水,使平衡最大限度地向生成酯的方向移动,提高酯的产率。
(3)在酸或碱存在的条件下,酯都能发生水解反应生成相应的羧酸(盐)和醇。
R—C—OR’+ H2O
R—C—OH+H—O—R’
O
O
稀硫酸
△
R—C—ONa + H—O—R’
△
O
R—C—OR’+ NaOH
O
酸性水解:
碱性水解:
油脂
PART 03
1.油脂的组成和结构
油脂的成分主要是高级脂肪酸与甘油形成的酯,由C、H、O三种元素组成,官能团是酯基,结构表示如下:
R1-C-O-CH2
R2-C-O-CH
R3-C-O-CH2
O
=
O
=
O
=
油脂的结构
①R1、R2、R3代表高级脂肪酸的饱和烃基或不饱和烃基(含碳碳双键);
②如果R1、R2、R3相同,这样的油脂称为简单甘油酯;如果R1、R2、R3不相同,这样的油脂称为混合甘油酯;
③在天然油脂中,R1、R2、R3一般不相同,属于混合甘油酯。
1.油脂的组成和结构
形成油脂的几种重要的高级脂肪酸:
酸名 软脂酸 硬脂酸 油酸 亚油酸
分子式 C15H31COOH C17H35COOH C17H33COOH C17H31COOH
饱和高级脂肪酸甘油酯在常温常压下呈固态或半固态,称为脂肪;
不饱和高级脂肪酸甘油酯在常温常压下呈液态,称为油。
2.油脂的化学性质
请写出硬脂酸、油酸分别与丙三醇反应的化学方程式。
HO—CH2
HO—CH
HO—CH2
3C17H35COOH +
C17H35COOCH2
C17H35COOCH
C17H35COOCH2
+ 3H2O
HO—CH2
HO—CH
HO—CH2
3C17H33COOH +
C17H33COOCH2
C17H33COOCH
C17H33COOCH2
+ 3H2O
催化剂
△
催化剂
△
2.油脂的化学性质
(1)水解反应
油脂是高级脂肪酸的甘油酯,能够发生水解反应;而高级脂肪酸中又有不饱和的,因此许多油脂又兼有烯烃的化学性质,可以发生加成反应。
油脂在酸、碱或酶等催化剂的作用下,均可发生水解反应。1mol油脂完全水解可生成1mol甘油和3mol高级脂肪酸。
a.酸性水解:油脂在酸作催化剂的条件下,发生水解反应,生成甘油和高级脂肪酸。如:
C17H35COOCH2
C17H35COOCH
C17H35COOCH2
+ 3H2O
3C17H35COOH
+
硬脂酸
CH2OH
CH2OH
CHOH
甘油
硬脂酸甘油酯
稀硫酸
△
2.油脂的化学性质
(1)水解反应
b.碱性水解:油脂在碱性溶液中的水解反应又称为皂化反应,如:
C17H35COOCH2
C17H35COOCH
C17H35COOCH2
+ 3NaOH
3C17H35COONa
+
硬脂酸钠
CH2OH
CH2OH
CHOH
甘油
硬脂酸甘油酯
高级脂肪酸钠(或钾)盐是肥皂的有效成分,工业上利用油脂的皂化反应来制造肥皂。
2.油脂的化学性质
(2)油脂的氢化——(加成反应)
CH2OOCC17H33
CHOOCC17H33
CH2OOCC17H33
CH2OOCC17H35
CHOOCC17H35
CH2OOCC17H35
+3H2
催化剂
不饱和程度较高、熔点较低的液态油,通过催化加氢可提高饱和度,转变成半固态的脂肪,这个过程称为油脂的氢化,也称为油脂的硬化。如:
油酸甘油酯
硬脂酸甘油酯(脂肪)
2.油脂的化学性质
3.胺
(1)定义:烃基取代氨分子中的氢原子而形成的化合物;胺也可以看作是烃分子中的氢原子被氨基所替代的化合物。
甲胺:CH3—NH2
苯胺:
—NH2
一般可写作R—NH2
(2)化学性质
①胺类化合物具有碱性
—NH2+HCl
—NH3Cl
甲胺和苯胺都是合成医药、农药和染料等的重要原料。
“氨”“铵”“胺”的区别:氨是指氨气(NH3);铵一般出现在铵盐中;胺是指一类含氨基(—NH2)或取代的氨基(—NRR’)的有机物。
4.酰胺
(1)结构
酰胺是羧酸分子中羟基被氨基所替代得到的化合物。
(2)常见物质
①乙酰胺
②苯甲酰胺
③N,N-二甲基甲酰胺
CH3—C—NH2
O
H—C—N(CH3)2
O
—C—NH2
O
4.酰胺
(3)化学性质
①与盐酸:
②与氢氧化钠溶液:
(4)应用
酰胺常被用作溶剂和化工原料。例如,N,N 二甲基甲酰胺是良好的溶剂,可以溶解很多有机化合物和无机化合物,是生产多种化学纤维的溶剂,也用于合成农药、医药等。
酰胺键,与酯基类似,在酸或碱存在并加热的条件下可以发生水解反应。请写出下列化学方程式。
△
△
RCONH2+H2O+HCl RCOOH+NH4Cl
RCONH2+NaOH RCOONa+NH3↑
随堂训练
1.判断正误
(1)酯类在碱性条件下的水解程度大。 ( )
(2)油脂的相对分子质量较大,故属于有机高分子。( )
(3)汽油、甘油都属于油脂。( )
(4)油脂的水解反应叫做皂化反应。( )
(5)酯化反应与酯的水解反应均为取代反应。( )
(6)乙酸乙酯在碱性条件下也能发生水解反应,也称皂化反应。( )
随堂训练
2.油脂皂化反应后,使肥皂从反应混合液中分离的方法有①分液 ②蒸馏 ③过滤 ④盐析,其中正确的顺序是( )
A.①②③
B.④③②
C.④③
D.③②
C
随堂训练
3.可以判断油脂皂化反应基本完成的现象是( )
A.反应液使红色石蕊试纸变蓝色
B.反应液使蓝色石蕊试纸变红色
C.反应后静置,反应液分为两层
D. 反应后静置,反应液不分层
D
随堂训练
4.在一定条件下,动植物油脂与醇反应可制备生物柴油,化学方程式如下:
下列叙述错误的是( )
A.生物柴油由可再生资源制得 B.生物柴油是不同酯组成的混合物
C.动植物油脂是高分子化合物 D.“地沟油”可用于制备生物柴油
C
随堂训练
5.某中性有机物,在酸性条件下可以发生水解,生成相对分子
质量相同的A和B,A是中性物质,B可以与碳酸钠反应放出气体,
该有机物是( )
A.CH3COOC3H7 B.CH3COOC2H5
C.CH3COONa D.CH3CH2Br
A
随堂训练
6.某有机物的结构简式是
关于它的性质描述正确的是( )
①能发生加成反应 ②能消耗NaOH 3 mol
③能水解生成两种酸 ④不能使溴水褪色
⑤能发生酯化反应 ⑥有酸性
A.①②③ B.②③⑤ C.仅⑥ D.全部正确
D
谢谢观看
