6.2.1蛋白质(教学课件) (共28张PPT)高中化学苏教版选择性必修三(2019)
文档属性
| 名称 | 6.2.1蛋白质(教学课件) (共28张PPT)高中化学苏教版选择性必修三(2019) |  | |
| 格式 | pptx | ||
| 文件大小 | 3.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-08 00:14:20 | ||
图片预览








文档简介
(共28张PPT)
专题六 生命活动的物质基础——糖类、油脂、蛋白质
第二单元 蛋白质
6.2.1 氨基酸的组成、结构与性质
核心素养目标
宏观辨识与微观探析:
学生能从宏观角度认识氨基酸在生命活动中的重要作用,微观层面理解氨基酸的组成、结构,包括官能团、α- 氨基酸的结构特点等。
证据推理与模型认知:
通过对氨基酸同分异构体的分析培养学生基于证据进行推理的能力,构建判断氨基酸及其同分异构体的思维模型,能运用模型解决相关化学问题。
科学态度与社会责任:
认识氨基酸在生命科学中的重要意义,体会化学与生命健康的紧密联系,培养学生关注科学前沿、热爱科学的态度,增强学生运用化学知识服务社会、促进人类健康发展的责任感。
教学重难点
重点
氨基酸的组成、结构,包括分类、结构简式的书写、手性碳原子等;
氨基酸的两性和缩合反应等化学性质,以及相关化学方程式的书写;
氨基酸的检验方法 —— 茚三酮反应。
难点
理解氨基酸两性的原理,分析其在不同酸碱性条件下的存在形态;
掌握氨基酸缩合反应的规律,包括二肽、多肽形成过程中肽键的形成方式及可能出现的不同结构,以及氨基酸分子内或分子间脱水成环、缩聚成高分子化合物的反应机理;
同分异构体的书写及判断,特别是氨基酸与硝基化合物同分异构体的关系。
课前导入
氨基酸是构建细胞、修复组织的基础材料,氨基酸被人体用于制造抗体蛋白质以对抗细菌和病毒的侵染,制造血红蛋白以传送氧气,制造酶和激素以维持和调节新陈代谢。氨基酸是合成神经介质不可缺少的前提物质,它能够为机体和大脑活动提供能源,是一切生命之元。那么氨基酸具有怎样的结构和性质呢
氨基酸的组成、结构
PART 01
概念及结构
★概念:
羧酸分子中烃基上的一个或几个氢原子被氨基取代后生成的化合物称为氨基酸
★结构:
氨基酸
官能团
氨基(—NH2)
羧基(—COOH)
α—氨基酸
连在同一个碳原子上
表示方法
氨基酸分子的手性
迄今为止,人类在自然界已发现了数百种氨基酸,但是从生物体内的蛋白质水解得到 的氨基酸,最常见的有20种,被称为蛋白质氨基酸。这20种常见氨基酸中,除甘氨酸外, 其余都是手性分子,且都是L型
氨基酸分子的命名
★由于氨基酸的系统命名通常比较复杂,实际使用较多的是其俗名。在表示多肽和蛋白质结构时,普遍使用的是氨基酸的缩写。
★通常情况下,氨基酸的英文缩写取其英文名称前三个字母,中文缩写则将其俗名中的“氨酸”省略。
如甘氨酸的英文缩写为“Gly”,中文缩写为“甘”;
亮氨酸的英文缩写为“Leu”,中文缩写为“亮”。
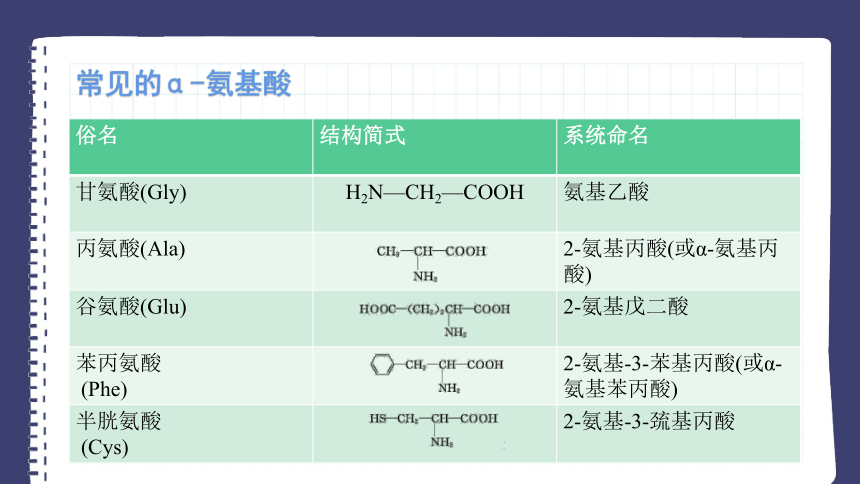
常见的α-氨基酸
俗名 结构简式 系统命名
甘氨酸(Gly) H2N—CH2—COOH 氨基乙酸
丙氨酸(Ala) 2-氨基丙酸(或α-氨基丙酸)
谷氨酸(Glu) 2-氨基戊二酸
苯丙氨酸 (Phe) 2-氨基-3-苯基丙酸(或α-氨基苯丙酸)
半胱氨酸 (Cys) 2-氨基-3-巯基丙酸
有关氨基酸的注意事项
★自然界中存在的氨基酸有数百种,但从生物体内的蛋白质水解得到的氨基酸,最常见的有20种,被称为蛋白质氨基酸。其中有8种氨基酸在人体内不能合成,必须通过食物供给,这些氨基酸称为必需氨基酸。20种常见氨基酸中除甘氨酸外,其余都是手性分子,且都是L型。
★人体合成精氨酸和组氨酸的能力也较差,这两种氨基酸被称为半必需氨基酸。人体若缺少这些氨基酸,就会引起病症。
★天然氨基酸大多数是α-氨基酸,组成蛋白质的氨基酸主要是α-氨基酸。
氨基酸的性质
PART 02
根据氨基酸的结构推测性质
从结构上推测,氨基酸分子中含有的氨基(—NH2),应具有一定的碱性;氨基酸分子中含有的羧基,又能表现出一定的酸性。实验也证明,氨基酸具有氨基和羧基的典型反应,如与酸的反应、酯化反应等,因此氨基酸也被称为两性化合物。氨基酸分子中的氨基和羧基发生相互作用,使氨基酸成为带有正电荷和负电荷的两性离子(称为内盐):
氨基酸的性质
★物理性质:
固态氨基酸主要以内盐形式存在,熔点较高,不易挥发,难溶于有机溶剂。常见的氨基酸均为无色结晶,熔点在200 ℃以上。
★化学性质:
①茚三酮反应
凡含有—NH2的α-氨基酸遇茚三酮均显紫色反应。该反应非常灵敏,是鉴定氨基酸最简便的方法。人的手汗中含有多种氨基酸,遇茚三酮可起显色反应,在法医学上曾通过该反应检验指纹。
【实验1】取1 mL 0.1%的茚三酮溶液,加入1%的甘氨酸溶液,将试管放入热水浴中,观察现象。
【实验2】用色氨酸溶液替代甘氨酸溶液,重复上述实验。
溶液酸碱性对氨基酸存在形态的影响
氨基酸是两性化合物,既能与酸发生反应,又能与碱发生反应。水溶液的pH不同,氨基酸在溶液中存在的形态也不同。
阳离子
两性离子
阴离子
近中性溶液中氨基酸的主要存在形式
在强酸性溶液(pH<1)中,氨基酸主要以阳离子形式存在
在强碱性溶液(pH>13)中,氨基酸主要以阴离子形式存在
溶液酸碱性对氨基酸存在形态的影响
★从平衡移动的角度看,在氨基酸中加入碱,电离平衡向酸式电离方向移动,溶解度增大;加入碱,电离平衡向碱式电离方向移动,溶解度也增大。当溶液中的氨基酸主要以两性离子的形态存在时,其在水中的溶解度最小,可以形成晶体析出。
★应用:
不同的氨基酸出现上述变化的pH各不相同,利用这一差异,可以通过控制溶液的pH分离不同的氨基酸。在多肽和蛋白质分子中,也存在氨基和羧基,同样可以通过这种方法分离它们。
氨基酸的两性
氨基酸中的羧基(—COOH)能电离出H+而显酸性,氨基(—NH2)能结合H+而显碱性,氨基酸是两性化合物
★与碱反应:
★与酸反应:
成肽反应
一分子α-氨基酸中的羧基与另一 分子α-氨基酸中的氨基可以发生像酯化反应那样的脱水反应,形成肽键(酰胺键)。我们通常把氨基酸分子间脱水的反应称为氨基酸的缩合反应,得到的产物称为肽,组成肽的氨基酸单元称为氨基酸残基。如:
肽的水解
通常把有氨基的一端叫N端,写在左边;有羧基的一端叫C端,写在右边。一般用氨基酸的缩写从左到右排列来表示肽分子的结构,图所示的二肽可简写为Gly-Ala
与酯能水解生成羧酸和醇一样,肽也可以在一定条件下水解生成氨基酸。
蛋白质种类多样的原因
◆氨基酸在结合成肽时,能够形成的异构体的种类十分繁多。
◆随着形成肽键的氨基酸的种类以及肽链长度的增加,理论上形成肽的种类将大幅度增加。
◆例如,3个不同的氨基酸可以形成6种不同的三肽,由4个不同的氨基酸可以形成24种不同的四肽,以此类推。
◆可见,氨基酸的种类和连接方式的不同,形成了种类繁多、结构各异的蛋白质。
课堂小结
PART 03
组成和结构
1
氨基酸
2
性质
官能团:氨基和羧基
分类
两性:能与酸碱反应
氨基酸的检验
缩合反应(成肽反应)
课堂练习
PART 04
1.下列有关α-氨基酸的说法中错误的是( )
A.结构简式一般可表示为
B.氨基酸是两性化合物
C.在酸溶液中主要以阳离子形式存在
D.发生加聚反应可生成蛋白质
D
2.下列关于氨基酸的叙述不正确的是( )
A.天然氨基酸都是晶体,一般都能溶于水
B.氨基酸不能发生水解反应
C.氨基酸是能与酸、碱反应生成盐的两性化合物
D.两个氨基酸分子脱水后形成的二肽中含有两个肽键
D
3.青霉素是医学上一种常用的抗生素,在体内经酸性水解后,得到青霉氨基酸,其结构简式如图所示(分子中的—SH 与—OH 具有类似的性质)。下列关于青霉氨基酸的推断合理的是( )
青霉氨基酸
A.青霉氨基酸分子中所有碳原子均在同一条直线上
B.青霉氨基酸只有酸性,没有碱性
C.青霉氨基酸分子间能形成多肽
D.1 mol 青霉氨基酸能与足量金属钠反应放出 0.5 mol H2
C
4.下列关于生物体内氨基酸的叙述错误的是( )
A.构成蛋白质的氨基酸分子的结构通式可表示为
B.人体内氨基酸的分解代谢最终产物是水、二氧化碳和尿素
C.人体内所有氨基酸均可以互相转化
D.两分子氨基酸通过脱水缩合可以形成二肽
C
Thanks
好好学习天天向上
专题六 生命活动的物质基础——糖类、油脂、蛋白质
第二单元 蛋白质
6.2.1 氨基酸的组成、结构与性质
核心素养目标
宏观辨识与微观探析:
学生能从宏观角度认识氨基酸在生命活动中的重要作用,微观层面理解氨基酸的组成、结构,包括官能团、α- 氨基酸的结构特点等。
证据推理与模型认知:
通过对氨基酸同分异构体的分析培养学生基于证据进行推理的能力,构建判断氨基酸及其同分异构体的思维模型,能运用模型解决相关化学问题。
科学态度与社会责任:
认识氨基酸在生命科学中的重要意义,体会化学与生命健康的紧密联系,培养学生关注科学前沿、热爱科学的态度,增强学生运用化学知识服务社会、促进人类健康发展的责任感。
教学重难点
重点
氨基酸的组成、结构,包括分类、结构简式的书写、手性碳原子等;
氨基酸的两性和缩合反应等化学性质,以及相关化学方程式的书写;
氨基酸的检验方法 —— 茚三酮反应。
难点
理解氨基酸两性的原理,分析其在不同酸碱性条件下的存在形态;
掌握氨基酸缩合反应的规律,包括二肽、多肽形成过程中肽键的形成方式及可能出现的不同结构,以及氨基酸分子内或分子间脱水成环、缩聚成高分子化合物的反应机理;
同分异构体的书写及判断,特别是氨基酸与硝基化合物同分异构体的关系。
课前导入
氨基酸是构建细胞、修复组织的基础材料,氨基酸被人体用于制造抗体蛋白质以对抗细菌和病毒的侵染,制造血红蛋白以传送氧气,制造酶和激素以维持和调节新陈代谢。氨基酸是合成神经介质不可缺少的前提物质,它能够为机体和大脑活动提供能源,是一切生命之元。那么氨基酸具有怎样的结构和性质呢
氨基酸的组成、结构
PART 01
概念及结构
★概念:
羧酸分子中烃基上的一个或几个氢原子被氨基取代后生成的化合物称为氨基酸
★结构:
氨基酸
官能团
氨基(—NH2)
羧基(—COOH)
α—氨基酸
连在同一个碳原子上
表示方法
氨基酸分子的手性
迄今为止,人类在自然界已发现了数百种氨基酸,但是从生物体内的蛋白质水解得到 的氨基酸,最常见的有20种,被称为蛋白质氨基酸。这20种常见氨基酸中,除甘氨酸外, 其余都是手性分子,且都是L型
氨基酸分子的命名
★由于氨基酸的系统命名通常比较复杂,实际使用较多的是其俗名。在表示多肽和蛋白质结构时,普遍使用的是氨基酸的缩写。
★通常情况下,氨基酸的英文缩写取其英文名称前三个字母,中文缩写则将其俗名中的“氨酸”省略。
如甘氨酸的英文缩写为“Gly”,中文缩写为“甘”;
亮氨酸的英文缩写为“Leu”,中文缩写为“亮”。
常见的α-氨基酸
俗名 结构简式 系统命名
甘氨酸(Gly) H2N—CH2—COOH 氨基乙酸
丙氨酸(Ala) 2-氨基丙酸(或α-氨基丙酸)
谷氨酸(Glu) 2-氨基戊二酸
苯丙氨酸 (Phe) 2-氨基-3-苯基丙酸(或α-氨基苯丙酸)
半胱氨酸 (Cys) 2-氨基-3-巯基丙酸
有关氨基酸的注意事项
★自然界中存在的氨基酸有数百种,但从生物体内的蛋白质水解得到的氨基酸,最常见的有20种,被称为蛋白质氨基酸。其中有8种氨基酸在人体内不能合成,必须通过食物供给,这些氨基酸称为必需氨基酸。20种常见氨基酸中除甘氨酸外,其余都是手性分子,且都是L型。
★人体合成精氨酸和组氨酸的能力也较差,这两种氨基酸被称为半必需氨基酸。人体若缺少这些氨基酸,就会引起病症。
★天然氨基酸大多数是α-氨基酸,组成蛋白质的氨基酸主要是α-氨基酸。
氨基酸的性质
PART 02
根据氨基酸的结构推测性质
从结构上推测,氨基酸分子中含有的氨基(—NH2),应具有一定的碱性;氨基酸分子中含有的羧基,又能表现出一定的酸性。实验也证明,氨基酸具有氨基和羧基的典型反应,如与酸的反应、酯化反应等,因此氨基酸也被称为两性化合物。氨基酸分子中的氨基和羧基发生相互作用,使氨基酸成为带有正电荷和负电荷的两性离子(称为内盐):
氨基酸的性质
★物理性质:
固态氨基酸主要以内盐形式存在,熔点较高,不易挥发,难溶于有机溶剂。常见的氨基酸均为无色结晶,熔点在200 ℃以上。
★化学性质:
①茚三酮反应
凡含有—NH2的α-氨基酸遇茚三酮均显紫色反应。该反应非常灵敏,是鉴定氨基酸最简便的方法。人的手汗中含有多种氨基酸,遇茚三酮可起显色反应,在法医学上曾通过该反应检验指纹。
【实验1】取1 mL 0.1%的茚三酮溶液,加入1%的甘氨酸溶液,将试管放入热水浴中,观察现象。
【实验2】用色氨酸溶液替代甘氨酸溶液,重复上述实验。
溶液酸碱性对氨基酸存在形态的影响
氨基酸是两性化合物,既能与酸发生反应,又能与碱发生反应。水溶液的pH不同,氨基酸在溶液中存在的形态也不同。
阳离子
两性离子
阴离子
近中性溶液中氨基酸的主要存在形式
在强酸性溶液(pH<1)中,氨基酸主要以阳离子形式存在
在强碱性溶液(pH>13)中,氨基酸主要以阴离子形式存在
溶液酸碱性对氨基酸存在形态的影响
★从平衡移动的角度看,在氨基酸中加入碱,电离平衡向酸式电离方向移动,溶解度增大;加入碱,电离平衡向碱式电离方向移动,溶解度也增大。当溶液中的氨基酸主要以两性离子的形态存在时,其在水中的溶解度最小,可以形成晶体析出。
★应用:
不同的氨基酸出现上述变化的pH各不相同,利用这一差异,可以通过控制溶液的pH分离不同的氨基酸。在多肽和蛋白质分子中,也存在氨基和羧基,同样可以通过这种方法分离它们。
氨基酸的两性
氨基酸中的羧基(—COOH)能电离出H+而显酸性,氨基(—NH2)能结合H+而显碱性,氨基酸是两性化合物
★与碱反应:
★与酸反应:
成肽反应
一分子α-氨基酸中的羧基与另一 分子α-氨基酸中的氨基可以发生像酯化反应那样的脱水反应,形成肽键(酰胺键)。我们通常把氨基酸分子间脱水的反应称为氨基酸的缩合反应,得到的产物称为肽,组成肽的氨基酸单元称为氨基酸残基。如:
肽的水解
通常把有氨基的一端叫N端,写在左边;有羧基的一端叫C端,写在右边。一般用氨基酸的缩写从左到右排列来表示肽分子的结构,图所示的二肽可简写为Gly-Ala
与酯能水解生成羧酸和醇一样,肽也可以在一定条件下水解生成氨基酸。
蛋白质种类多样的原因
◆氨基酸在结合成肽时,能够形成的异构体的种类十分繁多。
◆随着形成肽键的氨基酸的种类以及肽链长度的增加,理论上形成肽的种类将大幅度增加。
◆例如,3个不同的氨基酸可以形成6种不同的三肽,由4个不同的氨基酸可以形成24种不同的四肽,以此类推。
◆可见,氨基酸的种类和连接方式的不同,形成了种类繁多、结构各异的蛋白质。
课堂小结
PART 03
组成和结构
1
氨基酸
2
性质
官能团:氨基和羧基
分类
两性:能与酸碱反应
氨基酸的检验
缩合反应(成肽反应)
课堂练习
PART 04
1.下列有关α-氨基酸的说法中错误的是( )
A.结构简式一般可表示为
B.氨基酸是两性化合物
C.在酸溶液中主要以阳离子形式存在
D.发生加聚反应可生成蛋白质
D
2.下列关于氨基酸的叙述不正确的是( )
A.天然氨基酸都是晶体,一般都能溶于水
B.氨基酸不能发生水解反应
C.氨基酸是能与酸、碱反应生成盐的两性化合物
D.两个氨基酸分子脱水后形成的二肽中含有两个肽键
D
3.青霉素是医学上一种常用的抗生素,在体内经酸性水解后,得到青霉氨基酸,其结构简式如图所示(分子中的—SH 与—OH 具有类似的性质)。下列关于青霉氨基酸的推断合理的是( )
青霉氨基酸
A.青霉氨基酸分子中所有碳原子均在同一条直线上
B.青霉氨基酸只有酸性,没有碱性
C.青霉氨基酸分子间能形成多肽
D.1 mol 青霉氨基酸能与足量金属钠反应放出 0.5 mol H2
C
4.下列关于生物体内氨基酸的叙述错误的是( )
A.构成蛋白质的氨基酸分子的结构通式可表示为
B.人体内氨基酸的分解代谢最终产物是水、二氧化碳和尿素
C.人体内所有氨基酸均可以互相转化
D.两分子氨基酸通过脱水缩合可以形成二肽
C
Thanks
好好学习天天向上
