鲁科版高中化学必修二第二章第二节化学反应与能量转化第二课时教学课件(共26张PPT)
文档属性
| 名称 | 鲁科版高中化学必修二第二章第二节化学反应与能量转化第二课时教学课件(共26张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 85.7MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-09 00:00:00 | ||
图片预览






文档简介
(共26张PPT)
鲁科版必修第二册
第2章 第2节 化学反应与能量转化
第2课时
化学反应能量转化的重要应用——化学电池
1.氢能源被视为 21 世纪最具发展潜力的清洁能源,氢氧燃料电池被认为是利用氢能解决未来人类能源危机的途径之一。氢氧燃料电池的优点是什么?
2.氢氧燃料电池汽车推广使用,面临的主要问题是什么?
3.氢氧燃料电池是如何把化学能转化为电能的呢?
思考
新课导入
一、化学反应能量转化的重要应用——化学电池
形形色色的电池
知识梳理
根据原电池原理制成的电池。
原电池:
利用氧化还原反应将化学能直接转化成电能的装置。
化学电池:
原电池的发明历史可追溯到18世纪末期,当时意大利生物学家伽伐尼正在进行著名的青蛙实验,当用金属手术刀接触蛙腿时,发现蛙腿会抽搐。大名鼎鼎的伏特认为这是金属与蛙腿组织液(电解质溶液)之间产生的电流刺激造成的。1800年,伏特据此设计出了被称为伏打电堆的装置,锌为负极,银为正极,用盐水作电解质溶液。1836年,丹尼尔发明了世界上第一个实用电池,并用于早期铁路信号灯。
初识
氢氧
燃料
电池
原电池是由哪些部分组成的?原电池中各部分的作用是什么?
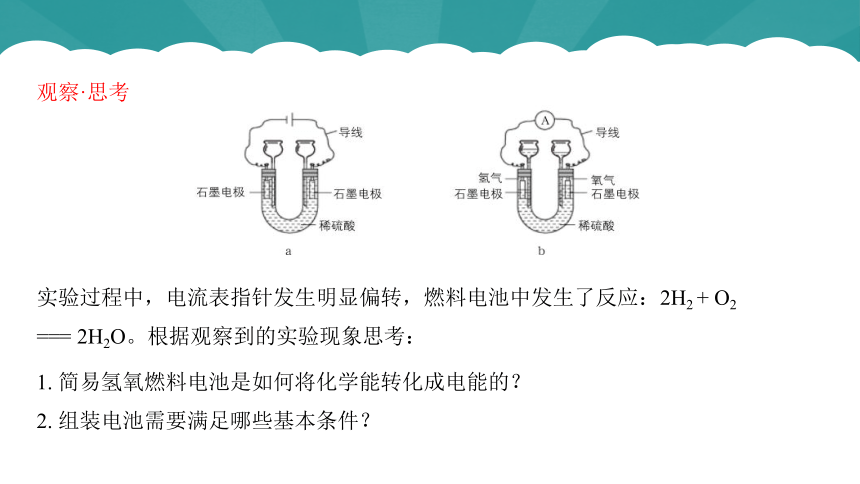
观察·思考
实验过程中,电流表指针发生明显偏转,燃料电池中发生了反应:2H2 + O2 === 2H2O。根据观察到的实验现象思考:
1. 简易氢氧燃料电池是如何将化学能转化成电能的?
2. 组装电池需要满足哪些基本条件?
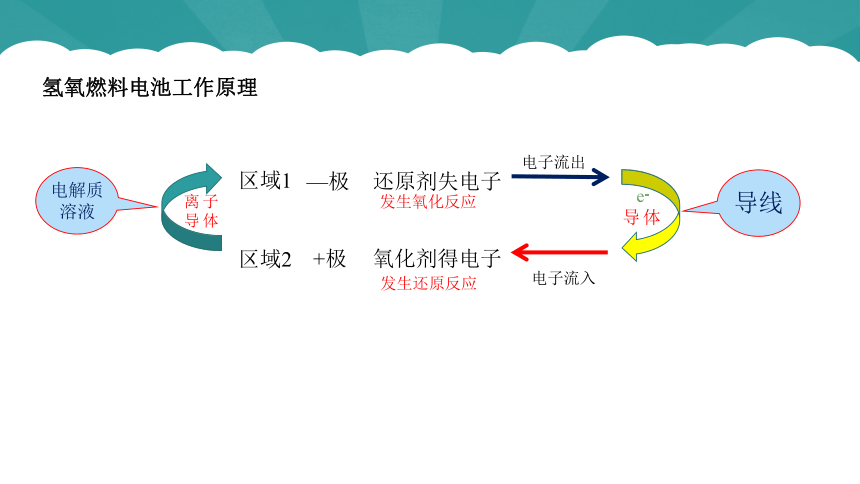
氢氧燃料电池工作原理
氢氧燃料电池工作原理
区域1
区域2
还原剂失电子
—极
氧化剂得电子
+极
电子流出
电子流入
离子
导体
e-
导体
导线
电解质溶液
发生氧化反应
发生还原反应
+
-
e-
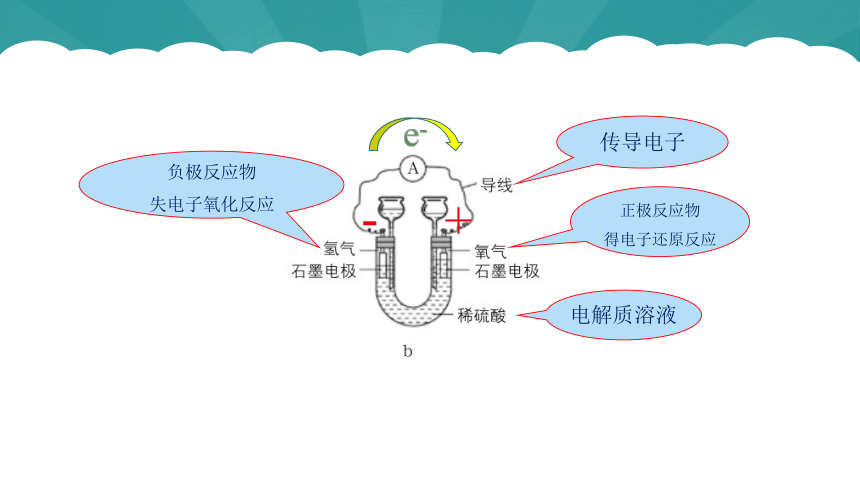
负极反应物
失电子氧化反应
正极反应物
得电子还原反应
电解质溶液
传导电子
【实验探究】原电池的工作原理
实验药品:锌片,铜片,稀硫酸
实验仪器:烧杯,导线,电极
实验步骤 现象
1.锌片插入稀硫酸
2.铜片插入稀硫酸
3.锌片和铜片上端连接在一起插入稀硫酸
思考:
1.锌片和铜片分别插入稀硫酸中有什么现象发生?
2.锌片和铜片用导线连接后插入稀硫酸中,现象又怎样?为什么?
3.锌片的质量有无变化?溶液中c(H+)如何变化?
4.锌片和铜片上变化的反应式怎样书写?
5.电子流动的方向如何?
工作原理分析
(1)分析装置图并填空
(2)原电池总反应式:Zn+2H+===Zn2++H2↑。
负极
氧化反应
Zn-2e-===Zn2+
正极
还原反应
2H++2e-===H2↑
原电池
的构成
2.两个电极
3. 电子导体
1.电极反应物
——导线
——传导电荷的电解质
——导电的固体
——在两极上自发进行氧化还原反应
闭合回路
4. 离子导体
原电池的构成条件
氢氧燃料电池的构造
组装原电池的基本条件
【思考】 如图装置中只有③⑤可以形成原电池,请分析构成原电池的条件是什么?
提示 原电池的构成条件:①活泼性不同的两极。
②电解质溶液作为离子导体。
③形成闭合回路。
交流·研讨
生活中平常使用的 5 号电池或 7 号电池都是锌锰干电池。锌锰干电池分为酸性锌锰干电池和碱性锌锰干电池两种。酸性锌锰干电池的组成如图所示。
在酸性锌锰干电池中,负极反应物和正极反应物分别是什么?正负极材料分别是什么?离子导体是什么?
负极反应物和负极材料
正极反应物
离子导体
正极材料
发展中的化学电源
干电池
(一次电池)
充电电池
(二次电池)
燃料电池
(1)干电池——一次电池
①特点:放电之后不能充电。
②实例:锌锰干电池。
锌
锌
碳棒
氯化铵、氯化锌
(2)充电电池——二次电池
①特点:放电时所进行的氧化还原反应,充电时可以逆向进行,使电池恢复到放电前的状态。
②实例:铅蓄电池,锂离子电池。
(3)燃料电池
①特点:燃料的利用率高、能量转换效率高,能长时间提供电能等。
②实例
以30%的KOH溶液为电解质溶液的氢氧燃料电池的电极反应如下:
负极: 。
正极: 。
总反应方程式:2H2+O2===2H2O。
2H2-4e-+4OH-===4H2O
O2+4e-+2H2O===4OH-
【思考】 铅蓄电池放电时的总反应:Pb+PbO2+2H2SO4===2PbSO4+2H2O。请依据原电池工作原理分析电池的组成和工作原理。
提示 电池的组成:负极为铅,正极为二氧化铅。电解质溶液为稀H2SO4。
工作原理:铅在负极失去电子生成PbSO4,二氧化铅在正极得到电子生成PbSO4,导线为电子导体,稀硫酸为离子导体,形成闭合回路。
化学电池
原电池
工作原理
构成
电极
离子导体(电解质溶液)
电子导体(导线)
自发氧化还原反应
课堂小结
鲁科版必修第二册
1. 列说法中正确的是 ( )
A.原电池是把电能转化为化学能的装置
B.原电池中电子流出的一极是正极,发生氧化反应
C.原电池中电流从负极流出,从正极流入
D.原电池中的阳离子向正极移动
当堂检测
D
2. X、Y两根金属棒插入Z溶液中构成如图所示装置,实验中电流表指针发生偏转,同时X棒变粗,Y棒变细,则X、Y、Z可能是下列中的( )
编号 X Y Z
A Zn Cu 稀硫酸
B Cu Zn 稀硫酸
C Cu Ag 硫酸铜溶液
D Ag Zn 硝酸银溶液
D
3. 如图所示电流表的指针发生偏转,同时A极的质量减小,B极上有气泡产生,C为电解质溶液,下列说法错误的是 ( )
A.B极为原电池的正极
B.A、B、C分别为Zn、Cu和稀盐酸
C.C中阳离子向A极移动
D.A极发生氧化反应
C
4. 氯铝电池是一种新型的燃料电池。试回答下列问题:
(1)通入Cl2(g)的电极是 (填“正”或“负”)极。
(2)投入Al(s)的电极是 (填“正”或“负”)极。
(3)电子从 (填“Al”或“Cl”)极流向 (填“正”或“负”)极。
(4)每消耗8.1 g Al(s),电路中通过的电子数目为 NA(NA表示阿伏加德罗常数的值)。
正
负
正
Al
0.9
鲁科版必修第二册
第2章 第2节 化学反应与能量转化
第2课时
化学反应能量转化的重要应用——化学电池
1.氢能源被视为 21 世纪最具发展潜力的清洁能源,氢氧燃料电池被认为是利用氢能解决未来人类能源危机的途径之一。氢氧燃料电池的优点是什么?
2.氢氧燃料电池汽车推广使用,面临的主要问题是什么?
3.氢氧燃料电池是如何把化学能转化为电能的呢?
思考
新课导入
一、化学反应能量转化的重要应用——化学电池
形形色色的电池
知识梳理
根据原电池原理制成的电池。
原电池:
利用氧化还原反应将化学能直接转化成电能的装置。
化学电池:
原电池的发明历史可追溯到18世纪末期,当时意大利生物学家伽伐尼正在进行著名的青蛙实验,当用金属手术刀接触蛙腿时,发现蛙腿会抽搐。大名鼎鼎的伏特认为这是金属与蛙腿组织液(电解质溶液)之间产生的电流刺激造成的。1800年,伏特据此设计出了被称为伏打电堆的装置,锌为负极,银为正极,用盐水作电解质溶液。1836年,丹尼尔发明了世界上第一个实用电池,并用于早期铁路信号灯。
初识
氢氧
燃料
电池
原电池是由哪些部分组成的?原电池中各部分的作用是什么?
观察·思考
实验过程中,电流表指针发生明显偏转,燃料电池中发生了反应:2H2 + O2 === 2H2O。根据观察到的实验现象思考:
1. 简易氢氧燃料电池是如何将化学能转化成电能的?
2. 组装电池需要满足哪些基本条件?
氢氧燃料电池工作原理
氢氧燃料电池工作原理
区域1
区域2
还原剂失电子
—极
氧化剂得电子
+极
电子流出
电子流入
离子
导体
e-
导体
导线
电解质溶液
发生氧化反应
发生还原反应
+
-
e-
负极反应物
失电子氧化反应
正极反应物
得电子还原反应
电解质溶液
传导电子
【实验探究】原电池的工作原理
实验药品:锌片,铜片,稀硫酸
实验仪器:烧杯,导线,电极
实验步骤 现象
1.锌片插入稀硫酸
2.铜片插入稀硫酸
3.锌片和铜片上端连接在一起插入稀硫酸
思考:
1.锌片和铜片分别插入稀硫酸中有什么现象发生?
2.锌片和铜片用导线连接后插入稀硫酸中,现象又怎样?为什么?
3.锌片的质量有无变化?溶液中c(H+)如何变化?
4.锌片和铜片上变化的反应式怎样书写?
5.电子流动的方向如何?
工作原理分析
(1)分析装置图并填空
(2)原电池总反应式:Zn+2H+===Zn2++H2↑。
负极
氧化反应
Zn-2e-===Zn2+
正极
还原反应
2H++2e-===H2↑
原电池
的构成
2.两个电极
3. 电子导体
1.电极反应物
——导线
——传导电荷的电解质
——导电的固体
——在两极上自发进行氧化还原反应
闭合回路
4. 离子导体
原电池的构成条件
氢氧燃料电池的构造
组装原电池的基本条件
【思考】 如图装置中只有③⑤可以形成原电池,请分析构成原电池的条件是什么?
提示 原电池的构成条件:①活泼性不同的两极。
②电解质溶液作为离子导体。
③形成闭合回路。
交流·研讨
生活中平常使用的 5 号电池或 7 号电池都是锌锰干电池。锌锰干电池分为酸性锌锰干电池和碱性锌锰干电池两种。酸性锌锰干电池的组成如图所示。
在酸性锌锰干电池中,负极反应物和正极反应物分别是什么?正负极材料分别是什么?离子导体是什么?
负极反应物和负极材料
正极反应物
离子导体
正极材料
发展中的化学电源
干电池
(一次电池)
充电电池
(二次电池)
燃料电池
(1)干电池——一次电池
①特点:放电之后不能充电。
②实例:锌锰干电池。
锌
锌
碳棒
氯化铵、氯化锌
(2)充电电池——二次电池
①特点:放电时所进行的氧化还原反应,充电时可以逆向进行,使电池恢复到放电前的状态。
②实例:铅蓄电池,锂离子电池。
(3)燃料电池
①特点:燃料的利用率高、能量转换效率高,能长时间提供电能等。
②实例
以30%的KOH溶液为电解质溶液的氢氧燃料电池的电极反应如下:
负极: 。
正极: 。
总反应方程式:2H2+O2===2H2O。
2H2-4e-+4OH-===4H2O
O2+4e-+2H2O===4OH-
【思考】 铅蓄电池放电时的总反应:Pb+PbO2+2H2SO4===2PbSO4+2H2O。请依据原电池工作原理分析电池的组成和工作原理。
提示 电池的组成:负极为铅,正极为二氧化铅。电解质溶液为稀H2SO4。
工作原理:铅在负极失去电子生成PbSO4,二氧化铅在正极得到电子生成PbSO4,导线为电子导体,稀硫酸为离子导体,形成闭合回路。
化学电池
原电池
工作原理
构成
电极
离子导体(电解质溶液)
电子导体(导线)
自发氧化还原反应
课堂小结
鲁科版必修第二册
1. 列说法中正确的是 ( )
A.原电池是把电能转化为化学能的装置
B.原电池中电子流出的一极是正极,发生氧化反应
C.原电池中电流从负极流出,从正极流入
D.原电池中的阳离子向正极移动
当堂检测
D
2. X、Y两根金属棒插入Z溶液中构成如图所示装置,实验中电流表指针发生偏转,同时X棒变粗,Y棒变细,则X、Y、Z可能是下列中的( )
编号 X Y Z
A Zn Cu 稀硫酸
B Cu Zn 稀硫酸
C Cu Ag 硫酸铜溶液
D Ag Zn 硝酸银溶液
D
3. 如图所示电流表的指针发生偏转,同时A极的质量减小,B极上有气泡产生,C为电解质溶液,下列说法错误的是 ( )
A.B极为原电池的正极
B.A、B、C分别为Zn、Cu和稀盐酸
C.C中阳离子向A极移动
D.A极发生氧化反应
C
4. 氯铝电池是一种新型的燃料电池。试回答下列问题:
(1)通入Cl2(g)的电极是 (填“正”或“负”)极。
(2)投入Al(s)的电极是 (填“正”或“负”)极。
(3)电子从 (填“Al”或“Cl”)极流向 (填“正”或“负”)极。
(4)每消耗8.1 g Al(s),电路中通过的电子数目为 NA(NA表示阿伏加德罗常数的值)。
正
负
正
Al
0.9
