8.3 酸和碱反应 教学课件(共38张PPT内嵌视频)_初中化学科粤版(2024)九年级下册教学
文档属性
| 名称 | 8.3 酸和碱反应 教学课件(共38张PPT内嵌视频)_初中化学科粤版(2024)九年级下册教学 |  | |
| 格式 | pptx | ||
| 文件大小 | 112.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 科粤版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-09 21:28:57 | ||
图片预览









文档简介
(共39张PPT)
8.3 酸和碱反应
核心素养目标
一、化学观念
形成 “酸和碱能发生中和反应,本质是氢离子和氢氧根离子结合生成水”
的观念;认识复分解反应的特点,能从物质变化和微粒角度理解化学反应 。
二、科学思维
通过实验探究酸和碱反应,培养分析、推理和归纳能力;
三、科学态度与责任
严谨对待实验,尊重实验事实;了解中和反应在生产生活中的应用,增
强将化学知识应用于实际、保护环境的责任感。
学习重难点
重点:
1. 中和反应的概念、实质及应用;
2. 复分解反应的概念。
难点:
1. 从微观角度理解中和反应的实质;
2. 判断化学反应所属的基本反应类型。
新课导入
酸和碱的组成
PART 01
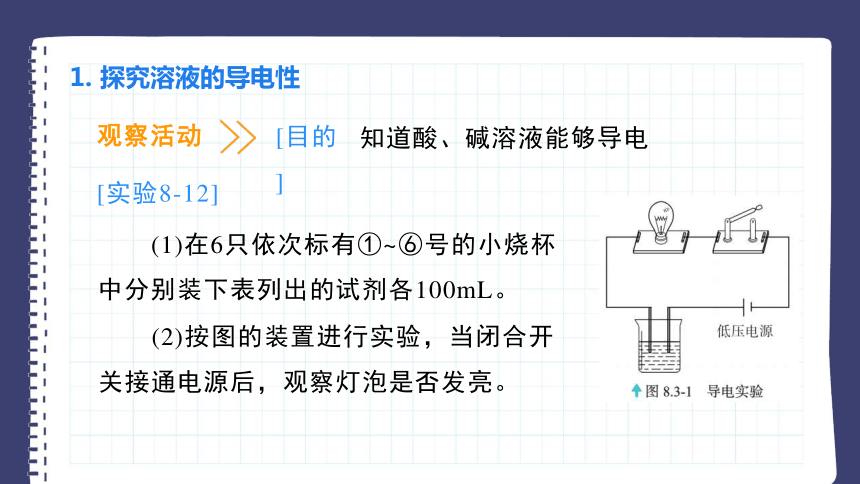
1. 探究溶液的导电性
[目的]
知道酸、碱溶液能够导电
观察活动
[实验8-12]
(1)在6只依次标有①~⑥号的小烧杯中分别装下表列出的试剂各100mL。
(2)按图的装置进行实验,当闭合开关接通电源后,观察灯泡是否发亮。
1. 探究溶液的导电性
[实验现象]
实验结论:蒸馏水、酒精不导电,稀盐酸、稀硫酸、烧碱溶液和澄清石灰水能够导电。
试剂 ①蒸馏水 ②酒精 ③稀盐酸 ④稀硫酸 ⑤稀烧碱溶液 ⑥澄清石灰水
灯泡是否发亮
不亮
不亮
发亮
发亮
发亮
发亮
(略暗)
溶液中存在可自由移动的带电微观粒子
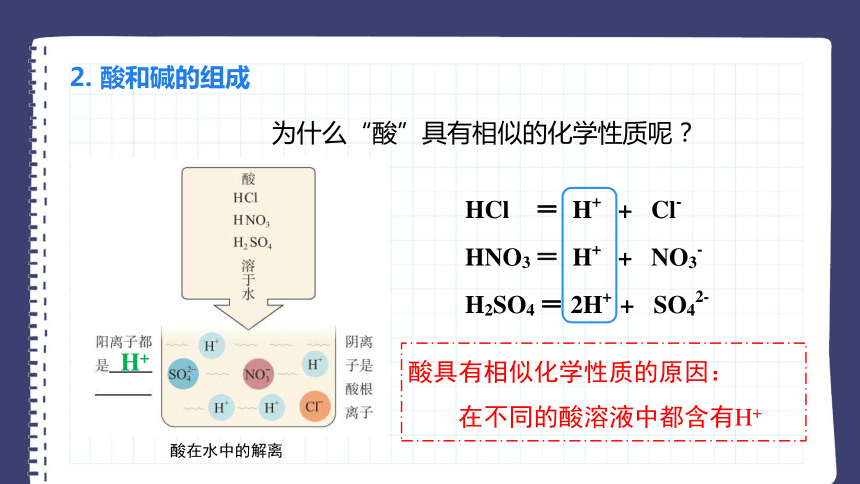
2. 酸和碱的组成
酸在水中的解离
HCl = H+ + Cl-
H2SO4 = 2H+ + SO42-
HNO3 = H+ + NO3-
为什么“酸”具有相似的化学性质呢?
酸具有相似化学性质的原因:
在不同的酸溶液中都含有H+
H+
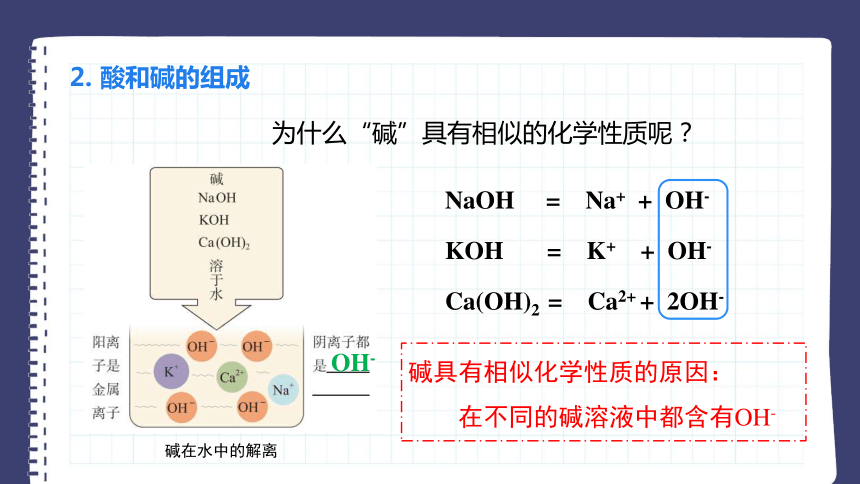
2. 酸和碱的组成
为什么“碱”具有相似的化学性质呢?
碱具有相似化学性质的原因:
在不同的碱溶液中都含有OH-
碱在水中的解离
OH-
NaOH = Na+ + OH-
Ca(OH)2 = Ca2+ + 2OH-
KOH = K+ + OH-
中和反应
PART 02
1. 实验探究——酸与碱反应
[目的]
认识酸与碱的中和反应
学生实验探究
[提出问题]
[实验8-13]在烧杯中加入约5mL稀氢氧化钠溶液,用滴管慢慢滴入稀盐酸,观察到什么现象?有没有反应发生?
思考:为了能观察到上述两种溶液混合后是否发生了化学反应,应采取什么方法
1. 实验探究——酸与碱反应
[实验设计与实施]
[实验用品]稀盐酸、稀硫酸、稀氢氧化钠溶液、澄清石灰水、紫色石蕊溶液、无色酚酞溶液。
1. 实验探究——酸与碱反应
实验序号 实验操作 实验现象
(1) 在烧杯中加入约 5 mL稀氢氧化钠溶液,滴入几滴无色酚酞溶液
用滴管逐滴滴入稀盐酸, 并不断搅拌
溶液由无色变为红色
溶液逐渐由红色变为无色
[实验设计与实施]
NaOH + HCl = NaCl + H2O
实验 实验设计 发生化学反应的证据 反应的化学方程式
(2)
(3)
(4)
你还能想到哪些实验方案呢 请设计实验(2)(3)和(4)并进行验证。
溶液由红色变为紫色,又变为蓝色
溶液由蓝色变为紫色,又变为红色
H2SO4+Ca(OH)2=CaSO4+2H2O
溶液由无色变为红色
H2SO4+2NaOH =Na2SO4+2H2O
澄清石灰水
5 mL稀硫酸+紫色石蕊溶液
稀氢氧化钠溶液
稀盐酸
5 mL澄清石灰水+紫色石蕊溶液
2HCl+Ca(OH)2=CaCl2+2H2O
指示剂颜色的变化说明酸溶液与碱溶液发生了化学反应。
2. 中和反应
中和反应
酸和碱作用生成盐和水的反应,叫作中和反应
表达式:酸 + 碱 → 盐 + 水
实质:酸溶液中的H+和碱溶液中的OH-结合生成 H2O,即 H+ + OH-=H2O
1. “凡是生成盐和水的反应,都是中和发应”该说法是否正确
思考讨论
2. 中和反应属于基本反应类型吗?我们学过几种基本反应类型?
不正确,例如CO2+2NaOH=Na2CO3+H2O生成物是盐和水,但是反应不是中和反应。
中和反应不属于基本反应类型。
目前学过的基本反应类型有分解反应、化合反应、置换反应。
拓展延伸
中和反应的判断依据
(1)借助酸碱指示剂;
(2)中和反应是放热反应,可借助温度的变化判断;
(3)并不是所有的中和反应都没有明显现象。如难溶性的碱与酸反应,难溶的碱会溶解。
Cu(OH)2+H2SO4=CuSO4+2H2O,蓝色固体溶解,生成蓝色溶液。
Fe(OH)3+3HCl=FeCl3+3H2O,红褐色固体溶解,生成黄色溶液。
信息技术与化学实验
利用手持技术数字化实验寻找酸碱中和反应发生的证据
对于没有明显实验现象的酸碱中和反应,同学们还可以运用手持技术数字化实验,通过pH传感器定量测量反应过程中溶液的pH,通过分析 pH 变化曲线寻找酸和碱发生反应的证据。也可以通过温度传感器定量测量反应过程中温度的变化。
3. 酸、碱的化学共性
项目 酸的主要化学性质 碱的主要化学性质
与指示剂作用 紫色石蕊 使紫色石蕊溶液变红 使紫色石蕊溶液变蓝
无色酚酞 使无色酚酞溶液不变 使无色酚酞溶液变红
酸碱相互作用 酸+碱→盐+水 与氧化物反应 酸+金属氧化物→盐+水 碱+非金属氧化物→盐+水
与盐反应 酸+盐→新酸+新盐 碱+盐→新碱+新盐
与较活泼金属反应 酸+较活泼金属→盐+氢气
复分解反应
PART 03
Na2CO3 + 2HCl == 2NaCl + H2O+CO2↑
NaHCO3 + HCl == NaCl + H2O+CO2↑
Na2CO3 + Ca(OH)2 == CaCO3↓ + 2NaOH
H2CO3
思考讨论
观察:上述几个反应有什么共同特点呢?
1. 复分解反应
复分解反应
由两种化合物相互交换成分,生成另外两种化合物的反应。
概念
在复分解反应中,反应前后所有元素的化合价不变
双交换,价不变
AB+CD→AD+CB
概念
特点
思考讨论
1. 两种化合物生成另外两种化合物的反应一定是复分解反应吗?
不一定,例如CO2+2NaOH=Na2CO3+H2O,不符合复分解反应“两交换”的特点,不属于复分解反应。
2. 中和反应和复分解反应有什么样的关系呢?
中和反应一定是复分解反应,但复分解反应不一定是中和反应,复分解反应包含中和反应。
复分解反应
中和反应
2. 四大基本反应类型比较
基本反应类型 反应物种类 生成物种类 反应表达式 特征 化合价变化
化合反应 两种或两种以上 一种 A+B+ →X 多变一 可变可不变
分解反应 一种 两种或两种以上 X→A+B+ 一变多 置换反应 一种单质、一种化合物 一种单质、一种化合物 A+BC→B+AC 单换单 一定改变
复分解反应 两种化合物 两种化合物 AB+CD→AD+CB 双交换,价不变 一定不变
中和反应的应用
PART 04
1. 改良酸性或碱性土壤
若土壤显酸性,可向土壤中加入适量的熟石灰,中和土壤的酸性。
夏天到农村去,常常看到养鱼的农户向放干的鱼塘底撒熟石灰,这是为了中和鱼塘底泥中过多的有机酸(同时达到杀菌消毒的目的),使放水后的鱼塘水达到适合鱼苗生长的pH。
由于工业生产排放的酸性物质随雨水落下,形成酸雨。酸雨对工业设备、石材建筑和文物古迹的腐蚀十分严重,对农作物等植物的危害也十分明显。我们可以利用熟石灰来中和土壤和某些水源中过多的酸,以减轻酸雨的危害。
2. 废水处理
如果废水中含有酸性物质(如硫酸、盐酸等),必须先用碱性物质(如烧碱、熟石灰等)将其中和成中性以后才能排放,否则会造成水体污染。
如用熟石灰中和硫酸厂的污水:
H2SO4+Ca(OH)2=CaSO4+2H2O
3. 医药应用
(1)人被蚊虫叮咬后(蚁虫能分泌出蚁酸),可在叮咬处涂抹弱碱性的肥皂水、稀氨水或清凉油,以减轻疼痛;
(2)有胃病的人常常胃酸(主要成分是盐酸)过多,可以口服碱性胃药(某些胃药的有效成分是氢氧化铝),以中和胃中过多的胃酸。3HCl+Al(OH)3=AlCl3+3H2O
思考讨论
1. 可不可以用NaOH来中和胃酸、蚁酸或改良酸性土壤?
不可以。因为NaOH的碱性太强,具有强的腐蚀性。
知识视窗
酸雨的形成
部分非金属氧化物能跟水化合生成酸,例如:
煤和石油燃烧后所产生的烟气中,含有二氧化硫和氮氧化物,排放到空气中被云层吸收,并经过化学作用形成酸雾,随同雨水下降便成为显酸性的雨水,若pH小于5.6,称为酸雨。
(亚硫酸)
SO2+H2O=H2SO3
SO3+H2O=H2SO4
知识视窗
酸雨的危害
酸雨的危害很大,影响人类健康,使森林大面积枯死,使湖水酸化、鱼类死亡,使农作物生长受到影响而减产,使名胜古迹、建筑物腐蚀损坏等
总结归纳
1. 中和反应在日常生活和工农业生产中有广泛的应用。下列关于中和反应的说法正确的是( )
A. 生成盐和水的反应都属于中和反应
B. 中和反应都能观察到溶液颜色发生改变
C. 碳酸钙和盐酸发生的反应是中和反应
D. 中和反应一定是放热反应
随堂练习
D
2. 用NaOH溶液与稀硫酸进行中和反应实验,开始时滴入几滴酚酞溶液,测得溶液的pH变化如图所示。下列说法不正确的是( )
A. 图像表明是向NaOH溶液中加入稀硫酸
B. ac段溶液颜色逐渐变浅,d点溶液为无色
C. d点溶液钠元素质量分数大于b点溶液钠元素质量分数
D. ac段溶液升温明显高于cd段,说明该反应放出热量
随堂练习
C
3. 为了证明中和反应已经发生,小文同学做了如图所示的四个实验,不能达到实验目的的是( )
A. 甲实验中,溶液仍为无色
B. 乙实验中,溶液由无色变为红色
C. 丙实验中,溶液由红色变为无色
D. 丁实验中,溶液由红色变为无色
随堂练习
B
4. 关于化学基本反应类型的说法正确的是( )
A. 分解反应一定有单质生成
B. 化合反应一定是两种物质生成一种新物质
C. 置换反应一定有元素的化合价发生改变
D. 两种化合物反应生成另外两种化合物的反应一定是复分解反应
随堂练习
C
5. 中和反应在生产、生活中应用广泛。下列应用的主要原理不涉及中和反应的是( )
A. 生石灰用于加热即热食品
B. 氢氧化铝用于治疗胃酸过多
C. 熟石灰用于改良酸性土壤
D. 硫酸处理印染厂的含碱废水
随堂练习
A
谢谢观看
8.3 酸和碱反应
核心素养目标
一、化学观念
形成 “酸和碱能发生中和反应,本质是氢离子和氢氧根离子结合生成水”
的观念;认识复分解反应的特点,能从物质变化和微粒角度理解化学反应 。
二、科学思维
通过实验探究酸和碱反应,培养分析、推理和归纳能力;
三、科学态度与责任
严谨对待实验,尊重实验事实;了解中和反应在生产生活中的应用,增
强将化学知识应用于实际、保护环境的责任感。
学习重难点
重点:
1. 中和反应的概念、实质及应用;
2. 复分解反应的概念。
难点:
1. 从微观角度理解中和反应的实质;
2. 判断化学反应所属的基本反应类型。
新课导入
酸和碱的组成
PART 01
1. 探究溶液的导电性
[目的]
知道酸、碱溶液能够导电
观察活动
[实验8-12]
(1)在6只依次标有①~⑥号的小烧杯中分别装下表列出的试剂各100mL。
(2)按图的装置进行实验,当闭合开关接通电源后,观察灯泡是否发亮。
1. 探究溶液的导电性
[实验现象]
实验结论:蒸馏水、酒精不导电,稀盐酸、稀硫酸、烧碱溶液和澄清石灰水能够导电。
试剂 ①蒸馏水 ②酒精 ③稀盐酸 ④稀硫酸 ⑤稀烧碱溶液 ⑥澄清石灰水
灯泡是否发亮
不亮
不亮
发亮
发亮
发亮
发亮
(略暗)
溶液中存在可自由移动的带电微观粒子
2. 酸和碱的组成
酸在水中的解离
HCl = H+ + Cl-
H2SO4 = 2H+ + SO42-
HNO3 = H+ + NO3-
为什么“酸”具有相似的化学性质呢?
酸具有相似化学性质的原因:
在不同的酸溶液中都含有H+
H+
2. 酸和碱的组成
为什么“碱”具有相似的化学性质呢?
碱具有相似化学性质的原因:
在不同的碱溶液中都含有OH-
碱在水中的解离
OH-
NaOH = Na+ + OH-
Ca(OH)2 = Ca2+ + 2OH-
KOH = K+ + OH-
中和反应
PART 02
1. 实验探究——酸与碱反应
[目的]
认识酸与碱的中和反应
学生实验探究
[提出问题]
[实验8-13]在烧杯中加入约5mL稀氢氧化钠溶液,用滴管慢慢滴入稀盐酸,观察到什么现象?有没有反应发生?
思考:为了能观察到上述两种溶液混合后是否发生了化学反应,应采取什么方法
1. 实验探究——酸与碱反应
[实验设计与实施]
[实验用品]稀盐酸、稀硫酸、稀氢氧化钠溶液、澄清石灰水、紫色石蕊溶液、无色酚酞溶液。
1. 实验探究——酸与碱反应
实验序号 实验操作 实验现象
(1) 在烧杯中加入约 5 mL稀氢氧化钠溶液,滴入几滴无色酚酞溶液
用滴管逐滴滴入稀盐酸, 并不断搅拌
溶液由无色变为红色
溶液逐渐由红色变为无色
[实验设计与实施]
NaOH + HCl = NaCl + H2O
实验 实验设计 发生化学反应的证据 反应的化学方程式
(2)
(3)
(4)
你还能想到哪些实验方案呢 请设计实验(2)(3)和(4)并进行验证。
溶液由红色变为紫色,又变为蓝色
溶液由蓝色变为紫色,又变为红色
H2SO4+Ca(OH)2=CaSO4+2H2O
溶液由无色变为红色
H2SO4+2NaOH =Na2SO4+2H2O
澄清石灰水
5 mL稀硫酸+紫色石蕊溶液
稀氢氧化钠溶液
稀盐酸
5 mL澄清石灰水+紫色石蕊溶液
2HCl+Ca(OH)2=CaCl2+2H2O
指示剂颜色的变化说明酸溶液与碱溶液发生了化学反应。
2. 中和反应
中和反应
酸和碱作用生成盐和水的反应,叫作中和反应
表达式:酸 + 碱 → 盐 + 水
实质:酸溶液中的H+和碱溶液中的OH-结合生成 H2O,即 H+ + OH-=H2O
1. “凡是生成盐和水的反应,都是中和发应”该说法是否正确
思考讨论
2. 中和反应属于基本反应类型吗?我们学过几种基本反应类型?
不正确,例如CO2+2NaOH=Na2CO3+H2O生成物是盐和水,但是反应不是中和反应。
中和反应不属于基本反应类型。
目前学过的基本反应类型有分解反应、化合反应、置换反应。
拓展延伸
中和反应的判断依据
(1)借助酸碱指示剂;
(2)中和反应是放热反应,可借助温度的变化判断;
(3)并不是所有的中和反应都没有明显现象。如难溶性的碱与酸反应,难溶的碱会溶解。
Cu(OH)2+H2SO4=CuSO4+2H2O,蓝色固体溶解,生成蓝色溶液。
Fe(OH)3+3HCl=FeCl3+3H2O,红褐色固体溶解,生成黄色溶液。
信息技术与化学实验
利用手持技术数字化实验寻找酸碱中和反应发生的证据
对于没有明显实验现象的酸碱中和反应,同学们还可以运用手持技术数字化实验,通过pH传感器定量测量反应过程中溶液的pH,通过分析 pH 变化曲线寻找酸和碱发生反应的证据。也可以通过温度传感器定量测量反应过程中温度的变化。
3. 酸、碱的化学共性
项目 酸的主要化学性质 碱的主要化学性质
与指示剂作用 紫色石蕊 使紫色石蕊溶液变红 使紫色石蕊溶液变蓝
无色酚酞 使无色酚酞溶液不变 使无色酚酞溶液变红
酸碱相互作用 酸+碱→盐+水 与氧化物反应 酸+金属氧化物→盐+水 碱+非金属氧化物→盐+水
与盐反应 酸+盐→新酸+新盐 碱+盐→新碱+新盐
与较活泼金属反应 酸+较活泼金属→盐+氢气
复分解反应
PART 03
Na2CO3 + 2HCl == 2NaCl + H2O+CO2↑
NaHCO3 + HCl == NaCl + H2O+CO2↑
Na2CO3 + Ca(OH)2 == CaCO3↓ + 2NaOH
H2CO3
思考讨论
观察:上述几个反应有什么共同特点呢?
1. 复分解反应
复分解反应
由两种化合物相互交换成分,生成另外两种化合物的反应。
概念
在复分解反应中,反应前后所有元素的化合价不变
双交换,价不变
AB+CD→AD+CB
概念
特点
思考讨论
1. 两种化合物生成另外两种化合物的反应一定是复分解反应吗?
不一定,例如CO2+2NaOH=Na2CO3+H2O,不符合复分解反应“两交换”的特点,不属于复分解反应。
2. 中和反应和复分解反应有什么样的关系呢?
中和反应一定是复分解反应,但复分解反应不一定是中和反应,复分解反应包含中和反应。
复分解反应
中和反应
2. 四大基本反应类型比较
基本反应类型 反应物种类 生成物种类 反应表达式 特征 化合价变化
化合反应 两种或两种以上 一种 A+B+ →X 多变一 可变可不变
分解反应 一种 两种或两种以上 X→A+B+ 一变多 置换反应 一种单质、一种化合物 一种单质、一种化合物 A+BC→B+AC 单换单 一定改变
复分解反应 两种化合物 两种化合物 AB+CD→AD+CB 双交换,价不变 一定不变
中和反应的应用
PART 04
1. 改良酸性或碱性土壤
若土壤显酸性,可向土壤中加入适量的熟石灰,中和土壤的酸性。
夏天到农村去,常常看到养鱼的农户向放干的鱼塘底撒熟石灰,这是为了中和鱼塘底泥中过多的有机酸(同时达到杀菌消毒的目的),使放水后的鱼塘水达到适合鱼苗生长的pH。
由于工业生产排放的酸性物质随雨水落下,形成酸雨。酸雨对工业设备、石材建筑和文物古迹的腐蚀十分严重,对农作物等植物的危害也十分明显。我们可以利用熟石灰来中和土壤和某些水源中过多的酸,以减轻酸雨的危害。
2. 废水处理
如果废水中含有酸性物质(如硫酸、盐酸等),必须先用碱性物质(如烧碱、熟石灰等)将其中和成中性以后才能排放,否则会造成水体污染。
如用熟石灰中和硫酸厂的污水:
H2SO4+Ca(OH)2=CaSO4+2H2O
3. 医药应用
(1)人被蚊虫叮咬后(蚁虫能分泌出蚁酸),可在叮咬处涂抹弱碱性的肥皂水、稀氨水或清凉油,以减轻疼痛;
(2)有胃病的人常常胃酸(主要成分是盐酸)过多,可以口服碱性胃药(某些胃药的有效成分是氢氧化铝),以中和胃中过多的胃酸。3HCl+Al(OH)3=AlCl3+3H2O
思考讨论
1. 可不可以用NaOH来中和胃酸、蚁酸或改良酸性土壤?
不可以。因为NaOH的碱性太强,具有强的腐蚀性。
知识视窗
酸雨的形成
部分非金属氧化物能跟水化合生成酸,例如:
煤和石油燃烧后所产生的烟气中,含有二氧化硫和氮氧化物,排放到空气中被云层吸收,并经过化学作用形成酸雾,随同雨水下降便成为显酸性的雨水,若pH小于5.6,称为酸雨。
(亚硫酸)
SO2+H2O=H2SO3
SO3+H2O=H2SO4
知识视窗
酸雨的危害
酸雨的危害很大,影响人类健康,使森林大面积枯死,使湖水酸化、鱼类死亡,使农作物生长受到影响而减产,使名胜古迹、建筑物腐蚀损坏等
总结归纳
1. 中和反应在日常生活和工农业生产中有广泛的应用。下列关于中和反应的说法正确的是( )
A. 生成盐和水的反应都属于中和反应
B. 中和反应都能观察到溶液颜色发生改变
C. 碳酸钙和盐酸发生的反应是中和反应
D. 中和反应一定是放热反应
随堂练习
D
2. 用NaOH溶液与稀硫酸进行中和反应实验,开始时滴入几滴酚酞溶液,测得溶液的pH变化如图所示。下列说法不正确的是( )
A. 图像表明是向NaOH溶液中加入稀硫酸
B. ac段溶液颜色逐渐变浅,d点溶液为无色
C. d点溶液钠元素质量分数大于b点溶液钠元素质量分数
D. ac段溶液升温明显高于cd段,说明该反应放出热量
随堂练习
C
3. 为了证明中和反应已经发生,小文同学做了如图所示的四个实验,不能达到实验目的的是( )
A. 甲实验中,溶液仍为无色
B. 乙实验中,溶液由无色变为红色
C. 丙实验中,溶液由红色变为无色
D. 丁实验中,溶液由红色变为无色
随堂练习
B
4. 关于化学基本反应类型的说法正确的是( )
A. 分解反应一定有单质生成
B. 化合反应一定是两种物质生成一种新物质
C. 置换反应一定有元素的化合价发生改变
D. 两种化合物反应生成另外两种化合物的反应一定是复分解反应
随堂练习
C
5. 中和反应在生产、生活中应用广泛。下列应用的主要原理不涉及中和反应的是( )
A. 生石灰用于加热即热食品
B. 氢氧化铝用于治疗胃酸过多
C. 熟石灰用于改良酸性土壤
D. 硫酸处理印染厂的含碱废水
随堂练习
A
谢谢观看
