江苏省高邮市送桥中学苏教版化学选修五 课件 专题4 第三单元 羧酸的性质和应用羧酸的性质和应用(共15张PPT)
文档属性
| 名称 | 江苏省高邮市送桥中学苏教版化学选修五 课件 专题4 第三单元 羧酸的性质和应用羧酸的性质和应用(共15张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 343.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-05-26 00:00:00 | ||
图片预览



文档简介
课件15张PPT。专题4 第三单元
——羧酸的性质和应用 复习:写出下列化学反应方程式乙醛与银氨溶液的反应:
乙醛与新制氢氧化铜的反应:
乙醛与氧气在催化剂作用下的反应: CH3CHO + 2Cu(OH)2 +NaOH
2CH3COONa +Cu2O↓+ 3H2O
一、羧酸1、定义:由烃基与羧基相连构成的有机化合物。2、分类: 下列属于脂肪酸的是( )
属于芳香酸的是( )
属于一元酸的是( )
属于二元或多元酸的是 ( )
A、B、C、D、E中属于饱和酸的是 ( )
属于不饱和酸的是 ( )
B、CH3COOHA、CH2=CHCOOHC、C17H35COOH 硬脂酸
D、C17H33COOH 油酸
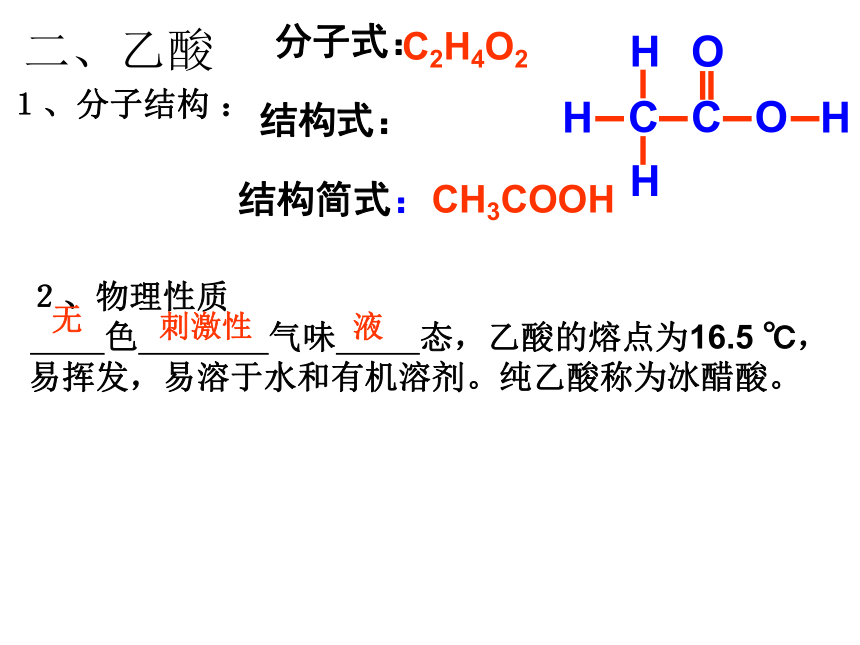
E、C15H31COOH软脂酸F、C6H5COOHG、HOOC-COOHA、B、C、D、E、H、G、B、C、EF、A、D、H、GA、B、C、D、E、F、二、乙酸1、分子结构 :
分子式:C2H4O2CH3COOH结构简式:结构式:2、物理性质
色 气味 态,乙酸的熔点为16.5 ℃,易挥发,易溶于水和有机溶剂。纯乙酸称为冰醋酸。
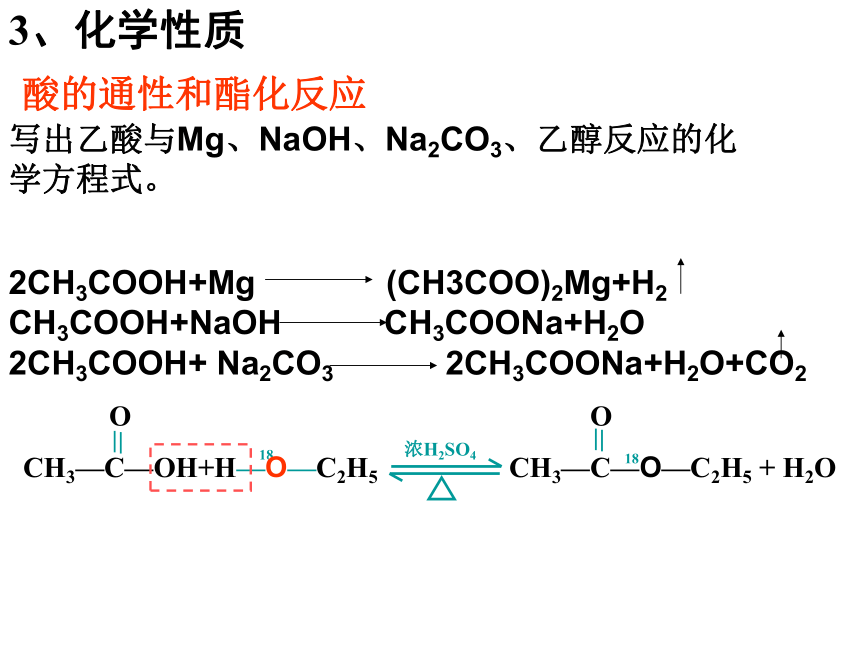
无刺激性液3、化学性质 酸的通性和酯化反应2CH3COOH+Mg (CH3COO)2Mg+H2
CH3COOH+NaOH CH3COONa+H2O
2CH3COOH+ Na2CO3 2CH3COONa+H2O+CO2 写出乙酸与Mg、NaOH、Na2CO3、乙醇反应的化学方程式。
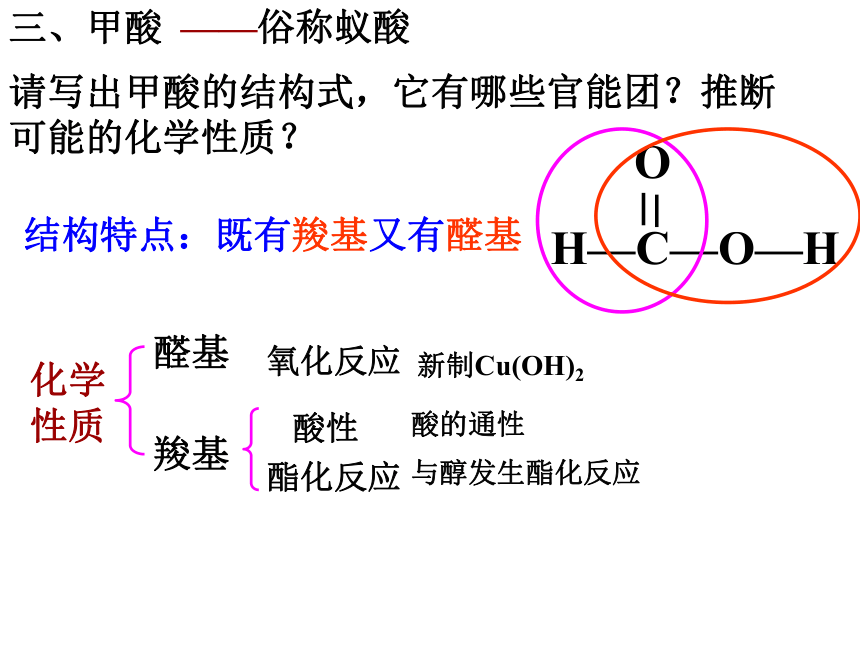
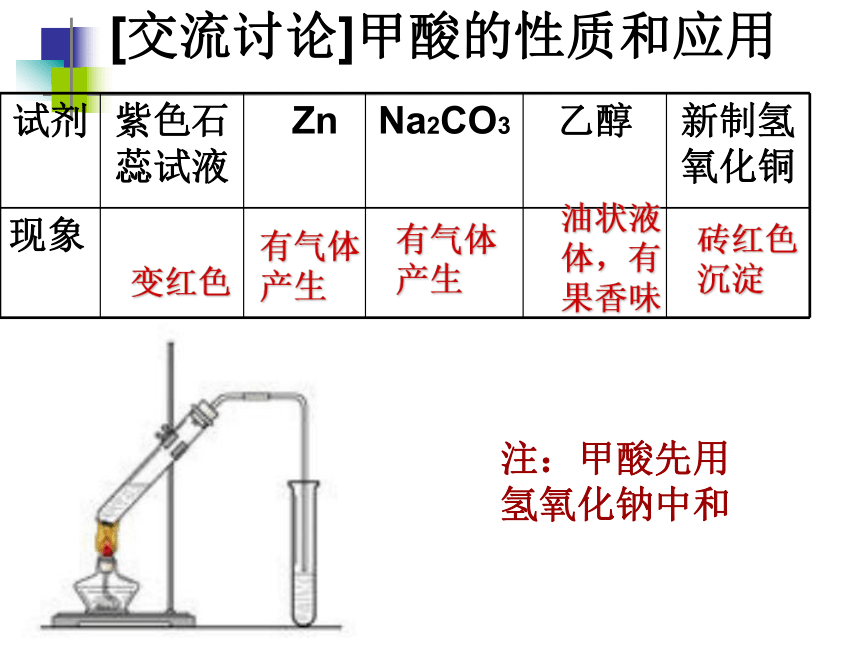
请写出甲酸的结构式,它有哪些官能团?推断可能的化学性质?三、甲酸——俗称蚁酸化学性质醛基羧基氧化反应酯化反应新制Cu(OH)2酸性酸的通性与醇发生酯化反应结构特点:既有羧基又有醛基[交流讨论]甲酸的性质和应用变红色有气体产生油状液体,有果香味有气体产生砖红色
沉淀注:甲酸先用氢氧化钠中和思考:写出甲酸与乙醇反应的化学方程式。结论1:有机物的化学性质由 决定;
官能团结论2:如果一个物质有多个官能团,它的性质由这些官能团 决定
共同
练习1:1mol有机物 最多消耗下列物质多少mol1) Na 2)NaOH 3)NaHCO3 4)Na2CO3
提示:1) 酸性–COOH>H2CO3> >HCO3-
2) 2CH3COOH+ Na2CO3
2CH3COONa+H2O+CO2
练习.可以把乙醇、乙酸、乙醛溶液区别开的一种试剂是 ( ) A.银氨溶液 B.新制Cu(OH)2悬浊液 D.酸性KMn04溶液 D.稀溴水练习2:HOOC-COOH乙二酸与下列物质反应,请写出对应的反应方程式C2H5OH(1:1)反应
C2H5OH(1:2)反应
HOCH2CH2OH (1:1)反应生成链状化合物
HOCH2CH2OH生成(1:1)反应六元环状化合物
HOCH2CH2OH生成高分子化合物
【知识回顾】1、加药品顺序:2、加碎瓷片3、导管通到饱和Na2CO3溶液的液面上方——防暴沸——防倒吸乙醇→浓硫酸→甲酸4、浓H2SO4的作用?5、为何用饱和的Na2CO3溶液吸收甲酸乙酯?①甲酸乙酯在无机盐溶液中溶解度减小,容易分层析出②吸收甲酸,溶解乙醇,便于闻到甲酸乙酯的香味催化剂、吸水剂【知识要点】一、羧酸二、乙酸
1、酸的通性
2、酯化反应三、甲酸1、羧基的性质
2、醛基的性质1.由于乙酸乙酯沸点比乙酸、乙醇低,因此从反应物中不断蒸出乙酸乙酯,可提高其产率;
2.使用过量的乙醇,可提高乙酸转化为乙酸乙酯产率。
3.使用浓H2SO4作吸水剂,提高乙醇、乙酸的转化率。 乙酸与乙醇的酯化反应是可逆的,实验中,如果要提高乙酸乙酯的产率,你认为应当采取哪些措施?阅读 P83 信息提示根据化学平衡原理,提高乙酸乙醋产率措施有: 在可逆反应中,若改变化学平衡的条件,平衡会向削弱这种改变的方向移动。若此时中和掉H+离子,则H+浓度降低,平衡要削弱这种改变,所以,平衡会向右移动,即继续电离出H+。拓展视野乳酸 分子中既有羟基,又有羧基, 在不同的条件下反应,思考可能生成的产物(1)n(2)+
乙醛与新制氢氧化铜的反应:
乙醛与氧气在催化剂作用下的反应: CH3CHO + 2Cu(OH)2 +NaOH
2CH3COONa +Cu2O↓+ 3H2O
一、羧酸1、定义:由烃基与羧基相连构成的有机化合物。2、分类: 下列属于脂肪酸的是( )
属于芳香酸的是( )
属于一元酸的是( )
属于二元或多元酸的是 ( )
A、B、C、D、E中属于饱和酸的是 ( )
属于不饱和酸的是 ( )
B、CH3COOHA、CH2=CHCOOHC、C17H35COOH 硬脂酸
D、C17H33COOH 油酸
E、C15H31COOH软脂酸F、C6H5COOHG、HOOC-COOHA、B、C、D、E、H、G、B、C、EF、A、D、H、GA、B、C、D、E、F、二、乙酸1、分子结构 :
分子式:C2H4O2CH3COOH结构简式:结构式:2、物理性质
色 气味 态,乙酸的熔点为16.5 ℃,易挥发,易溶于水和有机溶剂。纯乙酸称为冰醋酸。
无刺激性液3、化学性质 酸的通性和酯化反应2CH3COOH+Mg (CH3COO)2Mg+H2
CH3COOH+NaOH CH3COONa+H2O
2CH3COOH+ Na2CO3 2CH3COONa+H2O+CO2 写出乙酸与Mg、NaOH、Na2CO3、乙醇反应的化学方程式。
请写出甲酸的结构式,它有哪些官能团?推断可能的化学性质?三、甲酸——俗称蚁酸化学性质醛基羧基氧化反应酯化反应新制Cu(OH)2酸性酸的通性与醇发生酯化反应结构特点:既有羧基又有醛基[交流讨论]甲酸的性质和应用变红色有气体产生油状液体,有果香味有气体产生砖红色
沉淀注:甲酸先用氢氧化钠中和思考:写出甲酸与乙醇反应的化学方程式。结论1:有机物的化学性质由 决定;
官能团结论2:如果一个物质有多个官能团,它的性质由这些官能团 决定
共同
练习1:1mol有机物 最多消耗下列物质多少mol1) Na 2)NaOH 3)NaHCO3 4)Na2CO3
提示:1) 酸性–COOH>H2CO3> >HCO3-
2) 2CH3COOH+ Na2CO3
2CH3COONa+H2O+CO2
练习.可以把乙醇、乙酸、乙醛溶液区别开的一种试剂是 ( ) A.银氨溶液 B.新制Cu(OH)2悬浊液 D.酸性KMn04溶液 D.稀溴水练习2:HOOC-COOH乙二酸与下列物质反应,请写出对应的反应方程式C2H5OH(1:1)反应
C2H5OH(1:2)反应
HOCH2CH2OH (1:1)反应生成链状化合物
HOCH2CH2OH生成(1:1)反应六元环状化合物
HOCH2CH2OH生成高分子化合物
【知识回顾】1、加药品顺序:2、加碎瓷片3、导管通到饱和Na2CO3溶液的液面上方——防暴沸——防倒吸乙醇→浓硫酸→甲酸4、浓H2SO4的作用?5、为何用饱和的Na2CO3溶液吸收甲酸乙酯?①甲酸乙酯在无机盐溶液中溶解度减小,容易分层析出②吸收甲酸,溶解乙醇,便于闻到甲酸乙酯的香味催化剂、吸水剂【知识要点】一、羧酸二、乙酸
1、酸的通性
2、酯化反应三、甲酸1、羧基的性质
2、醛基的性质1.由于乙酸乙酯沸点比乙酸、乙醇低,因此从反应物中不断蒸出乙酸乙酯,可提高其产率;
2.使用过量的乙醇,可提高乙酸转化为乙酸乙酯产率。
3.使用浓H2SO4作吸水剂,提高乙醇、乙酸的转化率。 乙酸与乙醇的酯化反应是可逆的,实验中,如果要提高乙酸乙酯的产率,你认为应当采取哪些措施?阅读 P83 信息提示根据化学平衡原理,提高乙酸乙醋产率措施有: 在可逆反应中,若改变化学平衡的条件,平衡会向削弱这种改变的方向移动。若此时中和掉H+离子,则H+浓度降低,平衡要削弱这种改变,所以,平衡会向右移动,即继续电离出H+。拓展视野乳酸 分子中既有羟基,又有羧基, 在不同的条件下反应,思考可能生成的产物(1)n(2)+
