1.4物质性质的探究---2024-2025学年2024科粤版化学九年级上册教学同步课件
文档属性
| 名称 | 1.4物质性质的探究---2024-2025学年2024科粤版化学九年级上册教学同步课件 |

|
|
| 格式 | pptx | ||
| 文件大小 | 3.7MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 科粤版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-15 00:00:00 | ||
图片预览











文档简介
(共45张PPT)
1.4物质性质的探究
第一单元 大家都来学化学
科粤2024版化学九年级上册【精做课件】
授课教师:********
班 级:********
时 间:********
趣味导入(5 分钟)
播放一段古代青铜器制作和使用的视频,提问:“铜作为一种重要的金属,在古代就被广泛应用。大家知道铜具有哪些性质,使其能被制成各种精美的器具吗?” 引发学生的思考和讨论。
通过展示生活中常见的铜制品,如电线、铜锅等,引导学生思考这些用途背后铜所具有的性质,从而引出本节课的主题 —— 物质性质的探究。
(二)知识讲解:科学探究的步骤(8 分钟)
结合教材内容,利用 PPT 展示科学探究的一般步骤:提出问题、作出假设、制定计划、进行实验、收集证据、解释与结论、反思与评价。
通过简单的案例,如 “探究铁生锈的条件”,对每个步骤进行详细讲解,让学生初步理解科学探究的流程和方法。
(三)实验探究:铜的性质(20 分钟)
提出问题:展示铜片,引导学生观察铜片的外观,提出关于铜性质的问题,如 “铜在加热条件下会发生什么变化?”“铜与稀盐酸会发生反应吗?”“铜与硝酸银溶液能反应吗?”
作出假设:组织学生根据已有知识和生活经验,对提出的问题作出假设。例如,假设铜在加热时会与氧气反应,表面可能会变黑;假设铜不与稀盐酸反应;假设铜能将硝酸银溶液中的银置换出来。
制定计划:将学生分成小组,讨论并设计实验方案来验证假设。教师巡视各小组,给予指导和建议,确保实验方案的合理性和安全性。
进行实验:学生按照设计好的实验方案进行实验操作,教师在实验室巡回指导,提醒学生注意实验安全,规范使用实验仪器,仔细观察并记录实验现象。
实验 1:用砂纸打磨铜片,用坩埚钳夹持铜片,放在酒精灯火焰上加热,观察铜片表面的变化。
实验 2:将打磨后的铜片放入试管中,加入适量稀盐酸,观察试管内的现象。
实验 3:将打磨后的铜片放入盛有硝酸银溶液的试管中,观察铜片表面及溶液颜色的变化。
收集证据:学生如实记录实验现象,如实验 1 中铜片表面变黑;实验 2 中铜片表面无气泡产生,溶液颜色不变;实验 3 中铜片表面有银白色物质析出,溶液由无色变为蓝色。
解释与结论:组织学生根据实验现象进行分析和讨论,得出结论。如实验 1 表明铜在加热条件下能与氧气反应生成氧化铜;实验 2 说明铜的活动性比氢弱,不能与稀盐酸发生置换反应;实验 3 证明铜的活动性比银强,能将硝酸银溶液中的银置换出来。
(四)物质的性质与用途的关系(7 分钟)
引导学生回顾铜的性质探究实验,思考铜的性质与在生活中用途的关系。例如,铜具有良好的导电性,因此可用于制作电线;铜具有较好的导热性,所以可用来制造铜锅;铜的化学性质相对稳定,且具有一定的耐腐蚀性,适合制作装饰品。
展示其他常见物质的用途,如氧气用于医疗急救、氮气用于食品保鲜等,让学生分析这些物质的用途分别利用了它们的哪些性质,加深对物质性质与用途关系的理解。
(五)课堂小结(5 分钟)
请学生回顾本节课的主要内容,包括科学探究的步骤、铜的性质以及物质性质与用途的关系。
教师进行总结和补充,强调科学探究在化学学习中的重要性,鼓励学生在今后的学习和生活中,运用科学探究的方法去探索更多物质的奥秘。
(六)课堂练习(5 分钟)
展示几道与本节课内容相关的练习题,如根据给定的实验现象分析物质的性质、设计探究某种物质性质的实验方案等。
让学生独立完成练习,教师进行点评和讲解,及时反馈学生的学习情况。
六、板书设计
1.4 物质性质的探究
科学探究的步骤
提出问题
根据实验现象进行分析和讨论,得出结论。如实验 1 表明铜在加热条件下能与氧气反应生成氧化铜;实验 2 说明铜的活动性比氢弱,不能与稀盐酸发生置换反应;实验 3 证明铜的活动性比银强,能将硝酸银溶液中的银置换出来。
(四)物质的性质与用途的关系(7 分钟)
引导学生回顾铜的性质探究实验,思考铜的性质与在生活中用途的关系。例如,铜具有良好的导电性,因此可用于制作电线;铜具有较好的导热性,所以可用来制造铜锅;铜的化学性质相对稳定,且具有一定的耐腐蚀性,适合制作装饰品。
展示其他常见物质的用途,如氧气用于医疗急救、氮气用于食品保鲜等,让学生分析这些物质的用途分别利用了它们的哪些性质,加深对物质性质与用途关系的理解。
(五)课堂小结(5 分钟)
请学生回顾本节课的主要内容,包括科学探究的步骤、铜的性质以及物质性质与用途的关系。
教师进行总结和补充,强调科学探究在化学学习中的重要性,鼓励学生在今后的学习和生活中,运用科学探究的方法去探索更多物质的奥秘。
(六)课堂练习(5 分钟)
展示几道与本节课内容相关的练习题,如根据给定的实验现象分析物质的性质、设计探究某种物质性质的实验方案等。
让学生独立完成练习,教师进行点评和讲解,及时反馈学生的学习情况。
六、板书设计
1.4 物质性质的探究
科学探究的步骤
提出问题
根据实验现象进行分析和讨论,得出结论。如实验 1 表明铜在加热条件下能与氧气反应生成氧化铜;实验 2 说明铜的活动性比氢弱,不能与稀盐酸发生置换反应;实验 3 证明铜的活动性比银强,能将硝酸银溶液中的银置换出来。
(四)物质的性质与用途的关系(7 分钟)
引导学生回顾铜的性质探究实验,思考铜的性质与在生活中用途的关系。例如,铜具有良好的导电性,因此可用于制作电线;铜具有较好的导热性,所以可用来制造铜锅;铜的化学性质相对稳定,且具有一定的耐腐蚀性,适合制作装饰品。
展示其他常见物质的用途,如氧气用于医疗急救、氮气用于食品保鲜等,让学生分析这些物质的用途分别利用了它们的哪些性质,加深对物质性质与用途关系的理解。
(五)课堂小结(5 分钟)
请学生回顾本节课的主要内容,包括科学探究的步骤、铜的性质以及物质性质与用途的关系。
教师进行总结和补充,强调科学探究在化学学习中的重要性,鼓励学生在今后的学习和生活中,运用科学探究的方法去探索更多物质的奥秘。
(六)课堂练习(5 分钟)
展示几道与本节课内容相关的练习题,如根据给定的实验现象分析物质的性质、设计探究某种物质性质的实验方案等。
让学生独立完成练习,教师进行点评和讲解,及时反馈学生的学习情况。
六、板书设计
1.4 物质性质的探究
科学探究的步骤
提出问题
作出假设
制定计划
进行实验
收集证据
解释与结论
反思与评价
铜的性质探究
实验 1:加热铜片 —— 表面变黑,铜能与氧气反应。
实验 2:铜与稀盐酸 —— 不反应。
实验 3:铜与硝酸银溶液 —— 铜表面有银白色物质析出,溶液变蓝,铜能置换出银。
物质的性质与用途的关系:性质决定用途,用途反映性质。
七、教学反思
通过本节课的教学,学生对科学探究的步骤有了较为清晰的认识,并能通过实验探究铜的性质,初步理解物质性质与用途的关系。但在教学过程中,部分学生在设计实验方案时存在一定困难,对实验现象的分析和总结不够准确。在今后的教学中,应加强对学生实验设计和分析能力的培养,提供更多的实践机会,让学生在探究中不断提高科学素养。
5
课堂检测
4
新知讲解
6
变式训练
7
考试考法
8
小结梳理
学习目录
1
复习引入
2
新知讲解
3
典例讲解
物理性质 化学性质
概念 物质不需要发生化学变化就能表现出来的性质 物质在化学变化中才能表现
出来的性质
性质 确定 直接观察或用物理方法测定 通过化学实验去观察和确定
性质 内容 颜色、气味、硬度、熔点、沸点、挥发性、溶解性、导电性、导热性、吸附性和延展性等 可燃性、助燃性、稳定性、
还原性、氧化性、酸性、碱
性、毒性和腐蚀性等
区别 是否需要通过化学变化表现出来 典例1 下列物质的性质属于化学性质的是( )
D
A.铁呈固态 B.铜呈紫红色
C.蔗糖易溶于水 D.碳酸易分解成二氧化碳和水
[解析] 铁呈固态、铜的颜色及蔗糖的溶解性均不需要通过化学变
化就能表现出来,为物理性质;碳酸易分解成二氧化碳和水,属于
通过化学变化表现出来的化学性质。
物质的性质 物质的变化
区别 性质是物质本身固有的属性,可以直接 用感官感知或借助简单仪器测出,或通 过变化表现出来,描述物质的性质常用 “能”“会”“具有”“可以”等字眼 变化是一个动态
的过程,常用动
词描述
物质的性质 物质的变化
举例 汽油能燃烧——化学性质; 汽油易挥发——物理性质 汽油燃烧——化
学变化;
汽油挥发——物
理变化
联系 典例2 某同学对一瓶酒精进行了认真观察和实验,在查阅资料后,
总结出了下列材料:①无色、透明;②具有特殊气味的液体;③易
挥发;④能与水以任意比例互溶;⑤能溶解碘等物质;⑥易燃烧;
⑦点燃酒精灯时,酒精在灯芯上汽化;⑧酒精燃烧。根据上述文字
可归纳出:
(1)酒精的物理性质有____________(填序号,下同);
①②③④⑤
[解析] 物质的物理性质常表现为颜色、状态、气味、密度、硬度、
熔点、沸点、导电性、导热性、溶解性和挥发性等。酒精的物理性
质有无色、透明,具有特殊气味的液体,易挥发,能与水以任意比
例互溶,能溶解碘等物质。
(2)化学性质有____;
⑥
[解析] (2)易燃烧需要通过化学变化表现出来,为化学性质。
(3)物理变化有____;
⑦
(3)点燃酒精灯时,酒精在灯芯上汽化,由液态变为气态,没
有产生新物质,为物理变化。
(4)化学变化有____。
⑧
(4)酒精燃烧的过程中有新物质生成,发生了化学变化。
1.铜受热变黑原因的探究
探究步骤 内容
提出问题 将一小段光亮的铜片在酒精灯火焰上加热(加热铜片
时使用坩埚钳夹持,注意防止烫伤)片刻,铜片由紫
红色变为黑色。为什么?
________________
探究步骤 内容 形成假设 假设1:铜片变黑,是因为火焰中的烟灰附着在铜片上 假设2:铜片变黑是因为它在空气中发生了化学反应
预测1:若是烟灰,则应很容易抹去 预测2:加热铜片 时,若火焰没有与铜片接触,则金属将不会变黑 预测:若将铜片放在真空或隔绝空气的条件下加热,铜片的颜色将不变
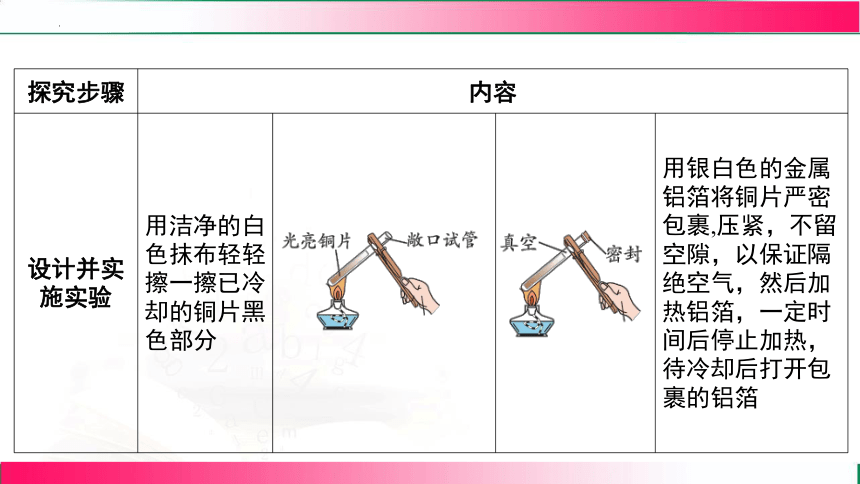
探究步骤 内容 设计并实 施实验 用洁净的白 色抹布轻轻 擦一擦已冷 却的铜片黑 色部分 _____________________________ _______________________ 用银白色的金属铝箔将铜片严密包裹,压紧,不留空隙,以保证隔绝空气,然后加热铝箔,一定时间后停止加热,待冷却后打开包裹的铝箔
探究步骤 内容 获取证 据、分 析解释 现象 黑色部分不 能被擦掉 铜片表面 变黑 铜片表面不变色
判断 假设1错误 假设2正确
解释 铜片在空气中用酒精灯加热后变黑,黑色物质不是烟灰 铜片在隔绝空气的条件下加热后不变 色;铜片在敞口的试管中加热后变黑,是因为铜片在空气中发生了化学 反应,生成黑色的新物质 形成结论 铜片在加热条件下,在空气中发生了化学反应, 生成黑色物质 探究步骤 内容
反思 评价 生成物的 鉴别 ________________________________________________________________________________
现象 黑色物质逐渐消失,溶液由无色变为蓝色
探究步骤 内容
反思 评价 结论 反应生成硫酸铜,原黑色物质为氧化铜
反思 评价 铜在空气或氧气中受热生成的黑色物质是氧化铜,
上述“形成结论”正确
表达交流
教材深挖
文字表达式的含义和读法
(1)文字表达式:
(2)读作:铜和氧气在加热的条件下反应生成氧化铜。
信息技术与化学实验
利用手持技术数字化实验探究铜和氧气的反应
在“铜受热变黑原因的探究”实验中,可利用手持技术改进实验。
已知:空气中氧气含量约占总体积的 。
【提出问题】铜片和空气中的什么物质发生了反应?
【实验验证】使用氧气传感器定量测定(如甲图所示)反应过程中
氧气含量的变化。
甲图 实验装置图
乙图 “氧气含量-时间”曲线图
【得出结论】铜受热一段时间后,装置中的氧气含量不断减少
(如乙图所示),证明铜与氧气发生了反应。
2.科学探究的一般过程
以上各环节中,化学实验是中心环节,假设需要用实验去证实,结
论来自实验事实。对于初学者,探究步骤不要求上述那么完整。
典例3 科学探究是学习化学的重要方式。悦悦需要通过查阅资料
了解“为何加热时试管内液体体积不能超过试管容积的 ”,这
属于科学探究中的( )
B
A.提出问题 B.获取证据 C.形成假设 D.形成结论
3.探究人体吸入和呼出气体成分含量的差异
【提出问题】我们一生中不断吸入空气和呼出气体,吸入和呼出的
气体成分含量有没有差别呢?
【形成假设】
1.吸入空气中氧气的含量大于呼出气体中氧气的含量。
2.呼出气体中二氧化碳的含量大于吸入空气中二氧化碳的含量。
【设计并实施实验】
提示信息:
1.木条燃烧要有氧气参与,氧气含量越多,燃烧越旺。
2.二氧化碳与澄清石灰水作用,使石灰水变浑浊。当参与作用的二
氧化碳含量较多时,浑浊现象出现得较快,且较明显。
实验准备:
1.取两个空集气瓶,用玻璃片将瓶口盖好,作为空气样品;
2.用排水法收集两瓶呼出气体。
知识链接
排水法收集呼出气体
1.集气瓶中装满水(不能留有气泡),盖好
玻璃片(毛面向下)倒扣在水槽里;
2.将导管插入瓶口,通过导管向集气瓶中
慢慢呼气,换气后再慢慢呼气,反复几次;
3.待集气瓶中的水排完(当瓶口有大气泡连续并均匀地冒出时)后,
在水下盖好玻璃片,将集气瓶小心地移出水槽,正放在桌子上。
图示 实验步骤 实验现象与结论
_____________________________________________ 将燃着的木条分 别伸入盛有空 气、呼出气体的 集气瓶中 现象:盛有呼出气体的集
气瓶中,木条很快熄灭;
盛有空气的集气瓶中,木
条正常燃烧
结论:假设1正确
图示 实验步骤 实验现象与结论
_______________________________________ 分别向盛有空气 和呼出气体的集 气瓶中滴加等量 且少量的澄清石 灰水,振荡 现象:盛有呼出气体的集
气瓶中,澄清石灰水变浑
浊;盛有空气的集气瓶中
澄清石灰水无明显变化
结论:假设2正确
【解释与结论】
知识点1 物质的性质
1. [2023·绥化改编]下列选项中,属于物质化学性质的是
( A )
A. 可燃性 B. 密度
C. 溶解性 D. 熔点
A
1
2
3
4
5
6
7
8
9
10
11
12
返回
2. [2024·泰安期末]以下铁的性质中,属于化学性质的是
( B )
A. 纯铁有银白色光泽 B. 铁会生锈
C. 铁可以导电、导热 D. 铁有延展性
1
2
3
4
5
6
7
8
9
10
11
12
【点拨】纯铁有银白色光泽,不需要通过化学变化就
能表现出来,属于物理性质,故A不符合题意;铁会
生锈,需要通过化学变化才能表现出来,属于化学性
质,故B符合题意;铁的导电性、导热性和延展性都
不需要通过化学变化就能表现出来,均属于物理性
质,故C、D不符合题意。
【答案】 B
1
2
3
4
5
6
7
8
9
10
11
12
返回
3. [情境题][2024·泰州期末]多维元素片可用于预防和治疗维
生素和矿物质缺乏所引起的各种疾病,该药品建议避光、
密封储存在干燥处。下列对多维元素片性质的推测中,不
属于化学性质的是( A )
A. 微溶于水 B. 见光易分解
C. 能与氧气反应 D. 受热易分解
A
1
2
3
4
5
6
7
8
9
10
11
12
返回
知识点2 物质的性质与用途
4. [2023·信阳期中]物质的性质决定用途。下列物质的用途体
现物质化学性质的是( B )
A. 金刚石的硬度大——切割玻璃
B. 氢气具有可燃性——用作燃料
C. 铜丝具有导电性——用作导线
D. 武德合金熔点低——用作保险丝
B
1
2
3
4
5
6
7
8
9
10
11
12
返回
5. [2022·成都]下列有关智能手表的性质的描述中,属于物质
的化学性质的是( B )
A. 玻璃透光性好,作表镜
B. 钛合金耐腐蚀,作表框
C. 不锈钢硬度大,作表扣
D. 橡胶弹性良好,作表带
B
【点拨】透光性、硬度、弹性都属于物质的物理性质,耐
腐蚀属于物质的化学性质。
1
2
3
4
5
6
7
8
9
10
11
12
返回
知识点3 科学探究的一般过程
6. [荣德原创]小明同学在探究人体呼出气体的成分时提出:
人体呼出的气体中可能含有二氧化碳和水蒸气。这属于科
学探究过程中的( A )
A. 形成假设 B. 设计并实施实验
C. 获取证据 D. 形成结论
【点拨】根据关键词“可能”判断这一过程属于科学探究环
节中的形成假设。
A
1
2
3
4
5
6
7
8
9
10
11
12
返回
7. 下列记录的加热铜片的实验现象与事实不相符的是
( D )
A. 铜片在空气中加热时,由亮红色变为黑色
B. 加热时铜片变黑主要是因为它与空气中的氧气发生了
化学反应
C. 把铜片装在敞口的试管中加热,铜片变为黑色
D. 把铜片严密包裹在金属铝箔中加热,铜片变为黑色
1
2
3
4
5
6
7
8
9
10
11
12
【点拨】铜片在空气中加热变黑,是因为铜在加热的条件
下与空气中的氧气反应,生成了氧化铜。铜片在隔绝空气
的条件下加热,铜片不会变黑。
【答案】 D
1
2
3
4
5
6
7
8
9
10
11
12
返回
纠易错 不能正确区分物质的变化与性质
8. 下列关于性质或变化的说法正确的是( A )
A 铁在潮湿环境中易生锈 化学性质
B 酒精挥发 化学变化
C 氧气用于急救病人 物理性质
D 木材燃烧 物理变化
1
2
3
4
5
6
7
8
9
10
11
12
【点拨】铁在潮湿环境中易生锈,需通过铁生锈这一化学
变化表现出来,属于化学性质,A正确;酒精挥发,是酒
精由液态变为气态,没有新物质生成,属于物理变化,B
错误;氧气用于急救病人,是氧气的用途,C错误;木材
燃烧有新物质生成,属于化学变化,D错误。
1
2
3
4
5
6
7
8
9
10
11
12
【点易错】区分物质的变化与性质时应注意:物质的变化
是一个过程,而性质是物质固有的属性,可根据叙述中的
关键字进行判断,物质性质的叙述中一般有
“能”“易”“会”等关键字。
【答案】 A
1
2
3
4
5
6
7
8
9
10
11
12
返回
9. [立德树人 文化自信][2024·陕西模拟]下列俗语与物质的化
学性质无关的是( B )
A. 真金不怕火炼 B. 玉不琢不成器
C. 纸里包不住火 D. 百炼方能成钢
【点拨】玉不琢不成器说的是对玉石进行雕刻琢磨,没有
新物质生成,利用了玉石的物理性质, B符合题意。
B
1
2
3
4
5
6
7
8
9
10
11
12
返回
10. [2024·西安模拟]实验小组探究人体吸入的空气和呼出的
气体的差别。如表实验对应的目的或结论不正确的是
( C )
选项 实验图示 目的或结论
A 收集呼出的气体
1
2
3
4
5
6
7
8
9
10
11
12
选项 实验图示 目的或结论
B 呼出气体中的氧气含量比空气中的低
C
呼出气体中只含有二氧化碳
D 呼出气体中的水蒸气含量比空气中的多
1
2
3
4
5
6
7
8
9
10
11
12
【点拨】可用排水法收集呼出的气体,A正确;氧气能支持燃烧,氧气含量越多,燃烧越剧烈,图中实验,伸入呼出气体中的小木条先熄灭,可得出呼出气体中的氧气含量比空气中的低,B正确;二氧化碳能使澄清石灰水变浑浊,图中实验,滴入呼出气体中的澄清石灰水变浑浊,可得出呼出气体中含有二氧化碳,但不能得出呼出气体中只含有二氧化碳,C错误;水蒸气遇冷凝结成水滴,对着哈气的干燥玻璃片上出现无色液滴,可得出呼出气体中的水蒸气含量比空气中的多,D正确。
【答案】 C
1
2
3
4
5
6
7
8
9
10
11
12
返回
课堂小结
谢谢观看!
1.4物质性质的探究
第一单元 大家都来学化学
科粤2024版化学九年级上册【精做课件】
授课教师:********
班 级:********
时 间:********
趣味导入(5 分钟)
播放一段古代青铜器制作和使用的视频,提问:“铜作为一种重要的金属,在古代就被广泛应用。大家知道铜具有哪些性质,使其能被制成各种精美的器具吗?” 引发学生的思考和讨论。
通过展示生活中常见的铜制品,如电线、铜锅等,引导学生思考这些用途背后铜所具有的性质,从而引出本节课的主题 —— 物质性质的探究。
(二)知识讲解:科学探究的步骤(8 分钟)
结合教材内容,利用 PPT 展示科学探究的一般步骤:提出问题、作出假设、制定计划、进行实验、收集证据、解释与结论、反思与评价。
通过简单的案例,如 “探究铁生锈的条件”,对每个步骤进行详细讲解,让学生初步理解科学探究的流程和方法。
(三)实验探究:铜的性质(20 分钟)
提出问题:展示铜片,引导学生观察铜片的外观,提出关于铜性质的问题,如 “铜在加热条件下会发生什么变化?”“铜与稀盐酸会发生反应吗?”“铜与硝酸银溶液能反应吗?”
作出假设:组织学生根据已有知识和生活经验,对提出的问题作出假设。例如,假设铜在加热时会与氧气反应,表面可能会变黑;假设铜不与稀盐酸反应;假设铜能将硝酸银溶液中的银置换出来。
制定计划:将学生分成小组,讨论并设计实验方案来验证假设。教师巡视各小组,给予指导和建议,确保实验方案的合理性和安全性。
进行实验:学生按照设计好的实验方案进行实验操作,教师在实验室巡回指导,提醒学生注意实验安全,规范使用实验仪器,仔细观察并记录实验现象。
实验 1:用砂纸打磨铜片,用坩埚钳夹持铜片,放在酒精灯火焰上加热,观察铜片表面的变化。
实验 2:将打磨后的铜片放入试管中,加入适量稀盐酸,观察试管内的现象。
实验 3:将打磨后的铜片放入盛有硝酸银溶液的试管中,观察铜片表面及溶液颜色的变化。
收集证据:学生如实记录实验现象,如实验 1 中铜片表面变黑;实验 2 中铜片表面无气泡产生,溶液颜色不变;实验 3 中铜片表面有银白色物质析出,溶液由无色变为蓝色。
解释与结论:组织学生根据实验现象进行分析和讨论,得出结论。如实验 1 表明铜在加热条件下能与氧气反应生成氧化铜;实验 2 说明铜的活动性比氢弱,不能与稀盐酸发生置换反应;实验 3 证明铜的活动性比银强,能将硝酸银溶液中的银置换出来。
(四)物质的性质与用途的关系(7 分钟)
引导学生回顾铜的性质探究实验,思考铜的性质与在生活中用途的关系。例如,铜具有良好的导电性,因此可用于制作电线;铜具有较好的导热性,所以可用来制造铜锅;铜的化学性质相对稳定,且具有一定的耐腐蚀性,适合制作装饰品。
展示其他常见物质的用途,如氧气用于医疗急救、氮气用于食品保鲜等,让学生分析这些物质的用途分别利用了它们的哪些性质,加深对物质性质与用途关系的理解。
(五)课堂小结(5 分钟)
请学生回顾本节课的主要内容,包括科学探究的步骤、铜的性质以及物质性质与用途的关系。
教师进行总结和补充,强调科学探究在化学学习中的重要性,鼓励学生在今后的学习和生活中,运用科学探究的方法去探索更多物质的奥秘。
(六)课堂练习(5 分钟)
展示几道与本节课内容相关的练习题,如根据给定的实验现象分析物质的性质、设计探究某种物质性质的实验方案等。
让学生独立完成练习,教师进行点评和讲解,及时反馈学生的学习情况。
六、板书设计
1.4 物质性质的探究
科学探究的步骤
提出问题
根据实验现象进行分析和讨论,得出结论。如实验 1 表明铜在加热条件下能与氧气反应生成氧化铜;实验 2 说明铜的活动性比氢弱,不能与稀盐酸发生置换反应;实验 3 证明铜的活动性比银强,能将硝酸银溶液中的银置换出来。
(四)物质的性质与用途的关系(7 分钟)
引导学生回顾铜的性质探究实验,思考铜的性质与在生活中用途的关系。例如,铜具有良好的导电性,因此可用于制作电线;铜具有较好的导热性,所以可用来制造铜锅;铜的化学性质相对稳定,且具有一定的耐腐蚀性,适合制作装饰品。
展示其他常见物质的用途,如氧气用于医疗急救、氮气用于食品保鲜等,让学生分析这些物质的用途分别利用了它们的哪些性质,加深对物质性质与用途关系的理解。
(五)课堂小结(5 分钟)
请学生回顾本节课的主要内容,包括科学探究的步骤、铜的性质以及物质性质与用途的关系。
教师进行总结和补充,强调科学探究在化学学习中的重要性,鼓励学生在今后的学习和生活中,运用科学探究的方法去探索更多物质的奥秘。
(六)课堂练习(5 分钟)
展示几道与本节课内容相关的练习题,如根据给定的实验现象分析物质的性质、设计探究某种物质性质的实验方案等。
让学生独立完成练习,教师进行点评和讲解,及时反馈学生的学习情况。
六、板书设计
1.4 物质性质的探究
科学探究的步骤
提出问题
根据实验现象进行分析和讨论,得出结论。如实验 1 表明铜在加热条件下能与氧气反应生成氧化铜;实验 2 说明铜的活动性比氢弱,不能与稀盐酸发生置换反应;实验 3 证明铜的活动性比银强,能将硝酸银溶液中的银置换出来。
(四)物质的性质与用途的关系(7 分钟)
引导学生回顾铜的性质探究实验,思考铜的性质与在生活中用途的关系。例如,铜具有良好的导电性,因此可用于制作电线;铜具有较好的导热性,所以可用来制造铜锅;铜的化学性质相对稳定,且具有一定的耐腐蚀性,适合制作装饰品。
展示其他常见物质的用途,如氧气用于医疗急救、氮气用于食品保鲜等,让学生分析这些物质的用途分别利用了它们的哪些性质,加深对物质性质与用途关系的理解。
(五)课堂小结(5 分钟)
请学生回顾本节课的主要内容,包括科学探究的步骤、铜的性质以及物质性质与用途的关系。
教师进行总结和补充,强调科学探究在化学学习中的重要性,鼓励学生在今后的学习和生活中,运用科学探究的方法去探索更多物质的奥秘。
(六)课堂练习(5 分钟)
展示几道与本节课内容相关的练习题,如根据给定的实验现象分析物质的性质、设计探究某种物质性质的实验方案等。
让学生独立完成练习,教师进行点评和讲解,及时反馈学生的学习情况。
六、板书设计
1.4 物质性质的探究
科学探究的步骤
提出问题
作出假设
制定计划
进行实验
收集证据
解释与结论
反思与评价
铜的性质探究
实验 1:加热铜片 —— 表面变黑,铜能与氧气反应。
实验 2:铜与稀盐酸 —— 不反应。
实验 3:铜与硝酸银溶液 —— 铜表面有银白色物质析出,溶液变蓝,铜能置换出银。
物质的性质与用途的关系:性质决定用途,用途反映性质。
七、教学反思
通过本节课的教学,学生对科学探究的步骤有了较为清晰的认识,并能通过实验探究铜的性质,初步理解物质性质与用途的关系。但在教学过程中,部分学生在设计实验方案时存在一定困难,对实验现象的分析和总结不够准确。在今后的教学中,应加强对学生实验设计和分析能力的培养,提供更多的实践机会,让学生在探究中不断提高科学素养。
5
课堂检测
4
新知讲解
6
变式训练
7
考试考法
8
小结梳理
学习目录
1
复习引入
2
新知讲解
3
典例讲解
物理性质 化学性质
概念 物质不需要发生化学变化就能表现出来的性质 物质在化学变化中才能表现
出来的性质
性质 确定 直接观察或用物理方法测定 通过化学实验去观察和确定
性质 内容 颜色、气味、硬度、熔点、沸点、挥发性、溶解性、导电性、导热性、吸附性和延展性等 可燃性、助燃性、稳定性、
还原性、氧化性、酸性、碱
性、毒性和腐蚀性等
区别 是否需要通过化学变化表现出来 典例1 下列物质的性质属于化学性质的是( )
D
A.铁呈固态 B.铜呈紫红色
C.蔗糖易溶于水 D.碳酸易分解成二氧化碳和水
[解析] 铁呈固态、铜的颜色及蔗糖的溶解性均不需要通过化学变
化就能表现出来,为物理性质;碳酸易分解成二氧化碳和水,属于
通过化学变化表现出来的化学性质。
物质的性质 物质的变化
区别 性质是物质本身固有的属性,可以直接 用感官感知或借助简单仪器测出,或通 过变化表现出来,描述物质的性质常用 “能”“会”“具有”“可以”等字眼 变化是一个动态
的过程,常用动
词描述
物质的性质 物质的变化
举例 汽油能燃烧——化学性质; 汽油易挥发——物理性质 汽油燃烧——化
学变化;
汽油挥发——物
理变化
联系 典例2 某同学对一瓶酒精进行了认真观察和实验,在查阅资料后,
总结出了下列材料:①无色、透明;②具有特殊气味的液体;③易
挥发;④能与水以任意比例互溶;⑤能溶解碘等物质;⑥易燃烧;
⑦点燃酒精灯时,酒精在灯芯上汽化;⑧酒精燃烧。根据上述文字
可归纳出:
(1)酒精的物理性质有____________(填序号,下同);
①②③④⑤
[解析] 物质的物理性质常表现为颜色、状态、气味、密度、硬度、
熔点、沸点、导电性、导热性、溶解性和挥发性等。酒精的物理性
质有无色、透明,具有特殊气味的液体,易挥发,能与水以任意比
例互溶,能溶解碘等物质。
(2)化学性质有____;
⑥
[解析] (2)易燃烧需要通过化学变化表现出来,为化学性质。
(3)物理变化有____;
⑦
(3)点燃酒精灯时,酒精在灯芯上汽化,由液态变为气态,没
有产生新物质,为物理变化。
(4)化学变化有____。
⑧
(4)酒精燃烧的过程中有新物质生成,发生了化学变化。
1.铜受热变黑原因的探究
探究步骤 内容
提出问题 将一小段光亮的铜片在酒精灯火焰上加热(加热铜片
时使用坩埚钳夹持,注意防止烫伤)片刻,铜片由紫
红色变为黑色。为什么?
________________
探究步骤 内容 形成假设 假设1:铜片变黑,是因为火焰中的烟灰附着在铜片上 假设2:铜片变黑是因为它在空气中发生了化学反应
预测1:若是烟灰,则应很容易抹去 预测2:加热铜片 时,若火焰没有与铜片接触,则金属将不会变黑 预测:若将铜片放在真空或隔绝空气的条件下加热,铜片的颜色将不变
探究步骤 内容 设计并实 施实验 用洁净的白 色抹布轻轻 擦一擦已冷 却的铜片黑 色部分 _____________________________ _______________________ 用银白色的金属铝箔将铜片严密包裹,压紧,不留空隙,以保证隔绝空气,然后加热铝箔,一定时间后停止加热,待冷却后打开包裹的铝箔
探究步骤 内容 获取证 据、分 析解释 现象 黑色部分不 能被擦掉 铜片表面 变黑 铜片表面不变色
判断 假设1错误 假设2正确
解释 铜片在空气中用酒精灯加热后变黑,黑色物质不是烟灰 铜片在隔绝空气的条件下加热后不变 色;铜片在敞口的试管中加热后变黑,是因为铜片在空气中发生了化学 反应,生成黑色的新物质 形成结论 铜片在加热条件下,在空气中发生了化学反应, 生成黑色物质 探究步骤 内容
反思 评价 生成物的 鉴别 ________________________________________________________________________________
现象 黑色物质逐渐消失,溶液由无色变为蓝色
探究步骤 内容
反思 评价 结论 反应生成硫酸铜,原黑色物质为氧化铜
反思 评价 铜在空气或氧气中受热生成的黑色物质是氧化铜,
上述“形成结论”正确
表达交流
教材深挖
文字表达式的含义和读法
(1)文字表达式:
(2)读作:铜和氧气在加热的条件下反应生成氧化铜。
信息技术与化学实验
利用手持技术数字化实验探究铜和氧气的反应
在“铜受热变黑原因的探究”实验中,可利用手持技术改进实验。
已知:空气中氧气含量约占总体积的 。
【提出问题】铜片和空气中的什么物质发生了反应?
【实验验证】使用氧气传感器定量测定(如甲图所示)反应过程中
氧气含量的变化。
甲图 实验装置图
乙图 “氧气含量-时间”曲线图
【得出结论】铜受热一段时间后,装置中的氧气含量不断减少
(如乙图所示),证明铜与氧气发生了反应。
2.科学探究的一般过程
以上各环节中,化学实验是中心环节,假设需要用实验去证实,结
论来自实验事实。对于初学者,探究步骤不要求上述那么完整。
典例3 科学探究是学习化学的重要方式。悦悦需要通过查阅资料
了解“为何加热时试管内液体体积不能超过试管容积的 ”,这
属于科学探究中的( )
B
A.提出问题 B.获取证据 C.形成假设 D.形成结论
3.探究人体吸入和呼出气体成分含量的差异
【提出问题】我们一生中不断吸入空气和呼出气体,吸入和呼出的
气体成分含量有没有差别呢?
【形成假设】
1.吸入空气中氧气的含量大于呼出气体中氧气的含量。
2.呼出气体中二氧化碳的含量大于吸入空气中二氧化碳的含量。
【设计并实施实验】
提示信息:
1.木条燃烧要有氧气参与,氧气含量越多,燃烧越旺。
2.二氧化碳与澄清石灰水作用,使石灰水变浑浊。当参与作用的二
氧化碳含量较多时,浑浊现象出现得较快,且较明显。
实验准备:
1.取两个空集气瓶,用玻璃片将瓶口盖好,作为空气样品;
2.用排水法收集两瓶呼出气体。
知识链接
排水法收集呼出气体
1.集气瓶中装满水(不能留有气泡),盖好
玻璃片(毛面向下)倒扣在水槽里;
2.将导管插入瓶口,通过导管向集气瓶中
慢慢呼气,换气后再慢慢呼气,反复几次;
3.待集气瓶中的水排完(当瓶口有大气泡连续并均匀地冒出时)后,
在水下盖好玻璃片,将集气瓶小心地移出水槽,正放在桌子上。
图示 实验步骤 实验现象与结论
_____________________________________________ 将燃着的木条分 别伸入盛有空 气、呼出气体的 集气瓶中 现象:盛有呼出气体的集
气瓶中,木条很快熄灭;
盛有空气的集气瓶中,木
条正常燃烧
结论:假设1正确
图示 实验步骤 实验现象与结论
_______________________________________ 分别向盛有空气 和呼出气体的集 气瓶中滴加等量 且少量的澄清石 灰水,振荡 现象:盛有呼出气体的集
气瓶中,澄清石灰水变浑
浊;盛有空气的集气瓶中
澄清石灰水无明显变化
结论:假设2正确
【解释与结论】
知识点1 物质的性质
1. [2023·绥化改编]下列选项中,属于物质化学性质的是
( A )
A. 可燃性 B. 密度
C. 溶解性 D. 熔点
A
1
2
3
4
5
6
7
8
9
10
11
12
返回
2. [2024·泰安期末]以下铁的性质中,属于化学性质的是
( B )
A. 纯铁有银白色光泽 B. 铁会生锈
C. 铁可以导电、导热 D. 铁有延展性
1
2
3
4
5
6
7
8
9
10
11
12
【点拨】纯铁有银白色光泽,不需要通过化学变化就
能表现出来,属于物理性质,故A不符合题意;铁会
生锈,需要通过化学变化才能表现出来,属于化学性
质,故B符合题意;铁的导电性、导热性和延展性都
不需要通过化学变化就能表现出来,均属于物理性
质,故C、D不符合题意。
【答案】 B
1
2
3
4
5
6
7
8
9
10
11
12
返回
3. [情境题][2024·泰州期末]多维元素片可用于预防和治疗维
生素和矿物质缺乏所引起的各种疾病,该药品建议避光、
密封储存在干燥处。下列对多维元素片性质的推测中,不
属于化学性质的是( A )
A. 微溶于水 B. 见光易分解
C. 能与氧气反应 D. 受热易分解
A
1
2
3
4
5
6
7
8
9
10
11
12
返回
知识点2 物质的性质与用途
4. [2023·信阳期中]物质的性质决定用途。下列物质的用途体
现物质化学性质的是( B )
A. 金刚石的硬度大——切割玻璃
B. 氢气具有可燃性——用作燃料
C. 铜丝具有导电性——用作导线
D. 武德合金熔点低——用作保险丝
B
1
2
3
4
5
6
7
8
9
10
11
12
返回
5. [2022·成都]下列有关智能手表的性质的描述中,属于物质
的化学性质的是( B )
A. 玻璃透光性好,作表镜
B. 钛合金耐腐蚀,作表框
C. 不锈钢硬度大,作表扣
D. 橡胶弹性良好,作表带
B
【点拨】透光性、硬度、弹性都属于物质的物理性质,耐
腐蚀属于物质的化学性质。
1
2
3
4
5
6
7
8
9
10
11
12
返回
知识点3 科学探究的一般过程
6. [荣德原创]小明同学在探究人体呼出气体的成分时提出:
人体呼出的气体中可能含有二氧化碳和水蒸气。这属于科
学探究过程中的( A )
A. 形成假设 B. 设计并实施实验
C. 获取证据 D. 形成结论
【点拨】根据关键词“可能”判断这一过程属于科学探究环
节中的形成假设。
A
1
2
3
4
5
6
7
8
9
10
11
12
返回
7. 下列记录的加热铜片的实验现象与事实不相符的是
( D )
A. 铜片在空气中加热时,由亮红色变为黑色
B. 加热时铜片变黑主要是因为它与空气中的氧气发生了
化学反应
C. 把铜片装在敞口的试管中加热,铜片变为黑色
D. 把铜片严密包裹在金属铝箔中加热,铜片变为黑色
1
2
3
4
5
6
7
8
9
10
11
12
【点拨】铜片在空气中加热变黑,是因为铜在加热的条件
下与空气中的氧气反应,生成了氧化铜。铜片在隔绝空气
的条件下加热,铜片不会变黑。
【答案】 D
1
2
3
4
5
6
7
8
9
10
11
12
返回
纠易错 不能正确区分物质的变化与性质
8. 下列关于性质或变化的说法正确的是( A )
A 铁在潮湿环境中易生锈 化学性质
B 酒精挥发 化学变化
C 氧气用于急救病人 物理性质
D 木材燃烧 物理变化
1
2
3
4
5
6
7
8
9
10
11
12
【点拨】铁在潮湿环境中易生锈,需通过铁生锈这一化学
变化表现出来,属于化学性质,A正确;酒精挥发,是酒
精由液态变为气态,没有新物质生成,属于物理变化,B
错误;氧气用于急救病人,是氧气的用途,C错误;木材
燃烧有新物质生成,属于化学变化,D错误。
1
2
3
4
5
6
7
8
9
10
11
12
【点易错】区分物质的变化与性质时应注意:物质的变化
是一个过程,而性质是物质固有的属性,可根据叙述中的
关键字进行判断,物质性质的叙述中一般有
“能”“易”“会”等关键字。
【答案】 A
1
2
3
4
5
6
7
8
9
10
11
12
返回
9. [立德树人 文化自信][2024·陕西模拟]下列俗语与物质的化
学性质无关的是( B )
A. 真金不怕火炼 B. 玉不琢不成器
C. 纸里包不住火 D. 百炼方能成钢
【点拨】玉不琢不成器说的是对玉石进行雕刻琢磨,没有
新物质生成,利用了玉石的物理性质, B符合题意。
B
1
2
3
4
5
6
7
8
9
10
11
12
返回
10. [2024·西安模拟]实验小组探究人体吸入的空气和呼出的
气体的差别。如表实验对应的目的或结论不正确的是
( C )
选项 实验图示 目的或结论
A 收集呼出的气体
1
2
3
4
5
6
7
8
9
10
11
12
选项 实验图示 目的或结论
B 呼出气体中的氧气含量比空气中的低
C
呼出气体中只含有二氧化碳
D 呼出气体中的水蒸气含量比空气中的多
1
2
3
4
5
6
7
8
9
10
11
12
【点拨】可用排水法收集呼出的气体,A正确;氧气能支持燃烧,氧气含量越多,燃烧越剧烈,图中实验,伸入呼出气体中的小木条先熄灭,可得出呼出气体中的氧气含量比空气中的低,B正确;二氧化碳能使澄清石灰水变浑浊,图中实验,滴入呼出气体中的澄清石灰水变浑浊,可得出呼出气体中含有二氧化碳,但不能得出呼出气体中只含有二氧化碳,C错误;水蒸气遇冷凝结成水滴,对着哈气的干燥玻璃片上出现无色液滴,可得出呼出气体中的水蒸气含量比空气中的多,D正确。
【答案】 C
1
2
3
4
5
6
7
8
9
10
11
12
返回
课堂小结
谢谢观看!
同课章节目录
