大单元九 有机化学基础 第28讲 烃的衍生物 学案 (含答案)2026届高三化学一轮大单元复习
文档属性
| 名称 | 大单元九 有机化学基础 第28讲 烃的衍生物 学案 (含答案)2026届高三化学一轮大单元复习 |

|
|
| 格式 | DOC | ||
| 文件大小 | 1.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-15 00:00:00 | ||
图片预览




文档简介
第28讲 烃的衍生物
备考导航
复习目标 1. 认识卤代烃、醇、醛、羧酸、酯、酚、醚、酮、胺和酰胺的结构、性质及应用。2. 认识加成反应、取代反应、消去反应、氧化反应及还原反应的特点及规律。3. 结合生产、生活实际了解某些烃及烃的衍生物对环境和健康可能产生的影响,体会“绿色化学”思想在有机合成中的重要意义,关注有机物的安全使用。
熟记网络
课前自测 判断正误(正确的打“√”,错误的打“×”)。(1) 溴乙烷可发生水解反应获得乙醇( )(2) 在浓硫酸、加热条件下可发生消去反应( )(3) 苯酚与苯甲醇均能与NaOH溶液反应( )(4) 一定条件下,水杨醛()可与甲醛发生缩聚反应( )(5) 苯酚与苯甲醇遇FeCl3溶液均显紫色( )(6) 1 mol 中含有2 mol碳氧π键( )(7) 与足量H2反应的产物分子中含有2个手性碳原子( )(8) 分子中的碳原子均采取sp3杂化( )(9) 1 mol 最多能与5 mol H2发生加成反应( )(10) 1 mol 最多可消耗2 mol NaOH( )
考点1 卤代烃
知 识 梳 理
卤代烃的性质
概念及官能团 烃分子里的氢原子被____________(F、Cl、Br、I)取代后生成的化合物
物理性质 ①比相同碳原子数的烷烃的沸点要高;②___溶于水,___溶于有机溶剂;③一般,一氟代烃、一氯代烃的密度比水小,其余液态卤代烃的密度比水大
化学性质 ①水解反应:R—X+NaOH________________________(R—代表烃基)R—CHX—CH2X+2NaOH______________________________________________________②消去反应:R—CH2—CH2—X+NaOH_______________________________________+2NaOH_____________________________________________
卤代烃的检验
1. 相关化学方程式
R—X+NaOHR—OH+NaX
HNO3+NaOH===NaNO3+H2O
AgNO3+NaX===AgX↓+NaNO3
2. 实验步骤
①取少量卤代烃;
②加入NaOH溶液;
③加热煮沸(或水浴加热);
④冷却;
⑤加入稀硝酸酸化;
⑥加入AgNO3溶液。
注意:加入硝酸银溶液之前,一定要加过量稀硝酸中和NaOH,否则OH-与Ag+反应,生成AgOH、Ag2O会影响卤素离子的检验。相关反应的化学方程式如下:NaOH+AgNO3===NaNO3+AgOH↓、
2AgOH===Ag2O+H2O。
卤代烃在有机合成中的转化
1. 官能团位置转化(写出合成路线)
(原料)
2. 官能团数目转化(写出合成路线)
(1) (原料)
(2) (原料)
(3) (原料)
(4) (原料)
(5) (原料)
3. 官能团的衍变(写出合成路线)
(1) (原料)
(2) (原料)
典 题 悟 法
卤代烃的取代反应和消去反应
(2024·盐城)下列有关卤代烃的叙述正确的是 ( )
A. CH2Cl2有和两种结构
B. 氯乙烯只有一种结构,而1,2 二氯乙烯有两种结构(考虑立体异构)
C. 检验溴乙烷中的溴元素可将其与过量NaOH水溶液共热充分反应后,再滴入AgNO3溶液,可观察到浅黄色沉淀生成
D. 1 溴丙烷和2 溴丙烷分别与NaOH的乙醇溶液共热,产物相同,反应类型不同
卤代烃的检验
(2024·江苏各地模拟重组)室温下,根据下列实验操作和现象所得到的结论不正确的是( )
选项 实验操作和现象 实验结论
A 卤代烃Y与NaOH溶液共热后,先加入足量稀硝酸酸化,再滴加AgNO3溶液,产生白色沉淀 卤代烃Y中含有氯原子
B 将卤代烃与NaOH水溶液混合加热,待冷却后加入硝酸银溶液,观察沉淀颜色 确定卤代烃中卤素原子种类
C 将1-溴丁烷与NaOH的乙醇溶液混合后加热,生成的气体通入Br2的CCl4溶液中,溶液褪色 1-溴丁烷发生消去反应
D 卤代烃和NaOH溶液充分反应后,用足量稀硝酸酸化,再加入AgNO3溶液,有黄色沉淀生成 卤代烃中含有碘元素
(2023·江苏各地模拟重组)下列实验操作能达到实验目的的是( )
选项 实验目的 实验操作
A 检验卤代烃中的卤素原子 向卤代烃中加入足量的NaOH的水溶液,加热,加入AgNO3溶液
B 证明溴乙烷发生消去反应 将溴乙烷和NaOH的乙醇溶液共热后产生的气体通入酸性KMnO4溶液中,溶液褪色
C 验证卤代烃Y不是溴代烃 卤代烃Y与NaOH的水溶液共热后,滴加AgNO3溶液,观察,无淡黄色沉淀产生
D 检验溴乙烷发生消去反应生成的乙烯 将反应生成的气体通入溴的CCl4溶液中
卤代烃在有机合成中的结构转化
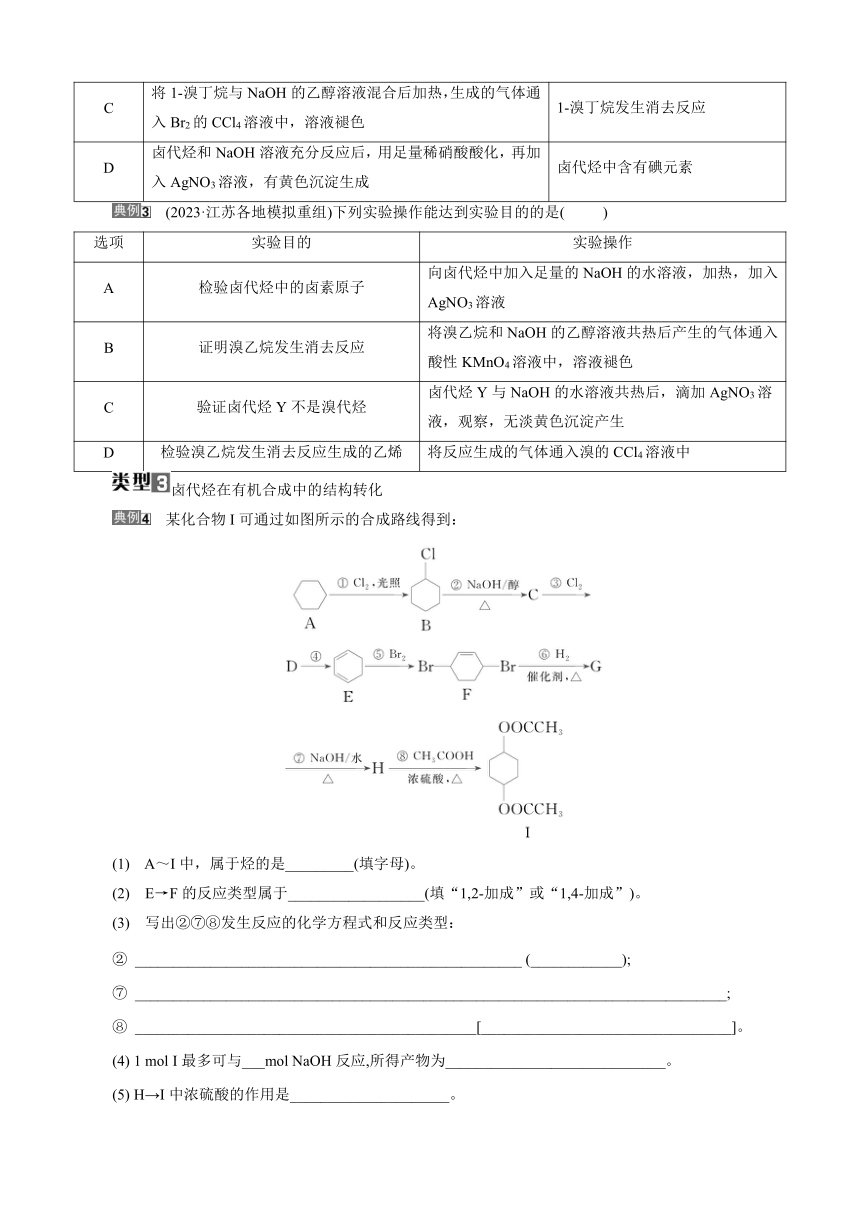
某化合物I可通过如图所示的合成路线得到:
(1) A~I中,属于烃的是_________(填字母)。
(2) E→F的反应类型属于__________________(填“1,2-加成”或“1,4-加成”)。
(3) 写出②⑦⑧发生反应的化学方程式和反应类型:
② ___________________________________________________ (____________);
⑦ ______________________________________________________________________________;
⑧ _____________________________________________[_________________________________]。
(4) 1 mol I最多可与___mol NaOH反应,所得产物为_____________________________。
(5) H→I中浓硫酸的作用是_____________________。
考点2 醇 酚
知 识 梳 理
醇(R—OH)
化学性质 化学方程式 反应类型
与钠反应 2CH3CH2OH+2Na2CH3CH2ONa+H2↑ 置换反应
与氢卤酸(如HBr)反应 CH3CH2OH+HBrCH3CH2Br+H2O 取代反应
醇分子内脱水 CH3CH2OHCH2CH2↑+H2O 消去反应
醇分子间脱水 ①2CH3CH2OHCH3CH2OCH2CH3+H2O②2HOCH2CH2OH+2H2O 取代反应
醇的催化氧化 ①2CH3CH2CH2OH+O22CH3CH2CHO+2H2O②+O2+2H2O③ 氧化反应
乙醇发生反应的断键位置
乙醇的结构式 乙醇的化学性质 断键的位置
与活泼金属反应 ①
催化氧化反应 ①③
酯化反应 ①
分子间脱水反应 ①②
分子内脱水反应 ②⑤
与卤化氢反应 ②
醇催化氧化的规律
醇的α-H氧化:羟基所连碳原子上有H原子,才能发生催化氧化。
酚(羟基直接与苯环相连)
1. 苯酚的物理性质及毒性
颜色、气味、状态 溶解性 毒性
______、有特殊气味的晶体,苯酚暴露在空气中因部分被氧化呈_________ 室温下,苯酚在水中的溶解度是9.2 g;当温度高于65 ℃时,能跟水______;易溶于乙醇等有机溶剂 有毒,对皮肤有强烈腐蚀性;其溶液沾到皮肤上应立即用______清洗
2. 化学性质
化学性质 说明
酸性 与钠反应:2+2Na2+H2↑ 酚羟基上的氢原子较活泼,易与Na反应
与NaOH反应:+NaOH+H2O 苯酚显弱酸性
与Na2CO3反应:+Na2CO3+NaHCO3 酸性由强到弱的顺序:H2CO3>>HC
向苯酚钠溶液中通入少量或过量的CO2:+CO2+H2O+NaHCO3
取代反应 向苯酚溶液中滴加过量浓溴水:+3Br2↓+3HBr 常用于溶液中苯酚的定性检验和定量测定(酚羟基的_________位上的H原子易被Br原子取代)
缩聚反应 n 合成线型(或体型)酚醛树脂条件:浓盐酸、加热
显色反应 苯酚与氯化铁溶液作用显紫色(注:酚类物质一般都可与FeCl3溶液作用显色,但不一定显紫色) 用氯化铁溶液检验酚羟基
苯酚的酸性及其除杂
1. 苯酚的酸性
实验方案及结论 判断(填“√”或“×”) 说明
向Na2CO3溶液中加入稀硫酸,将产生的气体通入苯酚钠溶液中,产生白色沉淀,酸性:硫酸>碳酸>苯酚 ___ 向Na2CO3溶液中加入具有挥发性的酸(如醋酸、浓盐酸、硝酸等),产生的气体中除了含有CO2外,还含有挥发出的酸,无法比较碳酸和苯酚的酸性强弱;只有选择不能挥发的酸(如稀硫酸)才能比较酸性
向Na2CO3溶液中加入冰醋酸,将产生的气体通入苯酚钠溶液中,产生白色沉淀,酸性:醋酸>碳酸>苯酚 ___
向Na2CO3溶液中加入盐酸,将产生的气体直接通入苯酚钠溶液中,苯酚钠溶液变浑浊;酸性:盐酸>碳酸>苯酚 ___
2. 苯酚的除杂
除杂 操作
苯(苯酚) 向混合溶液中加入NaOH溶液,分液取上层有机层,可得到苯注意:不可加浓溴水除杂,因为苯酚与溴反应生成白色的2,4,6-三溴苯酚沉淀可溶于苯
苯酚(苯) 向混合溶液中加入NaOH溶液,分液取下层水层,向水层中通入足量二氧化碳可得苯酚
典 题 悟 法
醇的性质
(2022·南京鼓楼阶段检测)乙醇的结构式如图。下列反应及断键部位不正确的是(B)
A. 乙醇与钠的反应:①键断裂
B. 乙醇的催化氧化反应:②③键断裂
C. 乙醇的消去反应:②⑤键断裂
D. 乙醇与HBr反应:②键断裂
(2024·淮安期中)某有机物M的结构简式为。下列说法正确的是( )
A. M中烃基上的氢被氯原子取代的一氯产物有4种
B. M能发生催化氧化反应生成酮
C. M与NaOH乙醇溶液共热发生消去反应产物有2种
D. M和乙二醇互为同系物
乙烯的制备
采用如图装置制备乙烯并研究乙烯与溴水的反应。实验观察到溴水褪色,得到无色透明的溶液。进一步分析发现反应产物主要为BrCH2CH2OH,含少量BrCH2CH2Br。下列说法不正确的是( )
A. 实验室制乙烯的化学方程式:CH3CH2OHCH2===CH2↑+H2O
B. 除杂试剂A为NaOH溶液
C. 乙烯与溴水反应后的溶液近乎呈中性
D. BrCH2CH2OH与H2O之间存在氢键
苯酚的性质
(2024·南通期末)酚酞是一种酸碱指示剂,合成方法如图所示。下列说法正确的是( )
A. 1 mol苯酚与足量的浓溴水反应,消耗1.5 mol Br2
B. 1 mol邻苯二甲酸酐中含16 mol σ键
C. 酚酞分子中含有手性碳原子
D. 常温下,酚酞易溶于水
(2022·常熟一模)苯酚的性质实验如下:
步骤1:常温下,取1 g苯酚晶体于试管中,向其中加入5 mL蒸馏水,充分振荡后液体变浑浊,将该液体平均分成三份。
步骤2:向第一份液体中滴加几滴FeCl3溶液,观察到溶液显紫色。查阅资料知,配离子[Fe(C6H5O)6]3-显紫色。
步骤3:向第二份液体中滴加少量浓溴水,振荡,无白色沉淀。
步骤4:向第三份液体中加入5% NaOH溶液并振荡,得到澄清溶液,再向其中通入少量CO2,溶液又变浑浊,静置后分层。
下列说法不正确的是( )
A. 步骤1说明常温下苯酚的溶解度小于20 g
B. 步骤2中紫色的配离子[Fe(C6H5O)6]3-由Fe3+提供空轨道
C. 步骤3中溴水与苯酚没有发生化学反应
D. 步骤4中CO2与苯酚钠溶液反应生成苯酚和NaHCO3
考点3 醛 酮
知 识 梳 理
醛与酮的比较
类别 醛 酮
概念 由________________________与______相连而构成的化合物 由_______________与____________相连而构成的化合物
官能团 名称为______,结构为 名称为_______________,结构为
官能团位置 碳链末端(最简单的醛是甲醛) 碳链中间(最简单的酮是丙酮)
化学性质 (1) 氧化反应①银镜反应:CH3CHO+2Ag(NH3)2OH______________________________________________②与新制Cu(OH)2反应:CH3CHO+2Cu(OH)2+NaOH______________________________________________③2CH3CHO+O22CH3COOH(2) 还原反应(催化加氢)CH3CHO+H2__________________(3) 加成反应CH3CHO+HCNCH3CHOHCN(Y为—NH2、—OR、—CN等) (1) 还原反应(催化加氢)CH3CHO+HCN(2) 加成反应(Y为—NH2、—OR、—CN等)
联系 碳原子数相同的饱和一元脂肪醛与饱和一元脂肪酮互为同分异构体
醛基的检验(人教版教材)
与新制的银氨溶液反应 与新制的氢氧化铜反应
实验原理 RCHO+2Ag(NH3)2OHRCOONH4+2Ag↓+3NH3+H2O RCHO+2Cu(OH)2+NaOHRCOONa+Cu2O↓+3H2O
实验装置
实验操作 在洁净的试管中加入1 mL 2% AgNO3溶液,然后边振荡试管边逐滴加入2%氨水至最初产生的沉淀____________溶解,制得银氨溶液;再滴入3滴乙醛,振荡后将试管放在热水浴中加热 在试管中加入2 mL 10% NaOH溶液,加入5滴5% CuSO4溶液,得到新制Cu(OH)2,振荡后加入0.5 mL乙醛溶液,加热
实验现象 产生光亮的银镜(1 mol RCHO~2 mol Ag) 产生砖红色沉淀(1 mol RCHO~1 mol Cu2O)
注意事项 ①试管内部必须洁净;②银氨溶液要随用随配,不可久置;③水浴加热 ①配制Cu(OH)2时,所用的NaOH溶液必须______(填“过量”或“少量”);②Cu(OH)2要随用随配,不可久置;③反应液直接加热煮沸
羟醛缩合反应 醛、酮与格氏试剂反应
1. 羟醛缩合反应
说明:(1) 第一步反应:含有α-H的醛在一定条件下可发生加成反应,生成β-羟基醛。
(2) 第二步脱水反应的方向:形成稳定的结构,与醛基形成共轭体系,生成α,β-不饱和醛。
(3) 酮羰基也能发生类似反应。
2. 醛、酮与格氏试剂(RMgX)反应
典 题 悟 法
醛基的检验
(2024·南通一调)物质Y是一种重要的药物中间体,其合成路线如下:
下列说法不正确的是( )
A. 1 mol X中含有3 mol碳氧π键
B. X与互为顺反异构体
C. Y分子中不含有手性碳原子
D. 可用新制的Cu(OH)2检验Y中是否含有X
醛、酮与格氏试剂反应
(2024·扬州期末)化合物Y是合成丹参醇的中间体,其合成路线如下:
下列说法正确的是( )
A. X分子中含手性碳原子
B. X转化为Y的过程中,与CH3MgBr反应生成
C. Y与Br2以物质的量1∶1发生加成反应时可得3种产物
D. X、Y可用酸性KMnO4溶液进行鉴别
考点4 羧酸 羧酸衍生物
知 识 梳 理
羧酸 酯
类别 羧酸 酯
概念 由________________________与______相连构成的有机化合物,官能团为 羧酸分子羧基中的_________被____________取代后的产物,可简写为R—COOR'(R与R'可以相同,也可以不同),官能团为或
分类 按羧基个数分为一元羧酸(如乙酸、苯甲酸)、二元羧酸(如乙二酸、对苯二甲酸)、多元羧酸等。饱和一元羧酸分子的通式为_________________(n≥2) 按酯基个数分为一元酯(如乙酸乙酯)、二元酯(如乙二酸乙二酯)、多元酯等。饱和一元酯分子的通式为__________________________________________________________________(n≥2)
化学性质 (1) 弱酸性(2) 酯化反应(或取代反应) 水解反应(或取代反应)_________________________________________________________+2NaOH―→CH3COONa+H2O
备注 (1) 酯化反应中一般是“羧酸脱羟基、醇脱氢”。(2) 甲酸是无色、易溶于水的弱酸,具有羧酸与醛的性质,酸性强于乙酸 (1) 酯在酸性条件下的水解反应为可逆反应,在碱性条件下的水解比较彻底。(2) 低级酯具有芳香气味,不溶于水,密度比水小
有机酸的酸性强弱比较 乙酸乙酯的制备 酯化反应
1. 有机酸的酸性强弱比较
吸电子基 酸性比较(填“>”或“<”)
卤素—X(—F、—Cl、—Br、—I)、—NO2、—CN、—CHO、—COOH等。吸电子基团对羧基产生了吸电性诱导效应,使得羧基中O—H更容易断裂,所以有机酸的酸性增强 ①FCH2COOH___ClCH2COOH___BrCH2COOH②Cl3CCOOH___Cl2CHCOOH___ClCH2COOH③O2NCH2COOH___CH3COOH
2. 乙酸乙酯的制备
原理
装置
特点 可逆反应;浓硫酸作催化剂和吸水剂(有SO2生成时,浓硫酸还体现强氧化性)
注意事项 ①加入试剂的顺序:将浓硫酸缓慢加入乙醇中,搅拌均匀,再加入乙酸;②导气管末端在饱和Na2CO3溶液的液面上;③饱和碳酸钠溶液的作用是中和乙酸、降低乙醇在乙酸乙酯中的溶解度;注意:不能用NaOH溶液替换饱和Na2CO3溶液
3. 酯化反应
一元羧酸与一元醇间的酯化反应 CH3COOH+CH3CH2OHCH3COOCH2CH3+H2O
一元羧酸与多元醇间的酯化反应 2CH3COOH++2H2O
多元羧酸与一元醇间的酯化反应 +2CH3CH2OH+2H2O
多元羧酸与多元醇形成酯 a. 形成普通酯+HOOC—COOCH2CH2OH+H2Ob. 形成环酯++2H2Oc. 形成聚酯(缩聚反应)n+n+(2n-1)H2O
羟基羧酸的酯化反应 a. 形成普通酯2+H2Ob. 形成环酯(取代反应)+2H2Oc. 形成聚酯(缩聚反应)
说明 以上反应均为酯化反应(也为取代反应),其中,有聚酯生成的反应属于缩聚反应
典 题 悟 法
乙酸分子的结构式为。下列关于断键部位的叙述正确的是( )
①乙酸在水溶液中电离时断裂a键
②乙酸与乙醇发生酯化反应时断裂b键
③在红磷存在时,Br2与CH3COOH反应的化学方程式可表示为CH3COOH+Br2CH2Br—COOH+HBr,乙酸在反应中断裂c键
④一定条件下,2 mol乙酸生成1 mol乙酸酐的化学反应可表示为2CH3COOH+H2O,乙酸在反应中分别断裂a、b键
A. ①②③ B. ①③④
C. ②③④ D. ①②③④
乙酸(CH3COOH)是弱酸,而氯乙酸(ClCH2COOH)的酸性强于乙酸,这是因为—Cl是一种强吸引电子的基团,能使—OH上的H原子活性增大;有的基团属斥电子基团,能减弱—OH上H原子的活性,这种作用称“诱导效应”。下列说法正确的是( )
A. HCOOH显酸性,H2O呈中性,是因为HCOOH中存在强吸引电子基团醛基
B. CH3COOH酸性弱于HCOOH,是因为CH3COOH中存在强吸引电子的基团甲基
C. 相同温度下,等物质的量浓度的ClCH2COONa溶液的pH比CH3CH2COONa溶液的pH大
D. “诱导效应”说明有机化合物的性质仅决定于官能团的结构
(2021·江苏卷)Z是合成抗多发性骨髓瘤药物帕比司他的重要中间体,可由下列反应制得。下列有关X、Y、Z的说法正确的是 ( )
A. 1 mol X中含有2 mol碳氧π键
B. Y与足量HBr反应生成的有机化合物中不含手性碳原子
C. Z在水中的溶解度比Y在水中的溶解度大
D. X、Y、Z分别与足量酸性KMnO4溶液反应所得芳香族化合物相同
乙酸乙酯广泛用于药物、染料、香料等工业,某学习小组设计a、b两套装置,用乙醇、乙酸和浓硫酸制备乙酸乙酯。下列说法不正确的是( )
a b
A. 浓硫酸能加快酯化反应速率
B. 温度越高,反应速率越快,装置a更佳
C. 装置b比装置a原料损失少
D. 用饱和碳酸钠溶液收集乙酸乙酯有利于酯的纯化
(2024·南通二调)化合物Z是一种药物合成中间体,其合成路线如图所示。
下列说法正确的是( )
A. X分子中只含有酮羰基、醚键2种含氧官能团
B. 1 mol Y与足量NaOH溶液反应,消耗2 mol NaOH
C. Z分子不存在顺反异构体
D. Z可以与HCHO在一定条件下发生缩聚反应
考点5 胺和酰胺
知 识 梳 理
胺
1. 胺的定义与结构
定义 氨分子中的氢原子被烃基取代而形成的一系列的衍生物
分子结构 胺的分子结构与氨气相似,都是三角锥形
2. 胺的分类
依据 类别 结构特点 举例
氢原子被烃基取代的数目 一级胺(伯胺) 一个氮原子连接两个氢原子和一个烃基,通式为____________(烃基用R表示,下同) CH3NH2(甲胺)、CH3CH2NH2(乙胺)
二级胺(仲胺) 一个氮原子连接1个氢原子和2个烃基,通式为_________ (CH3)2NH(二甲胺) 、(吡咯烷)
三级胺(叔胺) 一个氮原子连接3个烃基,通式为______ (CH3)3N(三甲胺)
烃基种类 脂肪胺 脂肪烃基 CH3CH2CH2NH2(丙胺)
芳香胺 芳香烃基 (苯胺)
含有氨基的数目 一元胺 一个氨基 CH3NH2(甲胺)
二元胺 两个氨基 H2NCH2CH2NH2(乙二胺)
多元胺 多个氨基 (二亚乙基三胺)
3. 胺的性质
(1) 碱性
胺与氨气结构相似,溶于水,溶液也具有碱性。
NH3+H2O??NH+OH-
RNH2+H2O??RNH+OH-
(2) 胺与酸反应
CH3NH2+HCl―→CH3NHCl-
(或CH3NH2·HCl)
+HCl (或)
胺易溶于有机溶剂,而铵盐易溶于水但不溶于有机溶剂,向铵盐溶液中加入强碱,可得到胺:
CH3NCl-(或CH3NH2·HCl)+NaOHCH3NH2+NaCl +H2O。
(3) 取代反应
+ClCH2CH3+HCl
酰胺
1. 酰胺的定义与结构
定义 羧酸分子羧基中的—OH被氨基(—NH2)或烃氨基(—NHR或—NR2)取代而成
结构(举例)
2. 酰胺的命名
(1) 根据酰基和氨基的名称而称为“某酰胺”,例如:
(2) 若氮原子上有取代基,则在取代基的名称前冠以“N”字,表示取代基在氮原子上,例如:
N 甲基甲酰胺 N,N 二甲基苯甲酰胺
3. 酰胺的化学性质
(1) 酸性条件下水解(生成羧酸和铵盐)
+HCl+H2O+ NH4Cl
+ H2SO4+2H2O+(NH4)2SO4
(2) 碱性条件下水解(生成羧酸盐和氨气)
+NaOH+NH3↑
典 题 悟 法
(2024·苏州二调)一种药物中间体的部分合成路线如下。下列说法正确的是( )
A. 1 mol X含有3 mol碳氧σ键
B. X、Y、Z均易溶于水
C. 1 mol Z最多能与1 mol NaOH反应
D. X→Y→Z的反应类型均为取代反应
(2024·连云港期中)化合物Z是合成药物的重要中间体,其合成路线如图所示。下列说法正确的是( )
A. X的化学式为C10H14O2N
B. Y分子中所有碳原子不可能在同一平面上
C. Z可以在催化剂作用下与HCHO发生缩聚反应
D. Y、Z既能与FeCl3发生显色反应,也能和NaHCO3反应放出CO2
酰化反应 有机物溶解度、熔沸点与结构的关系
1. 酰化反应
胺与酰卤或酸酐反应,胺的氮原子上的氢原子被酰基取代生成酰胺
反应物 举例 说明
胺与酰卤 乙酰氯中的Cl原子和苯胺中氨基上的H原子结合生成HCl,其余部分结合生成乙酰苯胺
胺与酸酐 乙胺中氨基上的H原子与乙酸酐提供的结合生成羧酸,其余部分结合生成乙酰乙胺
2. 有机物的溶解度、熔沸点与结构的关系
(1) 溶解度与结构的关系
溶解度大小比较 与结构的关系
羟基、羧基、氨基均是亲水基,酯基、烃基均是疏水基;含羟基、羧基、氨基的有机物分子能与水分子形成分子间氢键,溶解度较大
(2) 熔、沸点与结构的关系
熔、炥点高低比较 与结构的关系
CH3CH2CH2CH3>CH3CH3 组成和结构相似的有机物,随着碳原子数增大,熔、沸点升高
CH3CH2CH2CH3>CH3CH(CH3)CH3 有机物的分子式相同时,支链越多,熔、沸点越低
CH3OH>CH3CH3 CH3OH存在分子间氢键,熔、沸点较高
C2H5OH>CH3OCH3、C2H5Cl>CH3CH2CH2CH3 相对分子质量相近时,极性分子间作用力大于非极性分子间的作用力。分子中极性基团越多,分子间作用力越大,熔、沸点越高
硬脂酸(C17H35COOH)>油酸(C17H33COOH) 烯烃衍生物的熔、沸点低于同类烷烃衍生物
芳香烃的侧链相同时,熔、沸点:邻位>间位>对位
H2NCH2COOH>CH3CH2COOH H2NCH2COOH中的—COOH和—NH2可在分子内形成内盐,属于离子化合物,熔、沸点较高
CH3COOH>CH3CH2CH2CH3 CH3COOH能形成分子间氢键,熔、沸点较高
H2NCH2COOH>CH3CH2NO2 H2NCH2COOH能形成分子间氢键,熔、沸点较高
前者能形成分子间氢键,熔、沸点较高;后者能形成分子内氢键,熔、沸点较低
官能团与性质的推断
限定条件 可能含有的官能团或结构片段
能使溴水褪色 或或—CHO
能发生银镜反应 醛基或
能与FeCl3溶液发生显色反应 酚羟基
本身不能与FeCl3溶液发生显色反应,但水解产物之一可以 酚酯基()
能发生酯化反应 羟基(或羧基)
既能发生银镜反应,又能发生水解反应,仅有1个不饱和度
与Na2CO3、NaHCO3溶液反应放出CO2气体 —COOH
醇能被氧化为醛 —CH2OH(至少有2个α-H)
核磁共振氢谱中有n组峰 有n种处于不同化学环境的氢原子
属于α-氨基酸
能够水解,水解后得到α-氨基酸
被酸性KMnO4溶液氧化成 或
能够氧化生成对苯二甲酸 或
能发生消去反应
能发生水解反应 酯基或—X(卤素原子)或酰胺基
能与NaOH溶液反应 酚羟基或—COOH或酯基或—X(卤素原子)
能与Na反应放出氢气 羟基或—COOH
1. (2024·苏锡常镇一模)化合物Z是有机合成中的重要中间体,其部分合成路线如图所示。下列说法正确的是( )
A. Y与Z分子均存在顺反异构体
B. 用酸性高锰酸钾溶液鉴别X和Y
C. X、Y、Z三种物质中,Y在水中的溶解度最大
D. Z与足量H2加成后的产物中有3个手性碳原子
2. (2024·南京、盐城二模)化合物Z是合成药物艾氟康唑的中间体。下列说法不正确的是( )
A. X与CH3CH2MgBr发生加成反应
B. Y分子存在对映异构现象
C. Z分子中所有原子处于同一平面上
D. Y、Z可用溴的四氯化碳溶液鉴别
3. (2024·泰州期中)化合物Z是制备药物洛索洛芬钠的关键中间体,可由下列反应制得。
下列说法正确的是( )
A. X分子中含有1个手性碳原子
B. Y能发生消去反应
C. Z中的含氧官能团为羰基和醚键
D. 1 mol Z最多能与4 mol NaOH反应
4. (2025·南京、盐城一模)化合物Z是一种药物的重要中间体,部分合成路线如下:
下列说法正确的是( )
A. X分子中最多有12个原子共平面
B. 可以用NaHCO3溶液鉴别X、Y
C. Z分子不存在顺反异构体
D. 1 mol Z最多能与6 mol H2发生加成反应
第28讲 烃的衍生物
[备考导航]
(1) √ (2) × (3) × (4) √ (5) × (6) × (7) × (8) × (9) × (10) ×
考点1
[知识梳理]
知识1 卤素原子 难 易 R—OH+NaX
R—CH(OH)—CH2OH+2NaX
R—CH===CH2+NaX+H2O
CH≡CH↑+2NaX+2H2O
知识3
1.
2. (1)
(2)
(3)
(4)
(5)
3. (1)
(2)
[典题悟法]
典例1 B 【解析】 因甲烷为正四面体形结构,所以二氯甲烷没有同分异构体,A错误;氯乙烯只有一种结构,而1,2-二氯乙烯有两种结构:、,B正确;检验溴离子,需要在加入硝酸银溶液之前,加足量的稀硝酸中和NaOH,使溶液呈酸性,C错误;1-溴丙烷和2-溴丙烷分别与NaOH乙醇溶液共热,均发生消去反应,产物相同,均为丙烯,反应类型也相同,D错误。
典例2 B 【解析】 滴入AgNO3溶液之前,需要先加硝酸酸化,防止生成AgOH、Ag2O干扰实验,B错误。
典例3 D 【解析】 滴入AgNO3溶液之前,需要先加硝酸酸化,防止生成AgOH、Ag2O干扰实验,A、C错误;挥发的乙醇也可使酸性KMnO4溶液褪色,故溶液褪色不能证明生成乙烯,B错误;溴乙烷发生消去反应后生成乙烯,乙烯能使Br2的CCl4溶液褪色,本实验中挥发的乙醇不会干扰乙烯的检验,D正确。
典例4 (1) ACE (2) 1,4-加成
(3) +NaOH+NaCl+H2O 消去反应 +2NaOH+2NaBr+2NaBr 取代反应(或水解反应) ⑧2CH3COOH+2H2O+ 取代反应(或酯化反应)
(4) 2 、CH3COONa (5) 催化剂、吸水剂
考点2
[知识梳理]
知识1
解疑释惑35
① ①③ ① ①② ②⑤ ②
知识2
1. 无色 粉红色 混溶 酒精 2. 邻、对
解疑释惑36 1. √ × ×
[典题悟法]
典例5 B 【解析】 乙醇催化氧化生成乙醛,断裂的是①③键,同时在②处形成双键,B错误。
典例6 A 【解析】 烃基中有4种化学环境不同的氢原子,M中烃基上的氢被氯原子取代的一氯产物有4种,A正确;羟基所连的碳原子上没有H原子,该醇不能发生催化氧化,B错误;M属于醇类物质,在氢氧化钠醇溶液、加热条件下不能发生消去反应,C错误;M分子含有1个羟基,而乙二醇含有2个羟基,二者不互为同系物,D错误。
典例7 C 【解析】 乙烯中会混有挥发出来的乙醇和副产物二氧化硫等气体,故可用氢氧化钠溶液进行吸收,B正确;没反应完的溴使溶液呈酸性,C错误;羟基可与H2O分子形成氢键,故BrCH2CH2OH与H2O之间存在氢键,D正确。
典例8 B 【解析】 苯酚中酚羟基的邻、对位氢原子都能和浓溴水以1∶1发生取代反应,所以1 mol苯酚与足量的浓溴水反应,最多消耗3 mol Br2,A错误;邻苯二甲酸酐中含有8个C—C σ键、4个C—H σ键、2个C—O σ键,每个C===O键中含有1个σ键,则该分子中含有16个σ键,所以1 mol邻苯二甲酸酐中含16 mol σ键,B正确;连接4个不同原子或原子团的碳原子为手性碳原子,酚酞分子中不含手性碳原子,C错误;酚酞中含有亲水基和憎水基,但憎水基对其溶解性的影响能力大于亲水基,则常温下酚酞难溶于水,D错误。
典例9 C 【解析】 100 mL(即100 g)水中溶解的苯酚小于20 g,A正确;Fe3+的价层电子排布式为3d5,可提供空轨道,形成配离子[Fe(C6H5O)6]3-,溶液显紫色,B正确;苯酚与少量浓溴水反应生成的2,4,6-三溴苯酚可溶于过量的苯酚溶液中,故观察不到白色沉淀,C错误;苯酚显弱酸性,易与NaOH溶液反应生成易溶于水的苯酚钠,已知酸性:H2CO3>苯酚>HCO,则向苯酚钠溶液中通入少量CO2可生成苯酚和NaHCO3,D正确。
考点3
[知识梳理]
知识1
1. 烃基(或氢原子) 醛基 (酮)羰基 两个烃基 醛基 (酮)羰基 CH3COONH4+2Ag↓+3NH3+H2O CH3COONa+Cu2O↓+3H2O CH3CH2OH
知识2 恰好完全 过量
[典题悟法]
典例10 A 【解析】 X分子中的醛基和酯基中含有碳氧π键,故1 mol X中含有2 mol碳氧π键,A错误;X分子中含有碳碳双键,双键碳原子的两端所连基团各不相同,存在顺反异构体,B正确;Y分子的含N六元环是对称结构,该分子中没有手性碳原子,C正确;X分子中含有醛基,Y分子中没有醛基,可以用新制的Cu(OH)2检验Y中是否含有X,D正确。
典例11 C 【解析】 X分子中没有手性碳原子,A错误;X生成Y的中间产物为,B错误;Y分子中含有两个碳碳双键,发生1,2-加成的产物有2种,发生1,4-加成反应的产物有1种,C正确;X、Y分子中都含有碳碳双键,不能用酸性高锰酸钾溶液鉴别,D错误。
考点4
[知识梳理]
知识
烃基(或氢原子) 羧基 —OH —OR′ CnH2nO2 CnH2nO2 RCOOH+R′OH RCOONa+R′OH
解疑释惑38
1. ① > > ② > > ③ >
[典题悟法]
典例12 D 【解析】 乙酸的电离,断裂羧基中O—H,即a键断裂,①正确;酯化反应中酸去羟基、醇去氢,即b键断裂,②正确;在红磷存在时,Br2可与CH3COOH发生取代反应,甲基上H被取代,C—H断裂,即c键断裂,③正确;乙酸变成乙酸酐时,—COOH中的C—O、O—H断裂,即a、b键断裂,④正确;故选D。
典例13 A 【解析】 CH3COOH酸性弱于HCOOH,说明CH3COOH分子存在斥电子基团,能减弱—OH上H原子的活性而使该物质的酸性减弱,乙酸中含有—CH3,所以—CH3属于斥电子基团,导致乙酸的酸性小于甲酸,B错误;氯乙酸(CH2ClCOOH)的酸性强于乙酸,所以相同温度下,等物质的量浓度的CH2ClCOONa溶液的pH将比CH3CH2COONa的pH小,C错误;“诱导效应”说明有机化合物的性质不仅决定于官能团的结构,也会受所连取代基的影响,D错误。
典例14 D 【解析】 X中醛基上含有碳氧π键,1 mol X中含有1 mol碳氧π键,A错误;连接4个不同基团的碳原子为手性碳原子,Y中碳碳双键与HBr发生加成反应,加成后与溴原子直接相连的碳原子为手性碳原子,B错误;Y含羟基、羧基,均为亲水基,Z含羟基、酯基,酯基为疏水基,则Y在水中的溶解度更大,C错误;羟基、醛基、碳碳双键均可被酸性高锰酸钾溶液氧化,则X、Y、Z分别与足量酸性KMnO4溶液反应所得芳香族化合物均为对苯二甲酸,D正确。
典例15 B 【解析】 浓硫酸是酯化反应的催化剂,能加快酯化反应速率,A正确;温度过高,反应物挥发较多,且会发生副反应,采用水浴加热,可以受热均匀、便于控制温度,B错误,C正确;饱和碳酸钠溶液可中和乙酸、溶解乙醇、降低乙酸乙酯的溶解度,使得乙酸乙酯更加纯净,D正确。
典例16 C 【解析】 X分子中含有(酮)羰基、醚键、酯基3种含氧官能团,A错误;Y分子中的酚羟基以及酚酯基都能与NaOH反应,故1 mol Y与足量NaOH溶液反应,消耗3 mol NaOH,B错误;Z分子中酚羟基的邻、对位上都含有基团,Z分子不能与HCHO发生缩聚反应,D错误。
考点5
[知识梳理]
知识1 2. RNH2 R2NH R3N
[典题悟法]
典例17 A 【解析】 硝基、酯基都不是亲水基团,X难溶于水,B错误;酰胺键和酯基都能与NaOH反应,故1 mol Z最多能与2 mol NaOH反应,C错误;X生成Y的反应为还原反应,Y生成Z的反应为取代反应,D错误。
典例18 B 【解析】 X的化学式为C10H13O2N,A错误;Y分子中含有连接2个甲基的碳原子,故所有碳原子不可能在同一平面上,B正确;Z分子中酚羟基的对位和1个邻位有取代基,故在催化剂作用下不能与HCHO发生缩聚反应,C错误;Y、Z分子中均含酚羟基,能与FeCl3溶液发生显色反应,酚羟基的酸性较弱,不能和NaHCO3反应,D错误。
[质量评价]
1. D 【解析】 Y与Z分子均不存在顺反异构体,A错误;X、Y均含醛基,且酚羟基、碳碳双键均能使酸性高锰酸钾溶液褪色,不能鉴别,B错误;X含羟基、醛基,且不含其他烃基,则X在水中的溶解度最大,C错误;Z与足量H2加成后的产物如图:(标“*”碳原子为手性碳原子),有3个手性碳原子,D正确。
2. C 【解析】 X分子中含有酮羰基,能与CH3CH2MgBr发生加成反应,A正确;Y分子中,与—OH相连的碳原子为手性碳原子,则Y分子存在对映异构现象,B正确;Z分子中,含有—CH2Cl、—CH3,它们都形成四面体形结构,所有原子不可能处于同一平面上,C错误;Z分子中含有碳碳双键,能与溴发生加成反应,所以Y、Z可用溴的四氯化碳溶液鉴别,D正确。
3. A 【解析】 甲基的对位基团与苯环直接相连的C原子为手性碳原子,X分子中只有1个手性碳原子,A正确;与溴原子相连的β-C上无氢原子,不能发生消去反应,B错误;Z中的含氧官能团为酯基,C错误;溴原子、酯基可以和氢氧化钠发生反应,1 mol Z最多能与2 mol NaOH反应,D错误。
4. B 【解析】 X分子中最多有20个原子共平面 ,A错误;X分子能与NaHCO3溶液反应,有气泡产生,而Y分子不能与NaHCO3溶液反应,B正确;Z分子中与碳碳双键两端碳原子相连基团各不相同,故Z分子存在顺反异构体,C错误; 1 mol Z最多能与7 mol H2发生加成反应,D错误。
备考导航
复习目标 1. 认识卤代烃、醇、醛、羧酸、酯、酚、醚、酮、胺和酰胺的结构、性质及应用。2. 认识加成反应、取代反应、消去反应、氧化反应及还原反应的特点及规律。3. 结合生产、生活实际了解某些烃及烃的衍生物对环境和健康可能产生的影响,体会“绿色化学”思想在有机合成中的重要意义,关注有机物的安全使用。
熟记网络
课前自测 判断正误(正确的打“√”,错误的打“×”)。(1) 溴乙烷可发生水解反应获得乙醇( )(2) 在浓硫酸、加热条件下可发生消去反应( )(3) 苯酚与苯甲醇均能与NaOH溶液反应( )(4) 一定条件下,水杨醛()可与甲醛发生缩聚反应( )(5) 苯酚与苯甲醇遇FeCl3溶液均显紫色( )(6) 1 mol 中含有2 mol碳氧π键( )(7) 与足量H2反应的产物分子中含有2个手性碳原子( )(8) 分子中的碳原子均采取sp3杂化( )(9) 1 mol 最多能与5 mol H2发生加成反应( )(10) 1 mol 最多可消耗2 mol NaOH( )
考点1 卤代烃
知 识 梳 理
卤代烃的性质
概念及官能团 烃分子里的氢原子被____________(F、Cl、Br、I)取代后生成的化合物
物理性质 ①比相同碳原子数的烷烃的沸点要高;②___溶于水,___溶于有机溶剂;③一般,一氟代烃、一氯代烃的密度比水小,其余液态卤代烃的密度比水大
化学性质 ①水解反应:R—X+NaOH________________________(R—代表烃基)R—CHX—CH2X+2NaOH______________________________________________________②消去反应:R—CH2—CH2—X+NaOH_______________________________________+2NaOH_____________________________________________
卤代烃的检验
1. 相关化学方程式
R—X+NaOHR—OH+NaX
HNO3+NaOH===NaNO3+H2O
AgNO3+NaX===AgX↓+NaNO3
2. 实验步骤
①取少量卤代烃;
②加入NaOH溶液;
③加热煮沸(或水浴加热);
④冷却;
⑤加入稀硝酸酸化;
⑥加入AgNO3溶液。
注意:加入硝酸银溶液之前,一定要加过量稀硝酸中和NaOH,否则OH-与Ag+反应,生成AgOH、Ag2O会影响卤素离子的检验。相关反应的化学方程式如下:NaOH+AgNO3===NaNO3+AgOH↓、
2AgOH===Ag2O+H2O。
卤代烃在有机合成中的转化
1. 官能团位置转化(写出合成路线)
(原料)
2. 官能团数目转化(写出合成路线)
(1) (原料)
(2) (原料)
(3) (原料)
(4) (原料)
(5) (原料)
3. 官能团的衍变(写出合成路线)
(1) (原料)
(2) (原料)
典 题 悟 法
卤代烃的取代反应和消去反应
(2024·盐城)下列有关卤代烃的叙述正确的是 ( )
A. CH2Cl2有和两种结构
B. 氯乙烯只有一种结构,而1,2 二氯乙烯有两种结构(考虑立体异构)
C. 检验溴乙烷中的溴元素可将其与过量NaOH水溶液共热充分反应后,再滴入AgNO3溶液,可观察到浅黄色沉淀生成
D. 1 溴丙烷和2 溴丙烷分别与NaOH的乙醇溶液共热,产物相同,反应类型不同
卤代烃的检验
(2024·江苏各地模拟重组)室温下,根据下列实验操作和现象所得到的结论不正确的是( )
选项 实验操作和现象 实验结论
A 卤代烃Y与NaOH溶液共热后,先加入足量稀硝酸酸化,再滴加AgNO3溶液,产生白色沉淀 卤代烃Y中含有氯原子
B 将卤代烃与NaOH水溶液混合加热,待冷却后加入硝酸银溶液,观察沉淀颜色 确定卤代烃中卤素原子种类
C 将1-溴丁烷与NaOH的乙醇溶液混合后加热,生成的气体通入Br2的CCl4溶液中,溶液褪色 1-溴丁烷发生消去反应
D 卤代烃和NaOH溶液充分反应后,用足量稀硝酸酸化,再加入AgNO3溶液,有黄色沉淀生成 卤代烃中含有碘元素
(2023·江苏各地模拟重组)下列实验操作能达到实验目的的是( )
选项 实验目的 实验操作
A 检验卤代烃中的卤素原子 向卤代烃中加入足量的NaOH的水溶液,加热,加入AgNO3溶液
B 证明溴乙烷发生消去反应 将溴乙烷和NaOH的乙醇溶液共热后产生的气体通入酸性KMnO4溶液中,溶液褪色
C 验证卤代烃Y不是溴代烃 卤代烃Y与NaOH的水溶液共热后,滴加AgNO3溶液,观察,无淡黄色沉淀产生
D 检验溴乙烷发生消去反应生成的乙烯 将反应生成的气体通入溴的CCl4溶液中
卤代烃在有机合成中的结构转化
某化合物I可通过如图所示的合成路线得到:
(1) A~I中,属于烃的是_________(填字母)。
(2) E→F的反应类型属于__________________(填“1,2-加成”或“1,4-加成”)。
(3) 写出②⑦⑧发生反应的化学方程式和反应类型:
② ___________________________________________________ (____________);
⑦ ______________________________________________________________________________;
⑧ _____________________________________________[_________________________________]。
(4) 1 mol I最多可与___mol NaOH反应,所得产物为_____________________________。
(5) H→I中浓硫酸的作用是_____________________。
考点2 醇 酚
知 识 梳 理
醇(R—OH)
化学性质 化学方程式 反应类型
与钠反应 2CH3CH2OH+2Na2CH3CH2ONa+H2↑ 置换反应
与氢卤酸(如HBr)反应 CH3CH2OH+HBrCH3CH2Br+H2O 取代反应
醇分子内脱水 CH3CH2OHCH2CH2↑+H2O 消去反应
醇分子间脱水 ①2CH3CH2OHCH3CH2OCH2CH3+H2O②2HOCH2CH2OH+2H2O 取代反应
醇的催化氧化 ①2CH3CH2CH2OH+O22CH3CH2CHO+2H2O②+O2+2H2O③ 氧化反应
乙醇发生反应的断键位置
乙醇的结构式 乙醇的化学性质 断键的位置
与活泼金属反应 ①
催化氧化反应 ①③
酯化反应 ①
分子间脱水反应 ①②
分子内脱水反应 ②⑤
与卤化氢反应 ②
醇催化氧化的规律
醇的α-H氧化:羟基所连碳原子上有H原子,才能发生催化氧化。
酚(羟基直接与苯环相连)
1. 苯酚的物理性质及毒性
颜色、气味、状态 溶解性 毒性
______、有特殊气味的晶体,苯酚暴露在空气中因部分被氧化呈_________ 室温下,苯酚在水中的溶解度是9.2 g;当温度高于65 ℃时,能跟水______;易溶于乙醇等有机溶剂 有毒,对皮肤有强烈腐蚀性;其溶液沾到皮肤上应立即用______清洗
2. 化学性质
化学性质 说明
酸性 与钠反应:2+2Na2+H2↑ 酚羟基上的氢原子较活泼,易与Na反应
与NaOH反应:+NaOH+H2O 苯酚显弱酸性
与Na2CO3反应:+Na2CO3+NaHCO3 酸性由强到弱的顺序:H2CO3>>HC
向苯酚钠溶液中通入少量或过量的CO2:+CO2+H2O+NaHCO3
取代反应 向苯酚溶液中滴加过量浓溴水:+3Br2↓+3HBr 常用于溶液中苯酚的定性检验和定量测定(酚羟基的_________位上的H原子易被Br原子取代)
缩聚反应 n 合成线型(或体型)酚醛树脂条件:浓盐酸、加热
显色反应 苯酚与氯化铁溶液作用显紫色(注:酚类物质一般都可与FeCl3溶液作用显色,但不一定显紫色) 用氯化铁溶液检验酚羟基
苯酚的酸性及其除杂
1. 苯酚的酸性
实验方案及结论 判断(填“√”或“×”) 说明
向Na2CO3溶液中加入稀硫酸,将产生的气体通入苯酚钠溶液中,产生白色沉淀,酸性:硫酸>碳酸>苯酚 ___ 向Na2CO3溶液中加入具有挥发性的酸(如醋酸、浓盐酸、硝酸等),产生的气体中除了含有CO2外,还含有挥发出的酸,无法比较碳酸和苯酚的酸性强弱;只有选择不能挥发的酸(如稀硫酸)才能比较酸性
向Na2CO3溶液中加入冰醋酸,将产生的气体通入苯酚钠溶液中,产生白色沉淀,酸性:醋酸>碳酸>苯酚 ___
向Na2CO3溶液中加入盐酸,将产生的气体直接通入苯酚钠溶液中,苯酚钠溶液变浑浊;酸性:盐酸>碳酸>苯酚 ___
2. 苯酚的除杂
除杂 操作
苯(苯酚) 向混合溶液中加入NaOH溶液,分液取上层有机层,可得到苯注意:不可加浓溴水除杂,因为苯酚与溴反应生成白色的2,4,6-三溴苯酚沉淀可溶于苯
苯酚(苯) 向混合溶液中加入NaOH溶液,分液取下层水层,向水层中通入足量二氧化碳可得苯酚
典 题 悟 法
醇的性质
(2022·南京鼓楼阶段检测)乙醇的结构式如图。下列反应及断键部位不正确的是(B)
A. 乙醇与钠的反应:①键断裂
B. 乙醇的催化氧化反应:②③键断裂
C. 乙醇的消去反应:②⑤键断裂
D. 乙醇与HBr反应:②键断裂
(2024·淮安期中)某有机物M的结构简式为。下列说法正确的是( )
A. M中烃基上的氢被氯原子取代的一氯产物有4种
B. M能发生催化氧化反应生成酮
C. M与NaOH乙醇溶液共热发生消去反应产物有2种
D. M和乙二醇互为同系物
乙烯的制备
采用如图装置制备乙烯并研究乙烯与溴水的反应。实验观察到溴水褪色,得到无色透明的溶液。进一步分析发现反应产物主要为BrCH2CH2OH,含少量BrCH2CH2Br。下列说法不正确的是( )
A. 实验室制乙烯的化学方程式:CH3CH2OHCH2===CH2↑+H2O
B. 除杂试剂A为NaOH溶液
C. 乙烯与溴水反应后的溶液近乎呈中性
D. BrCH2CH2OH与H2O之间存在氢键
苯酚的性质
(2024·南通期末)酚酞是一种酸碱指示剂,合成方法如图所示。下列说法正确的是( )
A. 1 mol苯酚与足量的浓溴水反应,消耗1.5 mol Br2
B. 1 mol邻苯二甲酸酐中含16 mol σ键
C. 酚酞分子中含有手性碳原子
D. 常温下,酚酞易溶于水
(2022·常熟一模)苯酚的性质实验如下:
步骤1:常温下,取1 g苯酚晶体于试管中,向其中加入5 mL蒸馏水,充分振荡后液体变浑浊,将该液体平均分成三份。
步骤2:向第一份液体中滴加几滴FeCl3溶液,观察到溶液显紫色。查阅资料知,配离子[Fe(C6H5O)6]3-显紫色。
步骤3:向第二份液体中滴加少量浓溴水,振荡,无白色沉淀。
步骤4:向第三份液体中加入5% NaOH溶液并振荡,得到澄清溶液,再向其中通入少量CO2,溶液又变浑浊,静置后分层。
下列说法不正确的是( )
A. 步骤1说明常温下苯酚的溶解度小于20 g
B. 步骤2中紫色的配离子[Fe(C6H5O)6]3-由Fe3+提供空轨道
C. 步骤3中溴水与苯酚没有发生化学反应
D. 步骤4中CO2与苯酚钠溶液反应生成苯酚和NaHCO3
考点3 醛 酮
知 识 梳 理
醛与酮的比较
类别 醛 酮
概念 由________________________与______相连而构成的化合物 由_______________与____________相连而构成的化合物
官能团 名称为______,结构为 名称为_______________,结构为
官能团位置 碳链末端(最简单的醛是甲醛) 碳链中间(最简单的酮是丙酮)
化学性质 (1) 氧化反应①银镜反应:CH3CHO+2Ag(NH3)2OH______________________________________________②与新制Cu(OH)2反应:CH3CHO+2Cu(OH)2+NaOH______________________________________________③2CH3CHO+O22CH3COOH(2) 还原反应(催化加氢)CH3CHO+H2__________________(3) 加成反应CH3CHO+HCNCH3CHOHCN(Y为—NH2、—OR、—CN等) (1) 还原反应(催化加氢)CH3CHO+HCN(2) 加成反应(Y为—NH2、—OR、—CN等)
联系 碳原子数相同的饱和一元脂肪醛与饱和一元脂肪酮互为同分异构体
醛基的检验(人教版教材)
与新制的银氨溶液反应 与新制的氢氧化铜反应
实验原理 RCHO+2Ag(NH3)2OHRCOONH4+2Ag↓+3NH3+H2O RCHO+2Cu(OH)2+NaOHRCOONa+Cu2O↓+3H2O
实验装置
实验操作 在洁净的试管中加入1 mL 2% AgNO3溶液,然后边振荡试管边逐滴加入2%氨水至最初产生的沉淀____________溶解,制得银氨溶液;再滴入3滴乙醛,振荡后将试管放在热水浴中加热 在试管中加入2 mL 10% NaOH溶液,加入5滴5% CuSO4溶液,得到新制Cu(OH)2,振荡后加入0.5 mL乙醛溶液,加热
实验现象 产生光亮的银镜(1 mol RCHO~2 mol Ag) 产生砖红色沉淀(1 mol RCHO~1 mol Cu2O)
注意事项 ①试管内部必须洁净;②银氨溶液要随用随配,不可久置;③水浴加热 ①配制Cu(OH)2时,所用的NaOH溶液必须______(填“过量”或“少量”);②Cu(OH)2要随用随配,不可久置;③反应液直接加热煮沸
羟醛缩合反应 醛、酮与格氏试剂反应
1. 羟醛缩合反应
说明:(1) 第一步反应:含有α-H的醛在一定条件下可发生加成反应,生成β-羟基醛。
(2) 第二步脱水反应的方向:形成稳定的结构,与醛基形成共轭体系,生成α,β-不饱和醛。
(3) 酮羰基也能发生类似反应。
2. 醛、酮与格氏试剂(RMgX)反应
典 题 悟 法
醛基的检验
(2024·南通一调)物质Y是一种重要的药物中间体,其合成路线如下:
下列说法不正确的是( )
A. 1 mol X中含有3 mol碳氧π键
B. X与互为顺反异构体
C. Y分子中不含有手性碳原子
D. 可用新制的Cu(OH)2检验Y中是否含有X
醛、酮与格氏试剂反应
(2024·扬州期末)化合物Y是合成丹参醇的中间体,其合成路线如下:
下列说法正确的是( )
A. X分子中含手性碳原子
B. X转化为Y的过程中,与CH3MgBr反应生成
C. Y与Br2以物质的量1∶1发生加成反应时可得3种产物
D. X、Y可用酸性KMnO4溶液进行鉴别
考点4 羧酸 羧酸衍生物
知 识 梳 理
羧酸 酯
类别 羧酸 酯
概念 由________________________与______相连构成的有机化合物,官能团为 羧酸分子羧基中的_________被____________取代后的产物,可简写为R—COOR'(R与R'可以相同,也可以不同),官能团为或
分类 按羧基个数分为一元羧酸(如乙酸、苯甲酸)、二元羧酸(如乙二酸、对苯二甲酸)、多元羧酸等。饱和一元羧酸分子的通式为_________________(n≥2) 按酯基个数分为一元酯(如乙酸乙酯)、二元酯(如乙二酸乙二酯)、多元酯等。饱和一元酯分子的通式为__________________________________________________________________(n≥2)
化学性质 (1) 弱酸性(2) 酯化反应(或取代反应) 水解反应(或取代反应)_________________________________________________________+2NaOH―→CH3COONa+H2O
备注 (1) 酯化反应中一般是“羧酸脱羟基、醇脱氢”。(2) 甲酸是无色、易溶于水的弱酸,具有羧酸与醛的性质,酸性强于乙酸 (1) 酯在酸性条件下的水解反应为可逆反应,在碱性条件下的水解比较彻底。(2) 低级酯具有芳香气味,不溶于水,密度比水小
有机酸的酸性强弱比较 乙酸乙酯的制备 酯化反应
1. 有机酸的酸性强弱比较
吸电子基 酸性比较(填“>”或“<”)
卤素—X(—F、—Cl、—Br、—I)、—NO2、—CN、—CHO、—COOH等。吸电子基团对羧基产生了吸电性诱导效应,使得羧基中O—H更容易断裂,所以有机酸的酸性增强 ①FCH2COOH___ClCH2COOH___BrCH2COOH②Cl3CCOOH___Cl2CHCOOH___ClCH2COOH③O2NCH2COOH___CH3COOH
2. 乙酸乙酯的制备
原理
装置
特点 可逆反应;浓硫酸作催化剂和吸水剂(有SO2生成时,浓硫酸还体现强氧化性)
注意事项 ①加入试剂的顺序:将浓硫酸缓慢加入乙醇中,搅拌均匀,再加入乙酸;②导气管末端在饱和Na2CO3溶液的液面上;③饱和碳酸钠溶液的作用是中和乙酸、降低乙醇在乙酸乙酯中的溶解度;注意:不能用NaOH溶液替换饱和Na2CO3溶液
3. 酯化反应
一元羧酸与一元醇间的酯化反应 CH3COOH+CH3CH2OHCH3COOCH2CH3+H2O
一元羧酸与多元醇间的酯化反应 2CH3COOH++2H2O
多元羧酸与一元醇间的酯化反应 +2CH3CH2OH+2H2O
多元羧酸与多元醇形成酯 a. 形成普通酯+HOOC—COOCH2CH2OH+H2Ob. 形成环酯++2H2Oc. 形成聚酯(缩聚反应)n+n+(2n-1)H2O
羟基羧酸的酯化反应 a. 形成普通酯2+H2Ob. 形成环酯(取代反应)+2H2Oc. 形成聚酯(缩聚反应)
说明 以上反应均为酯化反应(也为取代反应),其中,有聚酯生成的反应属于缩聚反应
典 题 悟 法
乙酸分子的结构式为。下列关于断键部位的叙述正确的是( )
①乙酸在水溶液中电离时断裂a键
②乙酸与乙醇发生酯化反应时断裂b键
③在红磷存在时,Br2与CH3COOH反应的化学方程式可表示为CH3COOH+Br2CH2Br—COOH+HBr,乙酸在反应中断裂c键
④一定条件下,2 mol乙酸生成1 mol乙酸酐的化学反应可表示为2CH3COOH+H2O,乙酸在反应中分别断裂a、b键
A. ①②③ B. ①③④
C. ②③④ D. ①②③④
乙酸(CH3COOH)是弱酸,而氯乙酸(ClCH2COOH)的酸性强于乙酸,这是因为—Cl是一种强吸引电子的基团,能使—OH上的H原子活性增大;有的基团属斥电子基团,能减弱—OH上H原子的活性,这种作用称“诱导效应”。下列说法正确的是( )
A. HCOOH显酸性,H2O呈中性,是因为HCOOH中存在强吸引电子基团醛基
B. CH3COOH酸性弱于HCOOH,是因为CH3COOH中存在强吸引电子的基团甲基
C. 相同温度下,等物质的量浓度的ClCH2COONa溶液的pH比CH3CH2COONa溶液的pH大
D. “诱导效应”说明有机化合物的性质仅决定于官能团的结构
(2021·江苏卷)Z是合成抗多发性骨髓瘤药物帕比司他的重要中间体,可由下列反应制得。下列有关X、Y、Z的说法正确的是 ( )
A. 1 mol X中含有2 mol碳氧π键
B. Y与足量HBr反应生成的有机化合物中不含手性碳原子
C. Z在水中的溶解度比Y在水中的溶解度大
D. X、Y、Z分别与足量酸性KMnO4溶液反应所得芳香族化合物相同
乙酸乙酯广泛用于药物、染料、香料等工业,某学习小组设计a、b两套装置,用乙醇、乙酸和浓硫酸制备乙酸乙酯。下列说法不正确的是( )
a b
A. 浓硫酸能加快酯化反应速率
B. 温度越高,反应速率越快,装置a更佳
C. 装置b比装置a原料损失少
D. 用饱和碳酸钠溶液收集乙酸乙酯有利于酯的纯化
(2024·南通二调)化合物Z是一种药物合成中间体,其合成路线如图所示。
下列说法正确的是( )
A. X分子中只含有酮羰基、醚键2种含氧官能团
B. 1 mol Y与足量NaOH溶液反应,消耗2 mol NaOH
C. Z分子不存在顺反异构体
D. Z可以与HCHO在一定条件下发生缩聚反应
考点5 胺和酰胺
知 识 梳 理
胺
1. 胺的定义与结构
定义 氨分子中的氢原子被烃基取代而形成的一系列的衍生物
分子结构 胺的分子结构与氨气相似,都是三角锥形
2. 胺的分类
依据 类别 结构特点 举例
氢原子被烃基取代的数目 一级胺(伯胺) 一个氮原子连接两个氢原子和一个烃基,通式为____________(烃基用R表示,下同) CH3NH2(甲胺)、CH3CH2NH2(乙胺)
二级胺(仲胺) 一个氮原子连接1个氢原子和2个烃基,通式为_________ (CH3)2NH(二甲胺) 、(吡咯烷)
三级胺(叔胺) 一个氮原子连接3个烃基,通式为______ (CH3)3N(三甲胺)
烃基种类 脂肪胺 脂肪烃基 CH3CH2CH2NH2(丙胺)
芳香胺 芳香烃基 (苯胺)
含有氨基的数目 一元胺 一个氨基 CH3NH2(甲胺)
二元胺 两个氨基 H2NCH2CH2NH2(乙二胺)
多元胺 多个氨基 (二亚乙基三胺)
3. 胺的性质
(1) 碱性
胺与氨气结构相似,溶于水,溶液也具有碱性。
NH3+H2O??NH+OH-
RNH2+H2O??RNH+OH-
(2) 胺与酸反应
CH3NH2+HCl―→CH3NHCl-
(或CH3NH2·HCl)
+HCl (或)
胺易溶于有机溶剂,而铵盐易溶于水但不溶于有机溶剂,向铵盐溶液中加入强碱,可得到胺:
CH3NCl-(或CH3NH2·HCl)+NaOHCH3NH2+NaCl +H2O。
(3) 取代反应
+ClCH2CH3+HCl
酰胺
1. 酰胺的定义与结构
定义 羧酸分子羧基中的—OH被氨基(—NH2)或烃氨基(—NHR或—NR2)取代而成
结构(举例)
2. 酰胺的命名
(1) 根据酰基和氨基的名称而称为“某酰胺”,例如:
(2) 若氮原子上有取代基,则在取代基的名称前冠以“N”字,表示取代基在氮原子上,例如:
N 甲基甲酰胺 N,N 二甲基苯甲酰胺
3. 酰胺的化学性质
(1) 酸性条件下水解(生成羧酸和铵盐)
+HCl+H2O+ NH4Cl
+ H2SO4+2H2O+(NH4)2SO4
(2) 碱性条件下水解(生成羧酸盐和氨气)
+NaOH+NH3↑
典 题 悟 法
(2024·苏州二调)一种药物中间体的部分合成路线如下。下列说法正确的是( )
A. 1 mol X含有3 mol碳氧σ键
B. X、Y、Z均易溶于水
C. 1 mol Z最多能与1 mol NaOH反应
D. X→Y→Z的反应类型均为取代反应
(2024·连云港期中)化合物Z是合成药物的重要中间体,其合成路线如图所示。下列说法正确的是( )
A. X的化学式为C10H14O2N
B. Y分子中所有碳原子不可能在同一平面上
C. Z可以在催化剂作用下与HCHO发生缩聚反应
D. Y、Z既能与FeCl3发生显色反应,也能和NaHCO3反应放出CO2
酰化反应 有机物溶解度、熔沸点与结构的关系
1. 酰化反应
胺与酰卤或酸酐反应,胺的氮原子上的氢原子被酰基取代生成酰胺
反应物 举例 说明
胺与酰卤 乙酰氯中的Cl原子和苯胺中氨基上的H原子结合生成HCl,其余部分结合生成乙酰苯胺
胺与酸酐 乙胺中氨基上的H原子与乙酸酐提供的结合生成羧酸,其余部分结合生成乙酰乙胺
2. 有机物的溶解度、熔沸点与结构的关系
(1) 溶解度与结构的关系
溶解度大小比较 与结构的关系
羟基、羧基、氨基均是亲水基,酯基、烃基均是疏水基;含羟基、羧基、氨基的有机物分子能与水分子形成分子间氢键,溶解度较大
(2) 熔、沸点与结构的关系
熔、炥点高低比较 与结构的关系
CH3CH2CH2CH3>CH3CH3 组成和结构相似的有机物,随着碳原子数增大,熔、沸点升高
CH3CH2CH2CH3>CH3CH(CH3)CH3 有机物的分子式相同时,支链越多,熔、沸点越低
CH3OH>CH3CH3 CH3OH存在分子间氢键,熔、沸点较高
C2H5OH>CH3OCH3、C2H5Cl>CH3CH2CH2CH3 相对分子质量相近时,极性分子间作用力大于非极性分子间的作用力。分子中极性基团越多,分子间作用力越大,熔、沸点越高
硬脂酸(C17H35COOH)>油酸(C17H33COOH) 烯烃衍生物的熔、沸点低于同类烷烃衍生物
芳香烃的侧链相同时,熔、沸点:邻位>间位>对位
H2NCH2COOH>CH3CH2COOH H2NCH2COOH中的—COOH和—NH2可在分子内形成内盐,属于离子化合物,熔、沸点较高
CH3COOH>CH3CH2CH2CH3 CH3COOH能形成分子间氢键,熔、沸点较高
H2NCH2COOH>CH3CH2NO2 H2NCH2COOH能形成分子间氢键,熔、沸点较高
前者能形成分子间氢键,熔、沸点较高;后者能形成分子内氢键,熔、沸点较低
官能团与性质的推断
限定条件 可能含有的官能团或结构片段
能使溴水褪色 或或—CHO
能发生银镜反应 醛基或
能与FeCl3溶液发生显色反应 酚羟基
本身不能与FeCl3溶液发生显色反应,但水解产物之一可以 酚酯基()
能发生酯化反应 羟基(或羧基)
既能发生银镜反应,又能发生水解反应,仅有1个不饱和度
与Na2CO3、NaHCO3溶液反应放出CO2气体 —COOH
醇能被氧化为醛 —CH2OH(至少有2个α-H)
核磁共振氢谱中有n组峰 有n种处于不同化学环境的氢原子
属于α-氨基酸
能够水解,水解后得到α-氨基酸
被酸性KMnO4溶液氧化成 或
能够氧化生成对苯二甲酸 或
能发生消去反应
能发生水解反应 酯基或—X(卤素原子)或酰胺基
能与NaOH溶液反应 酚羟基或—COOH或酯基或—X(卤素原子)
能与Na反应放出氢气 羟基或—COOH
1. (2024·苏锡常镇一模)化合物Z是有机合成中的重要中间体,其部分合成路线如图所示。下列说法正确的是( )
A. Y与Z分子均存在顺反异构体
B. 用酸性高锰酸钾溶液鉴别X和Y
C. X、Y、Z三种物质中,Y在水中的溶解度最大
D. Z与足量H2加成后的产物中有3个手性碳原子
2. (2024·南京、盐城二模)化合物Z是合成药物艾氟康唑的中间体。下列说法不正确的是( )
A. X与CH3CH2MgBr发生加成反应
B. Y分子存在对映异构现象
C. Z分子中所有原子处于同一平面上
D. Y、Z可用溴的四氯化碳溶液鉴别
3. (2024·泰州期中)化合物Z是制备药物洛索洛芬钠的关键中间体,可由下列反应制得。
下列说法正确的是( )
A. X分子中含有1个手性碳原子
B. Y能发生消去反应
C. Z中的含氧官能团为羰基和醚键
D. 1 mol Z最多能与4 mol NaOH反应
4. (2025·南京、盐城一模)化合物Z是一种药物的重要中间体,部分合成路线如下:
下列说法正确的是( )
A. X分子中最多有12个原子共平面
B. 可以用NaHCO3溶液鉴别X、Y
C. Z分子不存在顺反异构体
D. 1 mol Z最多能与6 mol H2发生加成反应
第28讲 烃的衍生物
[备考导航]
(1) √ (2) × (3) × (4) √ (5) × (6) × (7) × (8) × (9) × (10) ×
考点1
[知识梳理]
知识1 卤素原子 难 易 R—OH+NaX
R—CH(OH)—CH2OH+2NaX
R—CH===CH2+NaX+H2O
CH≡CH↑+2NaX+2H2O
知识3
1.
2. (1)
(2)
(3)
(4)
(5)
3. (1)
(2)
[典题悟法]
典例1 B 【解析】 因甲烷为正四面体形结构,所以二氯甲烷没有同分异构体,A错误;氯乙烯只有一种结构,而1,2-二氯乙烯有两种结构:、,B正确;检验溴离子,需要在加入硝酸银溶液之前,加足量的稀硝酸中和NaOH,使溶液呈酸性,C错误;1-溴丙烷和2-溴丙烷分别与NaOH乙醇溶液共热,均发生消去反应,产物相同,均为丙烯,反应类型也相同,D错误。
典例2 B 【解析】 滴入AgNO3溶液之前,需要先加硝酸酸化,防止生成AgOH、Ag2O干扰实验,B错误。
典例3 D 【解析】 滴入AgNO3溶液之前,需要先加硝酸酸化,防止生成AgOH、Ag2O干扰实验,A、C错误;挥发的乙醇也可使酸性KMnO4溶液褪色,故溶液褪色不能证明生成乙烯,B错误;溴乙烷发生消去反应后生成乙烯,乙烯能使Br2的CCl4溶液褪色,本实验中挥发的乙醇不会干扰乙烯的检验,D正确。
典例4 (1) ACE (2) 1,4-加成
(3) +NaOH+NaCl+H2O 消去反应 +2NaOH+2NaBr+2NaBr 取代反应(或水解反应) ⑧2CH3COOH+2H2O+ 取代反应(或酯化反应)
(4) 2 、CH3COONa (5) 催化剂、吸水剂
考点2
[知识梳理]
知识1
解疑释惑35
① ①③ ① ①② ②⑤ ②
知识2
1. 无色 粉红色 混溶 酒精 2. 邻、对
解疑释惑36 1. √ × ×
[典题悟法]
典例5 B 【解析】 乙醇催化氧化生成乙醛,断裂的是①③键,同时在②处形成双键,B错误。
典例6 A 【解析】 烃基中有4种化学环境不同的氢原子,M中烃基上的氢被氯原子取代的一氯产物有4种,A正确;羟基所连的碳原子上没有H原子,该醇不能发生催化氧化,B错误;M属于醇类物质,在氢氧化钠醇溶液、加热条件下不能发生消去反应,C错误;M分子含有1个羟基,而乙二醇含有2个羟基,二者不互为同系物,D错误。
典例7 C 【解析】 乙烯中会混有挥发出来的乙醇和副产物二氧化硫等气体,故可用氢氧化钠溶液进行吸收,B正确;没反应完的溴使溶液呈酸性,C错误;羟基可与H2O分子形成氢键,故BrCH2CH2OH与H2O之间存在氢键,D正确。
典例8 B 【解析】 苯酚中酚羟基的邻、对位氢原子都能和浓溴水以1∶1发生取代反应,所以1 mol苯酚与足量的浓溴水反应,最多消耗3 mol Br2,A错误;邻苯二甲酸酐中含有8个C—C σ键、4个C—H σ键、2个C—O σ键,每个C===O键中含有1个σ键,则该分子中含有16个σ键,所以1 mol邻苯二甲酸酐中含16 mol σ键,B正确;连接4个不同原子或原子团的碳原子为手性碳原子,酚酞分子中不含手性碳原子,C错误;酚酞中含有亲水基和憎水基,但憎水基对其溶解性的影响能力大于亲水基,则常温下酚酞难溶于水,D错误。
典例9 C 【解析】 100 mL(即100 g)水中溶解的苯酚小于20 g,A正确;Fe3+的价层电子排布式为3d5,可提供空轨道,形成配离子[Fe(C6H5O)6]3-,溶液显紫色,B正确;苯酚与少量浓溴水反应生成的2,4,6-三溴苯酚可溶于过量的苯酚溶液中,故观察不到白色沉淀,C错误;苯酚显弱酸性,易与NaOH溶液反应生成易溶于水的苯酚钠,已知酸性:H2CO3>苯酚>HCO,则向苯酚钠溶液中通入少量CO2可生成苯酚和NaHCO3,D正确。
考点3
[知识梳理]
知识1
1. 烃基(或氢原子) 醛基 (酮)羰基 两个烃基 醛基 (酮)羰基 CH3COONH4+2Ag↓+3NH3+H2O CH3COONa+Cu2O↓+3H2O CH3CH2OH
知识2 恰好完全 过量
[典题悟法]
典例10 A 【解析】 X分子中的醛基和酯基中含有碳氧π键,故1 mol X中含有2 mol碳氧π键,A错误;X分子中含有碳碳双键,双键碳原子的两端所连基团各不相同,存在顺反异构体,B正确;Y分子的含N六元环是对称结构,该分子中没有手性碳原子,C正确;X分子中含有醛基,Y分子中没有醛基,可以用新制的Cu(OH)2检验Y中是否含有X,D正确。
典例11 C 【解析】 X分子中没有手性碳原子,A错误;X生成Y的中间产物为,B错误;Y分子中含有两个碳碳双键,发生1,2-加成的产物有2种,发生1,4-加成反应的产物有1种,C正确;X、Y分子中都含有碳碳双键,不能用酸性高锰酸钾溶液鉴别,D错误。
考点4
[知识梳理]
知识
烃基(或氢原子) 羧基 —OH —OR′ CnH2nO2 CnH2nO2 RCOOH+R′OH RCOONa+R′OH
解疑释惑38
1. ① > > ② > > ③ >
[典题悟法]
典例12 D 【解析】 乙酸的电离,断裂羧基中O—H,即a键断裂,①正确;酯化反应中酸去羟基、醇去氢,即b键断裂,②正确;在红磷存在时,Br2可与CH3COOH发生取代反应,甲基上H被取代,C—H断裂,即c键断裂,③正确;乙酸变成乙酸酐时,—COOH中的C—O、O—H断裂,即a、b键断裂,④正确;故选D。
典例13 A 【解析】 CH3COOH酸性弱于HCOOH,说明CH3COOH分子存在斥电子基团,能减弱—OH上H原子的活性而使该物质的酸性减弱,乙酸中含有—CH3,所以—CH3属于斥电子基团,导致乙酸的酸性小于甲酸,B错误;氯乙酸(CH2ClCOOH)的酸性强于乙酸,所以相同温度下,等物质的量浓度的CH2ClCOONa溶液的pH将比CH3CH2COONa的pH小,C错误;“诱导效应”说明有机化合物的性质不仅决定于官能团的结构,也会受所连取代基的影响,D错误。
典例14 D 【解析】 X中醛基上含有碳氧π键,1 mol X中含有1 mol碳氧π键,A错误;连接4个不同基团的碳原子为手性碳原子,Y中碳碳双键与HBr发生加成反应,加成后与溴原子直接相连的碳原子为手性碳原子,B错误;Y含羟基、羧基,均为亲水基,Z含羟基、酯基,酯基为疏水基,则Y在水中的溶解度更大,C错误;羟基、醛基、碳碳双键均可被酸性高锰酸钾溶液氧化,则X、Y、Z分别与足量酸性KMnO4溶液反应所得芳香族化合物均为对苯二甲酸,D正确。
典例15 B 【解析】 浓硫酸是酯化反应的催化剂,能加快酯化反应速率,A正确;温度过高,反应物挥发较多,且会发生副反应,采用水浴加热,可以受热均匀、便于控制温度,B错误,C正确;饱和碳酸钠溶液可中和乙酸、溶解乙醇、降低乙酸乙酯的溶解度,使得乙酸乙酯更加纯净,D正确。
典例16 C 【解析】 X分子中含有(酮)羰基、醚键、酯基3种含氧官能团,A错误;Y分子中的酚羟基以及酚酯基都能与NaOH反应,故1 mol Y与足量NaOH溶液反应,消耗3 mol NaOH,B错误;Z分子中酚羟基的邻、对位上都含有基团,Z分子不能与HCHO发生缩聚反应,D错误。
考点5
[知识梳理]
知识1 2. RNH2 R2NH R3N
[典题悟法]
典例17 A 【解析】 硝基、酯基都不是亲水基团,X难溶于水,B错误;酰胺键和酯基都能与NaOH反应,故1 mol Z最多能与2 mol NaOH反应,C错误;X生成Y的反应为还原反应,Y生成Z的反应为取代反应,D错误。
典例18 B 【解析】 X的化学式为C10H13O2N,A错误;Y分子中含有连接2个甲基的碳原子,故所有碳原子不可能在同一平面上,B正确;Z分子中酚羟基的对位和1个邻位有取代基,故在催化剂作用下不能与HCHO发生缩聚反应,C错误;Y、Z分子中均含酚羟基,能与FeCl3溶液发生显色反应,酚羟基的酸性较弱,不能和NaHCO3反应,D错误。
[质量评价]
1. D 【解析】 Y与Z分子均不存在顺反异构体,A错误;X、Y均含醛基,且酚羟基、碳碳双键均能使酸性高锰酸钾溶液褪色,不能鉴别,B错误;X含羟基、醛基,且不含其他烃基,则X在水中的溶解度最大,C错误;Z与足量H2加成后的产物如图:(标“*”碳原子为手性碳原子),有3个手性碳原子,D正确。
2. C 【解析】 X分子中含有酮羰基,能与CH3CH2MgBr发生加成反应,A正确;Y分子中,与—OH相连的碳原子为手性碳原子,则Y分子存在对映异构现象,B正确;Z分子中,含有—CH2Cl、—CH3,它们都形成四面体形结构,所有原子不可能处于同一平面上,C错误;Z分子中含有碳碳双键,能与溴发生加成反应,所以Y、Z可用溴的四氯化碳溶液鉴别,D正确。
3. A 【解析】 甲基的对位基团与苯环直接相连的C原子为手性碳原子,X分子中只有1个手性碳原子,A正确;与溴原子相连的β-C上无氢原子,不能发生消去反应,B错误;Z中的含氧官能团为酯基,C错误;溴原子、酯基可以和氢氧化钠发生反应,1 mol Z最多能与2 mol NaOH反应,D错误。
4. B 【解析】 X分子中最多有20个原子共平面 ,A错误;X分子能与NaHCO3溶液反应,有气泡产生,而Y分子不能与NaHCO3溶液反应,B正确;Z分子中与碳碳双键两端碳原子相连基团各不相同,故Z分子存在顺反异构体,C错误; 1 mol Z最多能与7 mol H2发生加成反应,D错误。
同课章节目录
