5.1 原子的结构 课件(共25张PPT)课件 2024-2025学年高二物理粤教版(2019)选择性必修3
文档属性
| 名称 | 5.1 原子的结构 课件(共25张PPT)课件 2024-2025学年高二物理粤教版(2019)选择性必修3 |

|
|
| 格式 | pptx | ||
| 文件大小 | 3.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版(2019) | ||
| 科目 | 物理 | ||
| 更新时间 | 2025-04-17 00:00:00 | ||
图片预览





文档简介
(共25张PPT)
第五章 原子与原子核
第一节 原子的结构
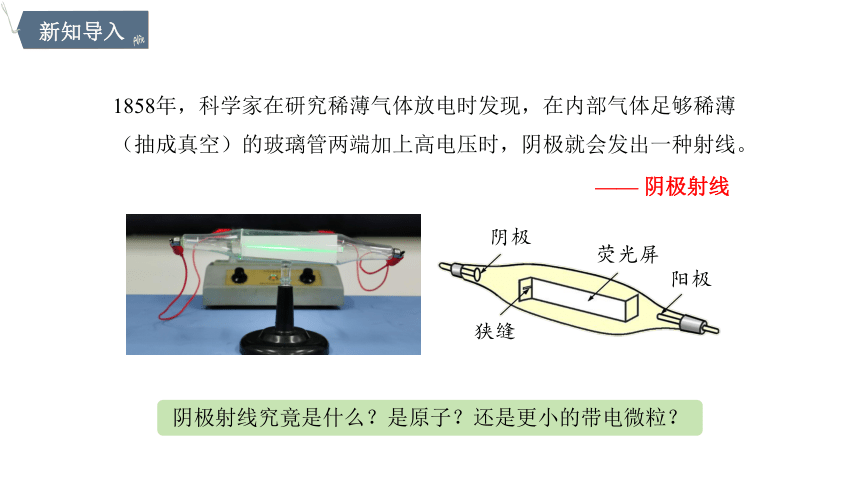
1858年,科学家在研究稀薄气体放电时发现,在内部气体足够稀薄(抽成真空)的玻璃管两端加上高电压时,阴极就会发出一种射线。
阳极
荧光屏
狭缝
阴极
—— 阴极射线
阴极射线究竟是什么?是原子?还是更小的带电微粒?
1.了解α粒子散射实验原理和实验现象;
2.了解卢瑟福的原子核式结构模型,
3.了解玻尔原子理论的基本假设的主要内容。
4.能用玻尔原子理论解释氢原子能级图及光谱。
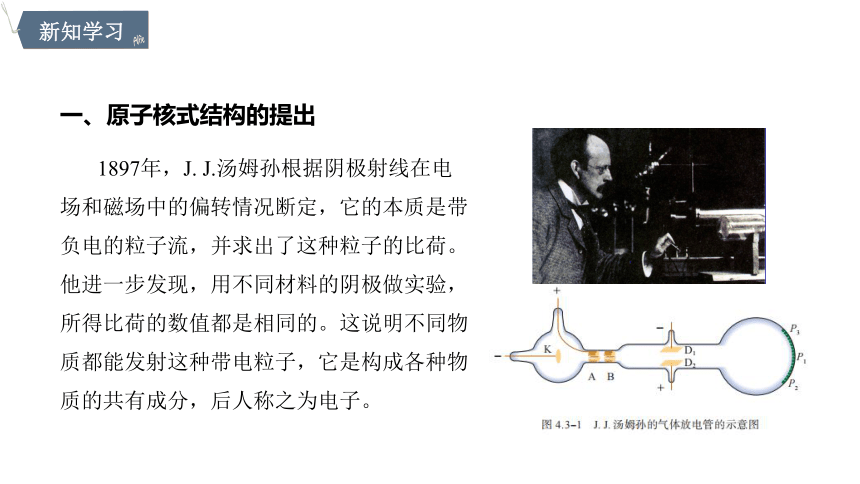
1897年,J. J.汤姆孙根据阴极射线在电场和磁场中的偏转情况断定,它的本质是带负电的粒子流,并求出了这种粒子的比荷。他进一步发现,用不同材料的阴极做实验,所得比荷的数值都是相同的。这说明不同物质都能发射这种带电粒子,它是构成各种物质的共有成分,后人称之为电子。
一、原子核式结构的提出
随着人们认为组成阴极射线的成分是电子,有关于电子理论的完善从未停止;
密立根通过著名的“油滴实验”精确测定了电子的电荷量:
而且电荷是量子化的;
电子的发现的意义:打破了传统的“原子不可分”的观念。
电子的发现打破了传统的“原子不可分”的观念,使人类对自然世界的认识又向前迈进了一步,也大大激发了人们研究原子内部结构的热情。由于原子呈电中性,既然电子带负电,那么原子内部一定还有带正电的部分.J.J.汤姆孙据此提出了一种原子结构模型.他设想原子是一个球体,正电荷均匀地分布在其中,质量很小的电子镶嵌其中(如图5-1-1所示)。有人形象地称其为“枣糕模型”,如图所示”。J.J.汤姆孙的模型能够解释一些实验事实,但是不久就被新的实验事实所否定
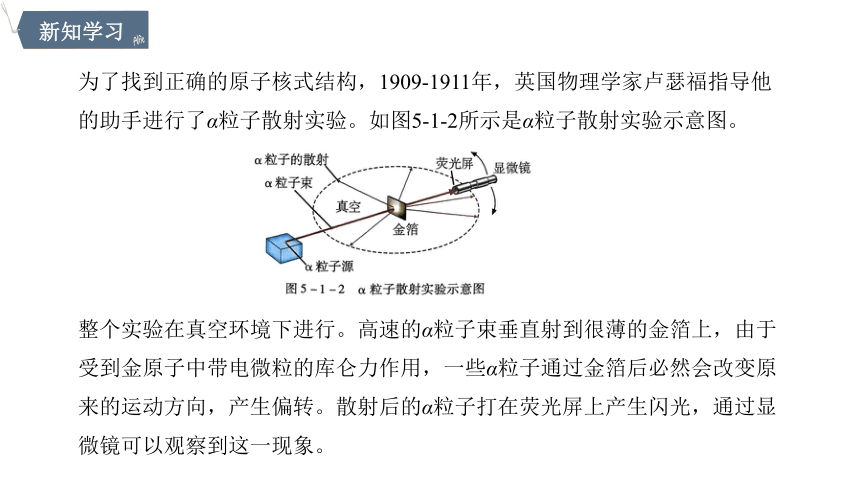
为了找到正确的原子核式结构,1909-1911年,英国物理学家卢瑟福指导他的助手进行了α粒子散射实验。如图5-1-2所示是α粒子散射实验示意图。
整个实验在真空环境下进行。高速的α粒子束垂直射到很薄的金箔上,由于受到金原子中带电微粒的库仑力作用,一些α粒子通过金箔后必然会改变原来的运动方向,产生偏转。散射后的α粒子打在荧光屏上产生闪光,通过显微镜可以观察到这一现象。
实验结果出人意料:绝大多数α粒子穿过金箔后仍沿原来的方向前进,但少数α粒子发生了较大的偏转,并且有极少数α粒子的偏转超过了90°,有的甚至达到180°。
为什么α粒子会出现大角度偏转呢?
卢瑟福认为,α粒子一定是受到原子内部正电荷产生的极强的电场斥力作用,运动方向才会发生如此大的改变,只有原子中的正电荷全部都集中在原子中心的一个很小的区域上,才有可能产生这种现象。
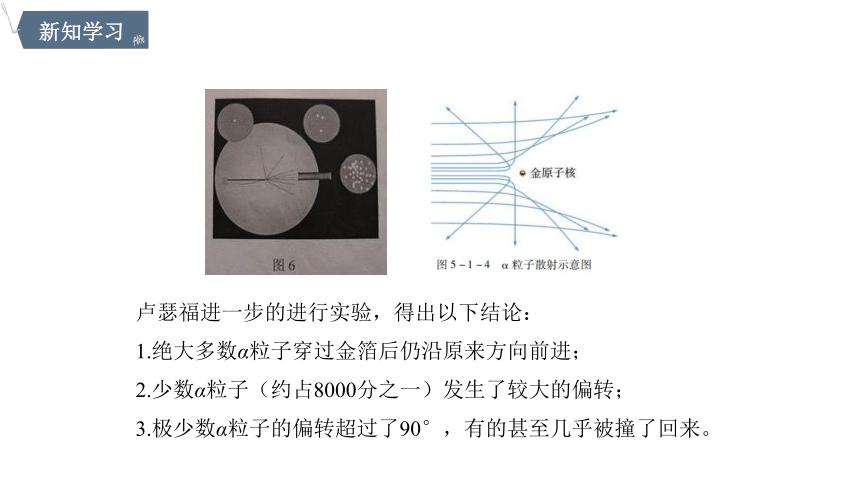
卢瑟福进一步的进行实验,得出以下结论:
1.绝大多数α粒子穿过金箔后仍沿原来方向前进;
2.少数α粒子(约占8000分之一)发生了较大的偏转;
3.极少数α粒子的偏转超过了90°,有的甚至几乎被撞了回来。
1911年,卢瑟福提出了原子的核式结构模型,得到了广泛的认同,模型内容如下:
1.原子核:原子中心有一个很小的核,集中了原子的全部正电荷和几乎全部质量。
2.带负电的电子在核外空间绕着核旋转。
二、氢原子光谱
早在17世纪,牛顿就发现了日光通过三棱镜后的色散现象,并把实验中得到的彩色光带叫做光谱。
1.发射光谱:
物体发光直接产生的光谱叫做发射光谱,发射光谱又分为两种:其一是连续光谱,其二是线状光谱。
①连续光谱:由波长连续分布的光组成的连在一起的光带叫连续光谱。
特点:光谱看起来不是一条条分立的谱线,而是连在一起的光带。
炽热的固体、液体和高压气体的发射光谱是连续光谱。
例如白炽灯丝发出的光、烛焰、炽热的钢水发出的光都形成连续光谱。
②线状光谱:只含有一些不连续的亮线的光谱叫做线状光谱。
线状光谱中的亮线叫谱线,各条谱线对应不同波长的光。
稀薄气体或金属的蒸气的发射光谱是明线光谱。
各种原子的发射光谱都是线状谱。
各种元素都只能发出具有本身特征的某些波长的光,明线光谱的谱线也叫原子的特征谱线。
除了发射光谱以外,还有着吸收光谱。高温物体发出的白光(其中包含连续分布的一切波长的光)通过物质时,某些波长的光被物质吸收后产生的光谱,叫做吸收光谱。
2.吸收光谱
三、原子的能级结构
丹麦物理学家玻尔在普朗克、爱因斯坦量子概念的启发下提出:电子绕原子核运动的轨道半径是分立的,电子只能在某些特定的轨道上运动。当电子在不同的轨道上运动时,原子处于不同的状态,具有不同的能量。这些分立的能量值被称为原子的能级。原子从一个能级变化到另一个能级的过程叫作跃迁。
处于高能级的原子会自发地向低能级跃迁,并且在这个过程中辐射光子,如图所示。
(1)自发跃迁:处于高能级的原子不稳定会自发地向低能级跃迁。同时辐射光子。
假定原子在跃迁前后的能级分别为Em和En,根据能量守恒定律,并结合爱因斯坦光子说,可得到辐射出光子的能量为:
(2)激发跃迁:原子吸收了特定的光子或其他途径获得能量时,低能级的原子会受激发地向高能级跃迁。
氢原子的能级结构
激发态:当电子受到外界激发时,可从外界吸收能量,并从基态跃迁到较高能级上,这些能级对应的状态称为激发态。
基态:在正常情况下,氢原子处于最低的能级,这个最低能级E1(n=1)对应的状态称为基态。
氢原子能级的跃迁条件
光子的能量:E=hv
如果电子想从n=1跃迁到n=2的轨道
E2-E1=10.2eV
如果电子想从n=1跃迁到n=3的轨道
E3-E1=12.09eV
则原子需要刚好吸收12.09eV的能量
实物粒子
玻尔的原子理论成功地解释了氢原子光谱的实验规律,是原子结构理论发展中的一个重大进展,但对于稍微复杂一点的原子,例如氦原子,就无法解释它的光谱现象。玻尔理论的局限性主要在于其保留了经典粒子的观念,把电子的运动仍然看做为经典理论下的轨道运动。我们知道,波粒二象性是包括电子在内的一切微观粒子的共同特征。对于电子的运动,我们只能用概率波对其作统计性的描述。当原子处于不同的状态时,电子在原子核周围各处出现的概率不同。图5-1-10氢原子处于基态时的电子云若用疏密不同的点表示电子在各处出现的概率,这样画出的概率分布图称为电子云。
1. (多选)关于α粒子散射实验,下列说法正确的是( )
A.绝大多数α粒穿过金箔后,发生了较大角度的偏转
B.极少数α粒子的偏转角度甚至大于90°
C.根据实验现象可知原子结构不是“西瓜模型”或“枣糕模型”
D.α粒子发生偏转的原因是由于受到金箔中电子的作用
BC
2.卢瑟福的α粒子散射实验装置如图所示,开有小孔的铅盒里面包裹着少量的放射性元素钋。铅能够很好地吸收α粒子,使得α粒子只能从小孔射出,形成一束很细的射线射到金箔上,最后打在荧光屏上产生闪烁的光点。下列说法正确的是( )
A.α粒子碰撞到了电子会反向弹回
B.极少数α粒子发生了大角度偏转
C.该实验为汤姆孙的“枣糕模型”奠定了基础
D.该实验说明原子具有核式结构,负电荷集中在原子中心
B
3.α粒子散射实验被评为世界十大经典物理实验之一,此实验开创了原子结构研究的先河,为建立现代原子核理论打下了基础,关于α粒子散射实验,下列说法正确的是( )
A.汤姆孙的α粒子散射实验,证明了原子核是可以再分的
B.该实验的数据否定了卢瑟福的“西瓜模型”,并估算了原子的大小
C.该实验表明原子中心有一个极大的核,它占有原子体积的极大部分
D.该实验表明占原子质量绝大部分的带正电的物质集中在很小的空间范围内
D
4.(多选)氢原子各个能级的能量如图所示,大量氢原子由n=1能级跃迁到n=4能级,在它回到n=1能级过程中,下列说法中正确的是( )
A.可能激发出频率不同的光子只有6种
B.可能激发出频率不同的光子只有3种
C.可能激发出的光子的最大能量为12.75 eV
D.可能激发出的光子的最大能量为0.66 eV
AC
第五章 原子与原子核
第一节 原子的结构
1858年,科学家在研究稀薄气体放电时发现,在内部气体足够稀薄(抽成真空)的玻璃管两端加上高电压时,阴极就会发出一种射线。
阳极
荧光屏
狭缝
阴极
—— 阴极射线
阴极射线究竟是什么?是原子?还是更小的带电微粒?
1.了解α粒子散射实验原理和实验现象;
2.了解卢瑟福的原子核式结构模型,
3.了解玻尔原子理论的基本假设的主要内容。
4.能用玻尔原子理论解释氢原子能级图及光谱。
1897年,J. J.汤姆孙根据阴极射线在电场和磁场中的偏转情况断定,它的本质是带负电的粒子流,并求出了这种粒子的比荷。他进一步发现,用不同材料的阴极做实验,所得比荷的数值都是相同的。这说明不同物质都能发射这种带电粒子,它是构成各种物质的共有成分,后人称之为电子。
一、原子核式结构的提出
随着人们认为组成阴极射线的成分是电子,有关于电子理论的完善从未停止;
密立根通过著名的“油滴实验”精确测定了电子的电荷量:
而且电荷是量子化的;
电子的发现的意义:打破了传统的“原子不可分”的观念。
电子的发现打破了传统的“原子不可分”的观念,使人类对自然世界的认识又向前迈进了一步,也大大激发了人们研究原子内部结构的热情。由于原子呈电中性,既然电子带负电,那么原子内部一定还有带正电的部分.J.J.汤姆孙据此提出了一种原子结构模型.他设想原子是一个球体,正电荷均匀地分布在其中,质量很小的电子镶嵌其中(如图5-1-1所示)。有人形象地称其为“枣糕模型”,如图所示”。J.J.汤姆孙的模型能够解释一些实验事实,但是不久就被新的实验事实所否定
为了找到正确的原子核式结构,1909-1911年,英国物理学家卢瑟福指导他的助手进行了α粒子散射实验。如图5-1-2所示是α粒子散射实验示意图。
整个实验在真空环境下进行。高速的α粒子束垂直射到很薄的金箔上,由于受到金原子中带电微粒的库仑力作用,一些α粒子通过金箔后必然会改变原来的运动方向,产生偏转。散射后的α粒子打在荧光屏上产生闪光,通过显微镜可以观察到这一现象。
实验结果出人意料:绝大多数α粒子穿过金箔后仍沿原来的方向前进,但少数α粒子发生了较大的偏转,并且有极少数α粒子的偏转超过了90°,有的甚至达到180°。
为什么α粒子会出现大角度偏转呢?
卢瑟福认为,α粒子一定是受到原子内部正电荷产生的极强的电场斥力作用,运动方向才会发生如此大的改变,只有原子中的正电荷全部都集中在原子中心的一个很小的区域上,才有可能产生这种现象。
卢瑟福进一步的进行实验,得出以下结论:
1.绝大多数α粒子穿过金箔后仍沿原来方向前进;
2.少数α粒子(约占8000分之一)发生了较大的偏转;
3.极少数α粒子的偏转超过了90°,有的甚至几乎被撞了回来。
1911年,卢瑟福提出了原子的核式结构模型,得到了广泛的认同,模型内容如下:
1.原子核:原子中心有一个很小的核,集中了原子的全部正电荷和几乎全部质量。
2.带负电的电子在核外空间绕着核旋转。
二、氢原子光谱
早在17世纪,牛顿就发现了日光通过三棱镜后的色散现象,并把实验中得到的彩色光带叫做光谱。
1.发射光谱:
物体发光直接产生的光谱叫做发射光谱,发射光谱又分为两种:其一是连续光谱,其二是线状光谱。
①连续光谱:由波长连续分布的光组成的连在一起的光带叫连续光谱。
特点:光谱看起来不是一条条分立的谱线,而是连在一起的光带。
炽热的固体、液体和高压气体的发射光谱是连续光谱。
例如白炽灯丝发出的光、烛焰、炽热的钢水发出的光都形成连续光谱。
②线状光谱:只含有一些不连续的亮线的光谱叫做线状光谱。
线状光谱中的亮线叫谱线,各条谱线对应不同波长的光。
稀薄气体或金属的蒸气的发射光谱是明线光谱。
各种原子的发射光谱都是线状谱。
各种元素都只能发出具有本身特征的某些波长的光,明线光谱的谱线也叫原子的特征谱线。
除了发射光谱以外,还有着吸收光谱。高温物体发出的白光(其中包含连续分布的一切波长的光)通过物质时,某些波长的光被物质吸收后产生的光谱,叫做吸收光谱。
2.吸收光谱
三、原子的能级结构
丹麦物理学家玻尔在普朗克、爱因斯坦量子概念的启发下提出:电子绕原子核运动的轨道半径是分立的,电子只能在某些特定的轨道上运动。当电子在不同的轨道上运动时,原子处于不同的状态,具有不同的能量。这些分立的能量值被称为原子的能级。原子从一个能级变化到另一个能级的过程叫作跃迁。
处于高能级的原子会自发地向低能级跃迁,并且在这个过程中辐射光子,如图所示。
(1)自发跃迁:处于高能级的原子不稳定会自发地向低能级跃迁。同时辐射光子。
假定原子在跃迁前后的能级分别为Em和En,根据能量守恒定律,并结合爱因斯坦光子说,可得到辐射出光子的能量为:
(2)激发跃迁:原子吸收了特定的光子或其他途径获得能量时,低能级的原子会受激发地向高能级跃迁。
氢原子的能级结构
激发态:当电子受到外界激发时,可从外界吸收能量,并从基态跃迁到较高能级上,这些能级对应的状态称为激发态。
基态:在正常情况下,氢原子处于最低的能级,这个最低能级E1(n=1)对应的状态称为基态。
氢原子能级的跃迁条件
光子的能量:E=hv
如果电子想从n=1跃迁到n=2的轨道
E2-E1=10.2eV
如果电子想从n=1跃迁到n=3的轨道
E3-E1=12.09eV
则原子需要刚好吸收12.09eV的能量
实物粒子
玻尔的原子理论成功地解释了氢原子光谱的实验规律,是原子结构理论发展中的一个重大进展,但对于稍微复杂一点的原子,例如氦原子,就无法解释它的光谱现象。玻尔理论的局限性主要在于其保留了经典粒子的观念,把电子的运动仍然看做为经典理论下的轨道运动。我们知道,波粒二象性是包括电子在内的一切微观粒子的共同特征。对于电子的运动,我们只能用概率波对其作统计性的描述。当原子处于不同的状态时,电子在原子核周围各处出现的概率不同。图5-1-10氢原子处于基态时的电子云若用疏密不同的点表示电子在各处出现的概率,这样画出的概率分布图称为电子云。
1. (多选)关于α粒子散射实验,下列说法正确的是( )
A.绝大多数α粒穿过金箔后,发生了较大角度的偏转
B.极少数α粒子的偏转角度甚至大于90°
C.根据实验现象可知原子结构不是“西瓜模型”或“枣糕模型”
D.α粒子发生偏转的原因是由于受到金箔中电子的作用
BC
2.卢瑟福的α粒子散射实验装置如图所示,开有小孔的铅盒里面包裹着少量的放射性元素钋。铅能够很好地吸收α粒子,使得α粒子只能从小孔射出,形成一束很细的射线射到金箔上,最后打在荧光屏上产生闪烁的光点。下列说法正确的是( )
A.α粒子碰撞到了电子会反向弹回
B.极少数α粒子发生了大角度偏转
C.该实验为汤姆孙的“枣糕模型”奠定了基础
D.该实验说明原子具有核式结构,负电荷集中在原子中心
B
3.α粒子散射实验被评为世界十大经典物理实验之一,此实验开创了原子结构研究的先河,为建立现代原子核理论打下了基础,关于α粒子散射实验,下列说法正确的是( )
A.汤姆孙的α粒子散射实验,证明了原子核是可以再分的
B.该实验的数据否定了卢瑟福的“西瓜模型”,并估算了原子的大小
C.该实验表明原子中心有一个极大的核,它占有原子体积的极大部分
D.该实验表明占原子质量绝大部分的带正电的物质集中在很小的空间范围内
D
4.(多选)氢原子各个能级的能量如图所示,大量氢原子由n=1能级跃迁到n=4能级,在它回到n=1能级过程中,下列说法中正确的是( )
A.可能激发出频率不同的光子只有6种
B.可能激发出频率不同的光子只有3种
C.可能激发出的光子的最大能量为12.75 eV
D.可能激发出的光子的最大能量为0.66 eV
AC
同课章节目录
- 第一章 分子动理论
- 第一节 物质是由大量分子组成的
- 第二节 分子热运动与分子力
- 第三节 气体分子运动的统计规律
- 第二章 气体、液体和固态
- 第一节 气体实验定律(Ⅰ)
- 第二节 气体实验定律(Ⅱ)
- 第三节 气体实验定律的微观解释
- 第四节 液体的表面张力
- 第五节 晶体
- 第六节 新材料
- 第三章 热力学定律
- 第一节 热力学第一定律
- 第二节 能量守恒定律及其应用
- 第三节 热力学第二定律
- 第四章 波粒二象性
- 第一节 光电效应
- 第二节 光电效应方程及其意义
- 第三节 光的波粒二象性
- 第四节 德布罗意波
- 第五节 不确定性关系
- 第五章 原子与原子核
- 第一节 原子的结构
- 第二节 放射性元素的衰变
- 第三节 核力与核反应方程
- 第四节 放射性同位素
- 第五节 裂变和聚变
