2.1.2 键参数 课件 (共15张PPT)
文档属性
| 名称 | 2.1.2 键参数 课件 (共15张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 995.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-18 00:00:00 | ||
图片预览






文档简介
(共15张PPT)
第一节 共价键
第1课时 键参数——键长、键能、键角
第二章 分子结构与性质
键参数1 —— 键能
1、概念:气态分子中 1 mol 化学键解离成气态原子所吸收的能量
2、单位:kJ mol-1
3、意义:键能越大,共价键越牢固,由此形成的分子越稳定。
键能
【补充说明】
通常是298.15 K(25 ℃)、101 kPa条件下的标准值,
可通过实验测定,更多的却是推算获得的,键能数据是平均值。
键能
键 键能
H-F 568
H-Cl 431.8
H-Br 366
H-I 298.7
C-C 347.7
C=C 615
C≡C 812
C-O 351
C=O 745
N-N 193
N=N 418
N≡N 946
观察下表,并找出键能数据中存在的规律
思考1
①、原子半径越长、键能越小
②、相同原子成键时,键能:单键<双键<三键
③、双键键能并不是单键的两倍
(原因:σ键 和 π键 键能不相等)
原因:
通常情况:σ键> π键; N与N之间:σ键< π键
④、通常情况下,双键键能 < 单键的两倍
N原子特殊:N=N > N-N的两倍
键能
键能的
应用
定量衡量共价键强弱
判断分子的稳定性
估算化学反应热效应
键能越大,共价键越牢固
一般来说,结构相似的分子,
共价键的键能越大,分子越稳定
ΔH=反应物的总键能-生成物的总键能
键能
【例1】正误判断
(1)N—H的键能是很多分子中的N—H的键能的平均值( )
(2)O—H的键能是指在298.15 K、101 kPa下,气态分子中1 mol O—H解离成气态原子所吸收的能量( )
(3)C=C的键能等于C—C的键能的2倍( )
(4)σ键一定比π键牢固( )
√
√
×
×
小于
不一定
键能
【例2】某些化学键的键能(kJ·mol-1)如下表所示。
(1)1 mol H2在2 mol Cl2中燃烧,放出热量______ kJ。
184.9
化学键 H—H Cl—Cl Br—Br I—I H—Cl H—Br H—I
键能 436 242.7 193 151 431.8 363 297
(2)在一定条件下,1 mol H2与足量的Cl2、Br2、I2分别反应,放出热量由多到少的顺序是____(填字母)。
a.Cl2>Br2>I2 b.I2>Br2>Cl2 c.Br2>I2>Cl2
预测1 mol H2在足量F2中燃烧比在Cl2中燃烧放热____(填“多”或“少”)。
a
多
键长
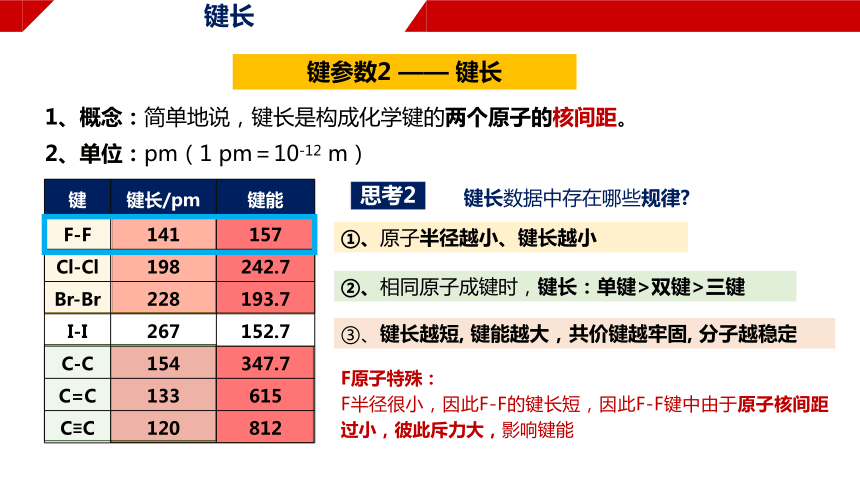
键参数2 —— 键长
1、概念:简单地说,键长是构成化学键的两个原子的核间距。
2、单位:pm(1 pm=10-12 m)
键 键长/pm 键能
F-F 141 157
Cl-Cl 198 242.7
Br-Br 228 193.7
I-I 267 152.7
C-C 154 347.7
C=C 133 615
C≡C 120 812
键长数据中存在哪些规律
思考2
①、原子半径越小、键长越小
②、相同原子成键时,键长:单键>双键>三键
③、键长越短, 键能越大,共价键越牢固, 分子越稳定
F原子特殊:
F半径很小,因此F-F的键长短,因此F-F键中由于原子核间距过小,彼此斥力大,影响键能
共价键稳定性强弱
判断方法
原子半径越小
共用电子对数越多
共价键越牢固
键能越大
共价键越牢固
共价键越牢固
键长越短
键长
根据原子半径和
共用电子对数目判断
根据键能判断
根据键长判断
【例3】下列说法正确的是( )
A、在分子中,两个成键的原子间的距离叫键长
B、键长:N—H>P—H
C、H-Cl的键能为431.8 kJ·mol-1,H-Br的键能为366 kJ·mol-1,这可以说明HCl比HBr分子稳定
D、键能越大,表示该分子越容易受热分解
C
键能越大,越不易分解
键能越大,含有该键的物质越稳定
半径越大,键长越长,原子半径:P>N
核间距
键长
键角
1、概念:两个相邻共价键之间的夹角称为键角。
2、意义:键角可反映分子的立体构型,是描述分子立体结构的重要参数,可进一步帮助我们判断分子的极性。
3、常见分子的键角
键参数3 —— 键角
H2O : 105°
V形(角形)
NH3 : 107°
三角锥形
CO2: 180°
直线形
CH4 : 109°28′
正四面体形
【课堂拓展】防晒霜的防晒原理
波长为 300 nm 的紫外光的光子所具有的能量约为 399 kJ mol-1,这一能量比蛋白质分子中重要的化学键C一C键、C-N 键和C—S 键的键能都大。因此,紫外光的能量足以使这些化学键断裂,从而破坏蛋白质分子。
防晒霜之所以能有效地减轻紫外光对人体的伤害,其原因之一是它的有效成分的分子中含有π键。这些分子中的π键的电子在吸收紫外光后被激发,从而能阻挡部分紫外光。
课堂拓展
【例4】关于键长、键能和键角,下列说法不正确的是
A.键长越长,键能越大,共价化合物越稳定
B.通过反应物和生成物分子中键能数据可以粗略预测反应热的大小
C.键角是确定多分子立体结构的重要参数
D.同种原子间形成的共价键键长:三键<双键<单键
课堂练习
A
【例5】氰气的化学式为(CN)2,结构式为N≡C-C≡N,性质与卤素相似。下列说法正确的是
A.不和氢氧化钠溶液发生反应
B.分子中N≡C的键长大于C-C的键长
C.分子中含有两个σ键和四个π键
D.分子中既有极性键又有非极性键
课堂练习
D
【例6】下列关于乙烷和乙烯的说法正确的是
A.二者的键角均相等
B.二者σ键个数之比为7:5
C.二者的键长均相等
D.碳碳键的键能后者是前者的两倍
课堂练习
B
【例7】下列说法中正确的是( )
A.双原子分子中化学键键能越大,分子越稳定
B.双原子分子中化学键键长越长,分子越稳定
C.双原子分子中化学键键角越大,分子越稳定
D.在双键中,σ键的键能要小于π键的键能
课堂练习
A
第一节 共价键
第1课时 键参数——键长、键能、键角
第二章 分子结构与性质
键参数1 —— 键能
1、概念:气态分子中 1 mol 化学键解离成气态原子所吸收的能量
2、单位:kJ mol-1
3、意义:键能越大,共价键越牢固,由此形成的分子越稳定。
键能
【补充说明】
通常是298.15 K(25 ℃)、101 kPa条件下的标准值,
可通过实验测定,更多的却是推算获得的,键能数据是平均值。
键能
键 键能
H-F 568
H-Cl 431.8
H-Br 366
H-I 298.7
C-C 347.7
C=C 615
C≡C 812
C-O 351
C=O 745
N-N 193
N=N 418
N≡N 946
观察下表,并找出键能数据中存在的规律
思考1
①、原子半径越长、键能越小
②、相同原子成键时,键能:单键<双键<三键
③、双键键能并不是单键的两倍
(原因:σ键 和 π键 键能不相等)
原因:
通常情况:σ键> π键; N与N之间:σ键< π键
④、通常情况下,双键键能 < 单键的两倍
N原子特殊:N=N > N-N的两倍
键能
键能的
应用
定量衡量共价键强弱
判断分子的稳定性
估算化学反应热效应
键能越大,共价键越牢固
一般来说,结构相似的分子,
共价键的键能越大,分子越稳定
ΔH=反应物的总键能-生成物的总键能
键能
【例1】正误判断
(1)N—H的键能是很多分子中的N—H的键能的平均值( )
(2)O—H的键能是指在298.15 K、101 kPa下,气态分子中1 mol O—H解离成气态原子所吸收的能量( )
(3)C=C的键能等于C—C的键能的2倍( )
(4)σ键一定比π键牢固( )
√
√
×
×
小于
不一定
键能
【例2】某些化学键的键能(kJ·mol-1)如下表所示。
(1)1 mol H2在2 mol Cl2中燃烧,放出热量______ kJ。
184.9
化学键 H—H Cl—Cl Br—Br I—I H—Cl H—Br H—I
键能 436 242.7 193 151 431.8 363 297
(2)在一定条件下,1 mol H2与足量的Cl2、Br2、I2分别反应,放出热量由多到少的顺序是____(填字母)。
a.Cl2>Br2>I2 b.I2>Br2>Cl2 c.Br2>I2>Cl2
预测1 mol H2在足量F2中燃烧比在Cl2中燃烧放热____(填“多”或“少”)。
a
多
键长
键参数2 —— 键长
1、概念:简单地说,键长是构成化学键的两个原子的核间距。
2、单位:pm(1 pm=10-12 m)
键 键长/pm 键能
F-F 141 157
Cl-Cl 198 242.7
Br-Br 228 193.7
I-I 267 152.7
C-C 154 347.7
C=C 133 615
C≡C 120 812
键长数据中存在哪些规律
思考2
①、原子半径越小、键长越小
②、相同原子成键时,键长:单键>双键>三键
③、键长越短, 键能越大,共价键越牢固, 分子越稳定
F原子特殊:
F半径很小,因此F-F的键长短,因此F-F键中由于原子核间距过小,彼此斥力大,影响键能
共价键稳定性强弱
判断方法
原子半径越小
共用电子对数越多
共价键越牢固
键能越大
共价键越牢固
共价键越牢固
键长越短
键长
根据原子半径和
共用电子对数目判断
根据键能判断
根据键长判断
【例3】下列说法正确的是( )
A、在分子中,两个成键的原子间的距离叫键长
B、键长:N—H>P—H
C、H-Cl的键能为431.8 kJ·mol-1,H-Br的键能为366 kJ·mol-1,这可以说明HCl比HBr分子稳定
D、键能越大,表示该分子越容易受热分解
C
键能越大,越不易分解
键能越大,含有该键的物质越稳定
半径越大,键长越长,原子半径:P>N
核间距
键长
键角
1、概念:两个相邻共价键之间的夹角称为键角。
2、意义:键角可反映分子的立体构型,是描述分子立体结构的重要参数,可进一步帮助我们判断分子的极性。
3、常见分子的键角
键参数3 —— 键角
H2O : 105°
V形(角形)
NH3 : 107°
三角锥形
CO2: 180°
直线形
CH4 : 109°28′
正四面体形
【课堂拓展】防晒霜的防晒原理
波长为 300 nm 的紫外光的光子所具有的能量约为 399 kJ mol-1,这一能量比蛋白质分子中重要的化学键C一C键、C-N 键和C—S 键的键能都大。因此,紫外光的能量足以使这些化学键断裂,从而破坏蛋白质分子。
防晒霜之所以能有效地减轻紫外光对人体的伤害,其原因之一是它的有效成分的分子中含有π键。这些分子中的π键的电子在吸收紫外光后被激发,从而能阻挡部分紫外光。
课堂拓展
【例4】关于键长、键能和键角,下列说法不正确的是
A.键长越长,键能越大,共价化合物越稳定
B.通过反应物和生成物分子中键能数据可以粗略预测反应热的大小
C.键角是确定多分子立体结构的重要参数
D.同种原子间形成的共价键键长:三键<双键<单键
课堂练习
A
【例5】氰气的化学式为(CN)2,结构式为N≡C-C≡N,性质与卤素相似。下列说法正确的是
A.不和氢氧化钠溶液发生反应
B.分子中N≡C的键长大于C-C的键长
C.分子中含有两个σ键和四个π键
D.分子中既有极性键又有非极性键
课堂练习
D
【例6】下列关于乙烷和乙烯的说法正确的是
A.二者的键角均相等
B.二者σ键个数之比为7:5
C.二者的键长均相等
D.碳碳键的键能后者是前者的两倍
课堂练习
B
【例7】下列说法中正确的是( )
A.双原子分子中化学键键能越大,分子越稳定
B.双原子分子中化学键键长越长,分子越稳定
C.双原子分子中化学键键角越大,分子越稳定
D.在双键中,σ键的键能要小于π键的键能
课堂练习
A
