中考化学复习第六单元控制燃烧课件
图片预览






文档简介
(共186张PPT)
第六单元 控制燃烧
枣庄考情分析
考点 考向 频次 分值 难度 常考题型
物质的燃烧与灭火 物质的燃烧与促进燃烧的方法 2024年·T10(A、B) 2 ** 选择题
填空题
灭火原理及措施 2024年·T10(C、D)
2023年·T6(A、D)
2022年·T7 2 ** 选择题
燃烧与爆炸 2023年·T6(B、C) 2 * 选择题
考点 考向 频次 分值 难度 常考题型
探究燃烧的条件 燃烧的条件的探究实验 2021年·T6(C) 1 * 填空题
化石燃料的利用 化石燃料的分类及综合利用 2024年·T5(C)
2023年·T11
2022年·T11 2 * 填空题
考点 考向 频次 分值 难度 常考题型
碳的单质和碳的氧化物 常见的碳单质 2023年·T12(4) 1 * 选择题
二氧化碳的性质 2024年·T18(4)
2021年·T6(A) 2 * 选择题
填空题
二氧化碳的制备 2024年·T18
2023年·T8(C)
2022年·T13(Ⅰ) 2 ** 填空题
考点 考向 频次 分值 难度 常考题型
碳达峰与
碳中和 碳达峰与碳中和概念及措施 2023年·T11(5)
2021年·T11(1) 2 * 选择题
填空题
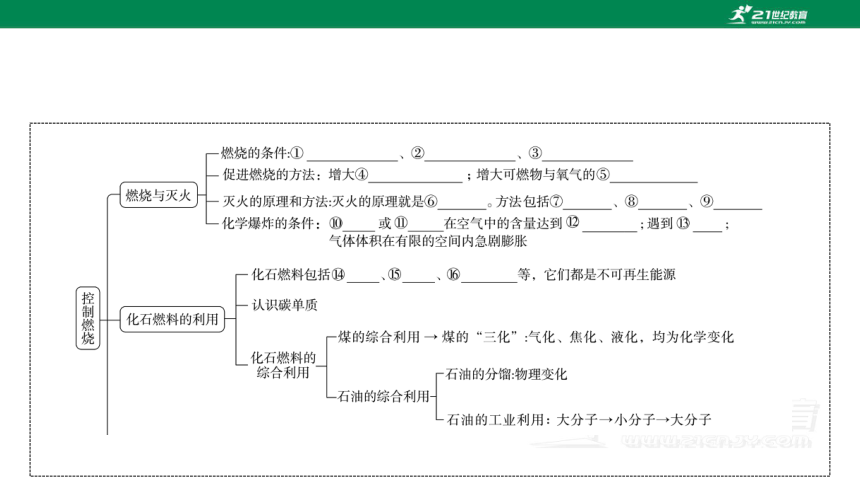
单元体系构建
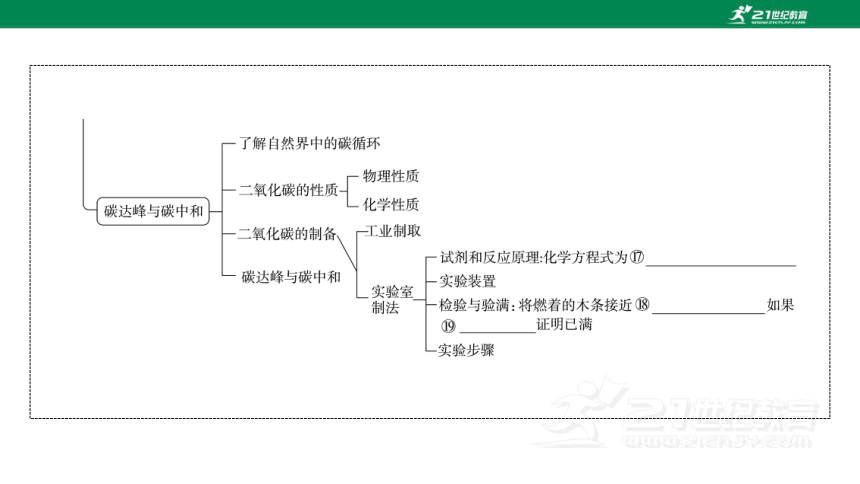
①物质具有可燃性 ②可燃物与充足的氧气接触 ③温度达到自身的着火点 ④氧气的浓度 ⑤接触面积 ⑥破坏物质燃烧的条件 ⑦移走可燃物 ⑧降低温度至可燃物着火点以下 ⑨隔绝氧气 ⑩可燃性气体 粉尘 爆炸极限 明火 煤 石油 天然气 CaCO3+2HCl===CaCl2+H2O+CO2↑ 集气瓶口 木条熄灭
1.[知识填充]
(1)燃烧是可燃物与氧气发生的一种________、________并________的________反应。
深化研讨 任务达成
任务一 物质的燃烧与灭火
剧烈的
氧化
发光
放热
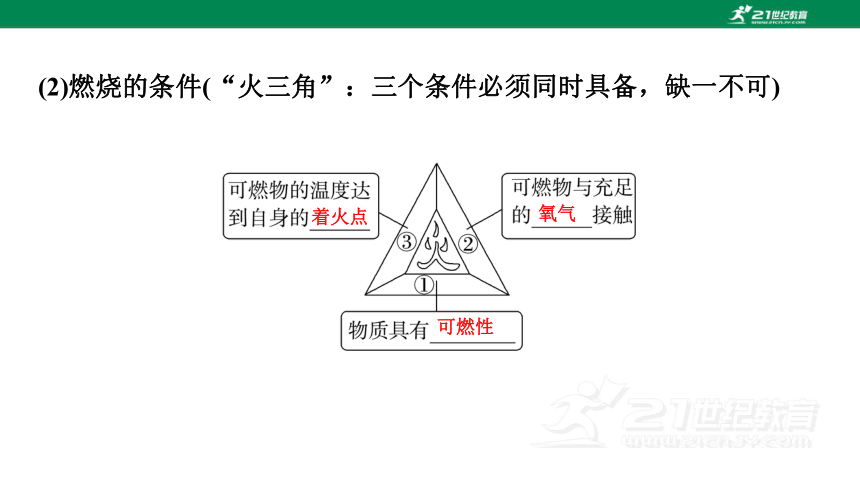
(2)燃烧的条件(“火三角”:三个条件必须同时具备,缺一不可)
可燃性
着火点
氧气
(3)灭火的方法
燃烧实例 灭火方法 灭火的原理
野炊时的篝火 向燃烧的木材上覆盖沙子 ____________
油锅着火 用锅盖盖灭 ____________
森林着火 砍伐树木,设置隔离带 ____________
建筑物着火 用高压水枪灭火 ______________
______________
降低温度至着
火点以下
隔绝氧气
隔绝氧气
移走可燃物
2.[应用体验]将下列使物质充分燃烧的方法归类
①工厂烧锅炉用的煤通常要加工成粉末状。
②化油器将汽油喷成雾状,进入内燃机气缸。
③用煤炭烧锅炉时,要用鼓风机不断向炉膛中吹入空气。
④家庭用的煤通常要加工成蜂窝煤。
⑤在空气中加热铁丝时,铁丝不会燃烧;如果在纯氧中加热铁丝,就会剧烈燃烧,火星四射。
上述方法中,属于增大氧气(空气)浓度的有________(填序号,后同),属于增大可燃物与氧气(空气)的接触面积的有________。
③⑤
①②④
3.[教材实验]下面是教材探究爆炸条件实验的改进,请根据有关知识回答下列问题。
(1)操作:在无盖小罐里放入干燥的面粉,点燃蜡烛,用塑料盖盖住金属筒,迅速鼓入大量空气。
(2)现象:不久,便会听到“砰”的一声,爆炸的气浪将金属筒上的塑料盖掀起。
分析并回答:
(1)在上述实验中,鼓入空气的作用是__________________________
___________________________________________________________。
(2)该实验中的面粉属于燃烧条件中的 ________ 。实验中发生爆炸,除具备了燃烧的三个条件外,还因为燃烧是发生在___________。
使面粉充满整个金属筒、使面
粉与空气混合均匀、增大与氧气的接触面积
可燃物
有限空间内
(3)下列情况下,会发生爆炸的是 ________ (填字母)。
A.金属筒不加盖时
B.蜡烛没有点燃时
C.小罐中装的是石灰石粉末时
D.小罐中装的是玉米粉末时
(4)在油库、面粉加工厂、纺织厂和煤矿的矿井内为了避免爆炸事故发生,应采取的安全措施有 _________________________ (写出一种即可)。
D
严禁烟火或保持通风透气等
物质的燃烧与促进燃烧的方法
1.(2024·湖南中考)花鼓戏《补锅》中唱到“手拉风箱呼呼响,火炉烧得红旺旺”。下列说法最合理的是( )
A.风箱拉动过程中增加了可燃物
B.手拉风箱为煤的燃烧提供了充足氧气
C.火炉烧得旺是因为降低了煤的着火点
D.氧气能支持燃烧,说明氧气具有可燃性
√
B [风箱拉动过程中没有增加可燃物,A错误;手拉风箱为煤的燃烧提供了充足氧气,使煤发生充分燃烧,放出更多的热量,B正确;火炉烧得旺是因为补充了充足的氧气,而不是降低了煤的着火点,C错误;氧气能支持燃烧,说明氧气具有助燃性,氧气没有可燃性,D错误。]
2.人类生活和生产活动离不开火。下列有关说法中,不合理的是
( )
A.炒菜时不慎油锅起火,可以盖上锅盖灭火
B.室内起火时,应立即打开所有门窗通风
C.控制燃烧条件可以达到防火、灭火的目的
D.增大可燃物与氧气的接触面积可以促进燃烧
√
B [炒菜时不慎油锅起火,可以盖上锅盖灭火,这是采用了隔绝氧气的原理来灭火,A项正确;室内起火时,不能立即打开所有门窗通风,以防空气流通造成火势蔓延,B项错误;物质燃烧必须同时具备三个条件:一是物质具有可燃性,二是可燃物与充足的氧气接触,三是温度达到可燃物的着火点,三个条件必须同时具备,缺一不可,因此控制燃烧的条件可以达到防火、灭火的目的,C项正确;增大可燃物与氧气的接触面积可以促进燃烧,D项正确。]
3.下列有关燃烧和灭火的说法正确的是( )
A.电器着火用水浇灭
B.温度达到着火点,可燃物不一定燃烧
C.遇到煤气泄漏,立即打开灯查看
D.水灭火的原理是降低可燃物的着火点
灭火原理及措施
√
B [家用电器着火,应先切断电源,然后可以用水浇灭,否则可能引起触电,A错误;可燃物燃烧需同时满足三个条件,如果可燃物不与氧气接触,温度达到着火点,可燃物也不燃烧,B正确;煤气泄漏时,应立即关闭煤气,打开门窗,打开灯查看会点燃煤气,C错误;水灭火的原理是降低温度至着火点以下,可燃物的着火点不可能改变,D错误。]
4.(2024·成都中考)“生命宝贵,安全第一”。下列情况的灭火方法或原理错误的是( )
选项 实例 方法 原理
A 森林发生火灾 开辟隔离带 隔离可燃物
B 家用电器着火 用水浇灭 降低温度
C 酒精洒在桌上起火 用湿毛巾盖灭 降低温度,隔绝空气
D 图书馆图书失火 用二氧化碳灭火器扑灭 降低温度,隔绝空气
√
B [森林发生火灾时,开辟隔离带的目的是使可燃物与燃烧物隔离,A正确;家用电器着火,不能用水浇灭,以免发生触电危险,B错误;酒精洒在桌上起火,用湿毛巾盖灭,可以起到降低温度,隔绝空气的作用,从而达到灭火的目的,C正确;二氧化碳不能燃烧、不支持燃烧,图书馆图书失火,用二氧化碳灭火器扑灭,可以起到降低温度,隔绝空气的作用,从而达到灭火的目的,D正确。]
5.如图,向容器(用塑料矿泉水瓶制作)内吹入一定量的空气,发生爆炸现象。硬纸板随热气流冲高,蜡烛熄灭。下列说法错误的是
( )
燃烧与爆炸
A.引起爆炸的可燃物是没有来得及燃烧的石蜡蒸气
B.硬纸板和矿泉水瓶为爆炸提供了有限空间
C.蜡烛熄灭主要是因为爆炸后周围空气中瞬时缺少氧气
D.面粉厂应该保持一定湿度,并严禁烟火
√
A [吹入空气的作用是将面粉分散到空气中,以使面粉颗粒和氧气充分接触,燃烧后发生爆炸,A错误;硬纸板和矿泉水瓶为爆炸提供了有限空间,B正确;发生的爆炸是面粉在有限空间内燃烧,燃烧放出大量的热,所以发生爆炸后容器内温度升高,消耗氧气,导致氧气不充足,蜡烛熄灭,C正确;面粉是可燃物,面粉厂空气中混有大量的可燃性粉尘,遇明火可能会发生爆炸,所以面粉厂应该保持一定湿度,并严禁烟火,以防发生爆炸事故,D正确。]
6.下列措施中,符合易燃易爆物的安全要求的是( )
A.为了安全,存放易燃物的仓库要尽可能封闭,不让风吹进来
B.为了节约运费,把酒精、鞭炮等物品同时装在货车上运送
C.只要不影响工作,面粉加工厂的工人可以在车间吸烟
D.生产酒精的车间里,所有的照明设备均采用隔离和封闭装置
√
D [存放易燃物的仓库封闭,空间有限,遇火易发生爆炸,为了安全,存放易燃物的仓库要经常通风,防止缓慢氧化积聚热量,导致危险,A不符合安全要求;酒精和鞭炮属于易燃易爆物品,装在一辆货车上运送,容易导致燃烧、爆炸,不安全,B不符合安全要求;面粉加工厂的空气中弥漫着可燃性粉尘,遇明火易发生爆炸,所以工人在车间吸烟不安全,C不符合安全要求;生产酒精的车间里,所有的照明设备均采用隔离和封闭装置,可以防止酒精蒸气遇到空气和电火花而燃烧起火,D符合安全要求。]
关于燃烧、灭火、爆炸的几个易错点
(1)燃烧的三个条件必须同时具备,缺一不可。
(2)不是所有的燃烧都要有氧气的参与,如金属镁可以在氮气和二氧化碳中燃烧。
(3)灭火的原理是破坏燃烧的条件,因而只要去掉一个燃烧的条件,就能灭火;选择灭火的方法时要注意结合着火燃烧的具体情况,如电器着火一定要先切断电源;着火点是物质的固有特性,不能降低。
(4)爆炸不一定是化学变化,如轮胎爆炸、锅炉爆炸一般都属于物理变化;可燃性气体与空气混合也不一定必然导致爆炸,还需要满足其他几个条件:如达到爆炸极限、有限空间等。
[教材实验]
任务二 探究燃烧的条件
1.实验装置
(1)薄铜片的作用:载体,还利用了铜片的_______性。
(2)热水的作用:对于铜片上的白磷,水的作用是________________
_____,对于水中的白磷,水的作用是______________________。
(3)①③处罩的烧杯的作用是__________________________________
___________。
2.实验原理:_______________________(用化学方程式表示)。
导热
提供燃烧所需的
温度
隔绝空气
防止产生的五氧化二磷逸散到空气中,
污染环境
3.实验现象及分析
对比实验 实验现象 现象分析
铜片上的白磷和红磷 _____________________
_____________________ ____________________________
____________________________
____________________________
铜片上的白磷、热水中的白磷 ________________________
________________________ _________________
通入氧气时热水中的白磷 ________________________
________________________ ____________________________
铜片上的白磷燃烧,红
磷不燃烧
铜片的温度达到了白磷的着
火点而未达到红磷的着火点
铜片上的白磷燃烧,热水中
的白磷不燃烧
热水中的白磷没有和氧气接触,
铜片上的白磷和氧气接触,说明
燃烧需要与氧气接触
通氧气后燃烧
说明可燃物燃烧需要与氧气接触
4.实验结论:
燃烧需要的条件:_______________、_______________、_________
__________________,三者缺一不可。
[问题思考]上述实验中采用了____________进行实验:当有若干个条件影响燃烧时,设计实验时只能改变____个条件(需要探究的条件),其余的条件要__________。另外,还要设计好需要观察的现象或测量的数据。
物质具有可燃性
与充足氧气接触
温度达到
可燃物的着火点
控制变量法
1
完全相同
探究燃烧的条件
1.“纸杯烧水”的实验中,当酒精灯加热盛水的纸杯时纸杯不会燃烧。下列解释合理的是( )
A.纸杯不是可燃物,不能燃烧
B.纸杯被水浸湿,导致着火点降低
C.空气不充足,纸杯不会燃烧
D.水蒸发时吸热,温度达不到纸杯的着火点
√
D [纸杯属于可燃物,达到燃烧条件时可以燃烧,A不符合题意;着火点是一个定值,不能被降低,B不符合题意;纸杯不燃烧,不是因为空气不充足,C不符合题意;当酒精灯加热盛水的纸杯时纸杯不会燃烧,是因为水蒸发吸热,温度达不到纸杯的着火点,D符合题意。]
2.(2024·乐山中考)为探究燃烧的条件,利用可调节温度的电炉设计如图所示装置进行实验。已知白磷的着火点是40 ℃,红磷的着火点是240 ℃,氯化钠不是可燃物。下列说法错误的是( )
A.当温度为60 ℃时,只有①处白磷燃烧
B.为控制变量,①②③④处所取白磷、红磷、氯化钠的质量应相等
C.当温度为260 ℃时,②处红磷燃烧、③处红磷不燃烧,说明燃烧需要氧气
D.当温度升至500 ℃时,④处氯化钠可能燃烧
√
D [当温度为60 ℃时,①处的白磷既与氧气接触,温度也达到了着火点,因此①处白磷燃烧;温度没有达到②处红磷的着火点,没有发生燃烧;③处的红磷既没有与氧气接触,温度也未达到其着火点,因此没有发生燃烧,A正确。为控制变量,①②③④处所取白磷、红磷、氯化钠的质量应相等,B正确。当温度为260 ℃时,温度达到了红磷的着火点,②处红磷燃烧(与氧气接触),③处红磷不燃烧(没有与氧气接触),说明燃烧需要氧气,C正确。氯化钠不是可燃物,温度升至500 ℃时,④处氯化钠也不可能燃烧,D错误。]
条件类探究实验成功的关键
1.种类:初中条件类探究性实验包括:燃烧条件的探究、催化剂的探究、金属生锈条件的探究、影响蜡烛燃烧时间长短的探究等。
2.探究方法:常用的方法是对比实验法和控制变量法。在实验时要根据实验原理确定对照组,设计要控制的变量,即在一组对照实验中只能有1个变量(要探究的因素),其他的量要完全相同。
1.[知识填充]
(1)化石燃料
化石燃料包括_____、________、________等,它们都是________再生能源。天然气主要成分的化学式为________ ,它燃烧的化学方程式为____________________________,可燃冰是在________、________的条件下形成的________________。
任务三 化石燃料的利用
天然气
煤
石油
不可
CH4
高压
天然气水合物
低温
(2)化石燃料的综合利用
①煤的综合利用,可以通过将煤隔绝空气加强热分解或煤与其他物质反应来实现,由此得到许多有用的物质,如________、________、煤气等,此过程属于________变化。
②石油的综合利用是利用各成分的________不同进行分离的,可得到汽油、煤油、柴油等,此过程属于________变化。
焦炭
煤焦油
化学
沸点
物理
2.[应用体验]判断下列说法的正误
(1)煤、石油不可再生,天然气可以再生。 ( )
(2)煤、石油是混合物,天然气属于纯净物。 ( )
(3)使用天然气可以有效防止温室效应。 ( )
×
×
×
化石燃料的分类及综合利用
1.(2024·常州中考)下列关于化石燃料的说法正确的是( )
A.化石燃料都属于可再生能源
B.煤完全燃烧时不会产生污染
C.石油为原料能制造合成纤维
D.天然气主要成分为一氧化碳
√
C [化石燃料包括煤、石油和天然气,化石燃料在短期内不能从自然界得到补充,属于不可再生能源,A错误;煤中含有硫元素、氮元素,完全燃烧时生成的二氧化硫、二氧化氮等溶于水会形成酸雨,对环境造成污染,B错误;以石油为原料能制造合成纤维,C正确;天然气主要成分是甲烷,D错误。]
2.能源、环境和安全已成为人类日益关注的问题。请回答下列问题。
(1)目前世界上多数国家利用的能量主要来自化石燃料的燃烧,其中石油的使用最为广泛,可以从中制得煤油、柴油等,此变化为________(填“物理”或“化学”)变化。
(2)科技发展可促进新能源的开发利用。下列能源不属于新能源的是_______(填字母)。
A.煤 B.地热能
C.太阳能 D.核能
物理
A
(3)室温下,充分燃烧1 g天然气和1 g煤,产生的CO2及热量的对比如图所示。据图分析,与煤相比,用天然气作燃料的优点有____________________________________。
产生的二氧化碳少、释放的热量多
(4)天然气的主要成分是甲烷,已知甲烷和二氧化碳在高温下催化重整(Ni作催化剂)可制得CO和H2,该反应的化学方程式为
______________________________。
(5)燃料的充分燃烧对于节约能源、减少环境污染非常重要。汽车化油器将汽油喷成雾状进入内燃机气缸,使汽油充分燃烧。这是通过___________________________________的方法使汽油充分燃烧。
增大可燃物与氧气的接触面积
(6)我市家庭管道气的燃料为天然气,若天然气不完全燃烧,火焰为黄色,同时产生炭黑、一氧化碳等污染物,当出现这种情况时,应该把燃气灶的进风口调______(填“大”或“小”)。
大
(5)燃料充分燃烧的条件是要有足够多的空气,燃料与空气要有足够大的接触面积,汽车化油器将汽油喷成雾状进入内燃机气缸,使汽油充分燃烧。这是通过增大汽油与氧气接触面积的方法使汽油充分燃烧。
(6)若天然气不完全燃烧,火焰为黄色,同时产生炭黑、一氧化碳等污染物,当出现这种情况时,应该把燃气灶的进风口调大,增大空气的进气量,从而使天然气充分燃烧。
解答关于能源、化石燃料的题目时,要注意的几个问题
1.能源的分类:可再生和不可再生两大类,煤、石油、天然气(可燃冰)都是不可再生的,风能、潮汐能、太阳能等是可再生的。
2.煤的三化(煤的气化、焦化、液化)都是化学变化,石油分馏是物理变化。
3.使用化石燃料的三大危害:①温室效应(CO2)、②酸雨(SO2、氮氧化物)、③粉尘。
4.本部分题目涉及许多陌生化学方程式的书写,在解题时要结合题给信息进行书写。
1.[应用体验]将下列物质的性质与用途用线连接
金刚石最硬 食品工业除去色素
石墨导电性 超导、催化、能源领域
木炭吸附性 高铁列车受电弓滑板
C60特殊性质 切割玻璃
任务四 碳的单质和碳的氧化物
2.[知识填充]碳单质的化学性质
(1)常温下,单质碳的化学性质____________。
(2)单质碳与氧气的反应,说明单质碳具有__________。
(3)单质碳与某些氧化物反应说明单质碳具有________。
3.[概念对比]氧化反应、还原反应
(1)概念:__________________________的反应属于还原反应,________________的反应属于氧化反应。
非常稳定
可燃性
还原性
含氧化合物的氧被夺取
物质与氧发生
(2)关系:
4.[教材实验]CO2的制取与性质
(1)原理:实验室制取CO2的化学方程式是______________________
___________________。
CaCO3+2HCl===CaCl2
+H2O+CO2↑
(2)装置:分液漏斗的优点是 ________________,收集二氧化碳可用__________法,原因是_______________________,装置中浓硫酸的作用是____________________。
(3)性质
①实验时,甲、乙中现象为___________________________________,说明了二氧化碳能与______________,反应的化学方程式为___________________________。
控制反应的速率
向上排空气
二氧化碳的密度比空气大
吸收水分,干燥气体
甲中纸花不变色,乙中纸花变红色
水反应生成酸
CO2+H2O===H2CO3
②澄清石灰水的现象为__________________,反应的化学方程式为_____________________________________。
③烧杯中现象为__________________________________,说明二氧化碳具有的性质是__________、_____________、______________。
石灰水变浑浊
Ca(OH)2+CO2===CaCO3↓+H2O
下层蜡烛先熄灭(或上层蜡烛后熄灭)
不燃烧
不支持燃烧
密度比空气大
常见的碳单质
1.(2024·盐城中考)阅读下列资料,完成下面小题:透明的金刚石、灰黑色的石墨和足球状、空心球体结构的C60都是由碳元素组成的单质;金刚石可用来切割大理石、加工坚硬的金属。石墨很软,有滑腻感。C60常温下为固体,能与K等金属反应
生成超导体材料,如图所示的独特结构使之
有可能在催化、医学等领域具有广泛应用。
(1)下列关于C60的说法不正确的是( )
A.分子具有空心球体结构
B.是一种新型有机高分子材料
C.每个分子由60个碳原子构成
D.有可能在催化领域具有广泛应用
√
(2)金刚石、石墨和C60都是由碳元素组成的单质,它们的性质存在着明显差异。其原因是构成它们的原子( )
A.种类不同 B.大小不同
C.质量不同 D.排列方式不同
√
解析:(1)根据题目中C60的分子结构,C60分子具有空心球体结构,A正确;有机高分子是相对分子质量上万的有机物分子,C60是由一种元素组成的纯净物,是单质,不是有机物,B错误;元素符号的右下角表示一个分子中含有的原子数,每个C60分子是由60个碳原子构成的,C正确;根据题目叙述,C60有可能在催化领域具有广泛应用,D正确。
(2)金刚石、石墨和C60都是由碳元素组成的单质,但是由于构成它们的原子排列方式不同,因此它们的性质存在着明显差异,D符合题意。
2.(2024·贵州中考)阅读下面科普短文,回答问题。
自然界中,天然金刚石较少。人工合成金刚石通常需要在高温、高压条件下才能进行。近期,科学家在一个标准大气压、1 025 ℃条件下,将硅融入镓、铁、镍组成的液态金属中,通入甲烷(CH4)气体,硅(Si)与甲烷反应生成四氢化硅(SiH4)和石墨(C),石墨在液态金属表面转化成金刚石薄膜,其转化过程如图1和图2。金刚石薄膜具有良好的光学透明性和高度的化学稳定性,在多领域有广泛的应用。
(1)从宏观上看,甲烷由________(填元素符号)元素组成。从微观上看,金刚石由________(填名称)构成。
(2)图1生成石墨的化学方程式为___________________________,图2变化的微观实质是______________________________。
(3)金刚石薄膜的性质有_____________________________________。
C、H
碳原子
碳原子的排列方式发生了改变
良好的光学透明性和高度的化学稳定性
3.某实验小组用如图装置探究CO2的性质,下列说法错误的是
( )
二氧化碳的性质
A.该装置不涉及CO2的物理性质
B.c处澄清石灰水变浑浊
C.比较a、b处现象,可得二氧化碳能与水反应
D.该装置具有一次性完成多个性质实验的优点
√
A [d中蜡烛自下而上依次熄灭,说明二氧化碳密度比空气大(物理性质),且不能燃烧也不支持燃烧(化学性质),该装置涉及CO2的物理性质,A错误;二氧化碳能与氢氧化钙反应生成碳酸钙沉淀和水,能使澄清石灰水变浑浊,故c处澄清石灰水变浑浊,B正确;二氧化碳与水反应生成碳酸,碳酸能使紫色石蕊变红,实验中a处紫色石蕊小花不变色,b处紫色石蕊小花变红,可得二氧化碳能与水反应,C正确;该装置验证了二氧化碳能与水、氢氧化钙反应,不能燃烧也不支持燃烧、密度比空气大等性质,具有一次性完成多个性质实验的优点,D正确。]
4.以典型物质为核心,进行问题的设置与整合,是我们全面认识物质性质及应用的有效途径。小明同学在复习过程中对物质X的性质和用途进行了科学整理和归纳。如图所示:
联系实际,解决问题:
(1)物质X的化学式为________。
(2)在①中,X用于灭火,其具有的性质是_______________________
_____________________。
(3)在③中将饮料中的X通入含有石蕊试液的水中,石蕊试液立即变为红色,其原因是_______________________(用化学方程式表示),反应类型为________反应。
CO2
不燃烧也不支持燃烧、密
度比空气大
CO2+H2O===H2CO3
化合
(4)过程②在自然界中通过________________实现转化。
(5)检验X使用澄清石灰水,发生反应的化学方程式为_______________________________________。
植物的光合作用
CO2+Ca(OH)2===CaCO3↓+H2O
解析:(1)物质X可使澄清石灰水变浑浊,可用于植物光合作用和灭火,由此可推测物质X是CO2。
(2)在①中,二氧化碳能用于灭火,是因为二氧化碳具有不燃烧也不支持燃烧、密度比空气大的性质。
(3)二氧化碳和水反应生成碳酸,碳酸能使紫色石蕊试液变红色,反应的化学方程式为CO2+H2O===H2CO3,该反应为多种物质生成一种物质的反应,属于化合反应。
(4)在自然界中绿色植物的光合作用把二氧化碳和水转化成有机物,并且释放出氧气,过程②在自然界中通过植物的光合作用实现转化。(5)检验二氧化碳使用澄清石灰水,二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,化学方程式为CO2+Ca(OH)2===CaCO3↓+H2O。
5.(2024·陕西中考A卷)实验室制取二氧化碳时,下列相关操作正确的是( )
二氧化碳的制备
A.检查气密性 B.装药品
C.收集气体 D.气体验满
√
A [图示中长颈漏斗下端伸入液面以下,形成液封,双手紧握试管外壁,装置内气体受热膨胀,导管口有气泡冒出,则说明该装置气密性良好,A正确;实验室利用稀盐酸和大理石制取二氧化碳,向试管中装药品时,应先装固体药品,再装液体试剂,且装块状固体试剂时,应“一横二放三慢竖”,先将试管横放,用镊子把固体放在试管口,再将试管慢慢竖起来,B错误;二氧化碳密度比空气大,应该用向上排空气法收集,C错误;二氧化碳不能燃烧且不支持燃烧,验满的方法为将燃着的木条放在集气瓶口,若木条熄灭,则说明已收集满,D错误。]
6.化学是一门以实验为基础的自然科学,化学实验是进行科学探究的重要途径。
(1)气体的制备
①实验室若用大理石和稀盐酸反应制取二氧化碳,则应该选用的发生装置为______(填字母),反应的化学方程式为_________________
__________________________________。
②实验室可以用加热高锰酸钾固体的方法来制取氧气,则用该方法制取并收集氧气可以选用的装置组合为____________(填字母)。
A
CaCO3+2HCl===
CaCl2+H2O+CO2↑
BC(或BE)
(2)气体的净化
实验室制得的二氧化碳气体中常含有少量的氯化氢气体和水蒸气,为了得到纯净干燥的二氧化碳气体,除杂装置的导管气流方向连接顺序正确的是________(填字母)(温馨提示:饱和碳酸氢钠溶液不能再溶解CO2气体,且不与CO2反应)。
A.a→b→c→d
B.b→a→d→c
C.c→d→a→b
D.d→c→b→a
C
(3)物质性质的探究
用下图装置探究二氧化碳的性质。乙中的现象是________________,丙中蜡烛由下而上依次熄灭,此现象证明二氧化碳具有的性质是______________________________________________________。
澄清石灰水变浑浊
二氧化碳不燃烧也不支持燃烧,密度比空气大
解析:(1)①实验室制取二氧化碳,常用大理石或石灰石与稀盐酸反应,大理石的主要成分是碳酸钙,碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,该反应的反应物是固体和液体,不需加热,属于固、液混合不加热型,发生装置可用A;反应的化学方程式是CaCO3+2HCl===CaCl2+H2O+CO2↑。
②高锰酸钾加热分解生成锰酸钾、二氧化锰和氧气,该反应的反应物是固体,反应条件是加热,属于固体加热型,氧气密度大于空气,不易溶于水,可用向上排空气法收集或排水法收集,用该方法制取并收集氧气可以选用的装置组合为BC或BE。
(2)HCl气体易挥发,碳酸氢钠能与HCl反应生成氯化钠、水和二氧化碳,碳酸氢钠溶液能除去二氧化碳中的氯化氢气体,浓硫酸具有吸水性且不与二氧化碳反应,能干燥二氧化碳,要先除杂后干燥,并且要长管进短管出,则流程为c→d→a→b 。故选C。
(3)乙中澄清石灰水的主要成分为氢氧化钙,二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,观察到澄清石灰水变浑浊;丙中蜡烛由下而上依次熄灭,说明二氧化碳具有不燃烧也不支持燃烧、密度比空气大的性质
实验室制取气体的一般思路和方法
1.[知识填充]碳达峰和碳中和
(1)碳排放的最高点即碳峰值被称为________,人为碳排放与植树造林、碳捕集与封存技术等人为碳吸收达到平衡,称为__________。
(2)实现双碳目标的思路:①_______________________;②_______
________________。
任务五 碳达峰与碳中和
碳达峰
碳中和
减少二氧化碳的排放
增加二
氧化碳的消耗
2.[问题思考]观察下面的两幅图,回答下列问题:
(1)从1960年到2010年空气中二氧化碳含量呈________趋势。
(2)基于“碳循环”视角,实现“碳中和”可以从两方面进行:①_____________________,②增加二氧化碳消耗。图中自然界中消耗二氧化碳的途径有___________________(写一条即可)。
(3)在海水吸收二氧化碳和光合作用两个反应中,反应物相同,产物不同的原因是______________________。
增大
减少二氧化碳的排放
植物的光合作用
反应条件不同
1.(2024·烟台中考)我国力争2060年前实现“碳中和”,彰显大国责任与担当。“碳中和”的“碳”是指( )
A.二氧化碳 B.碳元素
C.碳原子 D.所有含碳物质
碳中和与碳达峰概念及措施
√
A [“碳中和”是指某个地区在一定时间内,人类活动直接和间接排放的碳总量,与通过植树造林、工业固碳等方式吸收的碳总量相互抵消,实现碳“净零排放”,这里的“碳”指的是二氧化碳。]
2.(2024·镇江中考)助力“碳中和”,CO2的产生、捕集与资源化利用是重要研究课题。
(1)CO2的产生:化石燃料的燃烧排放大量CO2。
①化石燃料主要包括_____、石油和天然气。
②大气中CO2的含量过高,会造成____________(填环境问题)。
煤
温室效应
(2)CO2的捕集:工业上可用氨水、(NH4)2CO3溶液等化学物质捕集烟气中的CO2。
氨水捕集CO2的实验流程如下。
①转化中可循环使用的物质X的化学式为__________。
②氨水吸收室中反应温度不宜过高,原因是____________________
_______________________________。
NH3
一水合氨易分解,温
度过高,一水合氨又分解成氨气
(3)CO2的利用:CO2和H2在Ni/CaO表面发生反应生成CH4的原理如图所示。
①整个转化过程中Ni/CaO的作用为________。
②生成CH4的总反应化学方程式为_____________________________。
催化
解析:(1)①化石燃料主要包括煤、石油和天然气。
②二氧化碳气体具有吸热和隔热的功能,二氧化碳在大气中增多的结果是形成一种无形的玻璃罩,使太阳辐射到地球上的热量无法向外层空间发散,其结果是地球表面变热起来,因此,二氧化碳也被称为温室气体,能引起温室效应,大气中二氧化碳含量的增加是导致温室效应的主要原因。
(2)①由氨水捕集CO2的实验流程图可知,富含CO2的烟气,进入氨水吸收室,生成碳酸铵和碳酸氢铵,碳酸铵和碳酸氢铵加热分解,生成X和高纯度CO2,X能被氨水吸收室吸收,根据质量守恒定律宏观实质:化学反应前后,元素种类不变可知,反应前碳酸铵和碳酸氢铵中含有碳、氢、氧元素,加热分解,生成X和高纯度CO2(含有碳元素和氧元素),X中可能含有氮元素和氢元素,X能被氨水吸收室吸收,说明X能与水反应,生成氨水,因此X为氨气,化学式为NH3。
②氨水吸收室中反应温度不宜过高,原因是一水合氨易分解,温度过高,一水合氨又分解成氨气和水。
关于碳中和与碳达峰的几个易混概念
1.碳中和、碳达峰以及所谓的低碳行动等中的“碳”都是指的二氧化碳;碳循环、氧循环中的碳、氧指的是碳元素和氧元素
2.碳循环、氧循环中都有化学变化发生,水循环是物理变化。
3.碳中和的思路包含两个方面,即:(1)降低二氧化碳的排放,具体措施有改善能源结构,减少使用化石能源等。(2)增加二氧化碳的消耗,具体措施有植树造林、通过人工方法对二氧化碳进行捕集、利用与封存等。
① ② ③ ④
白燃不燃烧 白磷不燃烧 白磷不燃烧 白磷燃烧
1.用如图所示实验探究燃烧的条件,下列说法正确的是( )
题号
1
3
5
2
4
6
8
7
9
10
分层评价 即时反馈
A.对比①③说明燃烧的条件之一是可燃物接触氧气
B.对比①④说明燃烧的条件之一是需要有可燃物
C.对比③④说明燃烧的条件之一是达到可燃物的着火点
D.本实验用盘成螺旋状的细铁丝替代白磷,能得到相同的实验结论
题号
1
3
5
2
4
6
8
7
9
10
√
题号
1
3
5
2
4
6
8
7
9
10
C [①③中均为冷水,③中虽通入O2,也不燃烧,故不能得出燃烧需要O2的结论,A错误;①④中存在两组变量,即冷水和热水、是否通O2,故无法得出正确结论,B错误;③④都通入了O2,冷水中不燃烧,热水中燃烧,故可得出燃烧条件之一是达到可燃物的着火点的结论,C正确;铁丝着火点高,在冷水、热水中均不会燃烧,D错误。]
2.人类生活和生产活动离不开火。下列有关说法中,不合理的是
( )
A.室内起火时,应立即打开所有门窗通风
B.炒菜时不慎油锅起火,可以盖上锅盖灭火
C.发生火灾时,用湿毛巾捂住口鼻,蹲下靠近地面,迅速离开火灾现场
D.加油站、面粉厂等场所要严禁烟火
题号
1
3
5
2
4
6
8
7
9
10
√
A [室内起火时,打开所有门窗,会使空气流通,使火势更大,A不合理;油锅着火时,盖上锅盖,能隔绝氧气,从而灭火,B合理;火灾现场会产生大量的烟尘和有害气体,其烟尘和有害气体会随热空气向上流动,故逃离火灾现场时,可用湿毛巾捂住口鼻,并尽量贴近地面逃离,C合理;加油站、面粉厂等场所空气中可燃物较多,应严禁烟火,D合理。]
题号
1
3
5
2
4
6
8
7
9
10
3.(2024·长沙中考)物质的性质决定物质的用途。下列含碳物质中,常用于去除冰箱、汽车中的异味的是( )
A.活性炭 B.金刚石
C.石墨 D.C60
题号
1
3
5
2
4
6
8
7
9
10
√
A [活性炭具有疏松多孔的结构,具有吸附性,用于去除冰箱、汽车中的异味,A正确;金刚石无吸附性,不能用于去除冰箱、汽车中的异味,B错误;石墨无吸附性,不能用于去除冰箱、汽车中的异味,C错误;C60不能用于去除冰箱、汽车中的异味,D错误。]
题号
1
3
5
2
4
6
8
7
9
10
4.为了预防火灾发生,我们应当了解燃烧与灭火的相关知识。下列说法正确的是( )
A.救火时不要贸然打开所有门窗,以免空气对流促进火势蔓延
B.生活中常用水来灭火,其原理主要是降低可燃物的着火点
C.蜡烛用嘴一吹即灭,是因为吹出的气体主要是二氧化碳
D.图书、档案、贵重设备、精密仪器等物失火,用干粉灭火器来灭火
题号
1
3
5
2
4
6
8
7
9
10
√
A [救火时不要贸然打开所有门窗,以免空气对流,可燃物与氧气接触更充分,燃烧更旺,使火势蔓延,A正确;生活中常用水来灭火,水蒸发吸热,其原理主要是降低温度至可燃物的着火点以下,着火点是物质的固有属性,不能改变,B错误;蜡烛用嘴一吹即灭,是因为空气流通带走热量,使蜡烛温度低于其着火点而达到灭火的目的,C错误;干粉灭火器使用过程中会产生水等物质,不能用于贵重设备、精密仪器等物失火,贵重设备、精密仪器等物失火,为了防止造成二次损害,应用液态二氧化碳灭火器,不会留下任何痕迹,D错误。]
题号
1
3
5
2
4
6
8
7
9
10
5.实验室制取CO2的有关操作如下图,不正确的是( )
题号
1
3
5
2
4
6
8
7
9
10
A.推动注射器时,长颈漏斗下端管中液面上升说明气密性良好 B.加入药品制气 C.若图中试剂为足量澄清石灰水,则可检验二氧化碳 D.用燃烧的木条验满
√
B [推动注射器时,锥形瓶内压强变大,长颈漏斗下端管中液面上升说明气密性良好,A正确;实验室不能用稀硫酸和大理石制取CO2,因为产物CaSO4是微溶物,会附着在大理石表面,阻止了反应的进一步进行,B不正确;二氧化碳能使澄清石灰水变浑浊,若图C中试剂为足量澄清石灰水,则可检验二氧化碳,C正确;因为二氧化碳不能燃烧也不支持燃烧,可以用燃着的木条验满,D正确。]
题号
1
3
5
2
4
6
8
7
9
10
6.“画说化学”是学科融合的重要方式,关于二氧化碳的相关性质同学们设计、绘制了下面的海报图片,对图中画面分析不正确的是( )
题号
1
3
5
2
4
6
8
7
9
10
题号
1
3
5
2
4
6
8
7
9
10
A.二氧化碳灭火器能灭火说明二氧化碳不助燃、不可燃、密度大于空气
B.二氧化碳能为植物的光合作用提供原料
C.碳酸饮料生产时,有一步是将二氧化碳压入水中,操作中二氧化碳仅发生了物理变化
D.石灰浆(含有氢氧化钙)刷在墙上会硬,是因为石灰浆与空气中二氧化碳反应生成碳酸钙
√
C [二氧化碳灭火器能灭火,利用了二氧化碳不助燃、不可燃、密度大于空气的性质,A正确;光合作用是绿色植物吸入二氧化碳,释放氧气的过程,二氧化碳为植物的光合作用提供原料,B正确;碳酸饮料生产时,将二氧化碳压入水中,该操作中二氧化碳不仅仅发生了物理变化,还发生了二氧化碳与水反应生成碳酸的化学变化,C错误;石灰浆(含有氢氧化钙)刷在墙壁上会硬,是因为石灰浆中的氢氧化钙会与空气中的二氧化碳反应生成碳酸钙,D正确。]
题号
1
3
5
2
4
6
8
7
9
10
7.“学化学,用化学”。下列做法错误的是( )
A.点燃可燃性气体前,一定要检验气体纯度
B.冬天用煤炉取暖时,室内放盆水防止中毒
C.图书馆着火,用二氧化碳灭火器扑灭
D.冰箱内放活性炭,吸附异味净化冰箱气体
题号
1
3
5
2
4
6
8
7
9
10
√
B [可燃性的气体混有空气时,点燃可能会发生爆炸,点燃可燃性气体前,一定要检验气体的纯度,A正确;一氧化碳难溶于水,在室内放一盆水不能防止中毒,B错误;二氧化碳不燃烧、不支持燃烧、密度比空气大,不损伤图书,图书馆着火,可用二氧化碳灭火器扑灭,C正确;活性炭具有吸附性,可以吸附异味,冰箱内放入活性炭,可以吸附异味净化冰箱气体,D正确。]
题号
1
3
5
2
4
6
8
7
9
10
8.(2024·安徽中考)如图是我国西汉青铜雁鱼灯及其示意图。灯油燃烧时,烟气通过鱼身和雁颈导入雁体内水中,减少对室内空气的污染。下列说法错误的是( )
题号
1
3
5
2
4
6
8
7
9
10
题号
1
3
5
2
4
6
8
7
9
10
A.该灯使用的青铜是一种金属材料
B.产生烟尘的原因是灯油不完全燃烧
C.转动灯罩隔绝空气,可使灯火熄灭
D.水能吸收烟尘,还能吸收一氧化碳
√
D [金属材料包括纯金属及合金,青铜是合金,属于金属材料,A正确;灯油不完全燃烧产生碳粒等烟尘,B正确;清除可燃物,隔绝空气,使温度降到着火点以下,都能达到灭火目的,所以转动灯罩隔绝空气,可使灯火熄灭,C正确;由于一氧化碳难溶于水,所以水不能吸收一氧化碳,D错误。]
题号
1
3
5
2
4
6
8
7
9
10
9.(2024·长春中考)火的使用标志着人类文明的巨大进步。汉字作为载体也反映了我国古代人民对火的认识。
(1)甲骨文“ ”(焚)的字形像是要燃火烧掉树林。上方的“林”相当于燃烧条件中的__________。
(2)小篆“ ”(灭)的字形左边像是一川流水,意思是水能灭火。用水灭火的主要原理是______________________和隔绝氧气。
题号
1
3
5
2
4
6
8
7
9
10
可燃物
降低温度到着火点以下
(3)甲骨文“ ”(灾)的字形像是房屋着火,灾难降临。
①以下标志与消防安全有关的是________(填字母)。
题号
1
3
5
2
4
6
8
7
9
10
A. B. C.
②发现或遭遇火灾,可采取的措施有__________________________
_____________(答一条即可)。
A
打火警电话119报警(或其他合
理答案)
解析:(1)燃烧条件包括:可燃物,氧气(或空气),达到燃烧时所需的最低温度(着火点)。所以上方的“林”相当于燃烧条件中的可燃物。(2)灭火的原理是清除可燃物,隔绝氧气,降温到着火点以下。所以用水灭火的主要原理是水蒸发吸热可降低温度到着火点以下,同时隔绝氧气。(3)①A.该图标是禁止烟火标志,与消防安全有关,A符合题意;B.该图标是我国制定的塑料包装制品回收标志,与消防安全无关,B不符合题意;C.该图标是我国国家节水标志,与消防安全无关,C不符合题意。②发现或遭遇火灾,可采取的措施有打火警电话119报警;遇火灾不可乘坐电梯,要向安全出口方向逃生; 当火势不是很大时,应沿着消防通道迅速往楼下跑等。
题号
1
3
5
2
4
6
8
7
9
10
10.(2024·广东中考)【基础实验和跨学科实践】 回答下列问题:
(1)CO2的制取及性质
ⅰ.制取CO2
组装一套便于添加稀盐酸的发生装置,需用到图1中的仪器有________(填字母)。
题号
1
3
5
2
4
6
8
7
9
10
ade
操作 现象 性质
X为澄清石灰水时,现象为_________________ CO2能与石灰水反应
X为____________时,现象为_____________ CO2能与水反应生成酸性物质
ⅱ.性质实验
题号
1
3
5
2
4
6
8
7
9
10
澄清石灰水变浑浊
紫色石蕊试液
试液变红色
操作 现象 性质
低处的蜡烛先熄灭,高处的蜡烛后熄灭 __________________;CO2不燃烧,也不支持燃烧
题号
1
3
5
2
4
6
8
7
9
10
CO2密度比空气大
(2)低碳行动方案
同学们展示如图2所示的方案,并交流讨论、完善方案。
题号
1
3
5
2
4
6
8
7
9
10
ⅰ.完善方案中的内容(各补写一条):
a._____________________,b.__________,c._________。
ⅱ.CO2物理利用________(填“能”或“不能”)从总量上减少CO2。
ⅲ.植树造林,利用绿色植物的________作用吸收CO2。
题号
1
3
5
2
4
6
8
7
9
10
减少一次性餐具的使用
人工降雨
碳酸饮料
不能
光合
解析:(1)ⅰ.组装便于添加稀盐酸的发生装置,应该选择长颈漏斗e,制取二氧化碳的反应为固液常温型,可以选择锥形瓶d,长颈漏斗需要橡胶塞,选择双孔橡胶塞a,则需要的仪器有ade。ⅱ.若X为澄清石灰水,澄清石灰水与二氧化碳反应会生成碳酸钙沉淀和水,现象是澄清石灰水变浑浊。二氧化碳与水反应生成碳酸,碳酸呈酸性,可以用紫色石蕊试液检验,碳酸能使紫色石蕊试液变红色。将二氧化碳倒入烧杯中,观察到低处的蜡烛先熄灭,高处的蜡烛后熄灭,说明了二氧化碳密度比空气大,二氧化碳不燃烧,不支持燃烧。
题号
1
3
5
2
4
6
8
7
9
10
(2)ⅰ.a中低碳生活,是指减少碳的排放,低能量、低消耗、低开支的生活方式有很多,如光盘行动、减纸减塑、衣物回收利用、减少一次性餐具的使用、低碳出行等。b中二氧化碳的物理利用,不产生新物质的用途,包括冷藏保鲜、人工降雨、灭火等。c中二氧化碳化学利用,产生新的物质的用途,包括转化成甲醇、制作碳酸饮料、作气体肥料。ⅱ.根据图中“CO2物理利用”,可以知道利用二氧化碳冷藏保鲜、人工降雨,不能从总量上减少CO2。ⅲ.植树造林,绿色植物可以进行光合作用,二氧化碳和水在叶绿体中,在光照的条件下,反应生成有机物,并释放氧气,是利用植物的光合作用吸收二氧化碳。
题号
1
3
5
2
4
6
8
7
9
10
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
(时间:40分钟 满分:60分)
一、选择题(本题包括15小题,每小题2分,共30分)
1.(2024·东营中考)我国提出2030年前实现“碳达峰”,2060年前实现“碳中和”。下列做法不利于实现“碳达峰,碳中和”的是
( )
[A]绿色出行 [B]焚烧垃圾
[C]节约用纸 [D]随手关灯
限时提能训练(六) 控制燃烧
√
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
B [绿色出行,可以减少化石燃料的使用,减少二氧化碳的排放,利于实现“碳达峰,碳中和”,A不符合题意;焚烧垃圾,会产生大量的二氧化碳,不利于实现“碳达峰,碳中和”,B符合题意;节约用纸,可以节约资源,减少森林的砍伐,增加二氧化碳的吸收,利于实现“碳达峰,碳中和”,C不符合题意;随手关灯,可以节约能源,减少化石燃料的使用,减少二氧化碳的排放,利于实现“碳达峰,碳中和”,D不符合题意。]
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
2.(2024·北京中考)下列标志表示“禁止烟火”的是( )
[A] [B] [C] [D]
√
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
C [A.该标志是腐蚀品标志,不符合题意;B.该标志是爆炸品标志,不符合题意;C.该标志是禁止烟火标志,符合题意;D.该标志是禁止放易燃物标志,不符合题意。]
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
3.(2024·枣庄中考)生活处处即化学,对下列生活现象解释合理的是( )
[A]煤炉火越扇越旺——增大可燃物浓度
[B]煤粉比煤块燃烧更旺——增大与氧气的接触面积
[C]油锅着火放入青菜后熄灭——降低油的着火点
[D]移除炉灶内木柴后灶火熄灭——隔绝空气
√
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
B [煤炉火越扇越旺,是因为增大了氧气的浓度,A错误;煤粉比煤块燃烧更旺,是因为增大了可燃物与氧气的接触面积,B正确;油锅着火放入青菜后熄灭,是因为温度降低至油的着火点以下,C错误;移除炉灶内木柴后灶火熄灭,是因为移除了可燃物,D错误。]
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
4.(2024·枣庄中考)“碳家族”成员众多,用途广泛。下列说法错误的是( )
[A]一氧化碳可用于冶炼金属
[B]碳酸氢钠可用于配制波尔多液
[C]甲烷可用作燃料
[D]葡萄糖可用于配制注射液
√
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
B [一氧化碳具有还原性,能还原金属氧化物,则可用于冶炼金属,A正确;波尔多液是由硫酸铜和氢氧化钙配制成的,B错误;甲烷具有可燃性,可作燃料,C正确;葡萄糖属于糖类,可用于配制注射液,D正确。]
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
5.化学兴趣小组在进行可燃物燃烧条件探究时,设计了如下两个实验:实验①:在装满空气的试管内放入白磷,关闭弹簧夹,白磷不燃烧;实验②:将实验①的装置放到80 ℃热水中,白磷剧烈燃烧,气球胀大(已知:白磷的着火点为40 ℃)。下列说法不正确的是( )
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
[A]白磷在空气中充分燃烧,该化学反应属于氧化反应
[B]实验②中白磷剧烈燃烧时,试管内气体压强减小
[C]实验②结束后,试管内还有白磷残留,打开弹簧夹通入空气,白磷复燃,说明燃烧还需要与空气接触
[D]对比实验①②,说明可燃物燃烧需要的条件之一是温度达到可燃物的着火点
√
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
B [白磷在空气中与氧气充分燃烧,该化学反应是物质与氧气发生的反应,属于氧化反应,A正确;实验②中白磷剧烈燃烧时,放出大量的热,试管内气体压强增大,B错误;燃烧的条件三者缺一不可,实验②结束后,试管内还有白磷残留,打开弹簧夹通入空气,白磷复燃,说明燃烧还需要与空气接触,C正确;燃烧的条件三者缺一不可,对比实验①②,①中白磷温度没有达到着火点,与氧气接触,不燃烧,②中白磷温度达到着火点,与氧气接触,燃烧,说明可燃物燃烧需要的条件之一是温度达到可燃物的着火点,D正确。]
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
6.(2024·扬州中考)自然界存在多种元素及物质的循环。下图表示的是自然界中的( )
[A]氮循环 [B]硫循环 [C]碳循环 [D]水循环
√
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
C [由图可知,化石燃料燃烧产生二氧化碳,动植物呼吸作用生成二氧化碳,动植物的遗体和排泄物通过缓慢氧化生成二氧化碳,绿色植物通过光合作用吸收二氧化碳,故该图表示的是自然界中的碳循环。]
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
7.如图为我国不同年份的能源结构图。下列说法不正确的是( )
[A]我国能源结构中清洁能源占比呈增加趋势
[B]加大水电、风电的开发利用有利于减少环境污染
[C]天然气是比煤炭和石油更清洁的燃料
[D]液氢用作火箭燃料是因为氢气易于贮存和加注
√
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
D [由图示可知,我国能源结构中清洁能源占比呈增加趋势,A项正确;加大水电、风电的开发利用可以减少化石能源的利用,减少污染物的排放,有利于减少环境污染,B项正确;天然气燃烧生成二氧化碳和水,因此天然气是比煤炭和石油更清洁的燃料,C项正确;液氢用作火箭燃料是因为氢气热值高,并不是氢气易于贮存和加注,D项错误。]
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
8.下列有关燃烧与灭火的说法错误的是( )
[A]加油站、面粉加工厂必须严禁烟火
[B]用水灭火,其原理是降低了可燃物的着火点
[C]将煤球做成蜂窝状,其目的是增大煤与空气的接触面积,使燃料充分燃烧
[D]遭遇火灾要采取必要的自救措施,如用湿毛巾捂住口鼻,蹲下靠近地面跑离着火区域等
√
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
B [加油站、面粉加工厂周围的空气中可燃物含量比较高,则必须严禁烟火,防止发生爆炸,A正确;着火点为物质的固有属性,不能改变,用水灭火,是降低可燃物温度至着火点以下,B错误;将煤球做成蜂窝状,可增大煤与空气的接触面积,从而使燃料充分燃烧,C正确;湿毛巾有类似防毒面具作用,用湿毛巾捂住口鼻能防止吸入烟尘,气体受热密度变小,有毒气体上升聚集在高处,则应用湿毛巾捂住口鼻,D正确。]
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
9.(2024·福建中考)下列灭火方法主要是利用“使温度降到可燃物着火点以下”原理的是( )
[A]用灯帽盖灭酒精灯火焰 [B]关闭燃气灶阀门熄灭火焰
[C]用水浇灭炭火 [D]用锅盖盖灭油锅火焰
√
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
C [A.灯帽盖灭酒精灯,利用的是隔绝氧气的原理;B.关闭燃气灶阀门熄灭火焰,利用的是清除可燃物的原理;C.用水浇灭炭火,水汽化吸热,是利用使温度降到可燃物的着火点以下原理;D.用锅盖盖灭油锅火焰,利用的是隔绝氧气的原理。]
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
10.数字化实验化学兴趣小组同学采用图1装置对可燃性粉尘爆炸进行探究,爆炸的剧烈程度可用产生的最大压力来衡量。下列说法正确的是( )
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
[A]在有限的空间内,可燃性粉尘遇明火就会发生爆炸
[B]该实验中施加给打气筒的压力不同对实验结果没有影响
[C]根据图2可知,可燃性粉尘颗粒直径越大,爆炸威力越小
[D]根据图3可知,容器中可燃性粉尘的浓度越大,爆炸威力越大
√
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
C [可燃性粉尘在空气中的含量达到爆炸极限时,遇到明火才会发生爆炸,A错误;压力越大,可燃性粉尘与空气的接触越充分,爆炸的可能性越大、威力越大,B错误;根据题图2可知,可燃性粉尘颗粒直径越大,爆炸威力越小,C正确;根据题图3可知,开始时容器中可燃性粉尘的浓度越大,爆炸威力越大,当可燃性粉尘的浓度达到一定值后,可燃性粉尘浓度越大,爆炸威力反而越小,D错误。]
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
11.根据图示,分析下列说法,有关碳单质的说法正确的是( )
[A]石墨是最软的物质 [B]活性炭可以吸附异味
[C]金刚石不具有可燃性 [D]足球烯是由碳原子直接构成
√
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
B [石墨是最软的矿物之一,不是最软的物质,A错误;活性炭具有吸附性,可以吸附异味,B正确;金刚石是由碳组成的单质,具有可燃性,C错误;金刚石、石墨是由碳原子直接构成的,但足球烯是由足球烯分子构成的,D错误。]
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
12.(2023·宜宾中考)元素化合价和物质类别是研究物质的两个重要维度。如图为碳元素的部分“价—类”二维图。下列说法正确的是( )
[A]M为“混合物”
[B]X点对应的物质只有一种
[C]Y点对应的物质为CO2
[D]CO可与Ca(OH)2反应生成CaCO3
√
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
C [一氧化碳属于氧化物,A项错误;X点是碳元素组成的单质,X可以是金刚石、石墨等,B项错误;Y和一氧化碳的物质类别相同,所以Y点对应的物质为CO2,C项正确;一氧化碳不会与氢氧化钙反应生成碳酸钙沉淀,二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,D项错误。]
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
13.化学学习要形成科学的化学观念,比如分类观、变化观、转化观等。如右图所示是碳及其部分化合物的转化关系,请运用上述观念判断以下观点错误的是( )
[A]C和CO都有还原性
[B]反应②不可能是化合反应
[C]C和CO2也能发生化学反应
[D]②和③在一定条件下均能实现逆向转化
√
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
B [C和CO均能夺取氧化物中的氧,具有还原性,A项正确;反应②为一氧化碳转化为二氧化碳,可以是通过一氧化碳与氧气点燃生成二氧化碳,由两种物质生成一种物质,属于化合反应,B项错误;C和CO2高温下反应生成CO,有新物质生成,属于化学变化,C项正确;②的逆向转化可以通过C和CO2在高温下反应生成CO实现,③的逆向转化可通过CO2与Ca(OH)2生成CaCO3和H2O实现,D项正确。]
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
14.下列现象可用同一化学原理解释的是①久置石灰水的试剂瓶壁上有一层白膜;②用吸管向澄清石灰水中吹气,石灰水变浑浊;③检验二氧化碳气体;④向紫色石蕊试液中通入二氧化碳气体,试液变红;⑤蘸过石灰水的鸡蛋更易保存。( )
[A]②③④ [B]①②④ [C]①③④⑤ [D]①②③⑤
√
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
D [①久置的石灰水会和空气中的二氧化碳反应,生成碳酸钙沉淀;②用吸管向澄清石灰水中吹气,澄清石灰水会和呼出气体中的二氧化碳反应,生成碳酸钙沉淀;③二氧化碳能使澄清石灰水变浑浊,实验室常用澄清石灰水变浑浊检验二氧化碳气体;④向紫色石蕊试液中通入二氧化碳气体,试液变红的原因是二氧化碳和水反应生成碳酸,碳酸使紫色石蕊试液变红;⑤石灰水中的氢氧化钙会与二氧化碳反应生成碳酸钙沉淀,堵住了蛋壳上的气孔,隔绝了氧气,达到保鲜的目的,D项正确。]
[A]①装置的优点是能随时控制反应的发生与停止
[B]②处现象说明二氧化碳能使紫色石蕊试液变红
[C]③处溶液变浑浊,是因为生成了不溶于水的碳酸钙
[D]④处的实验说明二氧化碳不能燃烧也不能支持燃烧
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
15.某兴趣小组利用如图装置对二氧化碳的性质进行探究,下列说法错误的是( )
√
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
B [①装置可通过打开和关闭活塞,实现固液接触和分离,控制反应的发生与停止,A正确;②处紫色石蕊试液变红是由于二氧化碳和水反应生成了碳酸,碳酸显酸性,能使紫色石蕊试液变红,不是二氧化碳,B错误;二氧化碳和水反应生成碳酸钙沉淀和水,可观察到③处溶液变浑浊,C正确;D处蜡烛熄灭,说明二氧化碳能透过隔板下部小孔与燃着的蜡烛接触,导致蜡烛熄灭,说明二氧化碳密度比空气大,不能燃烧也不能支持燃烧,D正确。]
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
二、填空与简答题(本题包括3小题,共15分)
16.(3分)A、B、C、D、E是初中化学常见的五种物质,A是石灰石的主要成分,E是能与血红蛋白结合的有毒气体,→表示转化关系,部分反应条件未注明。回答下列问题
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
(1)写出物质B的化学式________。
(2)写出C与D反应转化为A的化学方程式_______________________
_______________________。
CaO
CO2+Ca(OH)2===
CaCO3↓+H2O
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
解析:(1)A、B、C、D、E是初中化学常见的五种物质,A是石灰石的主要成分,A是碳酸钙;E是能与血红蛋白结合的有毒气体,E是一氧化碳,碳酸钙高温条件下分解生成氧化钙和二氧化碳,二氧化碳与碳在高温条件下反应生成一氧化碳,故C是二氧化碳;物质B是氧化钙,化学式为CaO。
(2)氧化钙和水反应生成氢氧化钙,故D是氢氧化钙;一氧化碳燃烧生成二氧化碳,二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,C与D反应转化为A的化学方程式:CO2+Ca(OH)2===CaCO3↓+ H2O。
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
17.(6分)(2023·枣庄中考)天然气不仅是优质的能量来源,还是宝贵的化工资源。经过多年努力,我国在天然气的开发利用方面已取得重大突破。
方法一:煤气化生成一氧化碳和二氧化碳。在高温、高压和“甲烷化催化剂”的作用下,一氧化碳、二氧化碳分别与氢气反应生成甲烷,其中“甲烷化催化剂”在这两个化学反应过程中发挥着至关重要的作用。
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
方法二:开发煤层气。煤层气指储存在煤层中,以甲烷为主要成分的烃类物质,俗称“瓦斯”,是与煤伴生、共生的气体资源。
方法三:开发可燃冰。可燃冰的主要成分是甲烷水合物,甲烷水合物能稳定存在的压强和温度范围如图所示。可燃冰一旦离开海床便迅速分解,容易发生井喷意外,还可能会破坏地壳
稳定平衡,引发海底塌方,导致大规模
海啸,所以可燃冰的开采困难。
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
甲烷化催化剂
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
(3)从物质分类角度分析,方法二中的煤层气属于________(填“纯净物”或“混合物”)。
(4)根据方法三,判断有关可燃冰的说法正确的是________。
A.在15 ℃和100 atm时,可燃冰能稳定存在
B.可燃冰开采时若出现差错,可能导致严重的自然灾害
(5)“碳中和”中的“碳”是指________(填“CO”或“CO2”)。我国政府提出在2060年前实现“碳中和”,下列做法符合“碳中和”理念的是________。
A.植树造林 B.焚烧秸秆 C.节能减排 D.燃放烟花
混合物
B
CO2
AC
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
(3)煤层气以甲烷为主要成分,还含有其他物质,属于混合物。
(4)A.由图可知,在15 ℃和100 atm时,可燃冰不能稳定存在,已经转化为甲烷气体和水,不符合题意;B.可燃冰一旦离开海床便迅速分解,容易发生井喷意外,还可能会破坏地壳稳定平衡,引发海底塌方,导致大规模海啸,故可燃冰开采时若出现差错,可能导致严重的自然灾害,符合题意。
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
(5)“碳中和”中的“碳”是指CO2;A.植树造林,可以增加二氧化碳的吸收,减少二氧化碳的含量,符合“碳中和”理念,符合题意;B.焚烧秸秆会产生大量的二氧化碳,不符合“碳中和”理念,不符合题意;C.节能减排,可以减少二氧化碳的排放,符合“碳中和”理念,符合题意;D.燃放烟花,会产生大量的二氧化碳,不符合“碳中和”理念,不符合题意。
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
18.(6分)(2024·枣庄中考)气体制备与性质探究是初中化学实验的重要内容,相关装置如图所示。
回答下列问题:
(1)仪器甲的名称为________。
分液漏斗
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
(2)实验室制取二氧化碳气体应选择的发生装置为________(填字母序号);制取时发生反应的化学方程式为________________________
____________________________。
(3)若要收集一瓶干燥的二氧化碳,气体流经C装置时的入口端为________(填“a”或“b”)。
A
CaCO3+2HCl===CaCl2+
H2O+CO2↑
b
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
(4)在三颈烧瓶D中用排空气法收集CO2气体,检验气密性后,在t1时快速注入一种溶液,t3时快速注入另一种溶液,测得瓶内压强随时间变化曲线如图所示。下列说法正确的是________。
①三颈烧瓶D中收集的CO2气体不纯
②t1时注入的是氢氧化钠溶液
③t3后发生的只是中和反应
①②
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
解析:(1)根据仪器特征,仪器甲的名称为分液漏斗。
(2)实验室用大理石(或石灰石,主要成分都是碳酸钙)和稀盐酸制取二氧化碳,根据反应物的状态为固体和液体,反应条件为常温,实验室制取二氧化碳气体应选择的发生装置为固液常温型发生装置A;碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,该反应的化学方程式为CaCO3+2HCl===CaCl2+H2O+CO2↑。
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
(3)若要收集一瓶干燥的二氧化碳,气体流经C装置时的入口端为b,干燥剂能与气体充分接触,接反,容易把浓硫酸排出,造成事故。
(4)由压强随时间变化曲线图可知,在t1时快速注入一种溶液,瓶内压强迅速减小,t1时注入的溶液是氢氧化钠溶液,二氧化碳能与氢氧化钠溶液反应生成碳酸钠和水,使瓶内气体积减小,压强减小;t2~t3期间压强不变且大于0,可证明收集的二氧化碳气体不纯;t3时快速注入另一种溶液,瓶内压强增大,t3时注入的是稀盐酸,盐酸与碳酸钠反应生成氯化钠、水和二氧化碳,使瓶内气体积增大,压强增大,该反应不属于中和反应,盐酸与过量氢氧化钠的反应属于中和反应。所以①②正确,③错误。
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
三、实验与计算题(本题包括2小题,共15分)
19.(9分)(2024·青岛中考)化学反应需要一定的条件,控制条件可以调控化学反应。“启航”小组以“调控化学反应”为主题展开探究,请回答下列问题。
【生火有道】
(1)观察生活:小组同学观察到天然气、木炭能燃烧,而水和石头不能燃烧,得出燃烧的条件之一是________。
可燃物
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
实验探究:为继续探究燃烧的条件,小组同学设计并完成了图1所示实验。
已知:白磷着火点40 ℃,红磷着火点240 ℃。磷燃烧时产生污染空气的五氧化二磷白烟。
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
【现象与结论】
(2)①铜片上的白磷燃烧,红磷不燃烧,得出燃烧的条件之一是____________________________________。
②小红根据_________________________________________________
现象,得出燃烧的条件之一是可燃物与氧气接触。
温度达到可燃物的着火点
铜片上的白磷燃烧,而热水中的白磷不燃烧
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
【评价与反思】
(3)①实验中小组同学认为图1装置存在不足,于是设计了图2所示装置。图2装置的优点为____________。
环保
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
②小明对小红的结论提出质疑,设计了图3所示装置,对燃烧过程中的氧气含量进行测定,得到图4所示图像。结合图像分析,“可燃物与氧气接触”应准确地表述为____________________________。
可燃物与足够浓度的氧气接触
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
【调控有术】
化学反应速率与多种因素有关,为探究影响过氧化氢分解速率的因素,小组同学分别取足量且等质量的过氧化氢溶液完成了下列实验。
实验序号 过氧化氢溶液的浓度 二氧化锰粉末的质量/g 温度/℃ 10秒共收集到氧气的体积/mL
① 3% 0 10 几乎无
② 5% 0 20 几乎无
③ 5% 0.5 20 14
④ 10% 0.5 20 80
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
(4)探究催化剂对过氧化氢分解速率的影响,应选择的实验序号是________;对比实验③和实验④,可得出的结论是______________
_________________________________________;上述实验无法探究出__________________________因素对过氧化氢分解速率的影响(写一条即可)。
②③
相同条件下,
过氧化氢溶液浓度越大,反应速率越快
催化剂的种类(合理即可)
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
【应用有方】
(5)通过探究,小组同学认识到,生活中也可以通过控制条件促进或抑制化学反应。
①用天然气做饭,发现炉火火焰呈黄色,锅底出现黑色物质,这时需要________(填“调大”或“调小”)灶具的进风口。
②炒菜时如果油锅着火,可采取的灭火措施是__________________
_________(写一条即可)。
调大
用锅盖盖灭(合理即
可)
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
解析:(1)小组同学观察到天然气、木炭能燃烧,而水和石头不能燃烧,得出燃烧的条件之一是可燃物,天然气、木材具有可燃性,而水和石头不具有可燃性。
(2)①白磷和红磷都属于可燃物,且都与氧气接触,铜片上的白磷燃烧,红磷不燃烧,得出燃烧的条件之一是温度达到可燃物的着火点。
②铜片上的白磷和水中的白磷属于同一种物质,且着火点相同,小红根据铜片上的白磷燃烧,而热水中的白磷不燃烧现象,得出燃烧的条件之一是可燃物与氧气接触。
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
(3)①实验中小组同学认为图1装置存在不足,白磷燃烧有大量白烟生成,污染环境,图2所示装置是在密闭环境中进行实验,不会污染环境,装置的优点为环保。
②由图3和图4可知:白磷燃烧消耗试管中的氧气,氧气的含量逐渐减少,当氧气浓度小于10%时,白磷不再燃烧,结合图像分析,“可燃物与氧气接触”应准确地表述为可燃物与足够浓度的氧气接触。
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
(4)探究催化剂对过氧化氢分解速率的影响,变量是有无催化剂,过氧化氢溶液的浓度,反应时的温度必须相同,应选择的实验序号是②③;对比实验③和实验④,催化剂粉末质量相同,反应时温度相同,只有过氧化氢溶液的浓度不同,浓度越大,相同时间内收集氧气的体积越大,可得出的结论是相同条件下,过氧化氢溶液浓度越大,反应速率越快;上述实验无法探究出催化剂的种类因素对过氧化氢分解速率的影响。
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
(5)①用天然气做饭,发现炉火火焰呈黄色,锅底出现黑色物质,说明氧气不充足,燃烧不充分,这时需要调大灶具进风口,使燃烧更充分。
②炒菜时如果油锅着火,可采取的灭火措施是用锅盖盖灭,对应灭火的原理是隔绝空气。
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
20.(6分)(2024·枣庄期末)长期使用的花洒、热水壶底部和热水锅炉有一层水垢,主要成分是碳酸钙和氢氧化镁。项目小组为测定某水垢中碳酸钙的含量,取水垢样品,分成不同质量的4份于烧杯中,然后分别加入250 g相同质量分数的稀盐酸,充分反应后测得的实验数据如下:
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
计算水垢中碳酸钙的质量分数(要求写出计算过程)。
实验组数 一组 二组 三组 四组
水垢的质量/g 10 20 30 40
烧杯中剩余物质总质量/g 256.7 263.4 271.2 281.2
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
解:根据质量守恒定律,第一组加入10 g水垢时产生二氧化碳的质量为250 g+10 g-256.7 g=3.3 g;
第二组加入20 g水垢产生二氧化碳的质量为250 g+20 g-263.4 g=6.6 g;第三组加入30 g水垢产生二氧化碳的质量为250 g+30 g-271.2 g=8.8 g,如果第三组盐酸充足应产生9.9 g二氧化碳,计算数据说明第三组实验时盐酸不充足,所以用第一组实验数据进行计算。
设10 g水垢中碳酸钙的质量为x,则:
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
第六单元 控制燃烧
枣庄考情分析
考点 考向 频次 分值 难度 常考题型
物质的燃烧与灭火 物质的燃烧与促进燃烧的方法 2024年·T10(A、B) 2 ** 选择题
填空题
灭火原理及措施 2024年·T10(C、D)
2023年·T6(A、D)
2022年·T7 2 ** 选择题
燃烧与爆炸 2023年·T6(B、C) 2 * 选择题
考点 考向 频次 分值 难度 常考题型
探究燃烧的条件 燃烧的条件的探究实验 2021年·T6(C) 1 * 填空题
化石燃料的利用 化石燃料的分类及综合利用 2024年·T5(C)
2023年·T11
2022年·T11 2 * 填空题
考点 考向 频次 分值 难度 常考题型
碳的单质和碳的氧化物 常见的碳单质 2023年·T12(4) 1 * 选择题
二氧化碳的性质 2024年·T18(4)
2021年·T6(A) 2 * 选择题
填空题
二氧化碳的制备 2024年·T18
2023年·T8(C)
2022年·T13(Ⅰ) 2 ** 填空题
考点 考向 频次 分值 难度 常考题型
碳达峰与
碳中和 碳达峰与碳中和概念及措施 2023年·T11(5)
2021年·T11(1) 2 * 选择题
填空题
单元体系构建
①物质具有可燃性 ②可燃物与充足的氧气接触 ③温度达到自身的着火点 ④氧气的浓度 ⑤接触面积 ⑥破坏物质燃烧的条件 ⑦移走可燃物 ⑧降低温度至可燃物着火点以下 ⑨隔绝氧气 ⑩可燃性气体 粉尘 爆炸极限 明火 煤 石油 天然气 CaCO3+2HCl===CaCl2+H2O+CO2↑ 集气瓶口 木条熄灭
1.[知识填充]
(1)燃烧是可燃物与氧气发生的一种________、________并________的________反应。
深化研讨 任务达成
任务一 物质的燃烧与灭火
剧烈的
氧化
发光
放热
(2)燃烧的条件(“火三角”:三个条件必须同时具备,缺一不可)
可燃性
着火点
氧气
(3)灭火的方法
燃烧实例 灭火方法 灭火的原理
野炊时的篝火 向燃烧的木材上覆盖沙子 ____________
油锅着火 用锅盖盖灭 ____________
森林着火 砍伐树木,设置隔离带 ____________
建筑物着火 用高压水枪灭火 ______________
______________
降低温度至着
火点以下
隔绝氧气
隔绝氧气
移走可燃物
2.[应用体验]将下列使物质充分燃烧的方法归类
①工厂烧锅炉用的煤通常要加工成粉末状。
②化油器将汽油喷成雾状,进入内燃机气缸。
③用煤炭烧锅炉时,要用鼓风机不断向炉膛中吹入空气。
④家庭用的煤通常要加工成蜂窝煤。
⑤在空气中加热铁丝时,铁丝不会燃烧;如果在纯氧中加热铁丝,就会剧烈燃烧,火星四射。
上述方法中,属于增大氧气(空气)浓度的有________(填序号,后同),属于增大可燃物与氧气(空气)的接触面积的有________。
③⑤
①②④
3.[教材实验]下面是教材探究爆炸条件实验的改进,请根据有关知识回答下列问题。
(1)操作:在无盖小罐里放入干燥的面粉,点燃蜡烛,用塑料盖盖住金属筒,迅速鼓入大量空气。
(2)现象:不久,便会听到“砰”的一声,爆炸的气浪将金属筒上的塑料盖掀起。
分析并回答:
(1)在上述实验中,鼓入空气的作用是__________________________
___________________________________________________________。
(2)该实验中的面粉属于燃烧条件中的 ________ 。实验中发生爆炸,除具备了燃烧的三个条件外,还因为燃烧是发生在___________。
使面粉充满整个金属筒、使面
粉与空气混合均匀、增大与氧气的接触面积
可燃物
有限空间内
(3)下列情况下,会发生爆炸的是 ________ (填字母)。
A.金属筒不加盖时
B.蜡烛没有点燃时
C.小罐中装的是石灰石粉末时
D.小罐中装的是玉米粉末时
(4)在油库、面粉加工厂、纺织厂和煤矿的矿井内为了避免爆炸事故发生,应采取的安全措施有 _________________________ (写出一种即可)。
D
严禁烟火或保持通风透气等
物质的燃烧与促进燃烧的方法
1.(2024·湖南中考)花鼓戏《补锅》中唱到“手拉风箱呼呼响,火炉烧得红旺旺”。下列说法最合理的是( )
A.风箱拉动过程中增加了可燃物
B.手拉风箱为煤的燃烧提供了充足氧气
C.火炉烧得旺是因为降低了煤的着火点
D.氧气能支持燃烧,说明氧气具有可燃性
√
B [风箱拉动过程中没有增加可燃物,A错误;手拉风箱为煤的燃烧提供了充足氧气,使煤发生充分燃烧,放出更多的热量,B正确;火炉烧得旺是因为补充了充足的氧气,而不是降低了煤的着火点,C错误;氧气能支持燃烧,说明氧气具有助燃性,氧气没有可燃性,D错误。]
2.人类生活和生产活动离不开火。下列有关说法中,不合理的是
( )
A.炒菜时不慎油锅起火,可以盖上锅盖灭火
B.室内起火时,应立即打开所有门窗通风
C.控制燃烧条件可以达到防火、灭火的目的
D.增大可燃物与氧气的接触面积可以促进燃烧
√
B [炒菜时不慎油锅起火,可以盖上锅盖灭火,这是采用了隔绝氧气的原理来灭火,A项正确;室内起火时,不能立即打开所有门窗通风,以防空气流通造成火势蔓延,B项错误;物质燃烧必须同时具备三个条件:一是物质具有可燃性,二是可燃物与充足的氧气接触,三是温度达到可燃物的着火点,三个条件必须同时具备,缺一不可,因此控制燃烧的条件可以达到防火、灭火的目的,C项正确;增大可燃物与氧气的接触面积可以促进燃烧,D项正确。]
3.下列有关燃烧和灭火的说法正确的是( )
A.电器着火用水浇灭
B.温度达到着火点,可燃物不一定燃烧
C.遇到煤气泄漏,立即打开灯查看
D.水灭火的原理是降低可燃物的着火点
灭火原理及措施
√
B [家用电器着火,应先切断电源,然后可以用水浇灭,否则可能引起触电,A错误;可燃物燃烧需同时满足三个条件,如果可燃物不与氧气接触,温度达到着火点,可燃物也不燃烧,B正确;煤气泄漏时,应立即关闭煤气,打开门窗,打开灯查看会点燃煤气,C错误;水灭火的原理是降低温度至着火点以下,可燃物的着火点不可能改变,D错误。]
4.(2024·成都中考)“生命宝贵,安全第一”。下列情况的灭火方法或原理错误的是( )
选项 实例 方法 原理
A 森林发生火灾 开辟隔离带 隔离可燃物
B 家用电器着火 用水浇灭 降低温度
C 酒精洒在桌上起火 用湿毛巾盖灭 降低温度,隔绝空气
D 图书馆图书失火 用二氧化碳灭火器扑灭 降低温度,隔绝空气
√
B [森林发生火灾时,开辟隔离带的目的是使可燃物与燃烧物隔离,A正确;家用电器着火,不能用水浇灭,以免发生触电危险,B错误;酒精洒在桌上起火,用湿毛巾盖灭,可以起到降低温度,隔绝空气的作用,从而达到灭火的目的,C正确;二氧化碳不能燃烧、不支持燃烧,图书馆图书失火,用二氧化碳灭火器扑灭,可以起到降低温度,隔绝空气的作用,从而达到灭火的目的,D正确。]
5.如图,向容器(用塑料矿泉水瓶制作)内吹入一定量的空气,发生爆炸现象。硬纸板随热气流冲高,蜡烛熄灭。下列说法错误的是
( )
燃烧与爆炸
A.引起爆炸的可燃物是没有来得及燃烧的石蜡蒸气
B.硬纸板和矿泉水瓶为爆炸提供了有限空间
C.蜡烛熄灭主要是因为爆炸后周围空气中瞬时缺少氧气
D.面粉厂应该保持一定湿度,并严禁烟火
√
A [吹入空气的作用是将面粉分散到空气中,以使面粉颗粒和氧气充分接触,燃烧后发生爆炸,A错误;硬纸板和矿泉水瓶为爆炸提供了有限空间,B正确;发生的爆炸是面粉在有限空间内燃烧,燃烧放出大量的热,所以发生爆炸后容器内温度升高,消耗氧气,导致氧气不充足,蜡烛熄灭,C正确;面粉是可燃物,面粉厂空气中混有大量的可燃性粉尘,遇明火可能会发生爆炸,所以面粉厂应该保持一定湿度,并严禁烟火,以防发生爆炸事故,D正确。]
6.下列措施中,符合易燃易爆物的安全要求的是( )
A.为了安全,存放易燃物的仓库要尽可能封闭,不让风吹进来
B.为了节约运费,把酒精、鞭炮等物品同时装在货车上运送
C.只要不影响工作,面粉加工厂的工人可以在车间吸烟
D.生产酒精的车间里,所有的照明设备均采用隔离和封闭装置
√
D [存放易燃物的仓库封闭,空间有限,遇火易发生爆炸,为了安全,存放易燃物的仓库要经常通风,防止缓慢氧化积聚热量,导致危险,A不符合安全要求;酒精和鞭炮属于易燃易爆物品,装在一辆货车上运送,容易导致燃烧、爆炸,不安全,B不符合安全要求;面粉加工厂的空气中弥漫着可燃性粉尘,遇明火易发生爆炸,所以工人在车间吸烟不安全,C不符合安全要求;生产酒精的车间里,所有的照明设备均采用隔离和封闭装置,可以防止酒精蒸气遇到空气和电火花而燃烧起火,D符合安全要求。]
关于燃烧、灭火、爆炸的几个易错点
(1)燃烧的三个条件必须同时具备,缺一不可。
(2)不是所有的燃烧都要有氧气的参与,如金属镁可以在氮气和二氧化碳中燃烧。
(3)灭火的原理是破坏燃烧的条件,因而只要去掉一个燃烧的条件,就能灭火;选择灭火的方法时要注意结合着火燃烧的具体情况,如电器着火一定要先切断电源;着火点是物质的固有特性,不能降低。
(4)爆炸不一定是化学变化,如轮胎爆炸、锅炉爆炸一般都属于物理变化;可燃性气体与空气混合也不一定必然导致爆炸,还需要满足其他几个条件:如达到爆炸极限、有限空间等。
[教材实验]
任务二 探究燃烧的条件
1.实验装置
(1)薄铜片的作用:载体,还利用了铜片的_______性。
(2)热水的作用:对于铜片上的白磷,水的作用是________________
_____,对于水中的白磷,水的作用是______________________。
(3)①③处罩的烧杯的作用是__________________________________
___________。
2.实验原理:_______________________(用化学方程式表示)。
导热
提供燃烧所需的
温度
隔绝空气
防止产生的五氧化二磷逸散到空气中,
污染环境
3.实验现象及分析
对比实验 实验现象 现象分析
铜片上的白磷和红磷 _____________________
_____________________ ____________________________
____________________________
____________________________
铜片上的白磷、热水中的白磷 ________________________
________________________ _________________
通入氧气时热水中的白磷 ________________________
________________________ ____________________________
铜片上的白磷燃烧,红
磷不燃烧
铜片的温度达到了白磷的着
火点而未达到红磷的着火点
铜片上的白磷燃烧,热水中
的白磷不燃烧
热水中的白磷没有和氧气接触,
铜片上的白磷和氧气接触,说明
燃烧需要与氧气接触
通氧气后燃烧
说明可燃物燃烧需要与氧气接触
4.实验结论:
燃烧需要的条件:_______________、_______________、_________
__________________,三者缺一不可。
[问题思考]上述实验中采用了____________进行实验:当有若干个条件影响燃烧时,设计实验时只能改变____个条件(需要探究的条件),其余的条件要__________。另外,还要设计好需要观察的现象或测量的数据。
物质具有可燃性
与充足氧气接触
温度达到
可燃物的着火点
控制变量法
1
完全相同
探究燃烧的条件
1.“纸杯烧水”的实验中,当酒精灯加热盛水的纸杯时纸杯不会燃烧。下列解释合理的是( )
A.纸杯不是可燃物,不能燃烧
B.纸杯被水浸湿,导致着火点降低
C.空气不充足,纸杯不会燃烧
D.水蒸发时吸热,温度达不到纸杯的着火点
√
D [纸杯属于可燃物,达到燃烧条件时可以燃烧,A不符合题意;着火点是一个定值,不能被降低,B不符合题意;纸杯不燃烧,不是因为空气不充足,C不符合题意;当酒精灯加热盛水的纸杯时纸杯不会燃烧,是因为水蒸发吸热,温度达不到纸杯的着火点,D符合题意。]
2.(2024·乐山中考)为探究燃烧的条件,利用可调节温度的电炉设计如图所示装置进行实验。已知白磷的着火点是40 ℃,红磷的着火点是240 ℃,氯化钠不是可燃物。下列说法错误的是( )
A.当温度为60 ℃时,只有①处白磷燃烧
B.为控制变量,①②③④处所取白磷、红磷、氯化钠的质量应相等
C.当温度为260 ℃时,②处红磷燃烧、③处红磷不燃烧,说明燃烧需要氧气
D.当温度升至500 ℃时,④处氯化钠可能燃烧
√
D [当温度为60 ℃时,①处的白磷既与氧气接触,温度也达到了着火点,因此①处白磷燃烧;温度没有达到②处红磷的着火点,没有发生燃烧;③处的红磷既没有与氧气接触,温度也未达到其着火点,因此没有发生燃烧,A正确。为控制变量,①②③④处所取白磷、红磷、氯化钠的质量应相等,B正确。当温度为260 ℃时,温度达到了红磷的着火点,②处红磷燃烧(与氧气接触),③处红磷不燃烧(没有与氧气接触),说明燃烧需要氧气,C正确。氯化钠不是可燃物,温度升至500 ℃时,④处氯化钠也不可能燃烧,D错误。]
条件类探究实验成功的关键
1.种类:初中条件类探究性实验包括:燃烧条件的探究、催化剂的探究、金属生锈条件的探究、影响蜡烛燃烧时间长短的探究等。
2.探究方法:常用的方法是对比实验法和控制变量法。在实验时要根据实验原理确定对照组,设计要控制的变量,即在一组对照实验中只能有1个变量(要探究的因素),其他的量要完全相同。
1.[知识填充]
(1)化石燃料
化石燃料包括_____、________、________等,它们都是________再生能源。天然气主要成分的化学式为________ ,它燃烧的化学方程式为____________________________,可燃冰是在________、________的条件下形成的________________。
任务三 化石燃料的利用
天然气
煤
石油
不可
CH4
高压
天然气水合物
低温
(2)化石燃料的综合利用
①煤的综合利用,可以通过将煤隔绝空气加强热分解或煤与其他物质反应来实现,由此得到许多有用的物质,如________、________、煤气等,此过程属于________变化。
②石油的综合利用是利用各成分的________不同进行分离的,可得到汽油、煤油、柴油等,此过程属于________变化。
焦炭
煤焦油
化学
沸点
物理
2.[应用体验]判断下列说法的正误
(1)煤、石油不可再生,天然气可以再生。 ( )
(2)煤、石油是混合物,天然气属于纯净物。 ( )
(3)使用天然气可以有效防止温室效应。 ( )
×
×
×
化石燃料的分类及综合利用
1.(2024·常州中考)下列关于化石燃料的说法正确的是( )
A.化石燃料都属于可再生能源
B.煤完全燃烧时不会产生污染
C.石油为原料能制造合成纤维
D.天然气主要成分为一氧化碳
√
C [化石燃料包括煤、石油和天然气,化石燃料在短期内不能从自然界得到补充,属于不可再生能源,A错误;煤中含有硫元素、氮元素,完全燃烧时生成的二氧化硫、二氧化氮等溶于水会形成酸雨,对环境造成污染,B错误;以石油为原料能制造合成纤维,C正确;天然气主要成分是甲烷,D错误。]
2.能源、环境和安全已成为人类日益关注的问题。请回答下列问题。
(1)目前世界上多数国家利用的能量主要来自化石燃料的燃烧,其中石油的使用最为广泛,可以从中制得煤油、柴油等,此变化为________(填“物理”或“化学”)变化。
(2)科技发展可促进新能源的开发利用。下列能源不属于新能源的是_______(填字母)。
A.煤 B.地热能
C.太阳能 D.核能
物理
A
(3)室温下,充分燃烧1 g天然气和1 g煤,产生的CO2及热量的对比如图所示。据图分析,与煤相比,用天然气作燃料的优点有____________________________________。
产生的二氧化碳少、释放的热量多
(4)天然气的主要成分是甲烷,已知甲烷和二氧化碳在高温下催化重整(Ni作催化剂)可制得CO和H2,该反应的化学方程式为
______________________________。
(5)燃料的充分燃烧对于节约能源、减少环境污染非常重要。汽车化油器将汽油喷成雾状进入内燃机气缸,使汽油充分燃烧。这是通过___________________________________的方法使汽油充分燃烧。
增大可燃物与氧气的接触面积
(6)我市家庭管道气的燃料为天然气,若天然气不完全燃烧,火焰为黄色,同时产生炭黑、一氧化碳等污染物,当出现这种情况时,应该把燃气灶的进风口调______(填“大”或“小”)。
大
(5)燃料充分燃烧的条件是要有足够多的空气,燃料与空气要有足够大的接触面积,汽车化油器将汽油喷成雾状进入内燃机气缸,使汽油充分燃烧。这是通过增大汽油与氧气接触面积的方法使汽油充分燃烧。
(6)若天然气不完全燃烧,火焰为黄色,同时产生炭黑、一氧化碳等污染物,当出现这种情况时,应该把燃气灶的进风口调大,增大空气的进气量,从而使天然气充分燃烧。
解答关于能源、化石燃料的题目时,要注意的几个问题
1.能源的分类:可再生和不可再生两大类,煤、石油、天然气(可燃冰)都是不可再生的,风能、潮汐能、太阳能等是可再生的。
2.煤的三化(煤的气化、焦化、液化)都是化学变化,石油分馏是物理变化。
3.使用化石燃料的三大危害:①温室效应(CO2)、②酸雨(SO2、氮氧化物)、③粉尘。
4.本部分题目涉及许多陌生化学方程式的书写,在解题时要结合题给信息进行书写。
1.[应用体验]将下列物质的性质与用途用线连接
金刚石最硬 食品工业除去色素
石墨导电性 超导、催化、能源领域
木炭吸附性 高铁列车受电弓滑板
C60特殊性质 切割玻璃
任务四 碳的单质和碳的氧化物
2.[知识填充]碳单质的化学性质
(1)常温下,单质碳的化学性质____________。
(2)单质碳与氧气的反应,说明单质碳具有__________。
(3)单质碳与某些氧化物反应说明单质碳具有________。
3.[概念对比]氧化反应、还原反应
(1)概念:__________________________的反应属于还原反应,________________的反应属于氧化反应。
非常稳定
可燃性
还原性
含氧化合物的氧被夺取
物质与氧发生
(2)关系:
4.[教材实验]CO2的制取与性质
(1)原理:实验室制取CO2的化学方程式是______________________
___________________。
CaCO3+2HCl===CaCl2
+H2O+CO2↑
(2)装置:分液漏斗的优点是 ________________,收集二氧化碳可用__________法,原因是_______________________,装置中浓硫酸的作用是____________________。
(3)性质
①实验时,甲、乙中现象为___________________________________,说明了二氧化碳能与______________,反应的化学方程式为___________________________。
控制反应的速率
向上排空气
二氧化碳的密度比空气大
吸收水分,干燥气体
甲中纸花不变色,乙中纸花变红色
水反应生成酸
CO2+H2O===H2CO3
②澄清石灰水的现象为__________________,反应的化学方程式为_____________________________________。
③烧杯中现象为__________________________________,说明二氧化碳具有的性质是__________、_____________、______________。
石灰水变浑浊
Ca(OH)2+CO2===CaCO3↓+H2O
下层蜡烛先熄灭(或上层蜡烛后熄灭)
不燃烧
不支持燃烧
密度比空气大
常见的碳单质
1.(2024·盐城中考)阅读下列资料,完成下面小题:透明的金刚石、灰黑色的石墨和足球状、空心球体结构的C60都是由碳元素组成的单质;金刚石可用来切割大理石、加工坚硬的金属。石墨很软,有滑腻感。C60常温下为固体,能与K等金属反应
生成超导体材料,如图所示的独特结构使之
有可能在催化、医学等领域具有广泛应用。
(1)下列关于C60的说法不正确的是( )
A.分子具有空心球体结构
B.是一种新型有机高分子材料
C.每个分子由60个碳原子构成
D.有可能在催化领域具有广泛应用
√
(2)金刚石、石墨和C60都是由碳元素组成的单质,它们的性质存在着明显差异。其原因是构成它们的原子( )
A.种类不同 B.大小不同
C.质量不同 D.排列方式不同
√
解析:(1)根据题目中C60的分子结构,C60分子具有空心球体结构,A正确;有机高分子是相对分子质量上万的有机物分子,C60是由一种元素组成的纯净物,是单质,不是有机物,B错误;元素符号的右下角表示一个分子中含有的原子数,每个C60分子是由60个碳原子构成的,C正确;根据题目叙述,C60有可能在催化领域具有广泛应用,D正确。
(2)金刚石、石墨和C60都是由碳元素组成的单质,但是由于构成它们的原子排列方式不同,因此它们的性质存在着明显差异,D符合题意。
2.(2024·贵州中考)阅读下面科普短文,回答问题。
自然界中,天然金刚石较少。人工合成金刚石通常需要在高温、高压条件下才能进行。近期,科学家在一个标准大气压、1 025 ℃条件下,将硅融入镓、铁、镍组成的液态金属中,通入甲烷(CH4)气体,硅(Si)与甲烷反应生成四氢化硅(SiH4)和石墨(C),石墨在液态金属表面转化成金刚石薄膜,其转化过程如图1和图2。金刚石薄膜具有良好的光学透明性和高度的化学稳定性,在多领域有广泛的应用。
(1)从宏观上看,甲烷由________(填元素符号)元素组成。从微观上看,金刚石由________(填名称)构成。
(2)图1生成石墨的化学方程式为___________________________,图2变化的微观实质是______________________________。
(3)金刚石薄膜的性质有_____________________________________。
C、H
碳原子
碳原子的排列方式发生了改变
良好的光学透明性和高度的化学稳定性
3.某实验小组用如图装置探究CO2的性质,下列说法错误的是
( )
二氧化碳的性质
A.该装置不涉及CO2的物理性质
B.c处澄清石灰水变浑浊
C.比较a、b处现象,可得二氧化碳能与水反应
D.该装置具有一次性完成多个性质实验的优点
√
A [d中蜡烛自下而上依次熄灭,说明二氧化碳密度比空气大(物理性质),且不能燃烧也不支持燃烧(化学性质),该装置涉及CO2的物理性质,A错误;二氧化碳能与氢氧化钙反应生成碳酸钙沉淀和水,能使澄清石灰水变浑浊,故c处澄清石灰水变浑浊,B正确;二氧化碳与水反应生成碳酸,碳酸能使紫色石蕊变红,实验中a处紫色石蕊小花不变色,b处紫色石蕊小花变红,可得二氧化碳能与水反应,C正确;该装置验证了二氧化碳能与水、氢氧化钙反应,不能燃烧也不支持燃烧、密度比空气大等性质,具有一次性完成多个性质实验的优点,D正确。]
4.以典型物质为核心,进行问题的设置与整合,是我们全面认识物质性质及应用的有效途径。小明同学在复习过程中对物质X的性质和用途进行了科学整理和归纳。如图所示:
联系实际,解决问题:
(1)物质X的化学式为________。
(2)在①中,X用于灭火,其具有的性质是_______________________
_____________________。
(3)在③中将饮料中的X通入含有石蕊试液的水中,石蕊试液立即变为红色,其原因是_______________________(用化学方程式表示),反应类型为________反应。
CO2
不燃烧也不支持燃烧、密
度比空气大
CO2+H2O===H2CO3
化合
(4)过程②在自然界中通过________________实现转化。
(5)检验X使用澄清石灰水,发生反应的化学方程式为_______________________________________。
植物的光合作用
CO2+Ca(OH)2===CaCO3↓+H2O
解析:(1)物质X可使澄清石灰水变浑浊,可用于植物光合作用和灭火,由此可推测物质X是CO2。
(2)在①中,二氧化碳能用于灭火,是因为二氧化碳具有不燃烧也不支持燃烧、密度比空气大的性质。
(3)二氧化碳和水反应生成碳酸,碳酸能使紫色石蕊试液变红色,反应的化学方程式为CO2+H2O===H2CO3,该反应为多种物质生成一种物质的反应,属于化合反应。
(4)在自然界中绿色植物的光合作用把二氧化碳和水转化成有机物,并且释放出氧气,过程②在自然界中通过植物的光合作用实现转化。(5)检验二氧化碳使用澄清石灰水,二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,化学方程式为CO2+Ca(OH)2===CaCO3↓+H2O。
5.(2024·陕西中考A卷)实验室制取二氧化碳时,下列相关操作正确的是( )
二氧化碳的制备
A.检查气密性 B.装药品
C.收集气体 D.气体验满
√
A [图示中长颈漏斗下端伸入液面以下,形成液封,双手紧握试管外壁,装置内气体受热膨胀,导管口有气泡冒出,则说明该装置气密性良好,A正确;实验室利用稀盐酸和大理石制取二氧化碳,向试管中装药品时,应先装固体药品,再装液体试剂,且装块状固体试剂时,应“一横二放三慢竖”,先将试管横放,用镊子把固体放在试管口,再将试管慢慢竖起来,B错误;二氧化碳密度比空气大,应该用向上排空气法收集,C错误;二氧化碳不能燃烧且不支持燃烧,验满的方法为将燃着的木条放在集气瓶口,若木条熄灭,则说明已收集满,D错误。]
6.化学是一门以实验为基础的自然科学,化学实验是进行科学探究的重要途径。
(1)气体的制备
①实验室若用大理石和稀盐酸反应制取二氧化碳,则应该选用的发生装置为______(填字母),反应的化学方程式为_________________
__________________________________。
②实验室可以用加热高锰酸钾固体的方法来制取氧气,则用该方法制取并收集氧气可以选用的装置组合为____________(填字母)。
A
CaCO3+2HCl===
CaCl2+H2O+CO2↑
BC(或BE)
(2)气体的净化
实验室制得的二氧化碳气体中常含有少量的氯化氢气体和水蒸气,为了得到纯净干燥的二氧化碳气体,除杂装置的导管气流方向连接顺序正确的是________(填字母)(温馨提示:饱和碳酸氢钠溶液不能再溶解CO2气体,且不与CO2反应)。
A.a→b→c→d
B.b→a→d→c
C.c→d→a→b
D.d→c→b→a
C
(3)物质性质的探究
用下图装置探究二氧化碳的性质。乙中的现象是________________,丙中蜡烛由下而上依次熄灭,此现象证明二氧化碳具有的性质是______________________________________________________。
澄清石灰水变浑浊
二氧化碳不燃烧也不支持燃烧,密度比空气大
解析:(1)①实验室制取二氧化碳,常用大理石或石灰石与稀盐酸反应,大理石的主要成分是碳酸钙,碳酸钙与稀盐酸反应生成氯化钙、水和二氧化碳,该反应的反应物是固体和液体,不需加热,属于固、液混合不加热型,发生装置可用A;反应的化学方程式是CaCO3+2HCl===CaCl2+H2O+CO2↑。
②高锰酸钾加热分解生成锰酸钾、二氧化锰和氧气,该反应的反应物是固体,反应条件是加热,属于固体加热型,氧气密度大于空气,不易溶于水,可用向上排空气法收集或排水法收集,用该方法制取并收集氧气可以选用的装置组合为BC或BE。
(2)HCl气体易挥发,碳酸氢钠能与HCl反应生成氯化钠、水和二氧化碳,碳酸氢钠溶液能除去二氧化碳中的氯化氢气体,浓硫酸具有吸水性且不与二氧化碳反应,能干燥二氧化碳,要先除杂后干燥,并且要长管进短管出,则流程为c→d→a→b 。故选C。
(3)乙中澄清石灰水的主要成分为氢氧化钙,二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,观察到澄清石灰水变浑浊;丙中蜡烛由下而上依次熄灭,说明二氧化碳具有不燃烧也不支持燃烧、密度比空气大的性质
实验室制取气体的一般思路和方法
1.[知识填充]碳达峰和碳中和
(1)碳排放的最高点即碳峰值被称为________,人为碳排放与植树造林、碳捕集与封存技术等人为碳吸收达到平衡,称为__________。
(2)实现双碳目标的思路:①_______________________;②_______
________________。
任务五 碳达峰与碳中和
碳达峰
碳中和
减少二氧化碳的排放
增加二
氧化碳的消耗
2.[问题思考]观察下面的两幅图,回答下列问题:
(1)从1960年到2010年空气中二氧化碳含量呈________趋势。
(2)基于“碳循环”视角,实现“碳中和”可以从两方面进行:①_____________________,②增加二氧化碳消耗。图中自然界中消耗二氧化碳的途径有___________________(写一条即可)。
(3)在海水吸收二氧化碳和光合作用两个反应中,反应物相同,产物不同的原因是______________________。
增大
减少二氧化碳的排放
植物的光合作用
反应条件不同
1.(2024·烟台中考)我国力争2060年前实现“碳中和”,彰显大国责任与担当。“碳中和”的“碳”是指( )
A.二氧化碳 B.碳元素
C.碳原子 D.所有含碳物质
碳中和与碳达峰概念及措施
√
A [“碳中和”是指某个地区在一定时间内,人类活动直接和间接排放的碳总量,与通过植树造林、工业固碳等方式吸收的碳总量相互抵消,实现碳“净零排放”,这里的“碳”指的是二氧化碳。]
2.(2024·镇江中考)助力“碳中和”,CO2的产生、捕集与资源化利用是重要研究课题。
(1)CO2的产生:化石燃料的燃烧排放大量CO2。
①化石燃料主要包括_____、石油和天然气。
②大气中CO2的含量过高,会造成____________(填环境问题)。
煤
温室效应
(2)CO2的捕集:工业上可用氨水、(NH4)2CO3溶液等化学物质捕集烟气中的CO2。
氨水捕集CO2的实验流程如下。
①转化中可循环使用的物质X的化学式为__________。
②氨水吸收室中反应温度不宜过高,原因是____________________
_______________________________。
NH3
一水合氨易分解,温
度过高,一水合氨又分解成氨气
(3)CO2的利用:CO2和H2在Ni/CaO表面发生反应生成CH4的原理如图所示。
①整个转化过程中Ni/CaO的作用为________。
②生成CH4的总反应化学方程式为_____________________________。
催化
解析:(1)①化石燃料主要包括煤、石油和天然气。
②二氧化碳气体具有吸热和隔热的功能,二氧化碳在大气中增多的结果是形成一种无形的玻璃罩,使太阳辐射到地球上的热量无法向外层空间发散,其结果是地球表面变热起来,因此,二氧化碳也被称为温室气体,能引起温室效应,大气中二氧化碳含量的增加是导致温室效应的主要原因。
(2)①由氨水捕集CO2的实验流程图可知,富含CO2的烟气,进入氨水吸收室,生成碳酸铵和碳酸氢铵,碳酸铵和碳酸氢铵加热分解,生成X和高纯度CO2,X能被氨水吸收室吸收,根据质量守恒定律宏观实质:化学反应前后,元素种类不变可知,反应前碳酸铵和碳酸氢铵中含有碳、氢、氧元素,加热分解,生成X和高纯度CO2(含有碳元素和氧元素),X中可能含有氮元素和氢元素,X能被氨水吸收室吸收,说明X能与水反应,生成氨水,因此X为氨气,化学式为NH3。
②氨水吸收室中反应温度不宜过高,原因是一水合氨易分解,温度过高,一水合氨又分解成氨气和水。
关于碳中和与碳达峰的几个易混概念
1.碳中和、碳达峰以及所谓的低碳行动等中的“碳”都是指的二氧化碳;碳循环、氧循环中的碳、氧指的是碳元素和氧元素
2.碳循环、氧循环中都有化学变化发生,水循环是物理变化。
3.碳中和的思路包含两个方面,即:(1)降低二氧化碳的排放,具体措施有改善能源结构,减少使用化石能源等。(2)增加二氧化碳的消耗,具体措施有植树造林、通过人工方法对二氧化碳进行捕集、利用与封存等。
① ② ③ ④
白燃不燃烧 白磷不燃烧 白磷不燃烧 白磷燃烧
1.用如图所示实验探究燃烧的条件,下列说法正确的是( )
题号
1
3
5
2
4
6
8
7
9
10
分层评价 即时反馈
A.对比①③说明燃烧的条件之一是可燃物接触氧气
B.对比①④说明燃烧的条件之一是需要有可燃物
C.对比③④说明燃烧的条件之一是达到可燃物的着火点
D.本实验用盘成螺旋状的细铁丝替代白磷,能得到相同的实验结论
题号
1
3
5
2
4
6
8
7
9
10
√
题号
1
3
5
2
4
6
8
7
9
10
C [①③中均为冷水,③中虽通入O2,也不燃烧,故不能得出燃烧需要O2的结论,A错误;①④中存在两组变量,即冷水和热水、是否通O2,故无法得出正确结论,B错误;③④都通入了O2,冷水中不燃烧,热水中燃烧,故可得出燃烧条件之一是达到可燃物的着火点的结论,C正确;铁丝着火点高,在冷水、热水中均不会燃烧,D错误。]
2.人类生活和生产活动离不开火。下列有关说法中,不合理的是
( )
A.室内起火时,应立即打开所有门窗通风
B.炒菜时不慎油锅起火,可以盖上锅盖灭火
C.发生火灾时,用湿毛巾捂住口鼻,蹲下靠近地面,迅速离开火灾现场
D.加油站、面粉厂等场所要严禁烟火
题号
1
3
5
2
4
6
8
7
9
10
√
A [室内起火时,打开所有门窗,会使空气流通,使火势更大,A不合理;油锅着火时,盖上锅盖,能隔绝氧气,从而灭火,B合理;火灾现场会产生大量的烟尘和有害气体,其烟尘和有害气体会随热空气向上流动,故逃离火灾现场时,可用湿毛巾捂住口鼻,并尽量贴近地面逃离,C合理;加油站、面粉厂等场所空气中可燃物较多,应严禁烟火,D合理。]
题号
1
3
5
2
4
6
8
7
9
10
3.(2024·长沙中考)物质的性质决定物质的用途。下列含碳物质中,常用于去除冰箱、汽车中的异味的是( )
A.活性炭 B.金刚石
C.石墨 D.C60
题号
1
3
5
2
4
6
8
7
9
10
√
A [活性炭具有疏松多孔的结构,具有吸附性,用于去除冰箱、汽车中的异味,A正确;金刚石无吸附性,不能用于去除冰箱、汽车中的异味,B错误;石墨无吸附性,不能用于去除冰箱、汽车中的异味,C错误;C60不能用于去除冰箱、汽车中的异味,D错误。]
题号
1
3
5
2
4
6
8
7
9
10
4.为了预防火灾发生,我们应当了解燃烧与灭火的相关知识。下列说法正确的是( )
A.救火时不要贸然打开所有门窗,以免空气对流促进火势蔓延
B.生活中常用水来灭火,其原理主要是降低可燃物的着火点
C.蜡烛用嘴一吹即灭,是因为吹出的气体主要是二氧化碳
D.图书、档案、贵重设备、精密仪器等物失火,用干粉灭火器来灭火
题号
1
3
5
2
4
6
8
7
9
10
√
A [救火时不要贸然打开所有门窗,以免空气对流,可燃物与氧气接触更充分,燃烧更旺,使火势蔓延,A正确;生活中常用水来灭火,水蒸发吸热,其原理主要是降低温度至可燃物的着火点以下,着火点是物质的固有属性,不能改变,B错误;蜡烛用嘴一吹即灭,是因为空气流通带走热量,使蜡烛温度低于其着火点而达到灭火的目的,C错误;干粉灭火器使用过程中会产生水等物质,不能用于贵重设备、精密仪器等物失火,贵重设备、精密仪器等物失火,为了防止造成二次损害,应用液态二氧化碳灭火器,不会留下任何痕迹,D错误。]
题号
1
3
5
2
4
6
8
7
9
10
5.实验室制取CO2的有关操作如下图,不正确的是( )
题号
1
3
5
2
4
6
8
7
9
10
A.推动注射器时,长颈漏斗下端管中液面上升说明气密性良好 B.加入药品制气 C.若图中试剂为足量澄清石灰水,则可检验二氧化碳 D.用燃烧的木条验满
√
B [推动注射器时,锥形瓶内压强变大,长颈漏斗下端管中液面上升说明气密性良好,A正确;实验室不能用稀硫酸和大理石制取CO2,因为产物CaSO4是微溶物,会附着在大理石表面,阻止了反应的进一步进行,B不正确;二氧化碳能使澄清石灰水变浑浊,若图C中试剂为足量澄清石灰水,则可检验二氧化碳,C正确;因为二氧化碳不能燃烧也不支持燃烧,可以用燃着的木条验满,D正确。]
题号
1
3
5
2
4
6
8
7
9
10
6.“画说化学”是学科融合的重要方式,关于二氧化碳的相关性质同学们设计、绘制了下面的海报图片,对图中画面分析不正确的是( )
题号
1
3
5
2
4
6
8
7
9
10
题号
1
3
5
2
4
6
8
7
9
10
A.二氧化碳灭火器能灭火说明二氧化碳不助燃、不可燃、密度大于空气
B.二氧化碳能为植物的光合作用提供原料
C.碳酸饮料生产时,有一步是将二氧化碳压入水中,操作中二氧化碳仅发生了物理变化
D.石灰浆(含有氢氧化钙)刷在墙上会硬,是因为石灰浆与空气中二氧化碳反应生成碳酸钙
√
C [二氧化碳灭火器能灭火,利用了二氧化碳不助燃、不可燃、密度大于空气的性质,A正确;光合作用是绿色植物吸入二氧化碳,释放氧气的过程,二氧化碳为植物的光合作用提供原料,B正确;碳酸饮料生产时,将二氧化碳压入水中,该操作中二氧化碳不仅仅发生了物理变化,还发生了二氧化碳与水反应生成碳酸的化学变化,C错误;石灰浆(含有氢氧化钙)刷在墙壁上会硬,是因为石灰浆中的氢氧化钙会与空气中的二氧化碳反应生成碳酸钙,D正确。]
题号
1
3
5
2
4
6
8
7
9
10
7.“学化学,用化学”。下列做法错误的是( )
A.点燃可燃性气体前,一定要检验气体纯度
B.冬天用煤炉取暖时,室内放盆水防止中毒
C.图书馆着火,用二氧化碳灭火器扑灭
D.冰箱内放活性炭,吸附异味净化冰箱气体
题号
1
3
5
2
4
6
8
7
9
10
√
B [可燃性的气体混有空气时,点燃可能会发生爆炸,点燃可燃性气体前,一定要检验气体的纯度,A正确;一氧化碳难溶于水,在室内放一盆水不能防止中毒,B错误;二氧化碳不燃烧、不支持燃烧、密度比空气大,不损伤图书,图书馆着火,可用二氧化碳灭火器扑灭,C正确;活性炭具有吸附性,可以吸附异味,冰箱内放入活性炭,可以吸附异味净化冰箱气体,D正确。]
题号
1
3
5
2
4
6
8
7
9
10
8.(2024·安徽中考)如图是我国西汉青铜雁鱼灯及其示意图。灯油燃烧时,烟气通过鱼身和雁颈导入雁体内水中,减少对室内空气的污染。下列说法错误的是( )
题号
1
3
5
2
4
6
8
7
9
10
题号
1
3
5
2
4
6
8
7
9
10
A.该灯使用的青铜是一种金属材料
B.产生烟尘的原因是灯油不完全燃烧
C.转动灯罩隔绝空气,可使灯火熄灭
D.水能吸收烟尘,还能吸收一氧化碳
√
D [金属材料包括纯金属及合金,青铜是合金,属于金属材料,A正确;灯油不完全燃烧产生碳粒等烟尘,B正确;清除可燃物,隔绝空气,使温度降到着火点以下,都能达到灭火目的,所以转动灯罩隔绝空气,可使灯火熄灭,C正确;由于一氧化碳难溶于水,所以水不能吸收一氧化碳,D错误。]
题号
1
3
5
2
4
6
8
7
9
10
9.(2024·长春中考)火的使用标志着人类文明的巨大进步。汉字作为载体也反映了我国古代人民对火的认识。
(1)甲骨文“ ”(焚)的字形像是要燃火烧掉树林。上方的“林”相当于燃烧条件中的__________。
(2)小篆“ ”(灭)的字形左边像是一川流水,意思是水能灭火。用水灭火的主要原理是______________________和隔绝氧气。
题号
1
3
5
2
4
6
8
7
9
10
可燃物
降低温度到着火点以下
(3)甲骨文“ ”(灾)的字形像是房屋着火,灾难降临。
①以下标志与消防安全有关的是________(填字母)。
题号
1
3
5
2
4
6
8
7
9
10
A. B. C.
②发现或遭遇火灾,可采取的措施有__________________________
_____________(答一条即可)。
A
打火警电话119报警(或其他合
理答案)
解析:(1)燃烧条件包括:可燃物,氧气(或空气),达到燃烧时所需的最低温度(着火点)。所以上方的“林”相当于燃烧条件中的可燃物。(2)灭火的原理是清除可燃物,隔绝氧气,降温到着火点以下。所以用水灭火的主要原理是水蒸发吸热可降低温度到着火点以下,同时隔绝氧气。(3)①A.该图标是禁止烟火标志,与消防安全有关,A符合题意;B.该图标是我国制定的塑料包装制品回收标志,与消防安全无关,B不符合题意;C.该图标是我国国家节水标志,与消防安全无关,C不符合题意。②发现或遭遇火灾,可采取的措施有打火警电话119报警;遇火灾不可乘坐电梯,要向安全出口方向逃生; 当火势不是很大时,应沿着消防通道迅速往楼下跑等。
题号
1
3
5
2
4
6
8
7
9
10
10.(2024·广东中考)【基础实验和跨学科实践】 回答下列问题:
(1)CO2的制取及性质
ⅰ.制取CO2
组装一套便于添加稀盐酸的发生装置,需用到图1中的仪器有________(填字母)。
题号
1
3
5
2
4
6
8
7
9
10
ade
操作 现象 性质
X为澄清石灰水时,现象为_________________ CO2能与石灰水反应
X为____________时,现象为_____________ CO2能与水反应生成酸性物质
ⅱ.性质实验
题号
1
3
5
2
4
6
8
7
9
10
澄清石灰水变浑浊
紫色石蕊试液
试液变红色
操作 现象 性质
低处的蜡烛先熄灭,高处的蜡烛后熄灭 __________________;CO2不燃烧,也不支持燃烧
题号
1
3
5
2
4
6
8
7
9
10
CO2密度比空气大
(2)低碳行动方案
同学们展示如图2所示的方案,并交流讨论、完善方案。
题号
1
3
5
2
4
6
8
7
9
10
ⅰ.完善方案中的内容(各补写一条):
a._____________________,b.__________,c._________。
ⅱ.CO2物理利用________(填“能”或“不能”)从总量上减少CO2。
ⅲ.植树造林,利用绿色植物的________作用吸收CO2。
题号
1
3
5
2
4
6
8
7
9
10
减少一次性餐具的使用
人工降雨
碳酸饮料
不能
光合
解析:(1)ⅰ.组装便于添加稀盐酸的发生装置,应该选择长颈漏斗e,制取二氧化碳的反应为固液常温型,可以选择锥形瓶d,长颈漏斗需要橡胶塞,选择双孔橡胶塞a,则需要的仪器有ade。ⅱ.若X为澄清石灰水,澄清石灰水与二氧化碳反应会生成碳酸钙沉淀和水,现象是澄清石灰水变浑浊。二氧化碳与水反应生成碳酸,碳酸呈酸性,可以用紫色石蕊试液检验,碳酸能使紫色石蕊试液变红色。将二氧化碳倒入烧杯中,观察到低处的蜡烛先熄灭,高处的蜡烛后熄灭,说明了二氧化碳密度比空气大,二氧化碳不燃烧,不支持燃烧。
题号
1
3
5
2
4
6
8
7
9
10
(2)ⅰ.a中低碳生活,是指减少碳的排放,低能量、低消耗、低开支的生活方式有很多,如光盘行动、减纸减塑、衣物回收利用、减少一次性餐具的使用、低碳出行等。b中二氧化碳的物理利用,不产生新物质的用途,包括冷藏保鲜、人工降雨、灭火等。c中二氧化碳化学利用,产生新的物质的用途,包括转化成甲醇、制作碳酸饮料、作气体肥料。ⅱ.根据图中“CO2物理利用”,可以知道利用二氧化碳冷藏保鲜、人工降雨,不能从总量上减少CO2。ⅲ.植树造林,绿色植物可以进行光合作用,二氧化碳和水在叶绿体中,在光照的条件下,反应生成有机物,并释放氧气,是利用植物的光合作用吸收二氧化碳。
题号
1
3
5
2
4
6
8
7
9
10
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
(时间:40分钟 满分:60分)
一、选择题(本题包括15小题,每小题2分,共30分)
1.(2024·东营中考)我国提出2030年前实现“碳达峰”,2060年前实现“碳中和”。下列做法不利于实现“碳达峰,碳中和”的是
( )
[A]绿色出行 [B]焚烧垃圾
[C]节约用纸 [D]随手关灯
限时提能训练(六) 控制燃烧
√
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
B [绿色出行,可以减少化石燃料的使用,减少二氧化碳的排放,利于实现“碳达峰,碳中和”,A不符合题意;焚烧垃圾,会产生大量的二氧化碳,不利于实现“碳达峰,碳中和”,B符合题意;节约用纸,可以节约资源,减少森林的砍伐,增加二氧化碳的吸收,利于实现“碳达峰,碳中和”,C不符合题意;随手关灯,可以节约能源,减少化石燃料的使用,减少二氧化碳的排放,利于实现“碳达峰,碳中和”,D不符合题意。]
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
2.(2024·北京中考)下列标志表示“禁止烟火”的是( )
[A] [B] [C] [D]
√
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
C [A.该标志是腐蚀品标志,不符合题意;B.该标志是爆炸品标志,不符合题意;C.该标志是禁止烟火标志,符合题意;D.该标志是禁止放易燃物标志,不符合题意。]
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
3.(2024·枣庄中考)生活处处即化学,对下列生活现象解释合理的是( )
[A]煤炉火越扇越旺——增大可燃物浓度
[B]煤粉比煤块燃烧更旺——增大与氧气的接触面积
[C]油锅着火放入青菜后熄灭——降低油的着火点
[D]移除炉灶内木柴后灶火熄灭——隔绝空气
√
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
B [煤炉火越扇越旺,是因为增大了氧气的浓度,A错误;煤粉比煤块燃烧更旺,是因为增大了可燃物与氧气的接触面积,B正确;油锅着火放入青菜后熄灭,是因为温度降低至油的着火点以下,C错误;移除炉灶内木柴后灶火熄灭,是因为移除了可燃物,D错误。]
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
4.(2024·枣庄中考)“碳家族”成员众多,用途广泛。下列说法错误的是( )
[A]一氧化碳可用于冶炼金属
[B]碳酸氢钠可用于配制波尔多液
[C]甲烷可用作燃料
[D]葡萄糖可用于配制注射液
√
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
B [一氧化碳具有还原性,能还原金属氧化物,则可用于冶炼金属,A正确;波尔多液是由硫酸铜和氢氧化钙配制成的,B错误;甲烷具有可燃性,可作燃料,C正确;葡萄糖属于糖类,可用于配制注射液,D正确。]
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
5.化学兴趣小组在进行可燃物燃烧条件探究时,设计了如下两个实验:实验①:在装满空气的试管内放入白磷,关闭弹簧夹,白磷不燃烧;实验②:将实验①的装置放到80 ℃热水中,白磷剧烈燃烧,气球胀大(已知:白磷的着火点为40 ℃)。下列说法不正确的是( )
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
[A]白磷在空气中充分燃烧,该化学反应属于氧化反应
[B]实验②中白磷剧烈燃烧时,试管内气体压强减小
[C]实验②结束后,试管内还有白磷残留,打开弹簧夹通入空气,白磷复燃,说明燃烧还需要与空气接触
[D]对比实验①②,说明可燃物燃烧需要的条件之一是温度达到可燃物的着火点
√
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
B [白磷在空气中与氧气充分燃烧,该化学反应是物质与氧气发生的反应,属于氧化反应,A正确;实验②中白磷剧烈燃烧时,放出大量的热,试管内气体压强增大,B错误;燃烧的条件三者缺一不可,实验②结束后,试管内还有白磷残留,打开弹簧夹通入空气,白磷复燃,说明燃烧还需要与空气接触,C正确;燃烧的条件三者缺一不可,对比实验①②,①中白磷温度没有达到着火点,与氧气接触,不燃烧,②中白磷温度达到着火点,与氧气接触,燃烧,说明可燃物燃烧需要的条件之一是温度达到可燃物的着火点,D正确。]
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
6.(2024·扬州中考)自然界存在多种元素及物质的循环。下图表示的是自然界中的( )
[A]氮循环 [B]硫循环 [C]碳循环 [D]水循环
√
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
C [由图可知,化石燃料燃烧产生二氧化碳,动植物呼吸作用生成二氧化碳,动植物的遗体和排泄物通过缓慢氧化生成二氧化碳,绿色植物通过光合作用吸收二氧化碳,故该图表示的是自然界中的碳循环。]
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
7.如图为我国不同年份的能源结构图。下列说法不正确的是( )
[A]我国能源结构中清洁能源占比呈增加趋势
[B]加大水电、风电的开发利用有利于减少环境污染
[C]天然气是比煤炭和石油更清洁的燃料
[D]液氢用作火箭燃料是因为氢气易于贮存和加注
√
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
D [由图示可知,我国能源结构中清洁能源占比呈增加趋势,A项正确;加大水电、风电的开发利用可以减少化石能源的利用,减少污染物的排放,有利于减少环境污染,B项正确;天然气燃烧生成二氧化碳和水,因此天然气是比煤炭和石油更清洁的燃料,C项正确;液氢用作火箭燃料是因为氢气热值高,并不是氢气易于贮存和加注,D项错误。]
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
8.下列有关燃烧与灭火的说法错误的是( )
[A]加油站、面粉加工厂必须严禁烟火
[B]用水灭火,其原理是降低了可燃物的着火点
[C]将煤球做成蜂窝状,其目的是增大煤与空气的接触面积,使燃料充分燃烧
[D]遭遇火灾要采取必要的自救措施,如用湿毛巾捂住口鼻,蹲下靠近地面跑离着火区域等
√
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
B [加油站、面粉加工厂周围的空气中可燃物含量比较高,则必须严禁烟火,防止发生爆炸,A正确;着火点为物质的固有属性,不能改变,用水灭火,是降低可燃物温度至着火点以下,B错误;将煤球做成蜂窝状,可增大煤与空气的接触面积,从而使燃料充分燃烧,C正确;湿毛巾有类似防毒面具作用,用湿毛巾捂住口鼻能防止吸入烟尘,气体受热密度变小,有毒气体上升聚集在高处,则应用湿毛巾捂住口鼻,D正确。]
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
9.(2024·福建中考)下列灭火方法主要是利用“使温度降到可燃物着火点以下”原理的是( )
[A]用灯帽盖灭酒精灯火焰 [B]关闭燃气灶阀门熄灭火焰
[C]用水浇灭炭火 [D]用锅盖盖灭油锅火焰
√
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
C [A.灯帽盖灭酒精灯,利用的是隔绝氧气的原理;B.关闭燃气灶阀门熄灭火焰,利用的是清除可燃物的原理;C.用水浇灭炭火,水汽化吸热,是利用使温度降到可燃物的着火点以下原理;D.用锅盖盖灭油锅火焰,利用的是隔绝氧气的原理。]
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
10.数字化实验化学兴趣小组同学采用图1装置对可燃性粉尘爆炸进行探究,爆炸的剧烈程度可用产生的最大压力来衡量。下列说法正确的是( )
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
[A]在有限的空间内,可燃性粉尘遇明火就会发生爆炸
[B]该实验中施加给打气筒的压力不同对实验结果没有影响
[C]根据图2可知,可燃性粉尘颗粒直径越大,爆炸威力越小
[D]根据图3可知,容器中可燃性粉尘的浓度越大,爆炸威力越大
√
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
C [可燃性粉尘在空气中的含量达到爆炸极限时,遇到明火才会发生爆炸,A错误;压力越大,可燃性粉尘与空气的接触越充分,爆炸的可能性越大、威力越大,B错误;根据题图2可知,可燃性粉尘颗粒直径越大,爆炸威力越小,C正确;根据题图3可知,开始时容器中可燃性粉尘的浓度越大,爆炸威力越大,当可燃性粉尘的浓度达到一定值后,可燃性粉尘浓度越大,爆炸威力反而越小,D错误。]
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
11.根据图示,分析下列说法,有关碳单质的说法正确的是( )
[A]石墨是最软的物质 [B]活性炭可以吸附异味
[C]金刚石不具有可燃性 [D]足球烯是由碳原子直接构成
√
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
B [石墨是最软的矿物之一,不是最软的物质,A错误;活性炭具有吸附性,可以吸附异味,B正确;金刚石是由碳组成的单质,具有可燃性,C错误;金刚石、石墨是由碳原子直接构成的,但足球烯是由足球烯分子构成的,D错误。]
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
12.(2023·宜宾中考)元素化合价和物质类别是研究物质的两个重要维度。如图为碳元素的部分“价—类”二维图。下列说法正确的是( )
[A]M为“混合物”
[B]X点对应的物质只有一种
[C]Y点对应的物质为CO2
[D]CO可与Ca(OH)2反应生成CaCO3
√
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
C [一氧化碳属于氧化物,A项错误;X点是碳元素组成的单质,X可以是金刚石、石墨等,B项错误;Y和一氧化碳的物质类别相同,所以Y点对应的物质为CO2,C项正确;一氧化碳不会与氢氧化钙反应生成碳酸钙沉淀,二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,D项错误。]
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
13.化学学习要形成科学的化学观念,比如分类观、变化观、转化观等。如右图所示是碳及其部分化合物的转化关系,请运用上述观念判断以下观点错误的是( )
[A]C和CO都有还原性
[B]反应②不可能是化合反应
[C]C和CO2也能发生化学反应
[D]②和③在一定条件下均能实现逆向转化
√
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
B [C和CO均能夺取氧化物中的氧,具有还原性,A项正确;反应②为一氧化碳转化为二氧化碳,可以是通过一氧化碳与氧气点燃生成二氧化碳,由两种物质生成一种物质,属于化合反应,B项错误;C和CO2高温下反应生成CO,有新物质生成,属于化学变化,C项正确;②的逆向转化可以通过C和CO2在高温下反应生成CO实现,③的逆向转化可通过CO2与Ca(OH)2生成CaCO3和H2O实现,D项正确。]
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
14.下列现象可用同一化学原理解释的是①久置石灰水的试剂瓶壁上有一层白膜;②用吸管向澄清石灰水中吹气,石灰水变浑浊;③检验二氧化碳气体;④向紫色石蕊试液中通入二氧化碳气体,试液变红;⑤蘸过石灰水的鸡蛋更易保存。( )
[A]②③④ [B]①②④ [C]①③④⑤ [D]①②③⑤
√
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
D [①久置的石灰水会和空气中的二氧化碳反应,生成碳酸钙沉淀;②用吸管向澄清石灰水中吹气,澄清石灰水会和呼出气体中的二氧化碳反应,生成碳酸钙沉淀;③二氧化碳能使澄清石灰水变浑浊,实验室常用澄清石灰水变浑浊检验二氧化碳气体;④向紫色石蕊试液中通入二氧化碳气体,试液变红的原因是二氧化碳和水反应生成碳酸,碳酸使紫色石蕊试液变红;⑤石灰水中的氢氧化钙会与二氧化碳反应生成碳酸钙沉淀,堵住了蛋壳上的气孔,隔绝了氧气,达到保鲜的目的,D项正确。]
[A]①装置的优点是能随时控制反应的发生与停止
[B]②处现象说明二氧化碳能使紫色石蕊试液变红
[C]③处溶液变浑浊,是因为生成了不溶于水的碳酸钙
[D]④处的实验说明二氧化碳不能燃烧也不能支持燃烧
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
15.某兴趣小组利用如图装置对二氧化碳的性质进行探究,下列说法错误的是( )
√
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
B [①装置可通过打开和关闭活塞,实现固液接触和分离,控制反应的发生与停止,A正确;②处紫色石蕊试液变红是由于二氧化碳和水反应生成了碳酸,碳酸显酸性,能使紫色石蕊试液变红,不是二氧化碳,B错误;二氧化碳和水反应生成碳酸钙沉淀和水,可观察到③处溶液变浑浊,C正确;D处蜡烛熄灭,说明二氧化碳能透过隔板下部小孔与燃着的蜡烛接触,导致蜡烛熄灭,说明二氧化碳密度比空气大,不能燃烧也不能支持燃烧,D正确。]
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
二、填空与简答题(本题包括3小题,共15分)
16.(3分)A、B、C、D、E是初中化学常见的五种物质,A是石灰石的主要成分,E是能与血红蛋白结合的有毒气体,→表示转化关系,部分反应条件未注明。回答下列问题
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
(1)写出物质B的化学式________。
(2)写出C与D反应转化为A的化学方程式_______________________
_______________________。
CaO
CO2+Ca(OH)2===
CaCO3↓+H2O
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
解析:(1)A、B、C、D、E是初中化学常见的五种物质,A是石灰石的主要成分,A是碳酸钙;E是能与血红蛋白结合的有毒气体,E是一氧化碳,碳酸钙高温条件下分解生成氧化钙和二氧化碳,二氧化碳与碳在高温条件下反应生成一氧化碳,故C是二氧化碳;物质B是氧化钙,化学式为CaO。
(2)氧化钙和水反应生成氢氧化钙,故D是氢氧化钙;一氧化碳燃烧生成二氧化碳,二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,C与D反应转化为A的化学方程式:CO2+Ca(OH)2===CaCO3↓+ H2O。
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
17.(6分)(2023·枣庄中考)天然气不仅是优质的能量来源,还是宝贵的化工资源。经过多年努力,我国在天然气的开发利用方面已取得重大突破。
方法一:煤气化生成一氧化碳和二氧化碳。在高温、高压和“甲烷化催化剂”的作用下,一氧化碳、二氧化碳分别与氢气反应生成甲烷,其中“甲烷化催化剂”在这两个化学反应过程中发挥着至关重要的作用。
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
方法二:开发煤层气。煤层气指储存在煤层中,以甲烷为主要成分的烃类物质,俗称“瓦斯”,是与煤伴生、共生的气体资源。
方法三:开发可燃冰。可燃冰的主要成分是甲烷水合物,甲烷水合物能稳定存在的压强和温度范围如图所示。可燃冰一旦离开海床便迅速分解,容易发生井喷意外,还可能会破坏地壳
稳定平衡,引发海底塌方,导致大规模
海啸,所以可燃冰的开采困难。
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
甲烷化催化剂
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
(3)从物质分类角度分析,方法二中的煤层气属于________(填“纯净物”或“混合物”)。
(4)根据方法三,判断有关可燃冰的说法正确的是________。
A.在15 ℃和100 atm时,可燃冰能稳定存在
B.可燃冰开采时若出现差错,可能导致严重的自然灾害
(5)“碳中和”中的“碳”是指________(填“CO”或“CO2”)。我国政府提出在2060年前实现“碳中和”,下列做法符合“碳中和”理念的是________。
A.植树造林 B.焚烧秸秆 C.节能减排 D.燃放烟花
混合物
B
CO2
AC
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
(3)煤层气以甲烷为主要成分,还含有其他物质,属于混合物。
(4)A.由图可知,在15 ℃和100 atm时,可燃冰不能稳定存在,已经转化为甲烷气体和水,不符合题意;B.可燃冰一旦离开海床便迅速分解,容易发生井喷意外,还可能会破坏地壳稳定平衡,引发海底塌方,导致大规模海啸,故可燃冰开采时若出现差错,可能导致严重的自然灾害,符合题意。
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
(5)“碳中和”中的“碳”是指CO2;A.植树造林,可以增加二氧化碳的吸收,减少二氧化碳的含量,符合“碳中和”理念,符合题意;B.焚烧秸秆会产生大量的二氧化碳,不符合“碳中和”理念,不符合题意;C.节能减排,可以减少二氧化碳的排放,符合“碳中和”理念,符合题意;D.燃放烟花,会产生大量的二氧化碳,不符合“碳中和”理念,不符合题意。
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
18.(6分)(2024·枣庄中考)气体制备与性质探究是初中化学实验的重要内容,相关装置如图所示。
回答下列问题:
(1)仪器甲的名称为________。
分液漏斗
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
(2)实验室制取二氧化碳气体应选择的发生装置为________(填字母序号);制取时发生反应的化学方程式为________________________
____________________________。
(3)若要收集一瓶干燥的二氧化碳,气体流经C装置时的入口端为________(填“a”或“b”)。
A
CaCO3+2HCl===CaCl2+
H2O+CO2↑
b
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
(4)在三颈烧瓶D中用排空气法收集CO2气体,检验气密性后,在t1时快速注入一种溶液,t3时快速注入另一种溶液,测得瓶内压强随时间变化曲线如图所示。下列说法正确的是________。
①三颈烧瓶D中收集的CO2气体不纯
②t1时注入的是氢氧化钠溶液
③t3后发生的只是中和反应
①②
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
解析:(1)根据仪器特征,仪器甲的名称为分液漏斗。
(2)实验室用大理石(或石灰石,主要成分都是碳酸钙)和稀盐酸制取二氧化碳,根据反应物的状态为固体和液体,反应条件为常温,实验室制取二氧化碳气体应选择的发生装置为固液常温型发生装置A;碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,该反应的化学方程式为CaCO3+2HCl===CaCl2+H2O+CO2↑。
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
(3)若要收集一瓶干燥的二氧化碳,气体流经C装置时的入口端为b,干燥剂能与气体充分接触,接反,容易把浓硫酸排出,造成事故。
(4)由压强随时间变化曲线图可知,在t1时快速注入一种溶液,瓶内压强迅速减小,t1时注入的溶液是氢氧化钠溶液,二氧化碳能与氢氧化钠溶液反应生成碳酸钠和水,使瓶内气体积减小,压强减小;t2~t3期间压强不变且大于0,可证明收集的二氧化碳气体不纯;t3时快速注入另一种溶液,瓶内压强增大,t3时注入的是稀盐酸,盐酸与碳酸钠反应生成氯化钠、水和二氧化碳,使瓶内气体积增大,压强增大,该反应不属于中和反应,盐酸与过量氢氧化钠的反应属于中和反应。所以①②正确,③错误。
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
三、实验与计算题(本题包括2小题,共15分)
19.(9分)(2024·青岛中考)化学反应需要一定的条件,控制条件可以调控化学反应。“启航”小组以“调控化学反应”为主题展开探究,请回答下列问题。
【生火有道】
(1)观察生活:小组同学观察到天然气、木炭能燃烧,而水和石头不能燃烧,得出燃烧的条件之一是________。
可燃物
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
实验探究:为继续探究燃烧的条件,小组同学设计并完成了图1所示实验。
已知:白磷着火点40 ℃,红磷着火点240 ℃。磷燃烧时产生污染空气的五氧化二磷白烟。
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
【现象与结论】
(2)①铜片上的白磷燃烧,红磷不燃烧,得出燃烧的条件之一是____________________________________。
②小红根据_________________________________________________
现象,得出燃烧的条件之一是可燃物与氧气接触。
温度达到可燃物的着火点
铜片上的白磷燃烧,而热水中的白磷不燃烧
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
【评价与反思】
(3)①实验中小组同学认为图1装置存在不足,于是设计了图2所示装置。图2装置的优点为____________。
环保
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
②小明对小红的结论提出质疑,设计了图3所示装置,对燃烧过程中的氧气含量进行测定,得到图4所示图像。结合图像分析,“可燃物与氧气接触”应准确地表述为____________________________。
可燃物与足够浓度的氧气接触
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
【调控有术】
化学反应速率与多种因素有关,为探究影响过氧化氢分解速率的因素,小组同学分别取足量且等质量的过氧化氢溶液完成了下列实验。
实验序号 过氧化氢溶液的浓度 二氧化锰粉末的质量/g 温度/℃ 10秒共收集到氧气的体积/mL
① 3% 0 10 几乎无
② 5% 0 20 几乎无
③ 5% 0.5 20 14
④ 10% 0.5 20 80
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
(4)探究催化剂对过氧化氢分解速率的影响,应选择的实验序号是________;对比实验③和实验④,可得出的结论是______________
_________________________________________;上述实验无法探究出__________________________因素对过氧化氢分解速率的影响(写一条即可)。
②③
相同条件下,
过氧化氢溶液浓度越大,反应速率越快
催化剂的种类(合理即可)
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
【应用有方】
(5)通过探究,小组同学认识到,生活中也可以通过控制条件促进或抑制化学反应。
①用天然气做饭,发现炉火火焰呈黄色,锅底出现黑色物质,这时需要________(填“调大”或“调小”)灶具的进风口。
②炒菜时如果油锅着火,可采取的灭火措施是__________________
_________(写一条即可)。
调大
用锅盖盖灭(合理即
可)
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
解析:(1)小组同学观察到天然气、木炭能燃烧,而水和石头不能燃烧,得出燃烧的条件之一是可燃物,天然气、木材具有可燃性,而水和石头不具有可燃性。
(2)①白磷和红磷都属于可燃物,且都与氧气接触,铜片上的白磷燃烧,红磷不燃烧,得出燃烧的条件之一是温度达到可燃物的着火点。
②铜片上的白磷和水中的白磷属于同一种物质,且着火点相同,小红根据铜片上的白磷燃烧,而热水中的白磷不燃烧现象,得出燃烧的条件之一是可燃物与氧气接触。
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
(3)①实验中小组同学认为图1装置存在不足,白磷燃烧有大量白烟生成,污染环境,图2所示装置是在密闭环境中进行实验,不会污染环境,装置的优点为环保。
②由图3和图4可知:白磷燃烧消耗试管中的氧气,氧气的含量逐渐减少,当氧气浓度小于10%时,白磷不再燃烧,结合图像分析,“可燃物与氧气接触”应准确地表述为可燃物与足够浓度的氧气接触。
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
(4)探究催化剂对过氧化氢分解速率的影响,变量是有无催化剂,过氧化氢溶液的浓度,反应时的温度必须相同,应选择的实验序号是②③;对比实验③和实验④,催化剂粉末质量相同,反应时温度相同,只有过氧化氢溶液的浓度不同,浓度越大,相同时间内收集氧气的体积越大,可得出的结论是相同条件下,过氧化氢溶液浓度越大,反应速率越快;上述实验无法探究出催化剂的种类因素对过氧化氢分解速率的影响。
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
(5)①用天然气做饭,发现炉火火焰呈黄色,锅底出现黑色物质,说明氧气不充足,燃烧不充分,这时需要调大灶具进风口,使燃烧更充分。
②炒菜时如果油锅着火,可采取的灭火措施是用锅盖盖灭,对应灭火的原理是隔绝空气。
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
20.(6分)(2024·枣庄期末)长期使用的花洒、热水壶底部和热水锅炉有一层水垢,主要成分是碳酸钙和氢氧化镁。项目小组为测定某水垢中碳酸钙的含量,取水垢样品,分成不同质量的4份于烧杯中,然后分别加入250 g相同质量分数的稀盐酸,充分反应后测得的实验数据如下:
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
计算水垢中碳酸钙的质量分数(要求写出计算过程)。
实验组数 一组 二组 三组 四组
水垢的质量/g 10 20 30 40
烧杯中剩余物质总质量/g 256.7 263.4 271.2 281.2
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
解:根据质量守恒定律,第一组加入10 g水垢时产生二氧化碳的质量为250 g+10 g-256.7 g=3.3 g;
第二组加入20 g水垢产生二氧化碳的质量为250 g+20 g-263.4 g=6.6 g;第三组加入30 g水垢产生二氧化碳的质量为250 g+30 g-271.2 g=8.8 g,如果第三组盐酸充足应产生9.9 g二氧化碳,计算数据说明第三组实验时盐酸不充足,所以用第一组实验数据进行计算。
设10 g水垢中碳酸钙的质量为x,则:
题号
1
3
5
2
4
6
8
7
9
10
11
12
13
14
15
16
17
18
19
20
同课章节目录
