鲁教版高中化学选修三第三章第二节有机化合物结构的测定第二课时作业设计
文档属性
| 名称 | 鲁教版高中化学选修三第三章第二节有机化合物结构的测定第二课时作业设计 |

|
|
| 格式 | docx | ||
| 文件大小 | 456.5KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-20 00:00:00 | ||
图片预览

文档简介
选修3第3章第2节有机化合物结构的测定——有机化合物结构式的确定
第2课时 作业设计
【基础题组】
1.某有机化合物在氧气中充分燃烧,生成水蒸气和CO2物质的量之比为1∶1,由此得出的结论是( )
A.该有机化合物分子中C、H、O原子个数比为1∶2∶3 B.分子中C、H原子个数比为1∶2
C.有机化合物中必定含有氧 D.有机化合物中一定不含氧
2.下列说法不正确的是( )
A.有机分子中插入O原子对不饱和度没有影响
B.有机分子中去掉H原子对不饱和度没有影响
C.用CH原子团代替有机分子中的N原子对有机分子的不饱和度没有影响
D.烷烃和饱和一元醇的不饱和度都为0
3.下列化合物中核磁共振氢谱上只出现三个峰且峰面积之比为3∶2∶2的是( )
4.鉴别环己醇()和3,3 二甲基丁醛,可采用化学方法或物理方法,下列方法中不能对二者进行鉴别的是( )
A.利用金属钠或金属钾 B.利用质谱法
C.利用红外光谱法 D.利用核磁共振氢谱
5.某小组在实验室研究一种有机物,按顺序采取以下步骤确定其结构,采用的方法不正确的是( )
A.利用沸点不同蒸馏提纯该有机物
B.利用燃烧法确定该有机物的实验式为C2H6O
C.利用核磁共振氢谱确定该有机物的相对分子质量为46
D.利用红外光谱图确定该有机物分子中含O—H键
6.在核磁共振氢谱中出现两组峰,其氢原子数之比为 3∶2 的化合物是( )
7.将0.1 mol某有机物与0.3 mol O2混合,将燃烧产物通入过量的澄清石灰水中,可得到沉淀20.0 g,溶液质量减少5.8 g;剩余气体继续通过灼热的CuO,可以使CuO质量减少1.6 g,由此可知该有机物的分子式为( )
A.C2H6O B.C3H6O C.C3H6O2 D.C4H8O2
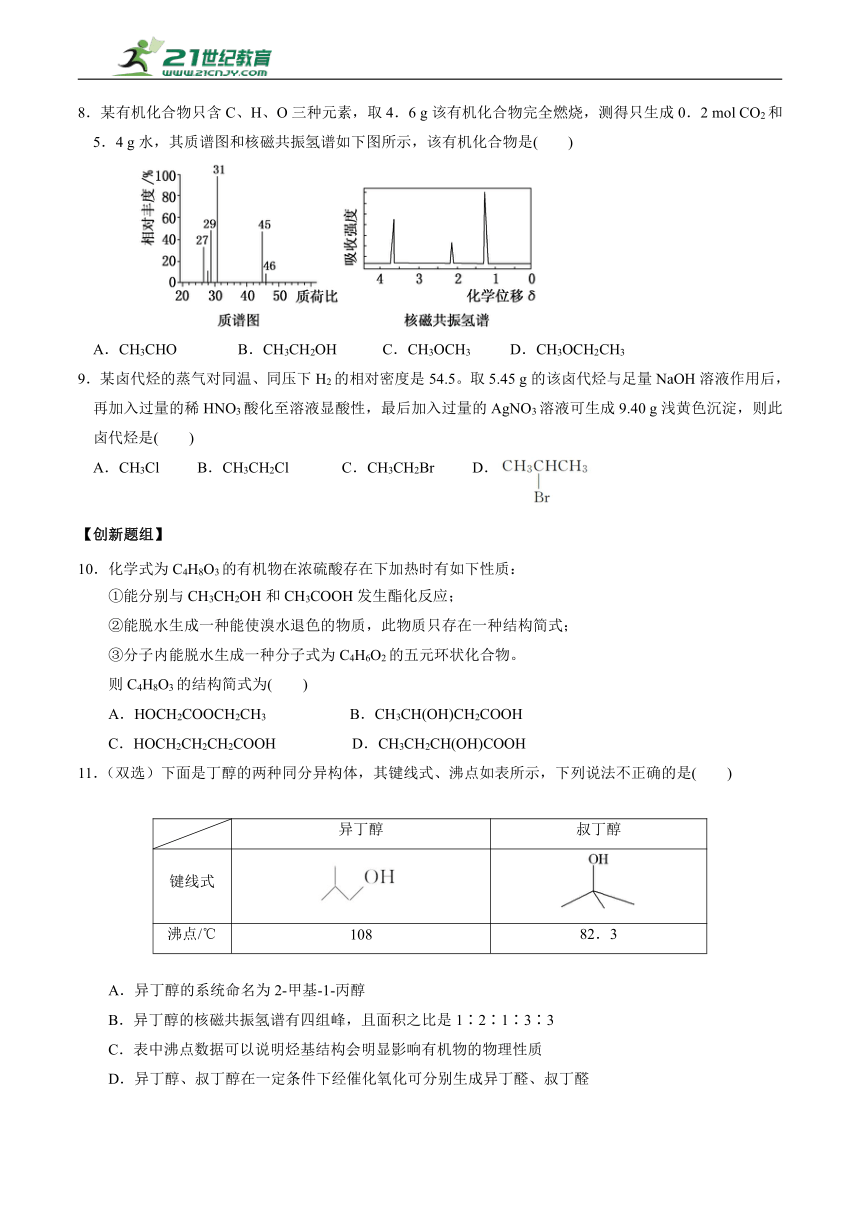
8.某有机化合物只含C、H、O三种元素,取4.6 g该有机化合物完全燃烧,测得只生成0.2 mol CO2和5.4 g水,其质谱图和核磁共振氢谱如下图所示,该有机化合物是( )
A.CH3CHO B.CH3CH2OH C.CH3OCH3 D.CH3OCH2CH3
9.某卤代烃的蒸气对同温、同压下H2的相对密度是54.5。取5.45 g的该卤代烃与足量NaOH溶液作用后,再加入过量的稀HNO3酸化至溶液显酸性,最后加入过量的AgNO3溶液可生成9.40 g浅黄色沉淀,则此卤代烃是( )
A.CH3Cl B.CH3CH2Cl C.CH3CH2Br D.
【创新题组】
10.化学式为C4H8O3的有机物在浓硫酸存在下加热时有如下性质:
①能分别与CH3CH2OH和CH3COOH发生酯化反应;
②能脱水生成一种能使溴水退色的物质,此物质只存在一种结构简式;
③分子内能脱水生成一种分子式为C4H6O2的五元环状化合物。
则C4H8O3的结构简式为( )
A.HOCH2COOCH2CH3 B.CH3CH(OH)CH2COOH
C.HOCH2CH2CH2COOH D.CH3CH2CH(OH)COOH
11.(双选)下面是丁醇的两种同分异构体,其键线式、沸点如表所示,下列说法不正确的是( )
异丁醇 叔丁醇
键线式
沸点/℃ 108 82.3
A.异丁醇的系统命名为2 甲基 1 丙醇
B.异丁醇的核磁共振氢谱有四组峰,且面积之比是1∶2∶1∶3∶3
C.表中沸点数据可以说明烃基结构会明显影响有机物的物理性质
D.异丁醇、叔丁醇在一定条件下经催化氧化可分别生成异丁醛、叔丁醛
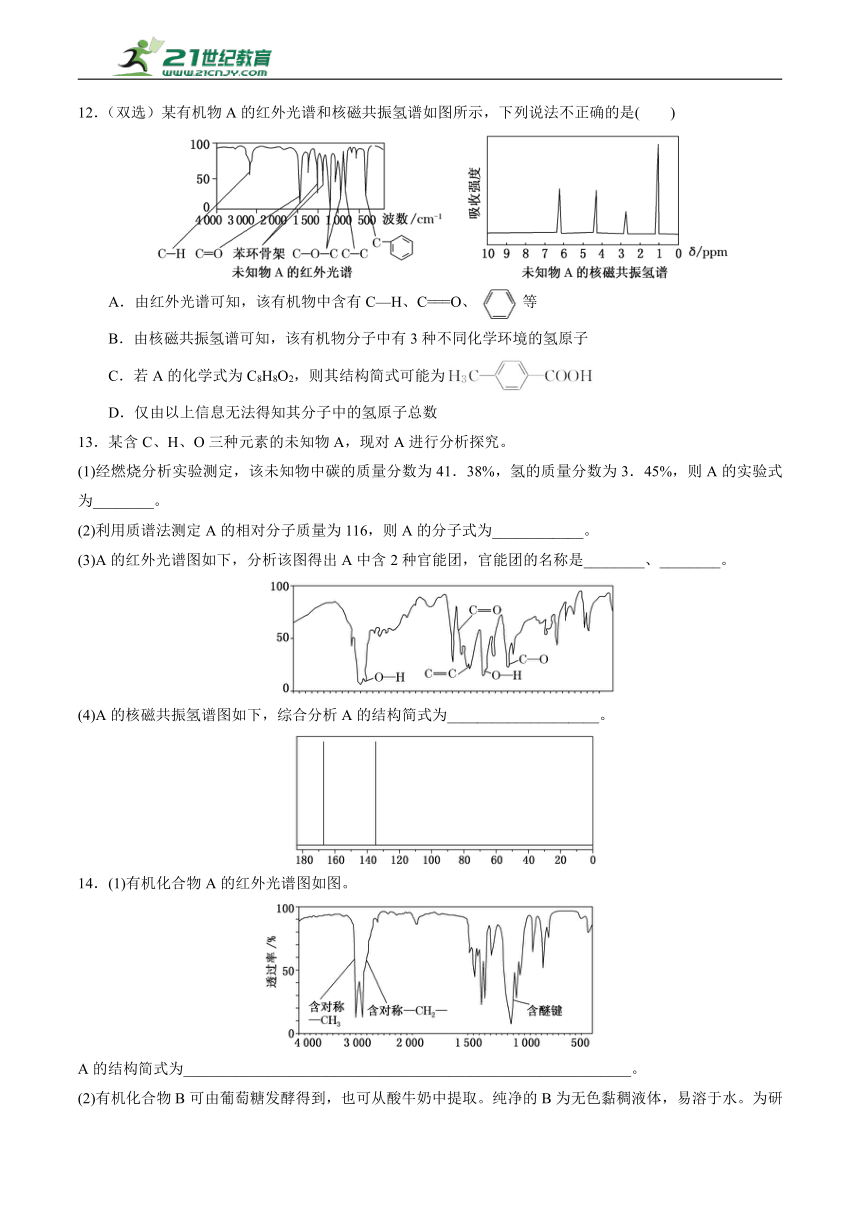
12.(双选)某有机物A的红外光谱和核磁共振氢谱如图所示,下列说法不正确的是( )
A.由红外光谱可知,该有机物中含有C—H、C===O、等
B.由核磁共振氢谱可知,该有机物分子中有3种不同化学环境的氢原子
C.若A的化学式为C8H8O2,则其结构简式可能为
D.仅由以上信息无法得知其分子中的氢原子总数
13.某含C、H、O三种元素的未知物A,现对A进行分析探究。
(1)经燃烧分析实验测定,该未知物中碳的质量分数为41.38%,氢的质量分数为3.45%,则A的实验式为________。
(2)利用质谱法测定A的相对分子质量为116,则A的分子式为____________。
(3)A的红外光谱图如下,分析该图得出A中含2种官能团,官能团的名称是________、________。
(4)A的核磁共振氢谱图如下,综合分析A的结构简式为____________________。
14.(1)有机化合物A的红外光谱图如图。
A的结构简式为___________________________________________________________。
(2)有机化合物B可由葡萄糖发酵得到,也可从酸牛奶中提取。纯净的B为无色黏稠液体,易溶于水。为研究B的组成与结构,进行了如下实验。
实验步骤 解释或实验结论
①称取B 9.0 g,升温使其气化,测其密度是相同条件下H2的45倍 试通过计算填空:B的相对分子质量为______
②将此9.0 g B在足量纯O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4 g和13.2 g B的分子式为________
③另取B 9.0 g,跟足量的NaHCO3粉末反应,生成2.24 L CO2(标准状况),若与足量金属钠反应则生成2.24 L H2(标准状况) 写出B中含有的官能团:________
④B的核磁共振氢谱如图: B中含有________种氢原子
⑤综上所述,B的结构简式为______________________
15.(全国卷Ⅱ)化合物G是治疗高血压的药物“比索洛尔”的中间体,一种合成G的路线如下:
已知以下信息:
①A的核磁共振氢谱为单峰;B的核磁共振氢谱为三组峰,峰面积比为6∶1∶1。
②D的苯环上仅有两种不同化学环境的氢;1 mol D可与1 mol NaOH或2 mol Na反应。
回答下列问题:
(1)A的结构简式为________________。
(2)B的化学名称为________________。
(3)C与D反应生成E的化学方程式为_______________________________________。
(4)由E生成F的反应类型为________________。
(5)G的分子式为________________。
(6)L是D的同分异构体,可与FeCl3溶液发生显色反应,1 mol的L可与2 mol的Na2CO3反应,L共有______种;其中核磁共振氢谱为四组峰,峰面积比为3∶2∶2∶1的结构简式为________、________。
选修3第3章第2节有机化合物结构的测定——有机化合物结构式的确定
第2课时 课时作业 参考答案
【基础题组】
1.B 【解析】 因生成CO2和H2O的物质的量比为1∶1则n(C)∶n(H)=1∶(1×2)=1∶2,不能判断有机物中是否含有氧元素。
2.B 【解析】 分子的不饱和度为n(C)+1-,可知去掉H原子不饱和度增大,B不正确;分子中含有氧原子时不予考虑,A、D正确;分子中含有氮原子时,在氢原子总数中减去氮原子数:不饱和度=n(C)+1-,若用CH代替N原子则多1个C和1个H,少一个N,不饱和度不变,C正确。
3.B 【解析】 A、D项的核磁共振氢谱中均有2个峰,且峰面积之比均为2∶3;C项的核磁共振氢谱中有2个峰,峰面积之比是1∶3。
4.B 【解析】 二者互为同分异构体,相对分子质量相同,无法利用质谱法鉴别。
5.C 【解析】 蒸馏是利用物质的沸点不同分离提纯的方法,故A正确;利用燃烧法可以确定生成的二氧化碳和水的量,从而确定碳氢比,根据质量守恒确定是否含有O,因此可以得到该有机物的实验式C2H6O,故B正确;利用核磁共振氢谱可以确定该有机物中氢原子的化学环境和个数比,不能确定相对分子质量,故C错误;利用红外光谱图可以确定有机物分子中的化学键类型和官能团,因此可以确定是否含O—H键,故D正确。
6.D 【解析】 A中有2种氢原子,个数比为3∶1;B中有3种氢原子,个数比为3∶1∶1;C中有3种氢原子,个数比为1∶3∶4;D中有2种氢原子,个数比为3∶2。
7.C 【解析】 将燃烧产物通入过量的澄清石灰水中,可得到沉淀20 g为生成CaCO3的质量,其物质的量为 =0.2 mol,根据碳原子守恒知生成CO2的物质的量为0.2 mol,该有机物的燃烧产物可以使CuO还原为Cu,说明有CO产生,可以使CuO减少1.6 g,则n(CO)=0.1 mol,故0.1 mol有机物含有C原子为0.2 mol+0.1 mol=0.3 mol;由题意知,溶液质量减少5.8 g,故燃烧生成水的质量为20 g-0.2 mol×44 g·mol-1-5.8 g=5.4 g,故n(H2O)= =0.3 mol,故0.1 mol有机物含有H原子为0.3 mol×2=0.6 mol;故n(有机物)∶n(C)∶n(H)∶n(O)=0.1 mol∶
0.3 mol∶0.6 mol∶(0.2×2+0.3+0.1-0.3×2)mol=1∶3∶6∶2,故该有机物分子式为C3H6O2。
8. B 【解析】 4.6 g该有机物完全燃烧,生成了0.2 mol CO2和5.4 g H2O,则n(H2O)= =0.3 mol,n(H)=0.6 mol,因m(C)+m(H)=0.2 mol×12 g·mol-1+0.6 mol×1 g·mol-1=3 g<4.6 g,故有机物含有O元素,且m(O)=4.6 g-3 g=1.6 g,故n(O)==0.1 mol,n(C)∶n(H)∶n(O)=0.2 mol∶0.6 mol∶0.1 mol=2∶6∶1,即该有机物的实验式为C2H6O,由质谱图可知相对分子质量为46,则有机物的分子式为C2H6O,因核磁共振氢谱中含3种H原子,三种H原子数目之比为1∶2∶3,所以有机物的结构简式为CH3CH2OH。
9.C 【解析】 Mr(卤代烃)=54.5×2=109,n(卤代烃)= =0.05 mol,n(AgBr)==0.05 mol,因此该卤代烃是一溴代烃,故分子式为RBr,Mr(R—)=109-80=29,即R—为CH3CH2—。
【创新题组】
10.C 【解析】 该有机物能够和CH3CH2OH及CH3COOH发生酯化反应,说明其分子内含有—COOH和—OH。能够脱水生成使溴水退色的物质,再结合C4H8O3的不饱和度,说明此生成物中含有,即和—OH相连的碳原子的邻位碳原子上必定有H原子。该有机物能够发生分子内脱水反应生成分子式为C4H6O2的五元环状化合物,则生成的五元环的结点为四个C原子和一个O原子,所以该有机物应为直链状,即HOCH2CH2CH2COOH。
11 .BD 【解析】异丁醇中羟基位于1号C,主链为1 丙醇,在2号C含有1个甲基,其名称为2 甲基 1 丙醇,故A正确;异丁醇分子中含有4种不同化学环境的H原子,则异丁醇的核磁共振氢谱有四组峰,且面积之比是1∶1∶2∶6,故B错误;叔丁醇沸点较低,异丁醇的沸点较高,可是二者官能团相同,相对分子质量相同,碳原子数相同,只有烃基结构不同,沸点数据可以说明烃基结构会明显影响有机物的物理性质,故C正确;叔丁醇与羟基相连的碳原子上没有氢原子,不能催化氧化,故D错误。
12.BC
【解析】 由红外光谱图可知A中含有C—H、C===O、等,故A正确;核磁共振氢谱有4组峰,则有机物分子中有4种不同化学环境的氢原子,故B错误;由红外光谱可知不含O—H,则不含有羧基,故C错误;红外光谱和核磁共振氢谱用于确定结构,确定不了分子式,故无法确定含有的H原子数,故D正确。
13. [答案] (1)CHO (2)C4H4O4 (3)羧基 碳碳双键 (4)HOOC—CH===CH—COOH
[解析] (1)根据已知碳的质量分数是41.38%,氢的质量分数是3.45%,则氧元素质量分数是1-41.38%-3.45%=55.17%,则该物质中碳、氢、氧原子个数之比= ≈1∶1∶1,由原子个数比可知该有机物的实验式为CHO;(2)根据A的实验式为CHO,设A的分子式为CnHnOn,则12×n+1×n+16×n=116,解得n=4,则A的分子式为C4H4O4;(3)根据A的红外光谱图得出A中含2种官能团分别为碳碳双键、羧基;(4)根据A的核磁共振氢谱图可知有两种类型的氢原子,且个数比为1∶1,则A的结构简式为HOOC—CH===CH—COOH。
14.【答案】(1)CH3CH2OCH2CH3 (2)①90 ②C3H6O3 ③—COOH、—OH ④4
【解析】(1)由A的红外光谱图可知,A分子中含有对称的甲基、对称的亚甲基和醚键,则A为二乙醚,结构简式为CH3CH2OCH2CH3;(2)①由其密度是相同条件下H2的45倍,可知B的相对分子质量为45×2=90;②由题意可知,B的物质的量为n(B)= =0.1 mol,n(C)=n(CO2)= =0.3 mol,n(H)=2n(H2O)= ×2=0.6 mol,n(O)==0.3 mol,n(B)∶n(C)∶n(H)∶n(O)=0.1 mol∶0.3 mol∶0.6 mol∶0.3 mol=1∶3∶6∶3,则B的分子式为C3H6O3;③0.1 mol B与足量的NaHCO3反应放出0.1 mol CO2,说明B分子中应含有1个羧基,与足量金属钠反应则生成0.1 mol H2,说明B分子中还含有1个羟基;④由B分子的核磁共振氢谱中有4个吸收峰,面积之比为1∶1∶1∶3,可知B中含有4种不同环境的氢原子;⑤B的分子式为C3H6O3,分子中含有1个羟基和1个羧基,且含有4种H原子,则B的结构简式为 。
15.
推得E的结构简式为 ,最后由G的结构简式及F→G的合成路线,逆推得F的结构简式为 。(6)根据L遇FeCl3溶液发生显色反应可知L中含酚羟基,再结合D的分子式和1 mol L能与2 mol Na2CO3反应,可知L中含2个酚羟基和1个—CH3,2个酚羟基位于苯环邻位、间位和对位时,—CH3所处的位置分别有2种、3种和1种,即L共有6种可能的结构。其中核磁共振氢谱中有四组峰,且峰面积之比为3∶2∶2∶1的结构。
第2课时 作业设计
【基础题组】
1.某有机化合物在氧气中充分燃烧,生成水蒸气和CO2物质的量之比为1∶1,由此得出的结论是( )
A.该有机化合物分子中C、H、O原子个数比为1∶2∶3 B.分子中C、H原子个数比为1∶2
C.有机化合物中必定含有氧 D.有机化合物中一定不含氧
2.下列说法不正确的是( )
A.有机分子中插入O原子对不饱和度没有影响
B.有机分子中去掉H原子对不饱和度没有影响
C.用CH原子团代替有机分子中的N原子对有机分子的不饱和度没有影响
D.烷烃和饱和一元醇的不饱和度都为0
3.下列化合物中核磁共振氢谱上只出现三个峰且峰面积之比为3∶2∶2的是( )
4.鉴别环己醇()和3,3 二甲基丁醛,可采用化学方法或物理方法,下列方法中不能对二者进行鉴别的是( )
A.利用金属钠或金属钾 B.利用质谱法
C.利用红外光谱法 D.利用核磁共振氢谱
5.某小组在实验室研究一种有机物,按顺序采取以下步骤确定其结构,采用的方法不正确的是( )
A.利用沸点不同蒸馏提纯该有机物
B.利用燃烧法确定该有机物的实验式为C2H6O
C.利用核磁共振氢谱确定该有机物的相对分子质量为46
D.利用红外光谱图确定该有机物分子中含O—H键
6.在核磁共振氢谱中出现两组峰,其氢原子数之比为 3∶2 的化合物是( )
7.将0.1 mol某有机物与0.3 mol O2混合,将燃烧产物通入过量的澄清石灰水中,可得到沉淀20.0 g,溶液质量减少5.8 g;剩余气体继续通过灼热的CuO,可以使CuO质量减少1.6 g,由此可知该有机物的分子式为( )
A.C2H6O B.C3H6O C.C3H6O2 D.C4H8O2
8.某有机化合物只含C、H、O三种元素,取4.6 g该有机化合物完全燃烧,测得只生成0.2 mol CO2和5.4 g水,其质谱图和核磁共振氢谱如下图所示,该有机化合物是( )
A.CH3CHO B.CH3CH2OH C.CH3OCH3 D.CH3OCH2CH3
9.某卤代烃的蒸气对同温、同压下H2的相对密度是54.5。取5.45 g的该卤代烃与足量NaOH溶液作用后,再加入过量的稀HNO3酸化至溶液显酸性,最后加入过量的AgNO3溶液可生成9.40 g浅黄色沉淀,则此卤代烃是( )
A.CH3Cl B.CH3CH2Cl C.CH3CH2Br D.
【创新题组】
10.化学式为C4H8O3的有机物在浓硫酸存在下加热时有如下性质:
①能分别与CH3CH2OH和CH3COOH发生酯化反应;
②能脱水生成一种能使溴水退色的物质,此物质只存在一种结构简式;
③分子内能脱水生成一种分子式为C4H6O2的五元环状化合物。
则C4H8O3的结构简式为( )
A.HOCH2COOCH2CH3 B.CH3CH(OH)CH2COOH
C.HOCH2CH2CH2COOH D.CH3CH2CH(OH)COOH
11.(双选)下面是丁醇的两种同分异构体,其键线式、沸点如表所示,下列说法不正确的是( )
异丁醇 叔丁醇
键线式
沸点/℃ 108 82.3
A.异丁醇的系统命名为2 甲基 1 丙醇
B.异丁醇的核磁共振氢谱有四组峰,且面积之比是1∶2∶1∶3∶3
C.表中沸点数据可以说明烃基结构会明显影响有机物的物理性质
D.异丁醇、叔丁醇在一定条件下经催化氧化可分别生成异丁醛、叔丁醛
12.(双选)某有机物A的红外光谱和核磁共振氢谱如图所示,下列说法不正确的是( )
A.由红外光谱可知,该有机物中含有C—H、C===O、等
B.由核磁共振氢谱可知,该有机物分子中有3种不同化学环境的氢原子
C.若A的化学式为C8H8O2,则其结构简式可能为
D.仅由以上信息无法得知其分子中的氢原子总数
13.某含C、H、O三种元素的未知物A,现对A进行分析探究。
(1)经燃烧分析实验测定,该未知物中碳的质量分数为41.38%,氢的质量分数为3.45%,则A的实验式为________。
(2)利用质谱法测定A的相对分子质量为116,则A的分子式为____________。
(3)A的红外光谱图如下,分析该图得出A中含2种官能团,官能团的名称是________、________。
(4)A的核磁共振氢谱图如下,综合分析A的结构简式为____________________。
14.(1)有机化合物A的红外光谱图如图。
A的结构简式为___________________________________________________________。
(2)有机化合物B可由葡萄糖发酵得到,也可从酸牛奶中提取。纯净的B为无色黏稠液体,易溶于水。为研究B的组成与结构,进行了如下实验。
实验步骤 解释或实验结论
①称取B 9.0 g,升温使其气化,测其密度是相同条件下H2的45倍 试通过计算填空:B的相对分子质量为______
②将此9.0 g B在足量纯O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重5.4 g和13.2 g B的分子式为________
③另取B 9.0 g,跟足量的NaHCO3粉末反应,生成2.24 L CO2(标准状况),若与足量金属钠反应则生成2.24 L H2(标准状况) 写出B中含有的官能团:________
④B的核磁共振氢谱如图: B中含有________种氢原子
⑤综上所述,B的结构简式为______________________
15.(全国卷Ⅱ)化合物G是治疗高血压的药物“比索洛尔”的中间体,一种合成G的路线如下:
已知以下信息:
①A的核磁共振氢谱为单峰;B的核磁共振氢谱为三组峰,峰面积比为6∶1∶1。
②D的苯环上仅有两种不同化学环境的氢;1 mol D可与1 mol NaOH或2 mol Na反应。
回答下列问题:
(1)A的结构简式为________________。
(2)B的化学名称为________________。
(3)C与D反应生成E的化学方程式为_______________________________________。
(4)由E生成F的反应类型为________________。
(5)G的分子式为________________。
(6)L是D的同分异构体,可与FeCl3溶液发生显色反应,1 mol的L可与2 mol的Na2CO3反应,L共有______种;其中核磁共振氢谱为四组峰,峰面积比为3∶2∶2∶1的结构简式为________、________。
选修3第3章第2节有机化合物结构的测定——有机化合物结构式的确定
第2课时 课时作业 参考答案
【基础题组】
1.B 【解析】 因生成CO2和H2O的物质的量比为1∶1则n(C)∶n(H)=1∶(1×2)=1∶2,不能判断有机物中是否含有氧元素。
2.B 【解析】 分子的不饱和度为n(C)+1-,可知去掉H原子不饱和度增大,B不正确;分子中含有氧原子时不予考虑,A、D正确;分子中含有氮原子时,在氢原子总数中减去氮原子数:不饱和度=n(C)+1-,若用CH代替N原子则多1个C和1个H,少一个N,不饱和度不变,C正确。
3.B 【解析】 A、D项的核磁共振氢谱中均有2个峰,且峰面积之比均为2∶3;C项的核磁共振氢谱中有2个峰,峰面积之比是1∶3。
4.B 【解析】 二者互为同分异构体,相对分子质量相同,无法利用质谱法鉴别。
5.C 【解析】 蒸馏是利用物质的沸点不同分离提纯的方法,故A正确;利用燃烧法可以确定生成的二氧化碳和水的量,从而确定碳氢比,根据质量守恒确定是否含有O,因此可以得到该有机物的实验式C2H6O,故B正确;利用核磁共振氢谱可以确定该有机物中氢原子的化学环境和个数比,不能确定相对分子质量,故C错误;利用红外光谱图可以确定有机物分子中的化学键类型和官能团,因此可以确定是否含O—H键,故D正确。
6.D 【解析】 A中有2种氢原子,个数比为3∶1;B中有3种氢原子,个数比为3∶1∶1;C中有3种氢原子,个数比为1∶3∶4;D中有2种氢原子,个数比为3∶2。
7.C 【解析】 将燃烧产物通入过量的澄清石灰水中,可得到沉淀20 g为生成CaCO3的质量,其物质的量为 =0.2 mol,根据碳原子守恒知生成CO2的物质的量为0.2 mol,该有机物的燃烧产物可以使CuO还原为Cu,说明有CO产生,可以使CuO减少1.6 g,则n(CO)=0.1 mol,故0.1 mol有机物含有C原子为0.2 mol+0.1 mol=0.3 mol;由题意知,溶液质量减少5.8 g,故燃烧生成水的质量为20 g-0.2 mol×44 g·mol-1-5.8 g=5.4 g,故n(H2O)= =0.3 mol,故0.1 mol有机物含有H原子为0.3 mol×2=0.6 mol;故n(有机物)∶n(C)∶n(H)∶n(O)=0.1 mol∶
0.3 mol∶0.6 mol∶(0.2×2+0.3+0.1-0.3×2)mol=1∶3∶6∶2,故该有机物分子式为C3H6O2。
8. B 【解析】 4.6 g该有机物完全燃烧,生成了0.2 mol CO2和5.4 g H2O,则n(H2O)= =0.3 mol,n(H)=0.6 mol,因m(C)+m(H)=0.2 mol×12 g·mol-1+0.6 mol×1 g·mol-1=3 g<4.6 g,故有机物含有O元素,且m(O)=4.6 g-3 g=1.6 g,故n(O)==0.1 mol,n(C)∶n(H)∶n(O)=0.2 mol∶0.6 mol∶0.1 mol=2∶6∶1,即该有机物的实验式为C2H6O,由质谱图可知相对分子质量为46,则有机物的分子式为C2H6O,因核磁共振氢谱中含3种H原子,三种H原子数目之比为1∶2∶3,所以有机物的结构简式为CH3CH2OH。
9.C 【解析】 Mr(卤代烃)=54.5×2=109,n(卤代烃)= =0.05 mol,n(AgBr)==0.05 mol,因此该卤代烃是一溴代烃,故分子式为RBr,Mr(R—)=109-80=29,即R—为CH3CH2—。
【创新题组】
10.C 【解析】 该有机物能够和CH3CH2OH及CH3COOH发生酯化反应,说明其分子内含有—COOH和—OH。能够脱水生成使溴水退色的物质,再结合C4H8O3的不饱和度,说明此生成物中含有,即和—OH相连的碳原子的邻位碳原子上必定有H原子。该有机物能够发生分子内脱水反应生成分子式为C4H6O2的五元环状化合物,则生成的五元环的结点为四个C原子和一个O原子,所以该有机物应为直链状,即HOCH2CH2CH2COOH。
11 .BD 【解析】异丁醇中羟基位于1号C,主链为1 丙醇,在2号C含有1个甲基,其名称为2 甲基 1 丙醇,故A正确;异丁醇分子中含有4种不同化学环境的H原子,则异丁醇的核磁共振氢谱有四组峰,且面积之比是1∶1∶2∶6,故B错误;叔丁醇沸点较低,异丁醇的沸点较高,可是二者官能团相同,相对分子质量相同,碳原子数相同,只有烃基结构不同,沸点数据可以说明烃基结构会明显影响有机物的物理性质,故C正确;叔丁醇与羟基相连的碳原子上没有氢原子,不能催化氧化,故D错误。
12.BC
【解析】 由红外光谱图可知A中含有C—H、C===O、等,故A正确;核磁共振氢谱有4组峰,则有机物分子中有4种不同化学环境的氢原子,故B错误;由红外光谱可知不含O—H,则不含有羧基,故C错误;红外光谱和核磁共振氢谱用于确定结构,确定不了分子式,故无法确定含有的H原子数,故D正确。
13. [答案] (1)CHO (2)C4H4O4 (3)羧基 碳碳双键 (4)HOOC—CH===CH—COOH
[解析] (1)根据已知碳的质量分数是41.38%,氢的质量分数是3.45%,则氧元素质量分数是1-41.38%-3.45%=55.17%,则该物质中碳、氢、氧原子个数之比= ≈1∶1∶1,由原子个数比可知该有机物的实验式为CHO;(2)根据A的实验式为CHO,设A的分子式为CnHnOn,则12×n+1×n+16×n=116,解得n=4,则A的分子式为C4H4O4;(3)根据A的红外光谱图得出A中含2种官能团分别为碳碳双键、羧基;(4)根据A的核磁共振氢谱图可知有两种类型的氢原子,且个数比为1∶1,则A的结构简式为HOOC—CH===CH—COOH。
14.【答案】(1)CH3CH2OCH2CH3 (2)①90 ②C3H6O3 ③—COOH、—OH ④4
【解析】(1)由A的红外光谱图可知,A分子中含有对称的甲基、对称的亚甲基和醚键,则A为二乙醚,结构简式为CH3CH2OCH2CH3;(2)①由其密度是相同条件下H2的45倍,可知B的相对分子质量为45×2=90;②由题意可知,B的物质的量为n(B)= =0.1 mol,n(C)=n(CO2)= =0.3 mol,n(H)=2n(H2O)= ×2=0.6 mol,n(O)==0.3 mol,n(B)∶n(C)∶n(H)∶n(O)=0.1 mol∶0.3 mol∶0.6 mol∶0.3 mol=1∶3∶6∶3,则B的分子式为C3H6O3;③0.1 mol B与足量的NaHCO3反应放出0.1 mol CO2,说明B分子中应含有1个羧基,与足量金属钠反应则生成0.1 mol H2,说明B分子中还含有1个羟基;④由B分子的核磁共振氢谱中有4个吸收峰,面积之比为1∶1∶1∶3,可知B中含有4种不同环境的氢原子;⑤B的分子式为C3H6O3,分子中含有1个羟基和1个羧基,且含有4种H原子,则B的结构简式为 。
15.
推得E的结构简式为 ,最后由G的结构简式及F→G的合成路线,逆推得F的结构简式为 。(6)根据L遇FeCl3溶液发生显色反应可知L中含酚羟基,再结合D的分子式和1 mol L能与2 mol Na2CO3反应,可知L中含2个酚羟基和1个—CH3,2个酚羟基位于苯环邻位、间位和对位时,—CH3所处的位置分别有2种、3种和1种,即L共有6种可能的结构。其中核磁共振氢谱中有四组峰,且峰面积之比为3∶2∶2∶1的结构。
