鲁教版高中化学选修三第三章第二节有机化合物结构的测定第一课时课件(共30张PPT)
文档属性
| 名称 | 鲁教版高中化学选修三第三章第二节有机化合物结构的测定第一课时课件(共30张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1007.5KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-20 00:00:00 | ||
图片预览









文档简介
(共30张PPT)
选择性必修3第3章第2节
有机化合物结构的测定——有机化合物分子式的确定第1课时
1.学会测定有机物元素含量、相对分子质量的一般方法,建立确定有
机物分子式的思维模型。
2.能通过燃烧分析法、质谱法等微观探析有机物分子的元素组成、相
对分子质量及元素的质量分数。
3.学会蒸馏法、萃取法、重结晶法的实验原理,根据有机物性质的差
异选择有机化合物分离、提纯的正确方法。
核心素养发展目标
当人们从自然界中得到某一新化合物并将其提纯以后,测定其结构就是最重要的工作了。只有确定了这种化合物分子的结构,才能进一步了解和应用这种化合物。
在有机合成中,对天然产物合成的首要工作就是测定目标化合物分子的结构;而对人工设计的有机化合物,在合成后也必须测定其结构才能确定它是否就是目标产物。
那么,怎样对有机化合物进行结构测定呢?结构测定在有机化学中有什么重要作用?
联想质疑
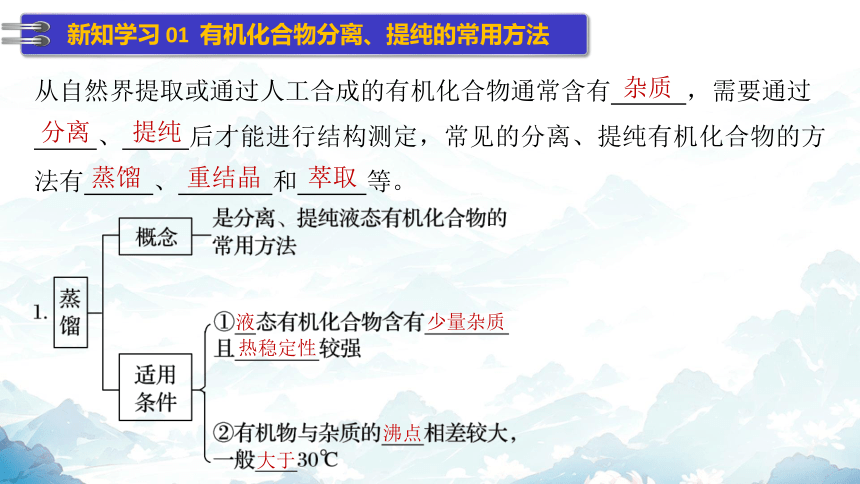
从自然界提取或通过人工合成的有机化合物通常含有 ,需要通过
、 后才能进行结构测定,常见的分离、提纯有机化合物的方法有 、 和 等。
杂质
分离
提纯
蒸馏
重结晶
萃取
液
大于
少量杂质
热稳定性
沸点
新知学习 01 有机化合物分离、提纯的常用方法
3.萃取是 有机化合物的常用方法。
类型 液-液萃取:利用待分离组分在两种 的溶剂中的______不同,将其从一种溶剂转移到另一种溶剂中的过程。一般是用有机溶剂从水中萃取有机化合物
固-液萃取:用 从 物质中 出待分离组分的过程
萃取剂 对萃取剂的要求:
①萃取剂与原溶剂 ;
②溶质在萃取剂中的溶解度 在原溶剂中的溶解度;
③萃取剂与原溶液中的成分不反应
常用萃取剂: 、 、 等
萃取剂与有机化合物的分离 (1) 法
(2) 法
富集
互不相溶
溶解性
溶剂
固体
溶解
互不相溶
远大于
蒸馏
反萃取
乙醚
石油醚
二氯甲烷
(1)能用分液的方法分离植物油和水的混合物( )
(2)Br2、I2在水中的溶解度较小,但易溶于有机溶剂,故可用酒精萃取溴水中的Br2或碘水中的I2( )
(3)利用蒸馏法分离液态有机物时,温度计可以插入液面以下( )
(4)在蒸馏实验中,发现忘记加沸石,应立即停止实验,马上加入( )
(5)重结晶要求杂质的溶解度比被提纯的物质小才能进行分离( )
(6)常用重结晶法提纯苯甲酸( )
√
×
×
×
×
√
正误判断
现拟分离乙酸乙酯、乙酸和乙醇的混合物,下图是分离操作步骤流程图。
已知各物质的沸点:
乙酸乙酯 77.1 ℃ 乙醇 78.5 ℃ 乙酸 118 ℃
请回答下列问题:
(1)试剂(a)为________________,试剂(b)为______。
饱和Na2CO3溶液
硫酸
理解应用
(2)图中的分离方法分别是①为______;②为______;③为______。
(3)写出下列有机物的化学式:
A_________________、B________________________、C____________、
D___________、E___________。
分液
蒸馏
蒸馏
CH3COOH
CH3COOCH2CH3
CH3CH2OH、CH3COONa
CH3COONa
CH3CH2OH
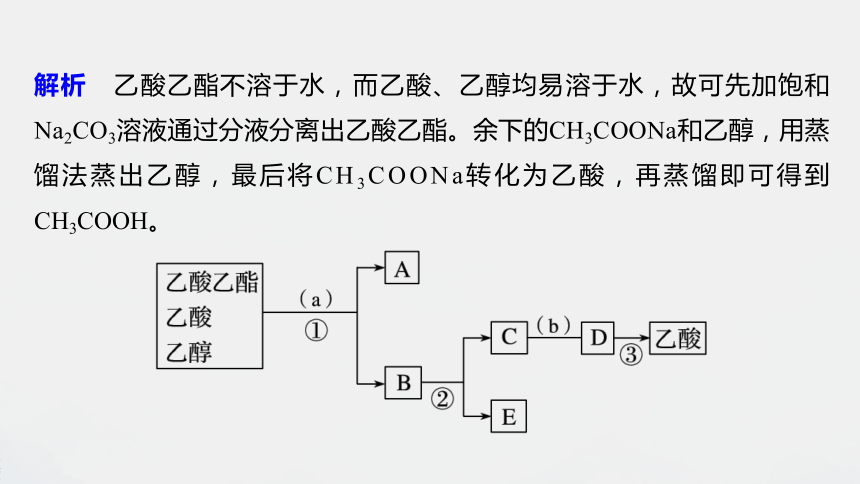
解析 乙酸乙酯不溶于水,而乙酸、乙醇均易溶于水,故可先加饱和Na2CO3溶液通过分液分离出乙酸乙酯。余下的CH3COONa和乙醇,用蒸馏法蒸出乙醇,最后将CH3COONa转化为乙酸,再蒸馏即可得到CH3COOH。
物质的性质与分离、提纯方法的选择
(1)根据物质的溶解性差异,可选用结晶、过滤的方法将混合物分离。
(2)根据物质的沸点差异,可选用蒸馏的方法将互溶性液体混合物分离。
(3)根据物质在不同溶剂中溶解性的差异,用萃取的方法把溶质从溶解性小的溶剂中转移到溶解性较大的溶剂中。
返回
归纳总结
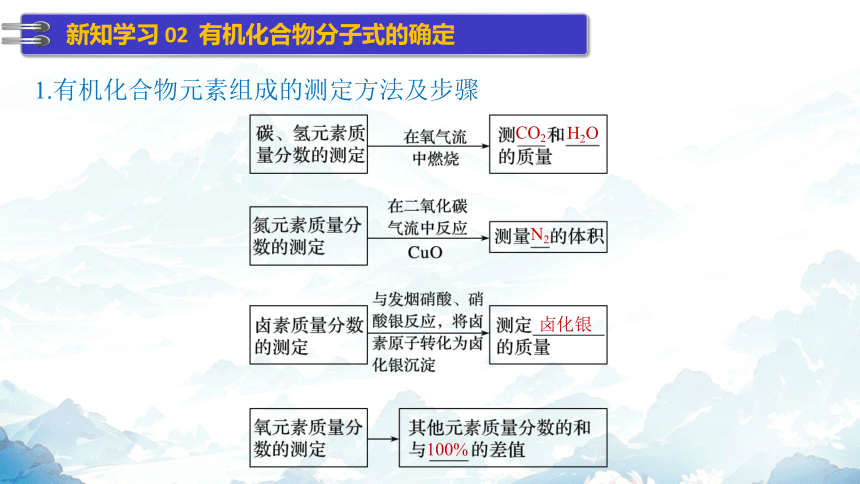
1.有机化合物元素组成的测定方法及步骤
100%
CO2
H2O
N2
卤化银
新知学习 02 有机化合物分子式的确定
2.有机物相对分子质量的测定
(1)通过实验,根据有关数据求算相对分子质量。
(2)有机物的相对分子质量一般用 进行测定。
3.有机化合物分子式的确定
质谱仪
(1)验证有机物属于烃时只需测定产物中的CO2和H2O的物质的量之比
( )
(2)有机物燃烧后只生成CO2和H2O的物质不一定只含有碳、氢两种元素
( )
(3)有机物的实验式、分子式一定不同( )
(4)元素分析法和质谱法能分别确定有机物的实验式和相对分子质量( )
(5)质谱图中最右边的谱线表示的数值为该有机物的相对分子质量( )
×
√
×
√
√
正误判断
1.实验测得某碳氢化合物A中,含碳80%,含氢20%,该化合物的实验式为______。又测得该化合物的相对分子质量是30,该化合物的分子式为______。
CH3
C2H6
理解应用
方法一:设该化合物分子式为(CH3)n,
方法二:A分子式中各元素原子的数目:
故该化合物A的分子式是C2H6。
2.某化合物6.4 g在氧气中完全燃烧,只生成8.8 g CO2和7.2 g H2O。
(1)计算确定该有机物实验式_______。
CH4O
m(C)=0.2 mol×12 g·mol-1=2.4 g
m(H)=0.4 mol×2×1 g·mol-1=0.8 g
m(C)+m(H)=2.4 g+0.8 g=3.2 g<6.4 g
所以n(C)∶n(H)∶n(O)=0.2∶0.8∶0.2=1∶4∶1。
则实验式为:CH4O。
(2)若该有机物的蒸气对空气的相对密度为1.10,则该有机物的分子式为_______。
CH4O
解析 该有机物的相对分子质量为1.10×29≈32
由于实验式的式量也为32,因而其分子式为CH4O。
1.确定有机物是否含O元素的方法
有机物完全燃烧产物为CO2和H2O,通过相关的实验可以先确定CO2和H2O的质量,进而求得有机物中所含碳元素和氢元素的质量。
①若m(有机物)=m(C)+m(H),则说明该有机物中只含C和H两种元素。
②若m(有机物)>m(C)+m(H),且完全燃烧只生成CO2和H2O,则说明有机物中含有C、H、O三种元素,其中m(O)=m(有机物)-m(C)-m(H)。
归纳总结
2.确定有机物分子式的一般途径
返回
1.下列说法不正确的是
A.蒸馏是分离、提纯液态有机化合物的常用方法
B.重结晶的首要工作是选择适当的溶剂
C.萃取包括液—液萃取和固—液萃取
D.研究有机化合物可首先进行元素定量分析,再分离、提纯
1
2
3
4
√
解析 研究有机化合物的基本步骤首先应该是分离、提纯,然后再进行元素定量分析,所以D不正确。
随堂演练
2.下列有关实验的说法错误的是
A.在蒸馏实验中,温度计的水银球位于支管口处是为了测出馏分的沸点
B.用结晶法分离硝酸钾和氯化钠的混合物,用分液法分离水和硝基苯的
混合物
C.在重结晶的实验中,使用短颈漏斗趁热过滤是为了减少被提纯物质的
损失
D.作为重结晶实验的溶剂,杂质在此溶液中的溶解度受温度影响应该很大
√
1
2
3
4
解析 在蒸馏实验中,温度计的水银球位于支管口处是为了测出馏分的沸点,故A正确;
硝酸钾的溶解度随温度升高而急剧增大,氯化钠的溶解度随温度变化很小,所以用结晶法分离硝酸钾和氯化钠的混合物,水和硝基苯不互溶,所以用分液法分离水和硝基苯的混合物,故B正确;
在重结晶实验中,要求被提纯物和杂质的溶解度随温度的变化差别很大,杂质在此溶液中的溶解度受温度影响不一定很大,故D错误。
1
2
3
4
3.(武汉高二月考)某有机物在氧气中充分燃烧,生成的水蒸气和CO2的物质的量比为1∶1, 由此可得出的结论是
A.分子中碳、氢原子个数比为1∶2
B.该有机物分子中C、H、O个数比为1∶2∶3
C.有机物中必定含氧
D.无法判断有机物中是否含有氧元素
1
2
3
4
√
√
解析 水蒸气和CO2的物质的量之比为1∶1,根据原子守恒可知,有机物分子中碳、氢原子个数比为1∶2,A正确;
有机物的相对分子质量未给出,无法判断有机物中是否含有氧元素,B、C错误,D正确。
1
2
3
4
1
2
3
4
4.为了测定一种气态烃A的化学式,取一定量的A与氧气置于一密闭容器中燃烧,定性实验表明产物是CO2、CO和水蒸气,学生甲、乙设计了两个方案,均认为根据自己的方案能求出A的最简式。他们测得的有关数据如下(箭头表示气流方向,实验前系统内的空气已排尽):
1
2
3
4
试回答:
(1)你认为能够求出A的最简式的方案是____(填“甲”或“乙”),理由是_______________________________________________________________
__________________________________________________________________________________________________________________________________________________________________________________________________________________________________。
甲
甲方案先将产物通过浓硫酸,其增重为H2O的质量,再通过碱石灰,其增重为CO2的质量,而点燃则将CO转化为1.76 g CO2。由此可求得A中的C、H原子个数比,从而确定出A的最简式,而乙方案先将产物通过碱石灰,增重的是燃烧产物中CO2和H2O的质量之和,而无法求出CO2和H2O的质量各为多少,无法确定出A的最简式
1
2
3
4
(2)根据你选择的方案,通过计算确定A的最简式为_____。
CH2
解析 浓硫酸增重1.26 g为H2O的质量,从而可求得气态烃A中,
n(H)=1.26 g÷18 g·mol-1×2=0.14 mol,
根据碳元素守恒,若有机物完全燃烧产生的CO2为
1.32 g+1.76 g=3.08 g
n(C)=3.08 g÷44 g·mol-1=0.07 mol
n(C)∶n(H)=0.07 mol∶0.14 mol=1∶2,故有机物最简式为CH2。
1
2
3
4
(3)若要确定A的化学式______(填“需要”或“不需要”)测定其他数据,其原因是_______________________________________________________
__________________。
需要
A的最简式中,氢原子数未达饱和,确定A的化学式,还需要测
定其相对分子质量
返回
选择性必修3第3章第2节
有机化合物结构的测定——有机化合物分子式的确定第1课时
1.学会测定有机物元素含量、相对分子质量的一般方法,建立确定有
机物分子式的思维模型。
2.能通过燃烧分析法、质谱法等微观探析有机物分子的元素组成、相
对分子质量及元素的质量分数。
3.学会蒸馏法、萃取法、重结晶法的实验原理,根据有机物性质的差
异选择有机化合物分离、提纯的正确方法。
核心素养发展目标
当人们从自然界中得到某一新化合物并将其提纯以后,测定其结构就是最重要的工作了。只有确定了这种化合物分子的结构,才能进一步了解和应用这种化合物。
在有机合成中,对天然产物合成的首要工作就是测定目标化合物分子的结构;而对人工设计的有机化合物,在合成后也必须测定其结构才能确定它是否就是目标产物。
那么,怎样对有机化合物进行结构测定呢?结构测定在有机化学中有什么重要作用?
联想质疑
从自然界提取或通过人工合成的有机化合物通常含有 ,需要通过
、 后才能进行结构测定,常见的分离、提纯有机化合物的方法有 、 和 等。
杂质
分离
提纯
蒸馏
重结晶
萃取
液
大于
少量杂质
热稳定性
沸点
新知学习 01 有机化合物分离、提纯的常用方法
3.萃取是 有机化合物的常用方法。
类型 液-液萃取:利用待分离组分在两种 的溶剂中的______不同,将其从一种溶剂转移到另一种溶剂中的过程。一般是用有机溶剂从水中萃取有机化合物
固-液萃取:用 从 物质中 出待分离组分的过程
萃取剂 对萃取剂的要求:
①萃取剂与原溶剂 ;
②溶质在萃取剂中的溶解度 在原溶剂中的溶解度;
③萃取剂与原溶液中的成分不反应
常用萃取剂: 、 、 等
萃取剂与有机化合物的分离 (1) 法
(2) 法
富集
互不相溶
溶解性
溶剂
固体
溶解
互不相溶
远大于
蒸馏
反萃取
乙醚
石油醚
二氯甲烷
(1)能用分液的方法分离植物油和水的混合物( )
(2)Br2、I2在水中的溶解度较小,但易溶于有机溶剂,故可用酒精萃取溴水中的Br2或碘水中的I2( )
(3)利用蒸馏法分离液态有机物时,温度计可以插入液面以下( )
(4)在蒸馏实验中,发现忘记加沸石,应立即停止实验,马上加入( )
(5)重结晶要求杂质的溶解度比被提纯的物质小才能进行分离( )
(6)常用重结晶法提纯苯甲酸( )
√
×
×
×
×
√
正误判断
现拟分离乙酸乙酯、乙酸和乙醇的混合物,下图是分离操作步骤流程图。
已知各物质的沸点:
乙酸乙酯 77.1 ℃ 乙醇 78.5 ℃ 乙酸 118 ℃
请回答下列问题:
(1)试剂(a)为________________,试剂(b)为______。
饱和Na2CO3溶液
硫酸
理解应用
(2)图中的分离方法分别是①为______;②为______;③为______。
(3)写出下列有机物的化学式:
A_________________、B________________________、C____________、
D___________、E___________。
分液
蒸馏
蒸馏
CH3COOH
CH3COOCH2CH3
CH3CH2OH、CH3COONa
CH3COONa
CH3CH2OH
解析 乙酸乙酯不溶于水,而乙酸、乙醇均易溶于水,故可先加饱和Na2CO3溶液通过分液分离出乙酸乙酯。余下的CH3COONa和乙醇,用蒸馏法蒸出乙醇,最后将CH3COONa转化为乙酸,再蒸馏即可得到CH3COOH。
物质的性质与分离、提纯方法的选择
(1)根据物质的溶解性差异,可选用结晶、过滤的方法将混合物分离。
(2)根据物质的沸点差异,可选用蒸馏的方法将互溶性液体混合物分离。
(3)根据物质在不同溶剂中溶解性的差异,用萃取的方法把溶质从溶解性小的溶剂中转移到溶解性较大的溶剂中。
返回
归纳总结
1.有机化合物元素组成的测定方法及步骤
100%
CO2
H2O
N2
卤化银
新知学习 02 有机化合物分子式的确定
2.有机物相对分子质量的测定
(1)通过实验,根据有关数据求算相对分子质量。
(2)有机物的相对分子质量一般用 进行测定。
3.有机化合物分子式的确定
质谱仪
(1)验证有机物属于烃时只需测定产物中的CO2和H2O的物质的量之比
( )
(2)有机物燃烧后只生成CO2和H2O的物质不一定只含有碳、氢两种元素
( )
(3)有机物的实验式、分子式一定不同( )
(4)元素分析法和质谱法能分别确定有机物的实验式和相对分子质量( )
(5)质谱图中最右边的谱线表示的数值为该有机物的相对分子质量( )
×
√
×
√
√
正误判断
1.实验测得某碳氢化合物A中,含碳80%,含氢20%,该化合物的实验式为______。又测得该化合物的相对分子质量是30,该化合物的分子式为______。
CH3
C2H6
理解应用
方法一:设该化合物分子式为(CH3)n,
方法二:A分子式中各元素原子的数目:
故该化合物A的分子式是C2H6。
2.某化合物6.4 g在氧气中完全燃烧,只生成8.8 g CO2和7.2 g H2O。
(1)计算确定该有机物实验式_______。
CH4O
m(C)=0.2 mol×12 g·mol-1=2.4 g
m(H)=0.4 mol×2×1 g·mol-1=0.8 g
m(C)+m(H)=2.4 g+0.8 g=3.2 g<6.4 g
所以n(C)∶n(H)∶n(O)=0.2∶0.8∶0.2=1∶4∶1。
则实验式为:CH4O。
(2)若该有机物的蒸气对空气的相对密度为1.10,则该有机物的分子式为_______。
CH4O
解析 该有机物的相对分子质量为1.10×29≈32
由于实验式的式量也为32,因而其分子式为CH4O。
1.确定有机物是否含O元素的方法
有机物完全燃烧产物为CO2和H2O,通过相关的实验可以先确定CO2和H2O的质量,进而求得有机物中所含碳元素和氢元素的质量。
①若m(有机物)=m(C)+m(H),则说明该有机物中只含C和H两种元素。
②若m(有机物)>m(C)+m(H),且完全燃烧只生成CO2和H2O,则说明有机物中含有C、H、O三种元素,其中m(O)=m(有机物)-m(C)-m(H)。
归纳总结
2.确定有机物分子式的一般途径
返回
1.下列说法不正确的是
A.蒸馏是分离、提纯液态有机化合物的常用方法
B.重结晶的首要工作是选择适当的溶剂
C.萃取包括液—液萃取和固—液萃取
D.研究有机化合物可首先进行元素定量分析,再分离、提纯
1
2
3
4
√
解析 研究有机化合物的基本步骤首先应该是分离、提纯,然后再进行元素定量分析,所以D不正确。
随堂演练
2.下列有关实验的说法错误的是
A.在蒸馏实验中,温度计的水银球位于支管口处是为了测出馏分的沸点
B.用结晶法分离硝酸钾和氯化钠的混合物,用分液法分离水和硝基苯的
混合物
C.在重结晶的实验中,使用短颈漏斗趁热过滤是为了减少被提纯物质的
损失
D.作为重结晶实验的溶剂,杂质在此溶液中的溶解度受温度影响应该很大
√
1
2
3
4
解析 在蒸馏实验中,温度计的水银球位于支管口处是为了测出馏分的沸点,故A正确;
硝酸钾的溶解度随温度升高而急剧增大,氯化钠的溶解度随温度变化很小,所以用结晶法分离硝酸钾和氯化钠的混合物,水和硝基苯不互溶,所以用分液法分离水和硝基苯的混合物,故B正确;
在重结晶实验中,要求被提纯物和杂质的溶解度随温度的变化差别很大,杂质在此溶液中的溶解度受温度影响不一定很大,故D错误。
1
2
3
4
3.(武汉高二月考)某有机物在氧气中充分燃烧,生成的水蒸气和CO2的物质的量比为1∶1, 由此可得出的结论是
A.分子中碳、氢原子个数比为1∶2
B.该有机物分子中C、H、O个数比为1∶2∶3
C.有机物中必定含氧
D.无法判断有机物中是否含有氧元素
1
2
3
4
√
√
解析 水蒸气和CO2的物质的量之比为1∶1,根据原子守恒可知,有机物分子中碳、氢原子个数比为1∶2,A正确;
有机物的相对分子质量未给出,无法判断有机物中是否含有氧元素,B、C错误,D正确。
1
2
3
4
1
2
3
4
4.为了测定一种气态烃A的化学式,取一定量的A与氧气置于一密闭容器中燃烧,定性实验表明产物是CO2、CO和水蒸气,学生甲、乙设计了两个方案,均认为根据自己的方案能求出A的最简式。他们测得的有关数据如下(箭头表示气流方向,实验前系统内的空气已排尽):
1
2
3
4
试回答:
(1)你认为能够求出A的最简式的方案是____(填“甲”或“乙”),理由是_______________________________________________________________
__________________________________________________________________________________________________________________________________________________________________________________________________________________________________。
甲
甲方案先将产物通过浓硫酸,其增重为H2O的质量,再通过碱石灰,其增重为CO2的质量,而点燃则将CO转化为1.76 g CO2。由此可求得A中的C、H原子个数比,从而确定出A的最简式,而乙方案先将产物通过碱石灰,增重的是燃烧产物中CO2和H2O的质量之和,而无法求出CO2和H2O的质量各为多少,无法确定出A的最简式
1
2
3
4
(2)根据你选择的方案,通过计算确定A的最简式为_____。
CH2
解析 浓硫酸增重1.26 g为H2O的质量,从而可求得气态烃A中,
n(H)=1.26 g÷18 g·mol-1×2=0.14 mol,
根据碳元素守恒,若有机物完全燃烧产生的CO2为
1.32 g+1.76 g=3.08 g
n(C)=3.08 g÷44 g·mol-1=0.07 mol
n(C)∶n(H)=0.07 mol∶0.14 mol=1∶2,故有机物最简式为CH2。
1
2
3
4
(3)若要确定A的化学式______(填“需要”或“不需要”)测定其他数据,其原因是_______________________________________________________
__________________。
需要
A的最简式中,氢原子数未达饱和,确定A的化学式,还需要测
定其相对分子质量
返回
