专题十 化学式与化合价(含答案)2025年中考一轮复习收官测试卷
文档属性
| 名称 | 专题十 化学式与化合价(含答案)2025年中考一轮复习收官测试卷 |  | |
| 格式 | docx | ||
| 文件大小 | 632.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-20 22:35:39 | ||
图片预览



文档简介
专题十 化学式与化合价——中考一轮复习收官测试卷
(试卷满分:60分;考试时间:60分钟)
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Cl-35.5 K-39 Fe-56 Cu-64 I-127
一、选择题(本大题共15小题,每题2分,共30分)
1.狮子糕是四川西充地区特色糕类美食。采用“白沙糯米”,辅以鲜花醇蜜、小磨香油(含油酸,化学式)等制成。下列关于油酸的说法错误的是( )
A.油酸的相对分子质量为282
B.油酸中碳元素的质量分数最大
C.油酸由18个碳原子、34个氢原子和2个氧原子构成
D.油酸是由碳、氢、氧三种元素组成的
2.下列化学用语,表达正确的是( )
A.2个氢原子: B.锌元素:ZN
C.钠原子结构示意图: D.氧化镁中镁元素的化合价:
3.端午节是我国的传统节日,民间有挂艾草的习俗。艾草中含有丰富的黄酮素,其药用价值非常高。下列关于黄酮素说法正确的是( )
A.黄酮素分子由碳、氢、氧三种元素组成
B.黄酮素由15个碳原子、10个氢原子和2个氧原子构成
C.黄酮素中碳、氢元素的质量比为15:10
D.黄酮素中氢元素的质量分数约为
4.将ag铁和碳的混合物在氧气中充分灼烧,冷却,称量,发现剩余固体的质量仍为ag,该混合物中碳的质量分数为( )
A.30.0% B.22.2% C.27.6% D.10.3%
5.我国科学家研制出一种新型催化剂,可将二氧化碳转化为汽油,主要转化过程如图所示。下列说法错误的是( )
A.若X是一种单质,可能是
B.与甲烷中碳氢元素质量比相同
C.该转化为“碳中和”提供了新途径
D.反应Ⅰ的化学方程式为
6.构建元素化合价和物质类别的二维图是学习化学的一种重要方法。如图是小明绘制的硫元素的“价类二维图”,图中各点对应物质正确的是( )
A. B. C. D.
7.火药是我国的四大发明之一。已知黑火药爆炸的化学方程式为,此反应涉及的化学用语表示方法正确的是( )
A.硝酸钾中的硝酸根离子:
B.3个碳原子:3C
C.单质硫中硫元素的化合价:
D.硫酸钾的化学式:
8.只含铜、氧两种元素的固体样品9.0 g,测得其中含铜元素的质量为8.0 g。已知铜的氧化物有CuO和,下列说法正确的是( )
A.固体样品的组成有2种情况
B.固体样品可能是CuO和的混合物
C.固体样品一定是
D.若固体样品由两种物质组成,则它们的质量比为5:4(或4:5)
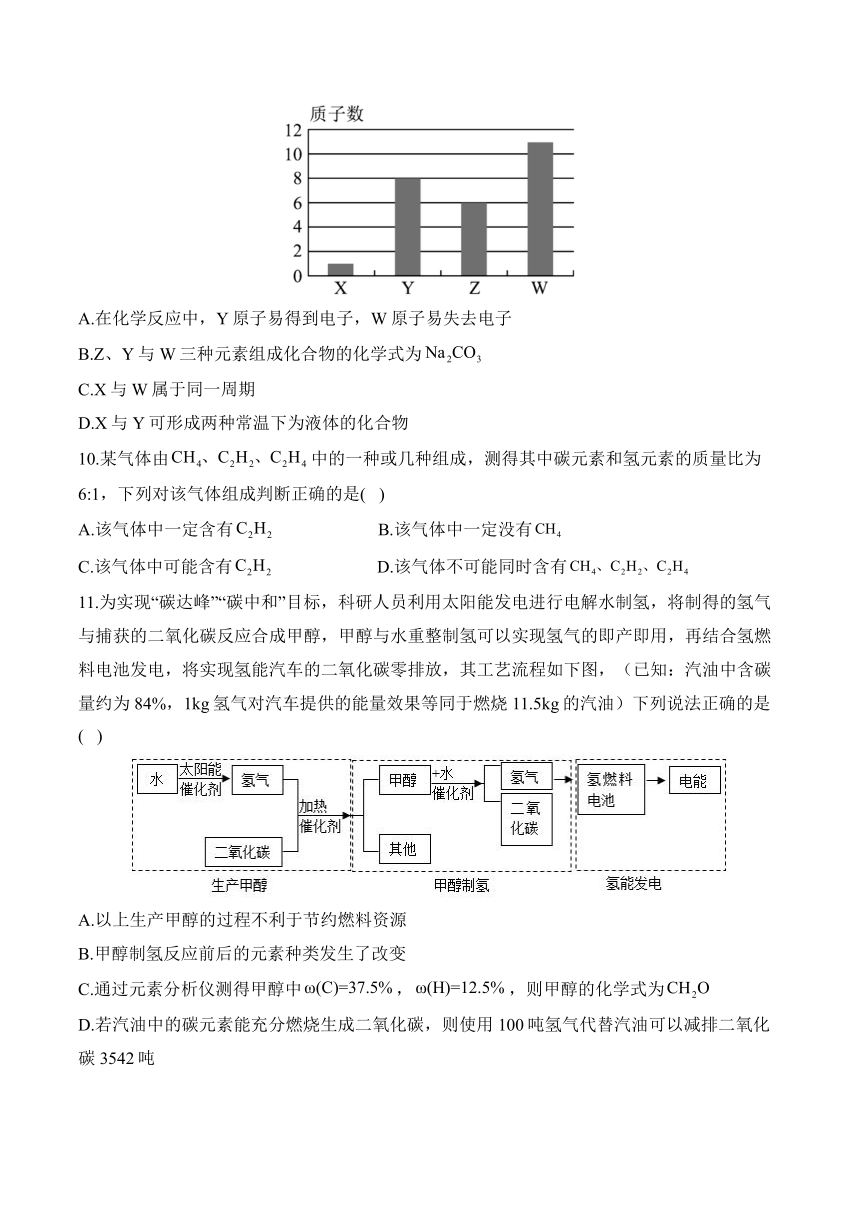
9.X、Y、Z、W四种元素的质子数如图所示。下列说法错误的是( )
A.在化学反应中,Y原子易得到电子,W原子易失去电子
B.Z、Y与W三种元素组成化合物的化学式为
C.X与W属于同一周期
D.X与Y可形成两种常温下为液体的化合物
10.某气体由中的一种或几种组成,测得其中碳元素和氢元素的质量比为6:1,下列对该气体组成判断正确的是( )
A.该气体中一定含有 B.该气体中一定没有
C.该气体中可能含有 D.该气体不可能同时含有
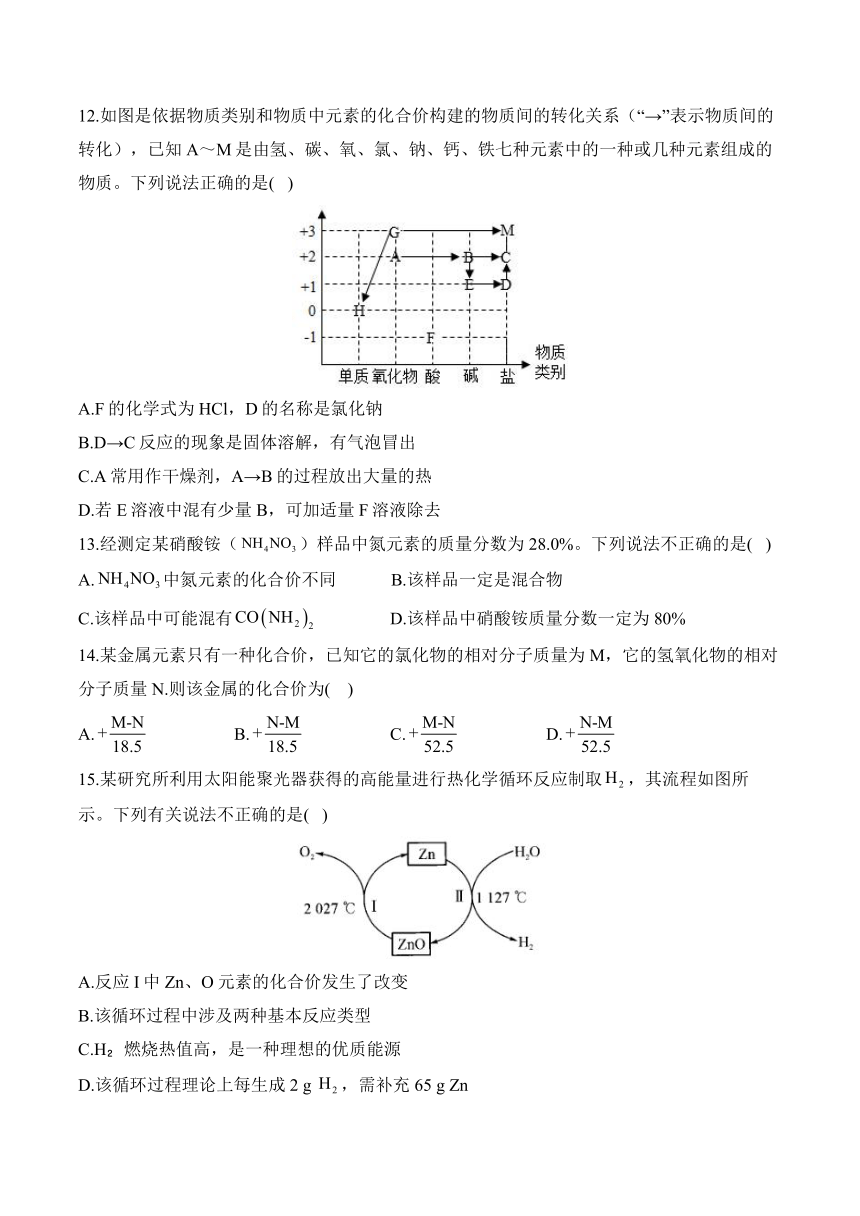
11.为实现“碳达峰”“碳中和”目标,科研人员利用太阳能发电进行电解水制氢,将制得的氢气与捕获的二氧化碳反应合成甲醇,甲醇与水重整制氢可以实现氢气的即产即用,再结合氢燃料电池发电,将实现氢能汽车的二氧化碳零排放,其工艺流程如下图,(已知:汽油中含碳量约为84%,1kg氢气对汽车提供的能量效果等同于燃烧11.5kg的汽油)下列说法正确的是( )
A.以上生产甲醇的过程不利于节约燃料资源
B.甲醇制氢反应前后的元素种类发生了改变
C.通过元素分析仪测得甲醇中,,则甲醇的化学式为
D.若汽油中的碳元素能充分燃烧生成二氧化碳,则使用100吨氢气代替汽油可以减排二氧化碳3542吨
12.如图是依据物质类别和物质中元素的化合价构建的物质间的转化关系(“→”表示物质间的转化),已知A~M是由氢、碳、氧、氯、钠、钙、铁七种元素中的一种或几种元素组成的物质。下列说法正确的是( )
A.F的化学式为HCl,D的名称是氯化钠
B.D→C反应的现象是固体溶解,有气泡冒出
C.A常用作干燥剂,A→B的过程放出大量的热
D.若E溶液中混有少量B,可加适量F溶液除去
13.经测定某硝酸铵()样品中氮元素的质量分数为28.0%。下列说法不正确的是( )
A.中氮元素的化合价不同 B.该样品一定是混合物
C.该样品中可能混有 D.该样品中硝酸铵质量分数一定为80%
14.某金属元素只有一种化合价,已知它的氯化物的相对分子质量为M,它的氢氧化物的相对分子质量N.则该金属的化合价为( )
A. B. C. D.
15.某研究所利用太阳能聚光器获得的高能量进行热化学循环反应制取,其流程如图所示。下列有关说法不正确的是( )
A.反应I中Zn、O元素的化合价发生了改变
B.该循环过程中涉及两种基本反应类型
C.H 燃烧热值高,是一种理想的优质能源
D.该循环过程理论上每生成2 g ,需补充65 g Zn
二、填空题(本题共5小题,每空1分,共26分)
16.用适当的化学用语填空。
(1)人体内含量最高的金属元素是_____。
(2)常用于医疗急救、航空航天中供给呼吸的气体是______。
(3)天然气的主要成分是_____。
(4)铵态氮肥中含有的阳离子是_________。
17.我国古代将炉甘石()、赤铜()和木炭粉混合后加热到约800 ℃时,可分解为一种金属氧化物和空气中含有的一种气态氧化物,最终得到一种外观似黄金的锌铜合金。请用化学用语回答:
(1)两个碳酸根离子:_________。
(2)标出中铜元素的化合价:_________。
(3)两个铜原子:__________。
(4)分解生成_____和 。
18.现有加碘低钠盐一袋,其标签如表所示。
(1)碘酸钾中钾、碘、氧三种元素的质量比是________;碘酸钾中氧元素的质量分数为________(精确到0.1%)。
(2)能防止细粉、结晶性食品板结的抗结剂亚铁氰化钾的相对分子质量为________。
(3)KCl有咸味,可以部分代替氯化钠,且达到减钠增钾的效果。钾是人体必需的________(填“微量”或“常量”)元素,缺钾会引起________(写一条即可)。
(4)人体每天摄入钠元素的质量不宜超过2.3 g。如果人体所需的钠元素全部来自该品牌食盐,那么一个人每天摄入该品牌低钠盐的质量最多不宜超过多少克?(写出计算过程)
19.宏观和微观相结合是认识物质结构与性质的重要方法。
(1)氧原子的结构示意图为,硫原子的结构示意图为。
①一个硫原子得到2个电子形成一种新粒子,该粒子的符号为__________。
②氧气和硫单质分别与氢气反应生成和。、中氧与硫元素的化合价均为-2价,从原子结构上分析它们化合价相同的原因是____________________。
(2)溶液和溶液反应的微观示意图如图1所示。该反应中实际参加反应的离子是________(填离子符号)。
(3)硫及其化合物的“化合价-物质类别”关系图如图2所示。物质X的化学式为_______。
20.电解水制氢联合碳酸钙分解制备氧化钙,能减少碳排放,助力碳中和。该新方法的示意图如图1所示。
(1)传统方法:在900 ℃以上完全分解生成CaO和_____(填化学式)。
(2)新方法:
①电解水属于_________(填基本反应类型)反应,反应前后氢元素的化合价_____(填“升高”“降低”或“不变”)。
②反应器1:一定的环境及较低温度下,可与反应生成CaO、CO和,生成的CO与的分子个数比为________。还可以直接分解。
反应器1中CO、的含量随反应温度的变化如图2所示,________℃时,抑制生成的效果最好。
③反应器2:一定条件下,CO与发生化合反应生成甲醇(),化学方程式为_____________________。
(3)与传统方法相比新方法的优点有______________(写两条)。
三、推断题(本题共1小题,每空1分,共4分)
21.A~F是含同一种金属元素的物质,它们的转化关系如图所示(“→”表示反应能一步实现,部分物质和反应条件已略去),图中标注了物质类别和这种金属元素的化合价。已知A与一氧化碳反应是工业制取B的主要原理,B是目前世界年产量最高的金属。
(1)这种金属元素属于人体必需的_____(填“常量元素”或“微量元素”)。
(2)A的化学式为_____;B与稀硫酸反应生成C的化学方程式为 。
(3)D与氧气、水可以发生化合反应生成E,该反应的化学方程式为 。
答案以及解析
1.答案:C
解析:A、油酸的相对分子质量为:,故A不符合题意;B、油酸中碳、氢、氧元素的质量比为:,所以碳元素的质量分数最大,故B不符合题意;C、油酸是由油酸分子构成,1个油酸分子由18个碳原子、34个氢原子和2个氧原子构成,故C符合题意;D、由油酸化学式知,油酸由碳、氢、氧三种元素组成,故D不符合题意。 故选C。
2.答案:C
解析:2个氢原子的符号为2H;锌元素的符号为Zn;氧化镁中镁元素的化合价为+2价。
3.答案:D
解析:黄酮素由碳、氢、氧三种元素组成,A错误;1个黄酮素分子由15个碳原子、10个氢原子和2个氧原子构成,B错误;黄酮素中碳、氢元素的质量比为,C错误;黄酮素中氢元素的质量分数为,D正确。
4.答案:C
5.答案:B
6.答案:D
解析:A点对应的物质是硫单质,故为S,A错误;B点对应的物质是含硫元素的氧化物,且硫元素的化合价为+4,故为,B错误;C点对应的物质是含硫元素的酸,且硫元素的化合价为+4,故为,C错误;D点对应的物质是含硫元素的盐,且硫元素的化合价为+6,故为硫酸盐,属于硫酸盐,D正确。
7.答案:B
解析:硝酸钾中的硝酸根离子表示为,A错误;3个碳原子表示为3C,B正确;单质硫中硫元素的化合价为0,表示为,C错误;硫酸钾的化学式为,硫化钾的化学式为,D错误。
8.答案:D
解析:铜元素质量为8.0 g,则固体样品中氧元素质量为9 g-8 g=1 g,固体样品中铜原子、氧原,即固体样品中铜、氧原子个数比为元素的平均组成为Cu O,可能为纯净物,也可能是Cu、CuO或Cu、、CuO,但不可能是CuO与两种物质组成的混合物;如果固体样品是由两种物质组成,则为Cu和CuO的组合,设固体样品中Cu的质量为x,则CuO的质量为(9.0 g-x),由题意可得,解得x=4 g,则氧化铜的质量为5 g。
9.答案:C
解析:A、Y是氧原子,最外层电子数为6,在化学反应中易得到电子,W是钠原子,最外层电子数为1,在化学反应中易失去电子,A选项说法正确,不符合题意;B、Z、Y、W三种元素是C、O、Na,形成的化合物是,B选项说法正确,不符合题意;C、X是氢元素,在第一周期,W是钠元素,在第三周期,不属于同一周期,C选项说法正确,符合题意;D、X是氢元素、Y是氧元素,它们能形成化合物:、,这两种化合物常温下为液体,D选项说法正确,不符合题意。故选:C。
10.答案:C
解析:碳元素和氢元素的质量比为6:1,故碳氢原子的个数比为:,
A、若气体中只含有,则碳氢原子个数比为1:2,该气体中不一定有,说法错误,不符合题意;B、若是含一个和一个,则能达到碳氢原子个数比是1:2,说法错误,不符合题意;C、该气体中可能含有,说法正确,符合题意;D、该气体可能同时含有、、,说法错误,不符合题意。故选C。
11.答案:D
解析:A、过程利用的是太阳能,生产甲醇的过程有利于节约燃料资源,故A不正确;B、由质量守恒定律可知,化学反应前后元素种类不变,甲醇制氢反应前后的元素种类不发生改变,故B不正确;C、通过元素分析仪测得甲醇中,,,设一个甲醇分子中碳、氢、氧原子的个数比为x:y:z,甲醇的相对分子质量为a,,,,,则甲醇的化学式为,故C不正确;D、1kg氢气对汽车提供的能量效果等同于燃烧11.5kg的汽油,若汽油中的碳元素能充分燃烧生成二氧化碳,100吨氢气相当于燃烧汽油,含碳量为,则使用100吨氢气代替汽油可以减排二氧化碳的质量为,故D正确。故选D。
12.答案:C
解析:A~M是由氢、碳、氧、氯、钠、钙、铁七种元素中的一种或几种元素组成的物质,图中氧化物G中有元素化合价为+3价,根据已学知识,G为;氧化铁可以转化为铁,则H为Fe,M为铁盐;A为含有+2价元素的氧化物,且可以转化为碱,以上元素中只有钙符合题意,因此A为CaO,B为;可以转化为NaOH,则E为NaOH,钠显+1价,符合题意;NaOH可以转化为或氯化钠,可以转化为含钙元素(化合价是+2价)的盐,如或氯化钙,因为氯化钠不能转化为氯化钙,而可以转化为,则C是,D是。
A、F是含有-1价元素的酸,在给定元素中只有氯符合题意,因此F的化学式为HCl。根据分析D为,不可能是氯化钠,因为氯化钠不能转化为钙盐,选项A不正确;
B、D为,C是,D→C的转化可以通过碳酸钠和氯化钙等可溶性钙盐或氢氧化钙反应实现,反应的现象是:有白色沉淀生成,选项B不正确;
C、A是氧化钙,氧化钙能和水反应生成氢氧化钙,因此常用作干燥剂。氧化钙和水的反应是放热反应,因此A→B的过程中放出大量的热,选项C正确;
D、E为NaOH,B为,若NaOH溶液中混有少量,如果加入适量盐酸溶液,虽然除去了氢氧化钙,但盐酸同时也和氢氧化钠反应,还带进新的杂质氯化钙、氯化钠,不符合“不增、不减、易分离”的除杂原则,选项D不正确。故选C。
13.答案:D
解析:A、中铵根中氮元素的化合价为 3价,硝酸根中氮元素的化合价为+5价,此选项表述正确;B、硝酸铵中氮元素的质量分数为,已知样品中氮元素的质量分数为28.0%,故该样品一定是混合物,此选项表述正确;C、中氮元素的质量分数为,硝酸铵中氮元素的质量分数为,而样品中氮元素的质量分数为28%,即杂质中氮元素的质量分数一定小于28%,若样品中混有,则必同时还含有另外一种氮元素质量分数小于28%的杂质,此选项表述正确;D、根据上述分析可知该样品中一定含有杂质,且杂质中氮元素的质量分数一定小于28%,由于杂质的种类不确定,杂质中氮元素的质量分数也不确定,故样品中硝酸铵的质量分数也不一定是80%,此选项表述不正确。故选D。
14.答案:A
解析:设金属的元素符号为A,设金属元素A的化合价为x,金属A的相对原子质量为y,
则氯化物的化学式为,由其相对分子质量为M,则可得到y+35.5x=M;
氢氧化物的化学式为,
由其相对分子质量为N,则可得到y+17x=N;解得。
15.答案:D
解析:反应I为氧化锌在高温下分解生成锌和氧气,锌单质中锌元素化合价为0,氧气中氧元素化合价为0,氧化锌中锌元素显+2价,氧元素显-2价,故反应I中Zn、O元素的化合价发生了改变;反应I属于分解反应,反应Ⅱ为锌和水在高温下反应生成氧化锌和氢气,属于置换反应;燃烧热值高,是一种理想的优质能源;由图可知,在反应I中锌是生成物,在反应Ⅱ中锌为反应物,锌可以循环利用,无需补充。
16.答案:(1)Ca
(2)
(3)
(4)
解析:(1)人体内含量最高的金属元素是钙元素,其元素符号为Ca。
(2)常用于医疗急救、航空航天中供给呼吸的气体是氧气,其化学式为。
(3)天然气的主要成分是甲烷,其化学式为。
(4)铵态氮肥是由铵根离子与氯离子构成的化合物,其中含有的阳离子是铵根离子。由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负号在后,带1个电荷时,1要省略,铵根离子表示为。
17.答案:(1)
(2)
(3)2Cu
(4)ZnO;
解析:(1)根据离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负号在后,带1个电荷时,1要省略,若表示多个该离子,就在其离子符号前加上相应的数字,则两个碳酸根离子表示为。
(2)氧化亚铜中氧的化合价是-2,根据化合物化合价代数和为零可计算出铜元素化合价是+1,物质中元素化合价标在化学式该元素正上方,正负号在左,数字在右,则中铜元素的化合价表示为。
(3)在元素符号前加数字表示原子个数,则在铜前面加上2,表示两个铜原子,即2Cu。
(4)由题意可得出ZnCO 可分解成的金属氧化物为氧化锌,空气中含有的一种气态氧化物为二氧化碳,化学式分别为ZnO、。
18.答案:(1)39:127:48;22.4%
(2)368
(3)常量肌肉无力
(4)解:设每天摄入该品牌低钠盐的质量最多不宜超过x,根据题意有,。
答:一个人每天摄入该品牌低钠盐的质量最多不宜超过7.3 g。
解析:(1)碘酸钾中钾、碘、氧三种元素的质量比是39:127:(16×3)=39:127:48;碘酸钾中氧元素的质量分数为。。
(2)亚铁氰化钾的相对分子质量为39×4+56+(12+14)×6=368。
(3)钾是人体必需的常量元素,钾对维持体内酸碱平衡和神经、肌肉的功能等具有重要意义,缺钾会引起肌无力和心律失常,影响肾功能。
19.答案:(1)①
②氧原子和硫原子的最外层均为6个电子,在化学反应中均易得到2个电子形成相对稳定的结构
(2)
(3)
20.答案:(1)
(2)①分解;降低
②1:1;750
③
(3)降低了反应温度;减少了生成
21.答案:(1)微量元素
(2)
(3)
解析:B是目前世界年产量最高的金属,则B为铁;A~F是含同一种金属元素的物质,则A~F中均含铁元素;A与一氧化碳反应是工业制取铁的主要原理,由题图可知,A为铁的氧化物,且A中铁元素的化合价为+3.则A为氧化铁,进而推知C为亚铁盐,F为铁盐,D为氢氧化亚铁,E为氢氧化铁。
(1)铁元素属于人体必需的微量元素。
(2)由以上分析可知,A为氧化铁,其化学式为;B为铁,铁与稀硫酸发生反应生成硫酸亚铁和氢气,反应的化学方程式为。
(3)D为氢氧化亚铁,E为氢氧化铁,氢氧化亚铁与氧气、水可以发生化合反应生成氢氧化铁,则反应的化学方程式为。
(试卷满分:60分;考试时间:60分钟)
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Cl-35.5 K-39 Fe-56 Cu-64 I-127
一、选择题(本大题共15小题,每题2分,共30分)
1.狮子糕是四川西充地区特色糕类美食。采用“白沙糯米”,辅以鲜花醇蜜、小磨香油(含油酸,化学式)等制成。下列关于油酸的说法错误的是( )
A.油酸的相对分子质量为282
B.油酸中碳元素的质量分数最大
C.油酸由18个碳原子、34个氢原子和2个氧原子构成
D.油酸是由碳、氢、氧三种元素组成的
2.下列化学用语,表达正确的是( )
A.2个氢原子: B.锌元素:ZN
C.钠原子结构示意图: D.氧化镁中镁元素的化合价:
3.端午节是我国的传统节日,民间有挂艾草的习俗。艾草中含有丰富的黄酮素,其药用价值非常高。下列关于黄酮素说法正确的是( )
A.黄酮素分子由碳、氢、氧三种元素组成
B.黄酮素由15个碳原子、10个氢原子和2个氧原子构成
C.黄酮素中碳、氢元素的质量比为15:10
D.黄酮素中氢元素的质量分数约为
4.将ag铁和碳的混合物在氧气中充分灼烧,冷却,称量,发现剩余固体的质量仍为ag,该混合物中碳的质量分数为( )
A.30.0% B.22.2% C.27.6% D.10.3%
5.我国科学家研制出一种新型催化剂,可将二氧化碳转化为汽油,主要转化过程如图所示。下列说法错误的是( )
A.若X是一种单质,可能是
B.与甲烷中碳氢元素质量比相同
C.该转化为“碳中和”提供了新途径
D.反应Ⅰ的化学方程式为
6.构建元素化合价和物质类别的二维图是学习化学的一种重要方法。如图是小明绘制的硫元素的“价类二维图”,图中各点对应物质正确的是( )
A. B. C. D.
7.火药是我国的四大发明之一。已知黑火药爆炸的化学方程式为,此反应涉及的化学用语表示方法正确的是( )
A.硝酸钾中的硝酸根离子:
B.3个碳原子:3C
C.单质硫中硫元素的化合价:
D.硫酸钾的化学式:
8.只含铜、氧两种元素的固体样品9.0 g,测得其中含铜元素的质量为8.0 g。已知铜的氧化物有CuO和,下列说法正确的是( )
A.固体样品的组成有2种情况
B.固体样品可能是CuO和的混合物
C.固体样品一定是
D.若固体样品由两种物质组成,则它们的质量比为5:4(或4:5)
9.X、Y、Z、W四种元素的质子数如图所示。下列说法错误的是( )
A.在化学反应中,Y原子易得到电子,W原子易失去电子
B.Z、Y与W三种元素组成化合物的化学式为
C.X与W属于同一周期
D.X与Y可形成两种常温下为液体的化合物
10.某气体由中的一种或几种组成,测得其中碳元素和氢元素的质量比为6:1,下列对该气体组成判断正确的是( )
A.该气体中一定含有 B.该气体中一定没有
C.该气体中可能含有 D.该气体不可能同时含有
11.为实现“碳达峰”“碳中和”目标,科研人员利用太阳能发电进行电解水制氢,将制得的氢气与捕获的二氧化碳反应合成甲醇,甲醇与水重整制氢可以实现氢气的即产即用,再结合氢燃料电池发电,将实现氢能汽车的二氧化碳零排放,其工艺流程如下图,(已知:汽油中含碳量约为84%,1kg氢气对汽车提供的能量效果等同于燃烧11.5kg的汽油)下列说法正确的是( )
A.以上生产甲醇的过程不利于节约燃料资源
B.甲醇制氢反应前后的元素种类发生了改变
C.通过元素分析仪测得甲醇中,,则甲醇的化学式为
D.若汽油中的碳元素能充分燃烧生成二氧化碳,则使用100吨氢气代替汽油可以减排二氧化碳3542吨
12.如图是依据物质类别和物质中元素的化合价构建的物质间的转化关系(“→”表示物质间的转化),已知A~M是由氢、碳、氧、氯、钠、钙、铁七种元素中的一种或几种元素组成的物质。下列说法正确的是( )
A.F的化学式为HCl,D的名称是氯化钠
B.D→C反应的现象是固体溶解,有气泡冒出
C.A常用作干燥剂,A→B的过程放出大量的热
D.若E溶液中混有少量B,可加适量F溶液除去
13.经测定某硝酸铵()样品中氮元素的质量分数为28.0%。下列说法不正确的是( )
A.中氮元素的化合价不同 B.该样品一定是混合物
C.该样品中可能混有 D.该样品中硝酸铵质量分数一定为80%
14.某金属元素只有一种化合价,已知它的氯化物的相对分子质量为M,它的氢氧化物的相对分子质量N.则该金属的化合价为( )
A. B. C. D.
15.某研究所利用太阳能聚光器获得的高能量进行热化学循环反应制取,其流程如图所示。下列有关说法不正确的是( )
A.反应I中Zn、O元素的化合价发生了改变
B.该循环过程中涉及两种基本反应类型
C.H 燃烧热值高,是一种理想的优质能源
D.该循环过程理论上每生成2 g ,需补充65 g Zn
二、填空题(本题共5小题,每空1分,共26分)
16.用适当的化学用语填空。
(1)人体内含量最高的金属元素是_____。
(2)常用于医疗急救、航空航天中供给呼吸的气体是______。
(3)天然气的主要成分是_____。
(4)铵态氮肥中含有的阳离子是_________。
17.我国古代将炉甘石()、赤铜()和木炭粉混合后加热到约800 ℃时,可分解为一种金属氧化物和空气中含有的一种气态氧化物,最终得到一种外观似黄金的锌铜合金。请用化学用语回答:
(1)两个碳酸根离子:_________。
(2)标出中铜元素的化合价:_________。
(3)两个铜原子:__________。
(4)分解生成_____和 。
18.现有加碘低钠盐一袋,其标签如表所示。
(1)碘酸钾中钾、碘、氧三种元素的质量比是________;碘酸钾中氧元素的质量分数为________(精确到0.1%)。
(2)能防止细粉、结晶性食品板结的抗结剂亚铁氰化钾的相对分子质量为________。
(3)KCl有咸味,可以部分代替氯化钠,且达到减钠增钾的效果。钾是人体必需的________(填“微量”或“常量”)元素,缺钾会引起________(写一条即可)。
(4)人体每天摄入钠元素的质量不宜超过2.3 g。如果人体所需的钠元素全部来自该品牌食盐,那么一个人每天摄入该品牌低钠盐的质量最多不宜超过多少克?(写出计算过程)
19.宏观和微观相结合是认识物质结构与性质的重要方法。
(1)氧原子的结构示意图为,硫原子的结构示意图为。
①一个硫原子得到2个电子形成一种新粒子,该粒子的符号为__________。
②氧气和硫单质分别与氢气反应生成和。、中氧与硫元素的化合价均为-2价,从原子结构上分析它们化合价相同的原因是____________________。
(2)溶液和溶液反应的微观示意图如图1所示。该反应中实际参加反应的离子是________(填离子符号)。
(3)硫及其化合物的“化合价-物质类别”关系图如图2所示。物质X的化学式为_______。
20.电解水制氢联合碳酸钙分解制备氧化钙,能减少碳排放,助力碳中和。该新方法的示意图如图1所示。
(1)传统方法:在900 ℃以上完全分解生成CaO和_____(填化学式)。
(2)新方法:
①电解水属于_________(填基本反应类型)反应,反应前后氢元素的化合价_____(填“升高”“降低”或“不变”)。
②反应器1:一定的环境及较低温度下,可与反应生成CaO、CO和,生成的CO与的分子个数比为________。还可以直接分解。
反应器1中CO、的含量随反应温度的变化如图2所示,________℃时,抑制生成的效果最好。
③反应器2:一定条件下,CO与发生化合反应生成甲醇(),化学方程式为_____________________。
(3)与传统方法相比新方法的优点有______________(写两条)。
三、推断题(本题共1小题,每空1分,共4分)
21.A~F是含同一种金属元素的物质,它们的转化关系如图所示(“→”表示反应能一步实现,部分物质和反应条件已略去),图中标注了物质类别和这种金属元素的化合价。已知A与一氧化碳反应是工业制取B的主要原理,B是目前世界年产量最高的金属。
(1)这种金属元素属于人体必需的_____(填“常量元素”或“微量元素”)。
(2)A的化学式为_____;B与稀硫酸反应生成C的化学方程式为 。
(3)D与氧气、水可以发生化合反应生成E,该反应的化学方程式为 。
答案以及解析
1.答案:C
解析:A、油酸的相对分子质量为:,故A不符合题意;B、油酸中碳、氢、氧元素的质量比为:,所以碳元素的质量分数最大,故B不符合题意;C、油酸是由油酸分子构成,1个油酸分子由18个碳原子、34个氢原子和2个氧原子构成,故C符合题意;D、由油酸化学式知,油酸由碳、氢、氧三种元素组成,故D不符合题意。 故选C。
2.答案:C
解析:2个氢原子的符号为2H;锌元素的符号为Zn;氧化镁中镁元素的化合价为+2价。
3.答案:D
解析:黄酮素由碳、氢、氧三种元素组成,A错误;1个黄酮素分子由15个碳原子、10个氢原子和2个氧原子构成,B错误;黄酮素中碳、氢元素的质量比为,C错误;黄酮素中氢元素的质量分数为,D正确。
4.答案:C
5.答案:B
6.答案:D
解析:A点对应的物质是硫单质,故为S,A错误;B点对应的物质是含硫元素的氧化物,且硫元素的化合价为+4,故为,B错误;C点对应的物质是含硫元素的酸,且硫元素的化合价为+4,故为,C错误;D点对应的物质是含硫元素的盐,且硫元素的化合价为+6,故为硫酸盐,属于硫酸盐,D正确。
7.答案:B
解析:硝酸钾中的硝酸根离子表示为,A错误;3个碳原子表示为3C,B正确;单质硫中硫元素的化合价为0,表示为,C错误;硫酸钾的化学式为,硫化钾的化学式为,D错误。
8.答案:D
解析:铜元素质量为8.0 g,则固体样品中氧元素质量为9 g-8 g=1 g,固体样品中铜原子、氧原,即固体样品中铜、氧原子个数比为元素的平均组成为Cu O,可能为纯净物,也可能是Cu、CuO或Cu、、CuO,但不可能是CuO与两种物质组成的混合物;如果固体样品是由两种物质组成,则为Cu和CuO的组合,设固体样品中Cu的质量为x,则CuO的质量为(9.0 g-x),由题意可得,解得x=4 g,则氧化铜的质量为5 g。
9.答案:C
解析:A、Y是氧原子,最外层电子数为6,在化学反应中易得到电子,W是钠原子,最外层电子数为1,在化学反应中易失去电子,A选项说法正确,不符合题意;B、Z、Y、W三种元素是C、O、Na,形成的化合物是,B选项说法正确,不符合题意;C、X是氢元素,在第一周期,W是钠元素,在第三周期,不属于同一周期,C选项说法正确,符合题意;D、X是氢元素、Y是氧元素,它们能形成化合物:、,这两种化合物常温下为液体,D选项说法正确,不符合题意。故选:C。
10.答案:C
解析:碳元素和氢元素的质量比为6:1,故碳氢原子的个数比为:,
A、若气体中只含有,则碳氢原子个数比为1:2,该气体中不一定有,说法错误,不符合题意;B、若是含一个和一个,则能达到碳氢原子个数比是1:2,说法错误,不符合题意;C、该气体中可能含有,说法正确,符合题意;D、该气体可能同时含有、、,说法错误,不符合题意。故选C。
11.答案:D
解析:A、过程利用的是太阳能,生产甲醇的过程有利于节约燃料资源,故A不正确;B、由质量守恒定律可知,化学反应前后元素种类不变,甲醇制氢反应前后的元素种类不发生改变,故B不正确;C、通过元素分析仪测得甲醇中,,,设一个甲醇分子中碳、氢、氧原子的个数比为x:y:z,甲醇的相对分子质量为a,,,,,则甲醇的化学式为,故C不正确;D、1kg氢气对汽车提供的能量效果等同于燃烧11.5kg的汽油,若汽油中的碳元素能充分燃烧生成二氧化碳,100吨氢气相当于燃烧汽油,含碳量为,则使用100吨氢气代替汽油可以减排二氧化碳的质量为,故D正确。故选D。
12.答案:C
解析:A~M是由氢、碳、氧、氯、钠、钙、铁七种元素中的一种或几种元素组成的物质,图中氧化物G中有元素化合价为+3价,根据已学知识,G为;氧化铁可以转化为铁,则H为Fe,M为铁盐;A为含有+2价元素的氧化物,且可以转化为碱,以上元素中只有钙符合题意,因此A为CaO,B为;可以转化为NaOH,则E为NaOH,钠显+1价,符合题意;NaOH可以转化为或氯化钠,可以转化为含钙元素(化合价是+2价)的盐,如或氯化钙,因为氯化钠不能转化为氯化钙,而可以转化为,则C是,D是。
A、F是含有-1价元素的酸,在给定元素中只有氯符合题意,因此F的化学式为HCl。根据分析D为,不可能是氯化钠,因为氯化钠不能转化为钙盐,选项A不正确;
B、D为,C是,D→C的转化可以通过碳酸钠和氯化钙等可溶性钙盐或氢氧化钙反应实现,反应的现象是:有白色沉淀生成,选项B不正确;
C、A是氧化钙,氧化钙能和水反应生成氢氧化钙,因此常用作干燥剂。氧化钙和水的反应是放热反应,因此A→B的过程中放出大量的热,选项C正确;
D、E为NaOH,B为,若NaOH溶液中混有少量,如果加入适量盐酸溶液,虽然除去了氢氧化钙,但盐酸同时也和氢氧化钠反应,还带进新的杂质氯化钙、氯化钠,不符合“不增、不减、易分离”的除杂原则,选项D不正确。故选C。
13.答案:D
解析:A、中铵根中氮元素的化合价为 3价,硝酸根中氮元素的化合价为+5价,此选项表述正确;B、硝酸铵中氮元素的质量分数为,已知样品中氮元素的质量分数为28.0%,故该样品一定是混合物,此选项表述正确;C、中氮元素的质量分数为,硝酸铵中氮元素的质量分数为,而样品中氮元素的质量分数为28%,即杂质中氮元素的质量分数一定小于28%,若样品中混有,则必同时还含有另外一种氮元素质量分数小于28%的杂质,此选项表述正确;D、根据上述分析可知该样品中一定含有杂质,且杂质中氮元素的质量分数一定小于28%,由于杂质的种类不确定,杂质中氮元素的质量分数也不确定,故样品中硝酸铵的质量分数也不一定是80%,此选项表述不正确。故选D。
14.答案:A
解析:设金属的元素符号为A,设金属元素A的化合价为x,金属A的相对原子质量为y,
则氯化物的化学式为,由其相对分子质量为M,则可得到y+35.5x=M;
氢氧化物的化学式为,
由其相对分子质量为N,则可得到y+17x=N;解得。
15.答案:D
解析:反应I为氧化锌在高温下分解生成锌和氧气,锌单质中锌元素化合价为0,氧气中氧元素化合价为0,氧化锌中锌元素显+2价,氧元素显-2价,故反应I中Zn、O元素的化合价发生了改变;反应I属于分解反应,反应Ⅱ为锌和水在高温下反应生成氧化锌和氢气,属于置换反应;燃烧热值高,是一种理想的优质能源;由图可知,在反应I中锌是生成物,在反应Ⅱ中锌为反应物,锌可以循环利用,无需补充。
16.答案:(1)Ca
(2)
(3)
(4)
解析:(1)人体内含量最高的金属元素是钙元素,其元素符号为Ca。
(2)常用于医疗急救、航空航天中供给呼吸的气体是氧气,其化学式为。
(3)天然气的主要成分是甲烷,其化学式为。
(4)铵态氮肥是由铵根离子与氯离子构成的化合物,其中含有的阳离子是铵根离子。由离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负号在后,带1个电荷时,1要省略,铵根离子表示为。
17.答案:(1)
(2)
(3)2Cu
(4)ZnO;
解析:(1)根据离子的表示方法,在表示该离子的元素符号右上角,标出该离子所带的正负电荷数,数字在前,正负号在后,带1个电荷时,1要省略,若表示多个该离子,就在其离子符号前加上相应的数字,则两个碳酸根离子表示为。
(2)氧化亚铜中氧的化合价是-2,根据化合物化合价代数和为零可计算出铜元素化合价是+1,物质中元素化合价标在化学式该元素正上方,正负号在左,数字在右,则中铜元素的化合价表示为。
(3)在元素符号前加数字表示原子个数,则在铜前面加上2,表示两个铜原子,即2Cu。
(4)由题意可得出ZnCO 可分解成的金属氧化物为氧化锌,空气中含有的一种气态氧化物为二氧化碳,化学式分别为ZnO、。
18.答案:(1)39:127:48;22.4%
(2)368
(3)常量肌肉无力
(4)解:设每天摄入该品牌低钠盐的质量最多不宜超过x,根据题意有,。
答:一个人每天摄入该品牌低钠盐的质量最多不宜超过7.3 g。
解析:(1)碘酸钾中钾、碘、氧三种元素的质量比是39:127:(16×3)=39:127:48;碘酸钾中氧元素的质量分数为。。
(2)亚铁氰化钾的相对分子质量为39×4+56+(12+14)×6=368。
(3)钾是人体必需的常量元素,钾对维持体内酸碱平衡和神经、肌肉的功能等具有重要意义,缺钾会引起肌无力和心律失常,影响肾功能。
19.答案:(1)①
②氧原子和硫原子的最外层均为6个电子,在化学反应中均易得到2个电子形成相对稳定的结构
(2)
(3)
20.答案:(1)
(2)①分解;降低
②1:1;750
③
(3)降低了反应温度;减少了生成
21.答案:(1)微量元素
(2)
(3)
解析:B是目前世界年产量最高的金属,则B为铁;A~F是含同一种金属元素的物质,则A~F中均含铁元素;A与一氧化碳反应是工业制取铁的主要原理,由题图可知,A为铁的氧化物,且A中铁元素的化合价为+3.则A为氧化铁,进而推知C为亚铁盐,F为铁盐,D为氢氧化亚铁,E为氢氧化铁。
(1)铁元素属于人体必需的微量元素。
(2)由以上分析可知,A为氧化铁,其化学式为;B为铁,铁与稀硫酸发生反应生成硫酸亚铁和氢气,反应的化学方程式为。
(3)D为氢氧化亚铁,E为氢氧化铁,氢氧化亚铁与氧气、水可以发生化合反应生成氢氧化铁,则反应的化学方程式为。
同课章节目录
