专题七 盐 化肥(含答案)2025年中考一轮复习收官测试卷
文档属性
| 名称 | 专题七 盐 化肥(含答案)2025年中考一轮复习收官测试卷 |  | |
| 格式 | docx | ||
| 文件大小 | 972.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-20 23:19:36 | ||
图片预览



文档简介
专题七 盐 化肥——中考一轮复习收官测试卷
(试卷满分:60分;考试时间:60分钟)
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 Cl-35.5 Ca-40
一、选择题(本大题共10小题,每题2分,共20分)
1.下列物质的名称、俗称、化学式及类别中,完全对应的是( )
选项 物质的名称 俗称 化学式 类别
A 碳酸钠 烧碱 盐
B 碳酸钙 生石灰 盐
C 氢氧化钙 熟石灰 CaO 金属氧化物
D 氢氧化钠 苛性钠 NaOH 碱
2.下图是硫酸氢钾溶液的微观示意图,下列预测错误的是( )
A.该溶液能与碳酸钠反应
B.该溶液能与锌粉反应
C.该溶液中含有氢离子,所以硫酸氢钾属于酸
D.该溶液能与硝酸钡溶液反应
3.下列有关化学肥料的知识错误的是( )
A.氯化铵不能与碱性物质混合使用
B.磷肥可以促进作物生长,增强作物抗寒、抗旱能力
C.鉴别和,取样然后加固体研磨,闻气味
D.无水种植需要肥料(含),是因为植物生长需要钾、氮肥
4.归纳与推理是化学学科核心素养之一,也是学习化学的重要方法。下列说法正确的是( )
A.单质中只有一种元素,则只有一种元素的物质一定是单质
B.盐中含有金属离子(或铵根离子)和酸根离子,但盐中不一定含有金属元素
C.置换反应中一定有元素化合价的升降,则有元素化合价升降的反应一定是置换反应
D.复分解反应中反应物与生成物都是化合物,因此反应物与生成物都是化合物的反应一定是复分解反应
5.如图是、、三种物质间的转化关系,根据所学知识判断,下列说法正确的是( )
A.通过加入氯化铜溶液或稀盐酸可实现①的转化
B.通过一步反应无法实现②的转化
C.通过加入氢氧化钠等可溶性碱可实现③的转化
D.通过一步反应可实现向的转化
6.粗盐中含有泥沙和、、杂质。某同学将粗盐样品溶解、过滤,除去泥沙后,取粗盐水按如图所示流程进行提纯。下列说法错误的是( )
A.过滤用到的玻璃仪器有漏斗、烧杯、玻璃棒
B.加入溶液的目的是除去粗盐中的
C.固体X中含有3种物质
D.整个除杂过程中共参与了3个反应
7.打开保险柜,同学们发现一瓶无色透明的液体。经测定,其pH=2,对其中可能存在的离子组合,推测合理的是( )
A. B.、、
C.、 D.、
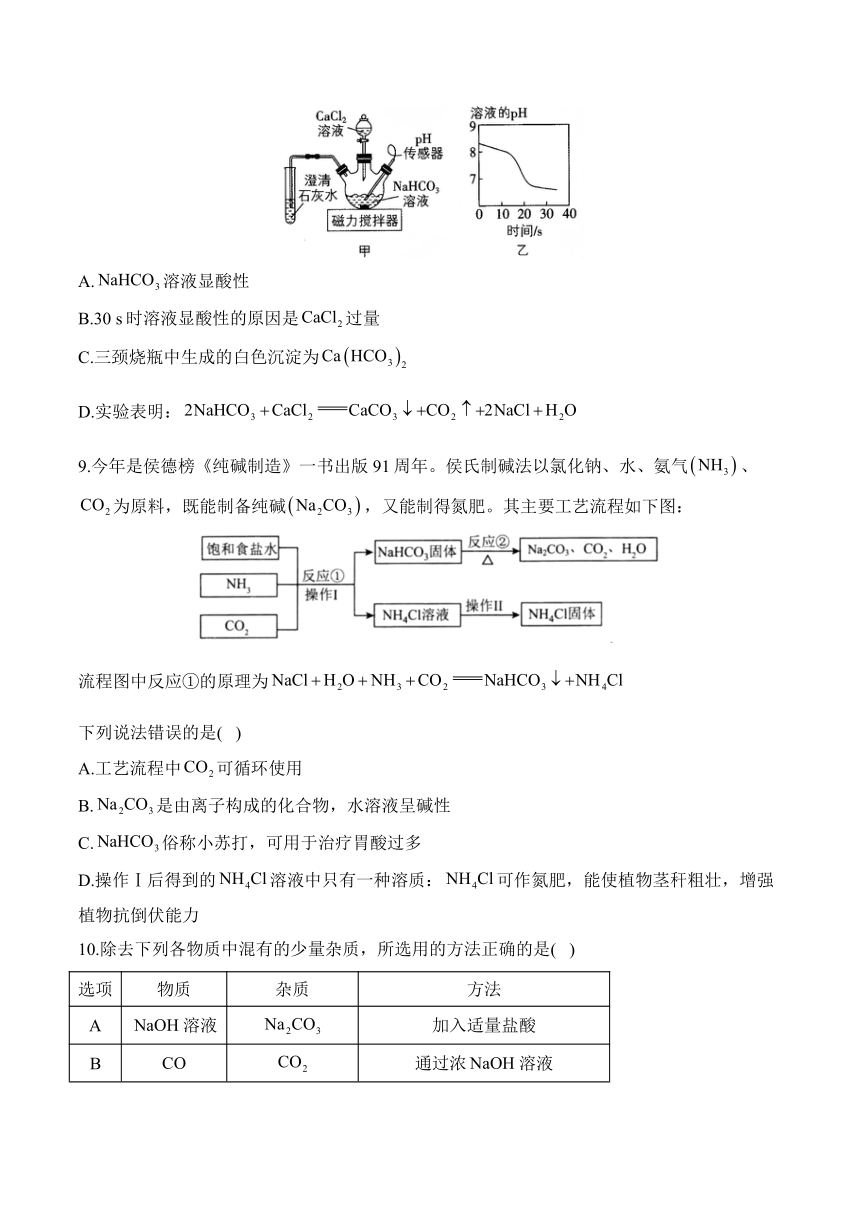
8.利用图甲所示装置探究溶液与溶液混合后发生的变化。常温下,向溶液中匀速滴加溶液,pH传感器测得溶液的pH随时间变化如图乙所示。一段时间后,三颈烧瓶和试管中均有白色沉淀生成。已知溶液呈中性。下列说法正确的是( )
A.溶液显酸性
B.30 s时溶液显酸性的原因是过量
C.三颈烧瓶中生成的白色沉淀为
D.实验表明:
9.今年是侯德榜《纯碱制造》一书出版91周年。侯氏制碱法以氯化钠、水、氨气、为原料,既能制备纯碱,又能制得氮肥。其主要工艺流程如下图:
流程图中反应①的原理为
下列说法错误的是( )
A.工艺流程中可循环使用
B.是由离子构成的化合物,水溶液呈碱性
C.俗称小苏打,可用于治疗胃酸过多
D.操作Ⅰ后得到的溶液中只有一种溶质:可作氮肥,能使植物茎秆粗壮,增强植物抗倒伏能力
10.除去下列各物质中混有的少量杂质,所选用的方法正确的是( )
选项 物质 杂质 方法
A 溶液 加入适量盐酸
B 通过浓溶液
C 固体 高温煅烧
D 溶液 溶液 加入适量的溶液,过滤
二、填空题(本题共5小题,每空1分,共20分)
11.为方便推测某些复杂物质的化学性质,可将其化学式改用常见物质的化学式表示。如碱式碳酸铜可改为,推测其兼具和的化学性质。
(1)举重运动员常用碱式碳酸镁粉末抹在手掌以增大摩擦力。
①参照上述方法,碱式碳酸镁的化学式可改写为 。
②该物质兼具_____(填“酸”或“碱”)和碳酸盐的化学性质。
③该物质分解的化学方程式为,X的化学式为______。
(2)某种茶垢清洁剂的主要成分为过碳酸钠(可表示为)。将过碳酸钠溶解于热水中,有大量气泡产生,其原因是 ;当不再产生气泡后,往溶液中加入足量澄清石灰水,反应的化学方程式为 。
12.施肥是使农业增产的重要手段。尿素[]是氮肥中主要的一种,它在土壤中的转化和吸收过程模拟如图。
尿素中氮元素的质量分数约为___________(结果精确到0.1%)。
(2)造成铵态氮肥()肥效降低的原因一是该化肥易分解生成和CO2两种氧化物,该反应的化学方程式为 ;二是雨水导致,结合图示和物质溶解性知识分析,可能是 。
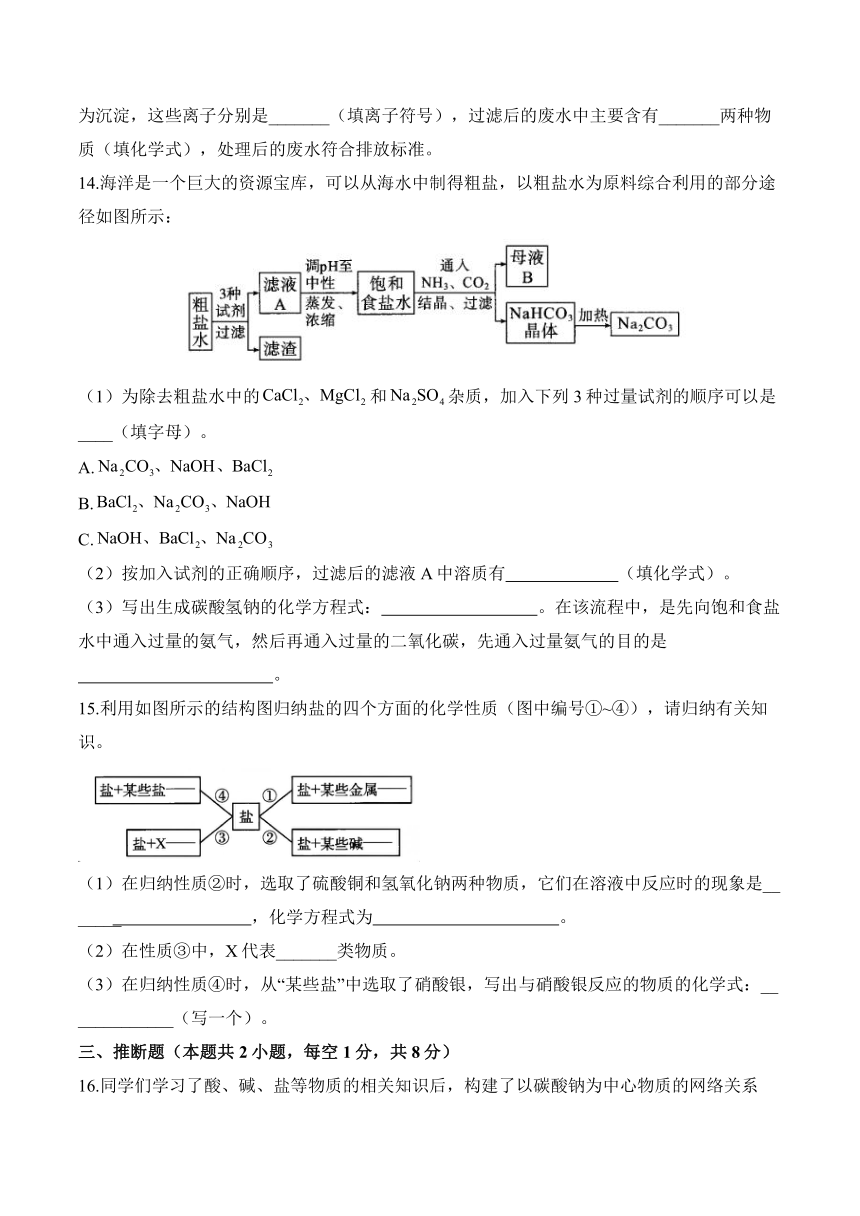
13.某工业园区甲、乙两化工厂排放的废水中含有、六种离子,甲厂含有其中的三种,乙厂含有另外三种,两厂废水的直接排放对当地水质带来严重影响。某课外实践小组对两厂废水进行实地检测,发现甲厂废水呈碱性。
(1)甲厂废水中一定含有的离子是_______,可能含有的离子是__________。
(2)经课外实践小组多次实验,发现两厂废水按适当比例混合,可将废水中的某些离子转化为沉淀,这些离子分别是_______(填离子符号),过滤后的废水中主要含有_______两种物质(填化学式),处理后的废水符合排放标准。
14.海洋是一个巨大的资源宝库,可以从海水中制得粗盐,以粗盐水为原料综合利用的部分途径如图所示:
(1)为除去粗盐水中的和杂质,加入下列3种过量试剂的顺序可以是____(填字母)。
A.
B.
C.
(2)按加入试剂的正确顺序,过滤后的滤液A中溶质有 (填化学式)。
(3)写出生成碳酸氢钠的化学方程式: 。在该流程中,是先向饱和食盐水中通入过量的氨气,然后再通入过量的二氧化碳,先通入过量氨气的目的是
。
15.利用如图所示的结构图归纳盐的四个方面的化学性质(图中编号①~④),请归纳有关知识。
(1)在归纳性质②时,选取了硫酸铜和氢氧化钠两种物质,它们在溶液中反应时的现象是_______ ,化学方程式为 。
(2)在性质③中,X代表_______类物质。
(3)在归纳性质④时,从“某些盐”中选取了硝酸银,写出与硝酸银反应的物质的化学式:_____________(写一个)。
三、推断题(本题共2小题,每空1分,共8分)
16.同学们学习了酸、碱、盐等物质的相关知识后,构建了以碳酸钠为中心物质的网络关系图。其中甲、乙、丙、丁分别是初中常见的不同类别化合物,丁是常见的温室气体。各物质间的关系如下图所示(“—”表示相邻两种物质能发生反应;“→”表示两种物质间的转化关系;图中部分反应物、生成物及反应条件已略去)。请回答:
(1)甲的化学式为_________。
(2)若乙中只含两种元素,反应①的化学方程式为 。
(3)若丙是大理石的主要成分,其用途是 (写一种)。
(4)甲和丁的反应_____(填“属于”或“不属于”)复分解反应。
17.A-H均是初中化学常见物质,它们之间的转化关系如图所示。其中D是补钙剂的有效成分。请回答下列问题:
(1)A的化学式为_________。
(2)反应②的化学方程式为 。
(3)反应③的基本反应类型是_________。
(4)物质F的一种用途是_________。
四、实验题(本题共1小题,每空1分,共7分)
18.化学兴趣小组在化学活动开放日,进行了以下两个实验探究活动。
【探究活动一】化学反应后溶液中溶质成分的探究。
某化学兴趣小组同学在学习完酸碱盐的化学性质后,进行了如下两个实验。
如图所示,向溶液和中分别滴加稀盐酸,甲试管中有气泡产生,乙试管中有气泡产生且固体消失。实验后将两支试管中的溶液倒入同一洁净烧杯丙中,观察到先有气泡产生,后有白色沉淀产生。然后将烧杯内的混合物过滤,得到滤液。
【提出问题】滤液中的溶质是什么?
【猜想与假设】
猜想1:溶质为。
猜想2:溶质为、。
猜想3:(1)溶质为_______________。
【验证与探究】
(2)甲同学取少量烧杯中的溶液于试管中,加入氯化钡溶液。若有_______________现象,则猜想3正确。
(3)乙同学取少量烧杯中的溶液于试管中,加入硝酸银溶液和稀硝酸。若有_______________现象,则猜想2正确。
【交流与反思】
(4)丙同学对乙同学的实验和结论提出了质疑,质疑的理由是 。经过讨论后,同学们一致认为甲同学实验方案和结论正确。
【探究活动二】制备与生产流程的探究。
氯碱工业以粗盐(主要成分是,含少量泥沙、、)为原料,生产氯气和氢氧化钠,需先除去粗盐中的杂质,模拟流程如下:
(1)加入过量溶液的目的是 。
(2)加入适量稀盐酸的目的是除去_________(填离子符号)。
(3)写出电解氯化钠溶液的化学方程式 。
五、计算题(本题共1小题,共5分)
19.将溶液逐滴加入100克溶液中,产生沉淀的质量与碳酸钠溶液关系如图所示。
(1)反应完全后生成沉淀的质量为_______;
(2)计算上述反应恰好完全反应时所得溶液的溶质质量分数(写出计算过程)。
答案以及解析
1.答案:D
解析:碳酸钠俗称纯碱、苏打,其化学式为,属于盐;氧化钙俗称生石灰;氢氧化钙俗称熟石灰或消石灰,其化学式为,属于碱;氢氧化钠俗称火碱、烧碱、苛性钠,其化学式为NaOH,属于碱。故选D。
2.答案:C
3.答案:C
解析:氯化铵不能与碱性物质混合使用,以防释放出氨气造成肥效降低,A正确;磷肥可以促进作物生长,增强作物抗寒、抗旱能力,B正确;和均属于铵态氮肥,取样然后加固体研磨,均产生有刺激性气味的气体,不能鉴别,C错误;无水种植需要肥料(含),是因为植物生长需要钾、氮肥,D正确。故选C。
4.答案:B
解析:A、单质中只有一种元素,但只有一种元素的物质不一定是单质,也可能是混合物,如氧气和臭氧的混合物、金刚石和石墨的混合物等,故选项推理错误。B、盐中含有金属离子(或铵根离子)和酸根离子,但盐中不一定含有金属元素,如硝酸铵,故选项推理正确。C、置换反应中一定有元素化合价的升降,但有元素化合价升降的反应不一定是置换反应,如电解水生成氢气和氧气,故选项推理错误。D、复分解反应中反应物与生成物都是化合物,但反应物与生成物都是化合物的反应不一定是复分解反应,如,故选项推理错误。故选:B。
5.答案:C
解析:氢氧化镁难溶于水,不能与氯化铜溶液反应,A错误。氯化镁能与硝酸银反应生成氯化银沉淀和硝酸镁,故通过一步反应能实现②的转化,B错误。硝酸镁溶液与可溶性碱反应能生成氢氧化镁沉淀,因此通过加入氢氧化钠等可溶性碱可实现③的转化,C正确。假设通过一步反应可实现向的转化,则对应的生成物是氯化镁和硝酸盐或硝酸,而氯化镁和硝酸盐或硝酸均可溶于水,故不能通过一步反应实现向的转化,D错误。
6.答案:C
解析:分析:粗盐水中含氯化镁、氯化钙、硫酸钠杂质,加入过量的氯化钡溶液,氯化钡和硫酸钠反应生成硫酸钡和氯化钠,可除去硫酸钠,加入过量的氢氧化钠溶液,氢氧化钠和氯化镁反应生成氢氧化镁和氯化钠,可除去氯化镁,加入过量的碳酸钠溶液,碳酸钠和氯化钙反应生成碳酸钙和氯化钠,碳酸钠和过量的氯化钡反应生成碳酸钡和氯化钠,可除去氯化钙和过量的氯化钡,过滤,除去碳酸钙、碳酸钡、氢氧化镁、硫酸钡,溶液Y中还含有过量的氢氧化钠和碳酸钠杂质,加入适量盐酸,氢氧化钠和盐酸反应生成氯化钠和水,碳酸钠和盐酸反应生成氯化钠、二氧化碳和水,除去氢氧化钠和碳酸钠,蒸发得到氯化钠。A、过滤所需的玻璃仪器是烧杯、漏斗、玻璃棒,不符合题意;B、由分析可知,加入氢氧化钠溶液,氢氧化钠和氯化镁反应生成氢氧化镁和氯化钠,可除去氯化镁,不符合题意;C、由分析可知,固体X中含硫酸钠、氢氧化镁、碳酸钙、碳酸钡四种物质,符合题意;D、整个除杂过程中,碳酸钠和氯化钙反应生成碳酸钙和氯化钠,碳酸钠和氯化钡反应生成碳酸钡和氯化钠,碳酸钠和稀盐酸反应生成氯化钠、二氧化碳和水,共参与了3个反应,不符合题意。故选C。
7.答案:C
解析:pH为2的水溶液显酸性,水溶液中含有大量的。
A.和在溶液中能结合生成水,且也不能共存,不符合题意,故选项错误。
B.能结合生成不溶于酸的硫酸钡沉淀,;和在溶液中能结合生成水和二氧化碳,不符合题意,故选项错误。
C.四种离子间不能结合生成沉淀、气体或水,能在酸性溶液中大量共存,且不存在有色离子,符合题意,故选项正确。
D.能结合生成水和二氧化碳,且也不能共存,不符合题意,故选项错误。
8.答案:D
解析:反应起始时的溶液为溶液,根据pH随时间变化图可知,起始时溶液pH范围为8~9,大于7,故溶液显碱性,A错误。由题意可知,反应后三颈烧瓶和试管中均有白色沉淀产生,说明反应会生成,与澄清石灰水反应产生碳酸钙白色沉淀,若与发生复分解反应生成和NaCl,不符合题意,故该反应的化学方程式为,三颈烧瓶中的沉淀是,C错误,D正确。已知溶液显中性,30 s时溶液显酸性是由于反应产生的二氧化碳与水反应生成了碳酸,B错误。
9.答案:D
10.答案:B
解析:A、溶液和均能与适量盐酸反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误。B、能与浓溶液反应生成碳酸钠和水,不与浓溶液反应,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确。C、固体高温煅烧生成氧化钙和二氧化碳,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误。D、溶液能与适量的溶液反应生成硫酸钡沉淀和硝酸钠,能除去杂质但引入了新的杂质硝酸钠,不符合除杂原则,故选项所采取的方法错误。故选:B。
11.答案:(1)①;②碱;③MgO
(2)受热分解生成水和氧气;
解析:(1)①根据碱式碳酸铜可改为可知,改写时阴离子的化合价不变,原子的种类和数目不变,故碱式碳酸镁可改写为。②该物质可写成的形式,推测其具有碱的性质和碳酸盐的性质。③根据质量守恒定律,反应前后原子的种类和数目不变,2X中含有2个Mg和2个O,则X中只含1个Mg和1个O,故X的化学式为MgO。
(2)过碳酸钠(可表示为)兼具碳酸钠和过氧化氢的化学性质,过氧化氢受热分解会生成水和氧气。当过氧化氢分解完后,溶液中的溶质为,加入澄清石灰水,反应生成碳酸钙和氢氧化钠,化学方程式为。
12.答案:(1)46.7%;
(2);碳酸氢铵溶于水流失造成的
解析:(1)尿素[]中氮元素的质量分数为。
(2)造成铵态氮肥()肥效降低的原因一是该化肥易分解生成和两种氧化物,根据质量守恒定律,反应前后元素种类不变,则这两种氧化物为二氧化碳和水,该反应的化学方程式为;二是雨水导致,结合题图和碳酸氢铵易溶于水分析,可能是碳酸氢铵溶于水流失造成的。
13.答案:(1);
(2);
解析:
(1)略。
(2)可分别与结合生成沉淀,故两厂废水按适当比例混合,可转化为沉淀,过滤后的废水中主要含有,则废水中主要含有的物质是。
14.答案:(1)BC
(2)
(3);使溶液显碱性,更有利于吸收二氧化碳
解析:(1)加入过量氢氧化钠溶液,和氯化镁反应生成氢氧化镁沉淀和氯化钠,从而除去氯化镁;加入过量氯化钡溶液,和硫酸钠反应,生成硫酸钡沉淀和氯化钠,从而除去硫酸钠;加入过量碳酸钠溶液,和氯化钙、过量的氯化钡反应生成碳酸钙沉淀、碳酸钡沉淀和氯化钠;过滤,向溶液中加适量的稀盐酸,把过量的氢氧化钠和碳酸钠除去,故碳酸钠溶液应放在氯化钡的后面,故符合的为B和C。
(2)根据以上分析,过滤后的滤液A中溶质有过量的氢氧化钠、过量的碳酸钠和氯化钠。
(3)根据题中流程图分析可知,氯化钠和二氧化碳、氨气、水反应生成碳酸氢钠和氯化铵,化学方程式为;先通入过量氨气的目的是使溶液显碱性,更有利于吸收二氧化碳。
15.答案:(1)产生蓝色沉淀;
(2)酸
(3)NaCl(或KCl、等)
解析:(1)硫酸铜和氢氧化钠反应会生成氢氧化铜蓝色沉淀和硫酸钠。
(2)盐除了能和某些金属、碱、盐反应外,还可以和某些酸反应,故X代表酸。
(3)与硝酸银反应的盐可以是含有的盐类。
16.答案:(1)
(2)
(3)作建筑材料(或作补钙剂)
(4)不属于
17.答案:(1)
(2)
(3)复分解反应
(4)作溶剂(合理即可)
解析:分析:D是补钙剂的有效成分,所以D是碳酸钙;碳酸钙和E反应生成三种物质,所以E是盐酸;碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,B又会与A反应产生碳酸钙,所以B是氯化钙,A是碳酸钠,C就是氯化钠;盐酸和H反应生成氯化钠和E,所以H是氢氧化钠,F是水,G是二氧化碳,二氧化碳和氢氧化钠反应生成碳酸钠和水,代入验证,推断正确。
详解:(1)根据分析,A的化学式为;
(2)反应②是碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,化学方程式为:;
(3)反应③是盐酸和氢氧化钠反应生成氯化钠和水,基本反应类型为复分解反应;
(4)根据分析,F是水,水可以作溶剂(合理即可)。
18.答案:【探究活动一】
(1)、
(2)白色沉淀生成
(3)白色沉淀生成
(4)滤液中也能与反应生成白色沉淀,影响的检验(合理即可)
【探究活动二】
(1)除去和过量
(2)、
(3)
19.答案:(1)5
(2)3%
解析:(1)据图可知,反应完全后生成沉淀的质量为5g。故填:5。
(2)设:恰好完全反应时所得氯化钠质量为x。
答:上述反应恰好完全反应时所得溶液的溶质质量分数为3%。
(试卷满分:60分;考试时间:60分钟)
可能用到的相对原子质量:H-1 C-12 O-16 Na-23 Cl-35.5 Ca-40
一、选择题(本大题共10小题,每题2分,共20分)
1.下列物质的名称、俗称、化学式及类别中,完全对应的是( )
选项 物质的名称 俗称 化学式 类别
A 碳酸钠 烧碱 盐
B 碳酸钙 生石灰 盐
C 氢氧化钙 熟石灰 CaO 金属氧化物
D 氢氧化钠 苛性钠 NaOH 碱
2.下图是硫酸氢钾溶液的微观示意图,下列预测错误的是( )
A.该溶液能与碳酸钠反应
B.该溶液能与锌粉反应
C.该溶液中含有氢离子,所以硫酸氢钾属于酸
D.该溶液能与硝酸钡溶液反应
3.下列有关化学肥料的知识错误的是( )
A.氯化铵不能与碱性物质混合使用
B.磷肥可以促进作物生长,增强作物抗寒、抗旱能力
C.鉴别和,取样然后加固体研磨,闻气味
D.无水种植需要肥料(含),是因为植物生长需要钾、氮肥
4.归纳与推理是化学学科核心素养之一,也是学习化学的重要方法。下列说法正确的是( )
A.单质中只有一种元素,则只有一种元素的物质一定是单质
B.盐中含有金属离子(或铵根离子)和酸根离子,但盐中不一定含有金属元素
C.置换反应中一定有元素化合价的升降,则有元素化合价升降的反应一定是置换反应
D.复分解反应中反应物与生成物都是化合物,因此反应物与生成物都是化合物的反应一定是复分解反应
5.如图是、、三种物质间的转化关系,根据所学知识判断,下列说法正确的是( )
A.通过加入氯化铜溶液或稀盐酸可实现①的转化
B.通过一步反应无法实现②的转化
C.通过加入氢氧化钠等可溶性碱可实现③的转化
D.通过一步反应可实现向的转化
6.粗盐中含有泥沙和、、杂质。某同学将粗盐样品溶解、过滤,除去泥沙后,取粗盐水按如图所示流程进行提纯。下列说法错误的是( )
A.过滤用到的玻璃仪器有漏斗、烧杯、玻璃棒
B.加入溶液的目的是除去粗盐中的
C.固体X中含有3种物质
D.整个除杂过程中共参与了3个反应
7.打开保险柜,同学们发现一瓶无色透明的液体。经测定,其pH=2,对其中可能存在的离子组合,推测合理的是( )
A. B.、、
C.、 D.、
8.利用图甲所示装置探究溶液与溶液混合后发生的变化。常温下,向溶液中匀速滴加溶液,pH传感器测得溶液的pH随时间变化如图乙所示。一段时间后,三颈烧瓶和试管中均有白色沉淀生成。已知溶液呈中性。下列说法正确的是( )
A.溶液显酸性
B.30 s时溶液显酸性的原因是过量
C.三颈烧瓶中生成的白色沉淀为
D.实验表明:
9.今年是侯德榜《纯碱制造》一书出版91周年。侯氏制碱法以氯化钠、水、氨气、为原料,既能制备纯碱,又能制得氮肥。其主要工艺流程如下图:
流程图中反应①的原理为
下列说法错误的是( )
A.工艺流程中可循环使用
B.是由离子构成的化合物,水溶液呈碱性
C.俗称小苏打,可用于治疗胃酸过多
D.操作Ⅰ后得到的溶液中只有一种溶质:可作氮肥,能使植物茎秆粗壮,增强植物抗倒伏能力
10.除去下列各物质中混有的少量杂质,所选用的方法正确的是( )
选项 物质 杂质 方法
A 溶液 加入适量盐酸
B 通过浓溶液
C 固体 高温煅烧
D 溶液 溶液 加入适量的溶液,过滤
二、填空题(本题共5小题,每空1分,共20分)
11.为方便推测某些复杂物质的化学性质,可将其化学式改用常见物质的化学式表示。如碱式碳酸铜可改为,推测其兼具和的化学性质。
(1)举重运动员常用碱式碳酸镁粉末抹在手掌以增大摩擦力。
①参照上述方法,碱式碳酸镁的化学式可改写为 。
②该物质兼具_____(填“酸”或“碱”)和碳酸盐的化学性质。
③该物质分解的化学方程式为,X的化学式为______。
(2)某种茶垢清洁剂的主要成分为过碳酸钠(可表示为)。将过碳酸钠溶解于热水中,有大量气泡产生,其原因是 ;当不再产生气泡后,往溶液中加入足量澄清石灰水,反应的化学方程式为 。
12.施肥是使农业增产的重要手段。尿素[]是氮肥中主要的一种,它在土壤中的转化和吸收过程模拟如图。
尿素中氮元素的质量分数约为___________(结果精确到0.1%)。
(2)造成铵态氮肥()肥效降低的原因一是该化肥易分解生成和CO2两种氧化物,该反应的化学方程式为 ;二是雨水导致,结合图示和物质溶解性知识分析,可能是 。
13.某工业园区甲、乙两化工厂排放的废水中含有、六种离子,甲厂含有其中的三种,乙厂含有另外三种,两厂废水的直接排放对当地水质带来严重影响。某课外实践小组对两厂废水进行实地检测,发现甲厂废水呈碱性。
(1)甲厂废水中一定含有的离子是_______,可能含有的离子是__________。
(2)经课外实践小组多次实验,发现两厂废水按适当比例混合,可将废水中的某些离子转化为沉淀,这些离子分别是_______(填离子符号),过滤后的废水中主要含有_______两种物质(填化学式),处理后的废水符合排放标准。
14.海洋是一个巨大的资源宝库,可以从海水中制得粗盐,以粗盐水为原料综合利用的部分途径如图所示:
(1)为除去粗盐水中的和杂质,加入下列3种过量试剂的顺序可以是____(填字母)。
A.
B.
C.
(2)按加入试剂的正确顺序,过滤后的滤液A中溶质有 (填化学式)。
(3)写出生成碳酸氢钠的化学方程式: 。在该流程中,是先向饱和食盐水中通入过量的氨气,然后再通入过量的二氧化碳,先通入过量氨气的目的是
。
15.利用如图所示的结构图归纳盐的四个方面的化学性质(图中编号①~④),请归纳有关知识。
(1)在归纳性质②时,选取了硫酸铜和氢氧化钠两种物质,它们在溶液中反应时的现象是_______ ,化学方程式为 。
(2)在性质③中,X代表_______类物质。
(3)在归纳性质④时,从“某些盐”中选取了硝酸银,写出与硝酸银反应的物质的化学式:_____________(写一个)。
三、推断题(本题共2小题,每空1分,共8分)
16.同学们学习了酸、碱、盐等物质的相关知识后,构建了以碳酸钠为中心物质的网络关系图。其中甲、乙、丙、丁分别是初中常见的不同类别化合物,丁是常见的温室气体。各物质间的关系如下图所示(“—”表示相邻两种物质能发生反应;“→”表示两种物质间的转化关系;图中部分反应物、生成物及反应条件已略去)。请回答:
(1)甲的化学式为_________。
(2)若乙中只含两种元素,反应①的化学方程式为 。
(3)若丙是大理石的主要成分,其用途是 (写一种)。
(4)甲和丁的反应_____(填“属于”或“不属于”)复分解反应。
17.A-H均是初中化学常见物质,它们之间的转化关系如图所示。其中D是补钙剂的有效成分。请回答下列问题:
(1)A的化学式为_________。
(2)反应②的化学方程式为 。
(3)反应③的基本反应类型是_________。
(4)物质F的一种用途是_________。
四、实验题(本题共1小题,每空1分,共7分)
18.化学兴趣小组在化学活动开放日,进行了以下两个实验探究活动。
【探究活动一】化学反应后溶液中溶质成分的探究。
某化学兴趣小组同学在学习完酸碱盐的化学性质后,进行了如下两个实验。
如图所示,向溶液和中分别滴加稀盐酸,甲试管中有气泡产生,乙试管中有气泡产生且固体消失。实验后将两支试管中的溶液倒入同一洁净烧杯丙中,观察到先有气泡产生,后有白色沉淀产生。然后将烧杯内的混合物过滤,得到滤液。
【提出问题】滤液中的溶质是什么?
【猜想与假设】
猜想1:溶质为。
猜想2:溶质为、。
猜想3:(1)溶质为_______________。
【验证与探究】
(2)甲同学取少量烧杯中的溶液于试管中,加入氯化钡溶液。若有_______________现象,则猜想3正确。
(3)乙同学取少量烧杯中的溶液于试管中,加入硝酸银溶液和稀硝酸。若有_______________现象,则猜想2正确。
【交流与反思】
(4)丙同学对乙同学的实验和结论提出了质疑,质疑的理由是 。经过讨论后,同学们一致认为甲同学实验方案和结论正确。
【探究活动二】制备与生产流程的探究。
氯碱工业以粗盐(主要成分是,含少量泥沙、、)为原料,生产氯气和氢氧化钠,需先除去粗盐中的杂质,模拟流程如下:
(1)加入过量溶液的目的是 。
(2)加入适量稀盐酸的目的是除去_________(填离子符号)。
(3)写出电解氯化钠溶液的化学方程式 。
五、计算题(本题共1小题,共5分)
19.将溶液逐滴加入100克溶液中,产生沉淀的质量与碳酸钠溶液关系如图所示。
(1)反应完全后生成沉淀的质量为_______;
(2)计算上述反应恰好完全反应时所得溶液的溶质质量分数(写出计算过程)。
答案以及解析
1.答案:D
解析:碳酸钠俗称纯碱、苏打,其化学式为,属于盐;氧化钙俗称生石灰;氢氧化钙俗称熟石灰或消石灰,其化学式为,属于碱;氢氧化钠俗称火碱、烧碱、苛性钠,其化学式为NaOH,属于碱。故选D。
2.答案:C
3.答案:C
解析:氯化铵不能与碱性物质混合使用,以防释放出氨气造成肥效降低,A正确;磷肥可以促进作物生长,增强作物抗寒、抗旱能力,B正确;和均属于铵态氮肥,取样然后加固体研磨,均产生有刺激性气味的气体,不能鉴别,C错误;无水种植需要肥料(含),是因为植物生长需要钾、氮肥,D正确。故选C。
4.答案:B
解析:A、单质中只有一种元素,但只有一种元素的物质不一定是单质,也可能是混合物,如氧气和臭氧的混合物、金刚石和石墨的混合物等,故选项推理错误。B、盐中含有金属离子(或铵根离子)和酸根离子,但盐中不一定含有金属元素,如硝酸铵,故选项推理正确。C、置换反应中一定有元素化合价的升降,但有元素化合价升降的反应不一定是置换反应,如电解水生成氢气和氧气,故选项推理错误。D、复分解反应中反应物与生成物都是化合物,但反应物与生成物都是化合物的反应不一定是复分解反应,如,故选项推理错误。故选:B。
5.答案:C
解析:氢氧化镁难溶于水,不能与氯化铜溶液反应,A错误。氯化镁能与硝酸银反应生成氯化银沉淀和硝酸镁,故通过一步反应能实现②的转化,B错误。硝酸镁溶液与可溶性碱反应能生成氢氧化镁沉淀,因此通过加入氢氧化钠等可溶性碱可实现③的转化,C正确。假设通过一步反应可实现向的转化,则对应的生成物是氯化镁和硝酸盐或硝酸,而氯化镁和硝酸盐或硝酸均可溶于水,故不能通过一步反应实现向的转化,D错误。
6.答案:C
解析:分析:粗盐水中含氯化镁、氯化钙、硫酸钠杂质,加入过量的氯化钡溶液,氯化钡和硫酸钠反应生成硫酸钡和氯化钠,可除去硫酸钠,加入过量的氢氧化钠溶液,氢氧化钠和氯化镁反应生成氢氧化镁和氯化钠,可除去氯化镁,加入过量的碳酸钠溶液,碳酸钠和氯化钙反应生成碳酸钙和氯化钠,碳酸钠和过量的氯化钡反应生成碳酸钡和氯化钠,可除去氯化钙和过量的氯化钡,过滤,除去碳酸钙、碳酸钡、氢氧化镁、硫酸钡,溶液Y中还含有过量的氢氧化钠和碳酸钠杂质,加入适量盐酸,氢氧化钠和盐酸反应生成氯化钠和水,碳酸钠和盐酸反应生成氯化钠、二氧化碳和水,除去氢氧化钠和碳酸钠,蒸发得到氯化钠。A、过滤所需的玻璃仪器是烧杯、漏斗、玻璃棒,不符合题意;B、由分析可知,加入氢氧化钠溶液,氢氧化钠和氯化镁反应生成氢氧化镁和氯化钠,可除去氯化镁,不符合题意;C、由分析可知,固体X中含硫酸钠、氢氧化镁、碳酸钙、碳酸钡四种物质,符合题意;D、整个除杂过程中,碳酸钠和氯化钙反应生成碳酸钙和氯化钠,碳酸钠和氯化钡反应生成碳酸钡和氯化钠,碳酸钠和稀盐酸反应生成氯化钠、二氧化碳和水,共参与了3个反应,不符合题意。故选C。
7.答案:C
解析:pH为2的水溶液显酸性,水溶液中含有大量的。
A.和在溶液中能结合生成水,且也不能共存,不符合题意,故选项错误。
B.能结合生成不溶于酸的硫酸钡沉淀,;和在溶液中能结合生成水和二氧化碳,不符合题意,故选项错误。
C.四种离子间不能结合生成沉淀、气体或水,能在酸性溶液中大量共存,且不存在有色离子,符合题意,故选项正确。
D.能结合生成水和二氧化碳,且也不能共存,不符合题意,故选项错误。
8.答案:D
解析:反应起始时的溶液为溶液,根据pH随时间变化图可知,起始时溶液pH范围为8~9,大于7,故溶液显碱性,A错误。由题意可知,反应后三颈烧瓶和试管中均有白色沉淀产生,说明反应会生成,与澄清石灰水反应产生碳酸钙白色沉淀,若与发生复分解反应生成和NaCl,不符合题意,故该反应的化学方程式为,三颈烧瓶中的沉淀是,C错误,D正确。已知溶液显中性,30 s时溶液显酸性是由于反应产生的二氧化碳与水反应生成了碳酸,B错误。
9.答案:D
10.答案:B
解析:A、溶液和均能与适量盐酸反应,不但能把杂质除去,也会把原物质除去,不符合除杂原则,故选项所采取的方法错误。B、能与浓溶液反应生成碳酸钠和水,不与浓溶液反应,能除去杂质且没有引入新的杂质,符合除杂原则,故选项所采取的方法正确。C、固体高温煅烧生成氧化钙和二氧化碳,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误。D、溶液能与适量的溶液反应生成硫酸钡沉淀和硝酸钠,能除去杂质但引入了新的杂质硝酸钠,不符合除杂原则,故选项所采取的方法错误。故选:B。
11.答案:(1)①;②碱;③MgO
(2)受热分解生成水和氧气;
解析:(1)①根据碱式碳酸铜可改为可知,改写时阴离子的化合价不变,原子的种类和数目不变,故碱式碳酸镁可改写为。②该物质可写成的形式,推测其具有碱的性质和碳酸盐的性质。③根据质量守恒定律,反应前后原子的种类和数目不变,2X中含有2个Mg和2个O,则X中只含1个Mg和1个O,故X的化学式为MgO。
(2)过碳酸钠(可表示为)兼具碳酸钠和过氧化氢的化学性质,过氧化氢受热分解会生成水和氧气。当过氧化氢分解完后,溶液中的溶质为,加入澄清石灰水,反应生成碳酸钙和氢氧化钠,化学方程式为。
12.答案:(1)46.7%;
(2);碳酸氢铵溶于水流失造成的
解析:(1)尿素[]中氮元素的质量分数为。
(2)造成铵态氮肥()肥效降低的原因一是该化肥易分解生成和两种氧化物,根据质量守恒定律,反应前后元素种类不变,则这两种氧化物为二氧化碳和水,该反应的化学方程式为;二是雨水导致,结合题图和碳酸氢铵易溶于水分析,可能是碳酸氢铵溶于水流失造成的。
13.答案:(1);
(2);
解析:
(1)略。
(2)可分别与结合生成沉淀,故两厂废水按适当比例混合,可转化为沉淀,过滤后的废水中主要含有,则废水中主要含有的物质是。
14.答案:(1)BC
(2)
(3);使溶液显碱性,更有利于吸收二氧化碳
解析:(1)加入过量氢氧化钠溶液,和氯化镁反应生成氢氧化镁沉淀和氯化钠,从而除去氯化镁;加入过量氯化钡溶液,和硫酸钠反应,生成硫酸钡沉淀和氯化钠,从而除去硫酸钠;加入过量碳酸钠溶液,和氯化钙、过量的氯化钡反应生成碳酸钙沉淀、碳酸钡沉淀和氯化钠;过滤,向溶液中加适量的稀盐酸,把过量的氢氧化钠和碳酸钠除去,故碳酸钠溶液应放在氯化钡的后面,故符合的为B和C。
(2)根据以上分析,过滤后的滤液A中溶质有过量的氢氧化钠、过量的碳酸钠和氯化钠。
(3)根据题中流程图分析可知,氯化钠和二氧化碳、氨气、水反应生成碳酸氢钠和氯化铵,化学方程式为;先通入过量氨气的目的是使溶液显碱性,更有利于吸收二氧化碳。
15.答案:(1)产生蓝色沉淀;
(2)酸
(3)NaCl(或KCl、等)
解析:(1)硫酸铜和氢氧化钠反应会生成氢氧化铜蓝色沉淀和硫酸钠。
(2)盐除了能和某些金属、碱、盐反应外,还可以和某些酸反应,故X代表酸。
(3)与硝酸银反应的盐可以是含有的盐类。
16.答案:(1)
(2)
(3)作建筑材料(或作补钙剂)
(4)不属于
17.答案:(1)
(2)
(3)复分解反应
(4)作溶剂(合理即可)
解析:分析:D是补钙剂的有效成分,所以D是碳酸钙;碳酸钙和E反应生成三种物质,所以E是盐酸;碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,B又会与A反应产生碳酸钙,所以B是氯化钙,A是碳酸钠,C就是氯化钠;盐酸和H反应生成氯化钠和E,所以H是氢氧化钠,F是水,G是二氧化碳,二氧化碳和氢氧化钠反应生成碳酸钠和水,代入验证,推断正确。
详解:(1)根据分析,A的化学式为;
(2)反应②是碳酸钠和盐酸反应生成氯化钠、水和二氧化碳,化学方程式为:;
(3)反应③是盐酸和氢氧化钠反应生成氯化钠和水,基本反应类型为复分解反应;
(4)根据分析,F是水,水可以作溶剂(合理即可)。
18.答案:【探究活动一】
(1)、
(2)白色沉淀生成
(3)白色沉淀生成
(4)滤液中也能与反应生成白色沉淀,影响的检验(合理即可)
【探究活动二】
(1)除去和过量
(2)、
(3)
19.答案:(1)5
(2)3%
解析:(1)据图可知,反应完全后生成沉淀的质量为5g。故填:5。
(2)设:恰好完全反应时所得氯化钠质量为x。
答:上述反应恰好完全反应时所得溶液的溶质质量分数为3%。
同课章节目录
