苏教版高中化学5选择性必修3有机化学基础专题3有机物的结构与分类3.2芳香烃课件(共22张PPT)
文档属性
| 名称 | 苏教版高中化学5选择性必修3有机化学基础专题3有机物的结构与分类3.2芳香烃课件(共22张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 3.3MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-23 00:00:00 | ||
图片预览



文档简介
(共22张PPT)
选修三
颜色 状态 气味 毒性 密度 溶解性 溶、沸点
无色 液态 特殊
气味 有毒易挥发
【实验】分别向酸性高锰酸钾溶液和溴水中加入适量苯,用力振荡,静置并观察。
【现象】
分层,上层为无色的苯,下层为紫红色的KMnO4溶液。
溶液分层,上层为橙红色的溴的苯溶液,下层为黄色的溴水。
【结论】苯不能被酸性KMnO4溶液氧化,也不能与溴水反应,苯能将溴从水溶液
中萃取出来。说明苯分子具有不同于烯烃和炔烃的特殊结构。
苯的物理性质
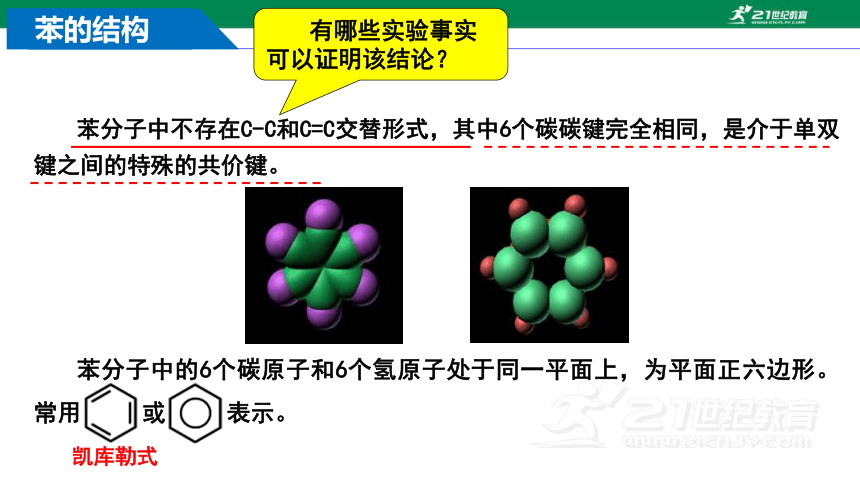
苯的结构
苯分子中不存在C-C和C=C交替形式,其中6个碳碳键完全相同,是介于单双键之间的特殊的共价键。
凯库勒式
苯分子中的6个碳原子和6个氢原子处于同一平面上,为平面正六边形。常用 或 表示。
有哪些实验事实可以证明该结论?
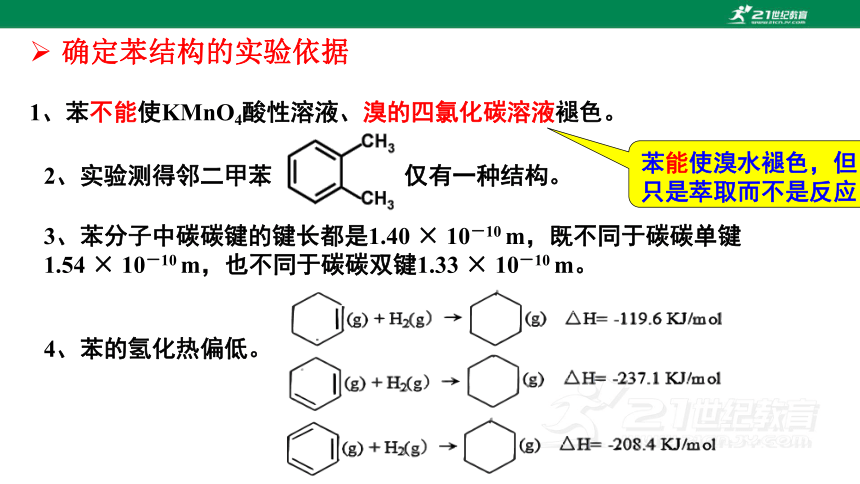
2、实验测得邻二甲苯 仅有一种结构。
3、苯分子中碳碳键的键长都是1.40 × 10-10 m,既不同于碳碳单键1.54 × 10-10 m,也不同于碳碳双键1.33 × 10-10 m。
1、苯不能使KMnO4酸性溶液、溴的四氯化碳溶液褪色。
4、苯的氢化热偏低。
确定苯结构的实验依据
苯能使溴水褪色,但只是萃取而不是反应!
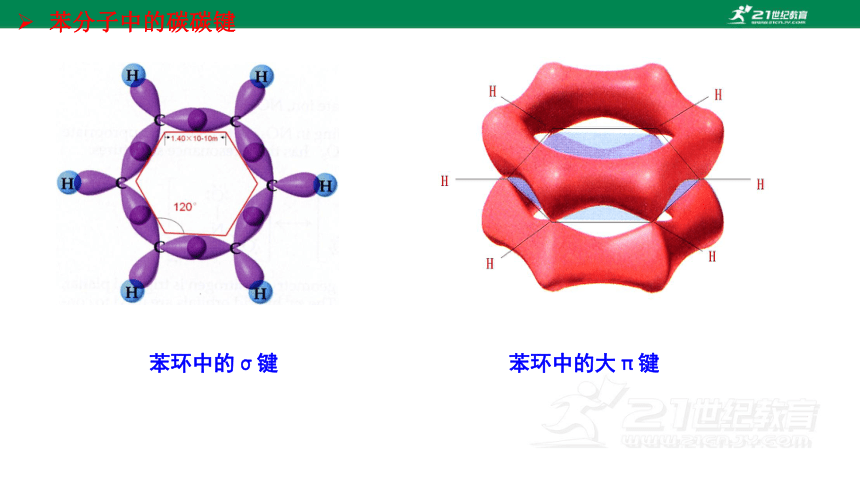
苯环中的大π键
苯环中的σ键
苯分子中的碳碳键
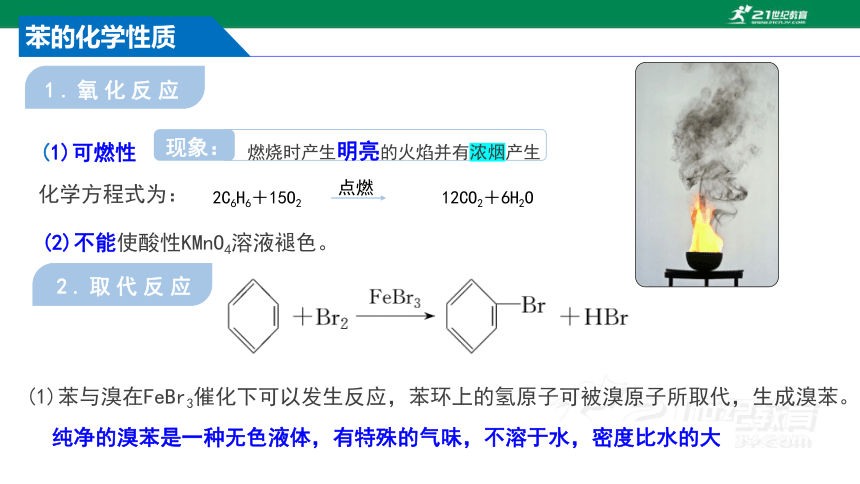
1.氧化反应
(1)可燃性
化学方程式为:
(2)不能使酸性KMnO4溶液褪色。
燃烧时产生明亮的火焰并有浓烟产生
现象:
2C6H6+15O2 12CO2+6H2O
点燃
苯的化学性质
2.取代反应
(1)苯与溴在FeBr3催化下可以发生反应,苯环上的氢原子可被溴原子所取代,生成溴苯。
纯净的溴苯是一种无色液体,有特殊的气味,不溶于水,密度比水的大
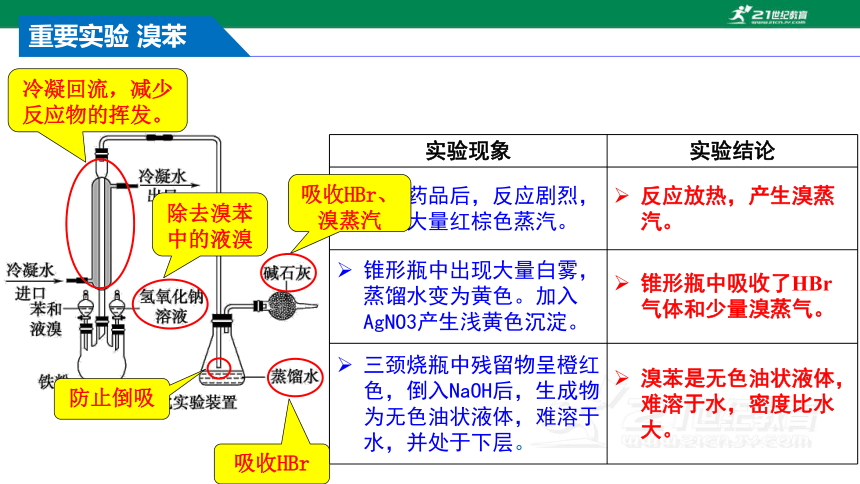
重要实验 溴苯
实验现象 实验结论
加入药品后,反应剧烈,产生大量红棕色蒸汽。
锥形瓶中出现大量白雾,蒸馏水变为黄色。加入AgNO3产生浅黄色沉淀。
三颈烧瓶中残留物呈橙红色,倒入NaOH后,生成物为无色油状液体,难溶于水,并处于下层。
反应放热,产生溴蒸汽。
锥形瓶中吸收了HBr气体和少量溴蒸气。
溴苯是无色油状液体,难溶于水,密度比水大。
除去溴苯中的液溴
冷凝回流,减少反应物的挥发。
吸收HBr
防止倒吸
吸收HBr、溴蒸汽
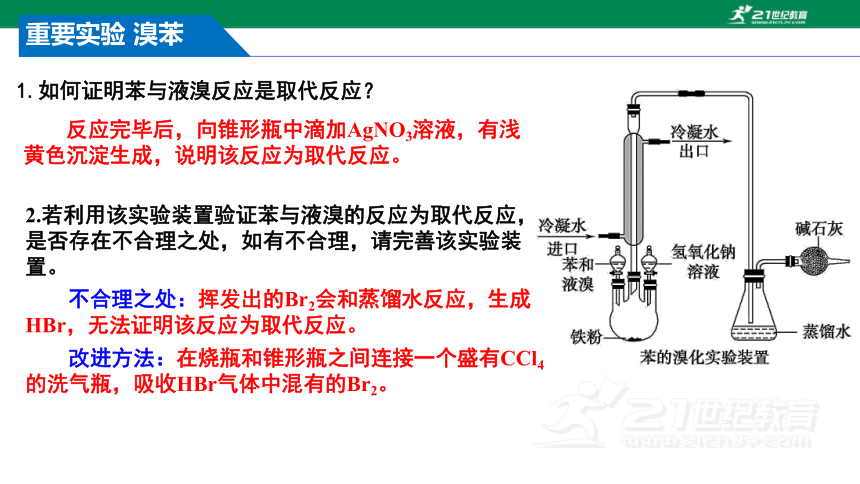
1.如何证明苯与液溴反应是取代反应?
反应完毕后,向锥形瓶中滴加AgNO3溶液,有浅黄色沉淀生成,说明该反应为取代反应。
不合理之处:挥发出的Br2会和蒸馏水反应,生成HBr,无法证明该反应为取代反应。
改进方法:在烧瓶和锥形瓶之间连接一个盛有CCl4的洗气瓶,吸收HBr气体中混有的Br2。
2.若利用该实验装置验证苯与液溴的反应为取代反应,是否存在不合理之处,如有不合理,请完善该实验装置。
重要实验 溴苯
纯净的硝基苯为无色液体,有苦杏仁气味,不溶于水,密度比水的大。
取代反应二:
在浓硫酸作用下,苯在50~60℃还能与浓硝酸发生硝化反应,生成硝基苯。
+HNO3(浓)
+H2O
浓H2SO4
重要实验 硝基苯
实验装置
实验步骤
①配制混合酸:先将1.5 mL浓硝酸注入大试管中,再慢慢注入2 mL浓硫酸,并及时摇匀和冷却;
②向冷却后的混合酸中逐滴加入1 mL苯,充分振荡,混合均匀;
③将大试管放在50~60 ℃的水浴中加热。
重要实验 硝基苯
生成物为淡黄色、有苦杏仁味的油状液体,难溶于水,并处于下层。
实验现象:
浓硫酸
浓硝酸
苯
50~60℃水浴加热
受热均匀;容易控制温度!
将浓硫酸慢慢加入到浓硝酸中,并不断振荡降温,冷却到50 ℃以下再逐滴滴入苯,边滴边振荡。
你知道水浴加热有哪些优点吗?
指出药品的加入的顺序及注意事项!
催化剂吸水剂
冷凝回流,减少反应物的挥发。
取代反应三:
(3)磺化反应:苯与浓硫酸在70~80℃可以发生取代反应。
+HO—SO3H + H2O
苯磺酸
苯磺酸易溶于水,是一种强酸,可以看作硫酸分子里的一个羟基被苯环取代的产物。磺化反应可用于制备合成洗涤剂。
加成反应:
在以Pt、Ni等为催化剂并加热的条件下,
苯能与氢气发生加成反应,生成环已烷。
苯的化学性质
物理性质 化学性质 化学方程式
无色有特殊气味的液体,难溶于水,ρ苯<ρ水,易挥发,有毒,常用作有机溶剂。
易取代
难氧化
难加成
反应较容易,苯的主要性质。与液溴、浓硝酸等在一定条件下发生取代反应。
可与氢气发生加成反应,用于工业制环己烷。
①易燃,火焰明亮,伴有浓烟。
②不能被KMnO4、H2O2等强氧化剂氧化。
苯的性质总结
芳香烃的来源
炼焦炉
煤的干馏
煤
煤焦油
芳香烃
干馏
分馏
焦炭
焦炉气
(苯、甲苯、萘、蒽、菲等)
苯的同系物
你知道芳香族化合物、芳香烃、苯的同系物之间的关系吗?请试着对下列物质分类!
芳香族化合物: ;
芳香烃: ;
苯的同系物: 。
⑴ ⑶ ⑸ ⑻ ⑼ ⑽ ⑿ ⒀
⑼ ⑿
全部都是
苯的同系物通式
CnH2n-6(n≥7)
1.组成和结构特点
苯环使甲基上的H变活泼,甲基易被高锰酸钾氧化成-COOH。自身被还原成二价锰离子。甲苯能便酸性高锰酸钾溶液褪色。
苯的同系物
概念:只有一个苯环,可以看成是由苯环上的H被烷基代替而得到的。
苯的同系物——甲苯
苯
(1)习惯命名法:
①一元烷基苯以苯为母体,烷基为取代基,如:
②二元烷基苯也是以苯为母体,分别有3种同分异构,可用邻、间、对位命名,如:
甲苯 乙苯
邻二甲苯 间二甲苯 对二甲苯
苯的同系物的命名
(2)系统命名法:
将苯环上的6个碳原子编号,以某个最简单的取代基(如甲基)所在的碳原子为1号,并按使 支链的位次和最小的原则给其他取代基编号,最后根据有机物名称的基本格式写出名称。如:
2.苯的同系物的命名
1,2–二甲苯 1,3–二甲苯
邻二甲苯 间二甲苯 对二甲苯
1,4–二甲基–2–乙基苯
1,4–二甲苯
1.一般具有类似苯的气味,无色液体,不溶于水,易溶于有机溶剂,密度比水的小。
2.随碳原子数增多,熔沸点依次升高。
3.同分异构体中,分子间作用力越弱,沸点越低。
如沸点:
144℃ 139℃ 138℃
> >
苯的同系物的物理性质
氧化反应
条件:与苯环直接相连的碳原子上有氢!
取代反应
1、硝化反应
结论:苯基(邻、对位活化)和烷基互相活化!
2,4,6—三硝基甲苯
甲苯能使酸性KMnO4溶液褪色,
这是由于甲苯上的甲基被酸性KMnO4氧化的结果。
苯的同系物的化学性质
取代反应
1、硝化反应
结论:苯基(邻、对位活化)和烷基互相活化!
2,4,6—三硝基甲苯
苯的同系物的化学性质
加成反应
2、卤代反应—与卤素单质
+ Cl2
+ HCl
光照
FeCl3
+ Cl2
+ HCl
结论:苯环和侧链都能发生取代反应,但条件不同。
反应条件苛刻,反应困难!
作业
总结苯与苯的同系物在分子组成、结构和性质上的异同
归纳总结
不同点 取代反应 易发生取代反应,主要得到一元取代产物 更容易发生取代反应,常得到多元取代产物
氧化反应 难被氧化,不能使酸性KMnO4溶液褪色 易被氧化剂氧化,能使酸性KMnO4溶液褪色
差异原因 苯的同系物分子中,苯环与侧链相互影响。苯环影响侧链,使侧链烃基活化而易被氧化;侧链烃基影响苯环,使苯环上烃基邻、对位的氢原子活化而被取代
选修三
颜色 状态 气味 毒性 密度 溶解性 溶、沸点
无色 液态 特殊
气味 有毒
【实验】分别向酸性高锰酸钾溶液和溴水中加入适量苯,用力振荡,静置并观察。
【现象】
分层,上层为无色的苯,下层为紫红色的KMnO4溶液。
溶液分层,上层为橙红色的溴的苯溶液,下层为黄色的溴水。
【结论】苯不能被酸性KMnO4溶液氧化,也不能与溴水反应,苯能将溴从水溶液
中萃取出来。说明苯分子具有不同于烯烃和炔烃的特殊结构。
苯的物理性质
苯的结构
苯分子中不存在C-C和C=C交替形式,其中6个碳碳键完全相同,是介于单双键之间的特殊的共价键。
凯库勒式
苯分子中的6个碳原子和6个氢原子处于同一平面上,为平面正六边形。常用 或 表示。
有哪些实验事实可以证明该结论?
2、实验测得邻二甲苯 仅有一种结构。
3、苯分子中碳碳键的键长都是1.40 × 10-10 m,既不同于碳碳单键1.54 × 10-10 m,也不同于碳碳双键1.33 × 10-10 m。
1、苯不能使KMnO4酸性溶液、溴的四氯化碳溶液褪色。
4、苯的氢化热偏低。
确定苯结构的实验依据
苯能使溴水褪色,但只是萃取而不是反应!
苯环中的大π键
苯环中的σ键
苯分子中的碳碳键
1.氧化反应
(1)可燃性
化学方程式为:
(2)不能使酸性KMnO4溶液褪色。
燃烧时产生明亮的火焰并有浓烟产生
现象:
2C6H6+15O2 12CO2+6H2O
点燃
苯的化学性质
2.取代反应
(1)苯与溴在FeBr3催化下可以发生反应,苯环上的氢原子可被溴原子所取代,生成溴苯。
纯净的溴苯是一种无色液体,有特殊的气味,不溶于水,密度比水的大
重要实验 溴苯
实验现象 实验结论
加入药品后,反应剧烈,产生大量红棕色蒸汽。
锥形瓶中出现大量白雾,蒸馏水变为黄色。加入AgNO3产生浅黄色沉淀。
三颈烧瓶中残留物呈橙红色,倒入NaOH后,生成物为无色油状液体,难溶于水,并处于下层。
反应放热,产生溴蒸汽。
锥形瓶中吸收了HBr气体和少量溴蒸气。
溴苯是无色油状液体,难溶于水,密度比水大。
除去溴苯中的液溴
冷凝回流,减少反应物的挥发。
吸收HBr
防止倒吸
吸收HBr、溴蒸汽
1.如何证明苯与液溴反应是取代反应?
反应完毕后,向锥形瓶中滴加AgNO3溶液,有浅黄色沉淀生成,说明该反应为取代反应。
不合理之处:挥发出的Br2会和蒸馏水反应,生成HBr,无法证明该反应为取代反应。
改进方法:在烧瓶和锥形瓶之间连接一个盛有CCl4的洗气瓶,吸收HBr气体中混有的Br2。
2.若利用该实验装置验证苯与液溴的反应为取代反应,是否存在不合理之处,如有不合理,请完善该实验装置。
重要实验 溴苯
纯净的硝基苯为无色液体,有苦杏仁气味,不溶于水,密度比水的大。
取代反应二:
在浓硫酸作用下,苯在50~60℃还能与浓硝酸发生硝化反应,生成硝基苯。
+HNO3(浓)
+H2O
浓H2SO4
重要实验 硝基苯
实验装置
实验步骤
①配制混合酸:先将1.5 mL浓硝酸注入大试管中,再慢慢注入2 mL浓硫酸,并及时摇匀和冷却;
②向冷却后的混合酸中逐滴加入1 mL苯,充分振荡,混合均匀;
③将大试管放在50~60 ℃的水浴中加热。
重要实验 硝基苯
生成物为淡黄色、有苦杏仁味的油状液体,难溶于水,并处于下层。
实验现象:
浓硫酸
浓硝酸
苯
50~60℃水浴加热
受热均匀;容易控制温度!
将浓硫酸慢慢加入到浓硝酸中,并不断振荡降温,冷却到50 ℃以下再逐滴滴入苯,边滴边振荡。
你知道水浴加热有哪些优点吗?
指出药品的加入的顺序及注意事项!
催化剂吸水剂
冷凝回流,减少反应物的挥发。
取代反应三:
(3)磺化反应:苯与浓硫酸在70~80℃可以发生取代反应。
+HO—SO3H + H2O
苯磺酸
苯磺酸易溶于水,是一种强酸,可以看作硫酸分子里的一个羟基被苯环取代的产物。磺化反应可用于制备合成洗涤剂。
加成反应:
在以Pt、Ni等为催化剂并加热的条件下,
苯能与氢气发生加成反应,生成环已烷。
苯的化学性质
物理性质 化学性质 化学方程式
无色有特殊气味的液体,难溶于水,ρ苯<ρ水,易挥发,有毒,常用作有机溶剂。
易取代
难氧化
难加成
反应较容易,苯的主要性质。与液溴、浓硝酸等在一定条件下发生取代反应。
可与氢气发生加成反应,用于工业制环己烷。
①易燃,火焰明亮,伴有浓烟。
②不能被KMnO4、H2O2等强氧化剂氧化。
苯的性质总结
芳香烃的来源
炼焦炉
煤的干馏
煤
煤焦油
芳香烃
干馏
分馏
焦炭
焦炉气
(苯、甲苯、萘、蒽、菲等)
苯的同系物
你知道芳香族化合物、芳香烃、苯的同系物之间的关系吗?请试着对下列物质分类!
芳香族化合物: ;
芳香烃: ;
苯的同系物: 。
⑴ ⑶ ⑸ ⑻ ⑼ ⑽ ⑿ ⒀
⑼ ⑿
全部都是
苯的同系物通式
CnH2n-6(n≥7)
1.组成和结构特点
苯环使甲基上的H变活泼,甲基易被高锰酸钾氧化成-COOH。自身被还原成二价锰离子。甲苯能便酸性高锰酸钾溶液褪色。
苯的同系物
概念:只有一个苯环,可以看成是由苯环上的H被烷基代替而得到的。
苯的同系物——甲苯
苯
(1)习惯命名法:
①一元烷基苯以苯为母体,烷基为取代基,如:
②二元烷基苯也是以苯为母体,分别有3种同分异构,可用邻、间、对位命名,如:
甲苯 乙苯
邻二甲苯 间二甲苯 对二甲苯
苯的同系物的命名
(2)系统命名法:
将苯环上的6个碳原子编号,以某个最简单的取代基(如甲基)所在的碳原子为1号,并按使 支链的位次和最小的原则给其他取代基编号,最后根据有机物名称的基本格式写出名称。如:
2.苯的同系物的命名
1,2–二甲苯 1,3–二甲苯
邻二甲苯 间二甲苯 对二甲苯
1,4–二甲基–2–乙基苯
1,4–二甲苯
1.一般具有类似苯的气味,无色液体,不溶于水,易溶于有机溶剂,密度比水的小。
2.随碳原子数增多,熔沸点依次升高。
3.同分异构体中,分子间作用力越弱,沸点越低。
如沸点:
144℃ 139℃ 138℃
> >
苯的同系物的物理性质
氧化反应
条件:与苯环直接相连的碳原子上有氢!
取代反应
1、硝化反应
结论:苯基(邻、对位活化)和烷基互相活化!
2,4,6—三硝基甲苯
甲苯能使酸性KMnO4溶液褪色,
这是由于甲苯上的甲基被酸性KMnO4氧化的结果。
苯的同系物的化学性质
取代反应
1、硝化反应
结论:苯基(邻、对位活化)和烷基互相活化!
2,4,6—三硝基甲苯
苯的同系物的化学性质
加成反应
2、卤代反应—与卤素单质
+ Cl2
+ HCl
光照
FeCl3
+ Cl2
+ HCl
结论:苯环和侧链都能发生取代反应,但条件不同。
反应条件苛刻,反应困难!
作业
总结苯与苯的同系物在分子组成、结构和性质上的异同
归纳总结
不同点 取代反应 易发生取代反应,主要得到一元取代产物 更容易发生取代反应,常得到多元取代产物
氧化反应 难被氧化,不能使酸性KMnO4溶液褪色 易被氧化剂氧化,能使酸性KMnO4溶液褪色
差异原因 苯的同系物分子中,苯环与侧链相互影响。苯环影响侧链,使侧链烃基活化而易被氧化;侧链烃基影响苯环,使苯环上烃基邻、对位的氢原子活化而被取代
