苏教版高中化学5选择性必修3有机化学基础专题5药物合成的重要原料卤代烃、胺、酰胺5.1卤代烃的性质及应用课件
文档属性
| 名称 | 苏教版高中化学5选择性必修3有机化学基础专题5药物合成的重要原料卤代烃、胺、酰胺5.1卤代烃的性质及应用课件 |

|
|
| 格式 | ppt | ||
| 文件大小 | 4.0MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-23 00:00:00 | ||
图片预览






文档简介
(共26张PPT)
卤代烃的性质及应用
(第1课时)卤代烃的化学性质
专题5 药物合成的重要原料 卤代烃、胺、酰胺
第一单元 卤代烃
课前回顾
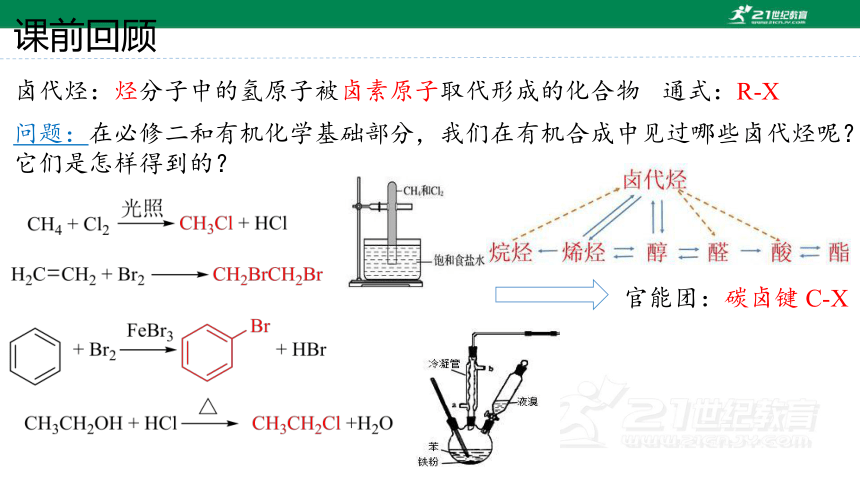
卤代烃:烃分子中的氢原子被卤素原子取代形成的化合物
通式:R-X
问题:在必修二和有机化学基础部分,我们在有机合成中见过哪些卤代烃呢?它们是怎样得到的?
官能团:碳卤键 C-X
情境引入
早在1930年,杜邦公司发明了氟利昂(一种含F、Cl的卤代烃)
生活中常见的塑料袋的主要成分是聚乙烯、聚氯乙烯
臭氧层遭到破坏,危害人体健康
难降解塑料造成“白色污染”
情境引入
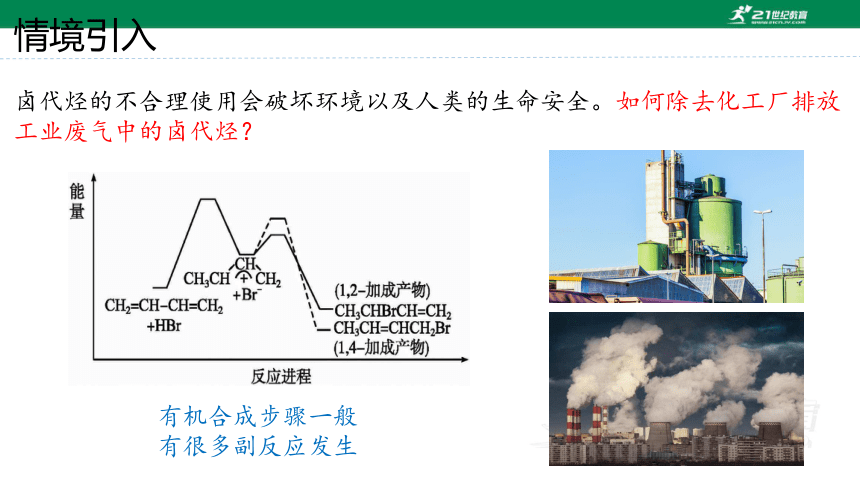
卤代烃的不合理使用会破坏环境以及人类的生命安全。如何除去化工厂排放工业废气中的卤代烃?
有机合成步骤一般有很多副反应发生
物质的检验方法
问题:对于铵根离子、卤素离子、硫酸根离子我们是怎么样检验的呢?
稀硝酸酸化的AgNO3溶液
产生白色沉淀
产生淡黄色沉淀
产生黄色沉淀
试液
稀盐酸
无沉淀
氯化钡溶液
白色沉淀
交流讨论:对于卤代烃中卤素的检验,我们是否可以使用上述检验卤离子的方法直接检验呢?
?
卤代烃的检验方法
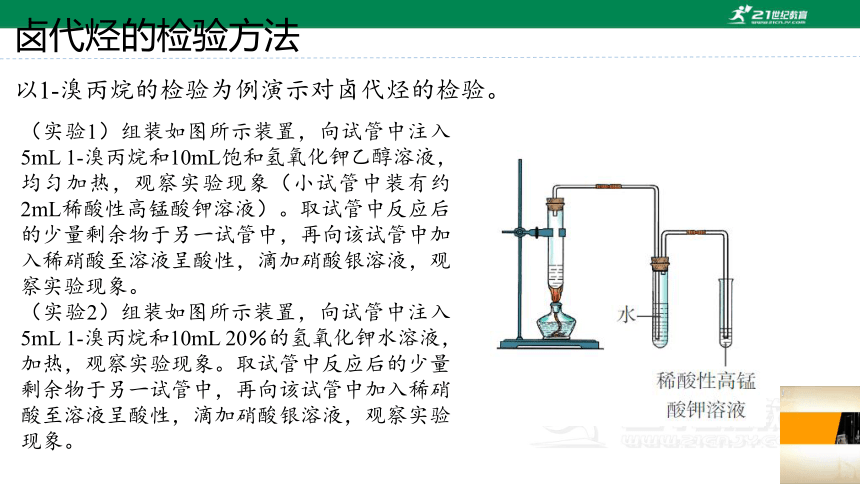
以1-溴丙烷的检验为例演示对卤代烃的检验。
(实验1)组装如图所示装置,向试管中注入5mL 1-溴丙烷和10mL饱和氢氧化钾乙醇溶液,均匀加热,观察实验现象(小试管中装有约2mL稀酸性高锰酸钾溶液)。取试管中反应后的少量剩余物于另一试管中,再向该试管中加入稀硝酸至溶液呈酸性,滴加硝酸银溶液,观察实验现象。
(实验2)组装如图所示装置,向试管中注入5mL 1-溴丙烷和10mL 20%的氢氧化钾水溶液,加热,观察实验现象。取试管中反应后的少量剩余物于另一试管中,再向该试管中加入稀硝酸至溶液呈酸性,滴加硝酸银溶液,观察实验现象。
卤代烃的检验方法
实验编号 反应物 实验现象 结论 生成物
实验一 氢氧化钾、1-溴丙烷 酸性高锰酸钾溶液褪色了;试管中产生了淡黄色沉淀
实验二 氢氧化钾、1-溴丙烷
酸性高锰酸钾溶液未褪色;试管中产生了淡黄色沉淀
生成了含有不饱和键的烃类化合物;实验产物含有Br-
实验产物含有Br-
1-溴丙烷和氢氧化钾在乙醇和加热的条件下生成了丙烯和溴化钾
1-溴丙烷和氢氧化钾在水和加热的条件下生成了1-丙醇和溴化钾
除去乙醇
卤代烃的检验方法
卤代烃的消去反应
卤代烃的取代反应
练一练:部分不饱和卤代烃也可在一定条件下发生加聚反应。请同学们尝试书写在一定条件下生成聚四氟乙烯的化学方程式。
卤代烃的检验方法
卤代烃发生取代反应、消去反应本质是发生碳卤键的断裂
交流讨论:为何C-X易发生断裂?
有机合成中引入碳碳双键
问题:在有机合成中,我们可以利用卤代烃的消去反应形成不饱和键,这样可以在有机合成中引入碳碳双键,而在之前的学习过程中,我们还学习过哪些在有机物中引入碳碳双键的方法呢?
迁移应用
【练习1】以环己烷为主要原料合成1,2-环己二醇。
迁移应用
【练习2】情境再现:设计实验方案检验工业废气(只含有机化合物)中是否含有卤代有机化合物。
方案一:将废气导入氢氧化钠的醇溶液中加热,将所得产物加入稀硝酸中和氢氧化钠,加入稀硝酸酸化的硝酸银溶液,观察沉淀的产生和颜色。
方案二:将废气导入氢氧化钠的水溶液中加热,将所得产物加入稀硝酸中和氢氧化钠,加入稀硝酸酸化的硝酸银溶液,观察沉淀的产生和颜色。
思考:两个方案哪一个可行性更高?
课堂小结
卤代烃的主要化学性质
卤代烃的取代反应
卤代烃的消去反应
卤代烃的加聚反应
卤代烃的应用
有机合成
卤代烃的鉴别
聚合材料的生产
课后作业
1. 阅读课本及相关资料,了解卤代烃的主要物理性质。
2.通过查阅资料,了解卤代烃在有机合成、药物生产等领域的其他具体应用。
卤代烃的性质及应用
(第2课时)卤代烃的物理性质及应用
专题5 药物合成的重要原料 卤代烃、胺、酰胺
第一单元 卤代烃
授课人:××
学校:××
日期:*
课前回顾
卤代烃:烃分子中的氢原子被卤素原子取代形成的化合物
通式:R-X
官能团:碳卤键 C-X
课前回顾
卤代烃的消去反应
卤代烃的取代反应
部分不饱和卤代烃也可在一定条件下发生加聚反应。
卤代烃的多样性
我们按照烃基结构的不同,可以将卤代烃分为卤代烷烃、卤代烯烃等,按照卤素原子的不同,可以将卤代烃分为氟代烃、氯代烃等,按照取代卤原子的多少,可以分为一卤代烃和多卤代烃等。
卤代烃:烃分子中的氢原子被卤素原子取代形成的化合物
通式:R-X
新课导入
思考:根据所学知识可以总结出卤代烃的哪些物理性质呢?结合我们对烃及其衍生物的学习,我们一般从哪些方面研究有机物的物理性质呢?
有机物的颜色、气味、状态、密度、溶解性、沸点等方面研究。
思考:常温下我们的卤代烃是什么状态?可以结合甲烷的卤代思考一下。
气体
氯仿
卤代烃的物理性质
颜色:有的卤代烃有颜色,大多数一卤代烷是无色。
状态:常温下,大多数的卤代烃为液体,除了一氯甲烷、氯乙烷、氯乙烯等少数为气体外,其余多为液体或固体。
气味:大多数的卤代烃都具有特殊气味。
密度:卤代烃的同系物的密度随碳原子数的增加而降低,除一氟代烃和一氯代烃的密度比水小,而溴代烃、碘代烃及多卤代烃的密度比水大。
溶解性:卤代烃难溶于水,但能溶于大多数有机溶剂,某些卤代烃本身就是很好的有机溶剂。
沸点:卤代烃的沸点随碳原子和卤素原子数目的增加而升高,且较相应的烷烃高。同一烃基的不同卤代烃的沸点随卤素原子的相对原子质量的增大而增大。
课堂练习
从密度、导电性等角度分析四氯化碳为什么可用作灭火剂?(提示:回顾燃烧的条件)
卤代烃的具体应用
卤代烃的发生取代反应、消去反应,可以用于有机合成中引入不饱和碳碳键和醇羟基。通过卤代烃与镁形成的烃基卤化镁(RMgX,称为格氏试剂)与其他物质反应可以实现碳链的增长。
RMgX+CH2CH2O(环氧乙烷)→R CH2CH2O MgX
不饱和卤代烃可以制备聚合物。聚氯乙烯是塑料的主要成分。我们在日常生活中常使用的塑料袋、塑料管道、电线绝缘外壳、医用输液管的成分中都含聚氯乙烯。
卤代烃的具体应用
氯乙烷常用作局部麻醉剂。因其沸点低,从加压容器中喷在皮肤表面时会迅速汽化,吸收大量的热,使皮肤迅速冷却导致该部位的神经末梢处于麻醉状态。由氯乙烷制成的喷雾剂被广泛应用于运动场所紧急处理运动员的伤痛。
卤代烃在农药、杀虫剂生产中的使用更为普遍。研究表明,含有氟原子的药物可增加分子在细胞膜上的脂溶性,提高药物的吸收和传递速率,具有用量少、低成本、低毒性、低残留、对环境友好等优点,对新药研制有重要的指导意义。据报道,近年来研制的农药新药中,含氟的新药就高达50%。
卤代烃的合理使用
DDT是在1939年由瑞士科学家穆勒合成的第一种有机农药,价格低廉、工艺简单,具有优异的光谱杀虫作用,因此穆勒获得1948年的诺贝尔奖。后来人们发现,DDT在自然界难降解,可通过食物链在动物体内形成累积性残留,给人体健康和生态环境造成不利影响,因此DDT被逐渐禁用,有人甚至认为这是一个发错的诺贝尔奖。
习近平总书记指出,大自然是人类赖以生存发展的基本条件。尊重自然、顺应自然、保护自然,是全面建设社会主义现代化国家的内在要求。必须牢固树立和践行绿水青山就是金山银山的理念,站在人与自然和谐共生的高度谋划发展。
课堂小结
卤代烃在有机合成、医学领域、材料生产等方面的应用
卤代烃的物理性质,(气味、颜色、状态、密度、沸点、溶解性等)
RMgX+CH2CH2O(环氧乙烷)→R CH2CH2O MgX
了解化学家
格氏试剂的主要作用是延长碳链,而格利雅获得成功也经历了一定的坎坷。
格利雅从来就没有认真读过书,离家出走来到里昂,本想入里昂大学就读,没有知识基础的他只好一切从头开始。路易·波尔韦教授很同情他的遭遇,花了两年的时间帮助他补习功课,经过辅导和他自己的刻苦努力,格利雅进入了里昂大学插班读书。他深知得到读书的机会来之不易,眼前只有一条路就是努力,经过他的刻苦求学,格利雅发现了格氏试剂而被授予博士学位,因此,获得了1912年的诺贝尔化学奖。
离家出走8年之后,格利雅实现了出走时留下的诺言。离开家乡时,他是一个人人讨厌的纨绔子弟,而8年之后他已成为杰出的化学家了。
卤代烃的性质及应用
(第1课时)卤代烃的化学性质
专题5 药物合成的重要原料 卤代烃、胺、酰胺
第一单元 卤代烃
课前回顾
卤代烃:烃分子中的氢原子被卤素原子取代形成的化合物
通式:R-X
问题:在必修二和有机化学基础部分,我们在有机合成中见过哪些卤代烃呢?它们是怎样得到的?
官能团:碳卤键 C-X
情境引入
早在1930年,杜邦公司发明了氟利昂(一种含F、Cl的卤代烃)
生活中常见的塑料袋的主要成分是聚乙烯、聚氯乙烯
臭氧层遭到破坏,危害人体健康
难降解塑料造成“白色污染”
情境引入
卤代烃的不合理使用会破坏环境以及人类的生命安全。如何除去化工厂排放工业废气中的卤代烃?
有机合成步骤一般有很多副反应发生
物质的检验方法
问题:对于铵根离子、卤素离子、硫酸根离子我们是怎么样检验的呢?
稀硝酸酸化的AgNO3溶液
产生白色沉淀
产生淡黄色沉淀
产生黄色沉淀
试液
稀盐酸
无沉淀
氯化钡溶液
白色沉淀
交流讨论:对于卤代烃中卤素的检验,我们是否可以使用上述检验卤离子的方法直接检验呢?
?
卤代烃的检验方法
以1-溴丙烷的检验为例演示对卤代烃的检验。
(实验1)组装如图所示装置,向试管中注入5mL 1-溴丙烷和10mL饱和氢氧化钾乙醇溶液,均匀加热,观察实验现象(小试管中装有约2mL稀酸性高锰酸钾溶液)。取试管中反应后的少量剩余物于另一试管中,再向该试管中加入稀硝酸至溶液呈酸性,滴加硝酸银溶液,观察实验现象。
(实验2)组装如图所示装置,向试管中注入5mL 1-溴丙烷和10mL 20%的氢氧化钾水溶液,加热,观察实验现象。取试管中反应后的少量剩余物于另一试管中,再向该试管中加入稀硝酸至溶液呈酸性,滴加硝酸银溶液,观察实验现象。
卤代烃的检验方法
实验编号 反应物 实验现象 结论 生成物
实验一 氢氧化钾、1-溴丙烷 酸性高锰酸钾溶液褪色了;试管中产生了淡黄色沉淀
实验二 氢氧化钾、1-溴丙烷
酸性高锰酸钾溶液未褪色;试管中产生了淡黄色沉淀
生成了含有不饱和键的烃类化合物;实验产物含有Br-
实验产物含有Br-
1-溴丙烷和氢氧化钾在乙醇和加热的条件下生成了丙烯和溴化钾
1-溴丙烷和氢氧化钾在水和加热的条件下生成了1-丙醇和溴化钾
除去乙醇
卤代烃的检验方法
卤代烃的消去反应
卤代烃的取代反应
练一练:部分不饱和卤代烃也可在一定条件下发生加聚反应。请同学们尝试书写在一定条件下生成聚四氟乙烯的化学方程式。
卤代烃的检验方法
卤代烃发生取代反应、消去反应本质是发生碳卤键的断裂
交流讨论:为何C-X易发生断裂?
有机合成中引入碳碳双键
问题:在有机合成中,我们可以利用卤代烃的消去反应形成不饱和键,这样可以在有机合成中引入碳碳双键,而在之前的学习过程中,我们还学习过哪些在有机物中引入碳碳双键的方法呢?
迁移应用
【练习1】以环己烷为主要原料合成1,2-环己二醇。
迁移应用
【练习2】情境再现:设计实验方案检验工业废气(只含有机化合物)中是否含有卤代有机化合物。
方案一:将废气导入氢氧化钠的醇溶液中加热,将所得产物加入稀硝酸中和氢氧化钠,加入稀硝酸酸化的硝酸银溶液,观察沉淀的产生和颜色。
方案二:将废气导入氢氧化钠的水溶液中加热,将所得产物加入稀硝酸中和氢氧化钠,加入稀硝酸酸化的硝酸银溶液,观察沉淀的产生和颜色。
思考:两个方案哪一个可行性更高?
课堂小结
卤代烃的主要化学性质
卤代烃的取代反应
卤代烃的消去反应
卤代烃的加聚反应
卤代烃的应用
有机合成
卤代烃的鉴别
聚合材料的生产
课后作业
1. 阅读课本及相关资料,了解卤代烃的主要物理性质。
2.通过查阅资料,了解卤代烃在有机合成、药物生产等领域的其他具体应用。
卤代烃的性质及应用
(第2课时)卤代烃的物理性质及应用
专题5 药物合成的重要原料 卤代烃、胺、酰胺
第一单元 卤代烃
授课人:××
学校:××
日期:*
课前回顾
卤代烃:烃分子中的氢原子被卤素原子取代形成的化合物
通式:R-X
官能团:碳卤键 C-X
课前回顾
卤代烃的消去反应
卤代烃的取代反应
部分不饱和卤代烃也可在一定条件下发生加聚反应。
卤代烃的多样性
我们按照烃基结构的不同,可以将卤代烃分为卤代烷烃、卤代烯烃等,按照卤素原子的不同,可以将卤代烃分为氟代烃、氯代烃等,按照取代卤原子的多少,可以分为一卤代烃和多卤代烃等。
卤代烃:烃分子中的氢原子被卤素原子取代形成的化合物
通式:R-X
新课导入
思考:根据所学知识可以总结出卤代烃的哪些物理性质呢?结合我们对烃及其衍生物的学习,我们一般从哪些方面研究有机物的物理性质呢?
有机物的颜色、气味、状态、密度、溶解性、沸点等方面研究。
思考:常温下我们的卤代烃是什么状态?可以结合甲烷的卤代思考一下。
气体
氯仿
卤代烃的物理性质
颜色:有的卤代烃有颜色,大多数一卤代烷是无色。
状态:常温下,大多数的卤代烃为液体,除了一氯甲烷、氯乙烷、氯乙烯等少数为气体外,其余多为液体或固体。
气味:大多数的卤代烃都具有特殊气味。
密度:卤代烃的同系物的密度随碳原子数的增加而降低,除一氟代烃和一氯代烃的密度比水小,而溴代烃、碘代烃及多卤代烃的密度比水大。
溶解性:卤代烃难溶于水,但能溶于大多数有机溶剂,某些卤代烃本身就是很好的有机溶剂。
沸点:卤代烃的沸点随碳原子和卤素原子数目的增加而升高,且较相应的烷烃高。同一烃基的不同卤代烃的沸点随卤素原子的相对原子质量的增大而增大。
课堂练习
从密度、导电性等角度分析四氯化碳为什么可用作灭火剂?(提示:回顾燃烧的条件)
卤代烃的具体应用
卤代烃的发生取代反应、消去反应,可以用于有机合成中引入不饱和碳碳键和醇羟基。通过卤代烃与镁形成的烃基卤化镁(RMgX,称为格氏试剂)与其他物质反应可以实现碳链的增长。
RMgX+CH2CH2O(环氧乙烷)→R CH2CH2O MgX
不饱和卤代烃可以制备聚合物。聚氯乙烯是塑料的主要成分。我们在日常生活中常使用的塑料袋、塑料管道、电线绝缘外壳、医用输液管的成分中都含聚氯乙烯。
卤代烃的具体应用
氯乙烷常用作局部麻醉剂。因其沸点低,从加压容器中喷在皮肤表面时会迅速汽化,吸收大量的热,使皮肤迅速冷却导致该部位的神经末梢处于麻醉状态。由氯乙烷制成的喷雾剂被广泛应用于运动场所紧急处理运动员的伤痛。
卤代烃在农药、杀虫剂生产中的使用更为普遍。研究表明,含有氟原子的药物可增加分子在细胞膜上的脂溶性,提高药物的吸收和传递速率,具有用量少、低成本、低毒性、低残留、对环境友好等优点,对新药研制有重要的指导意义。据报道,近年来研制的农药新药中,含氟的新药就高达50%。
卤代烃的合理使用
DDT是在1939年由瑞士科学家穆勒合成的第一种有机农药,价格低廉、工艺简单,具有优异的光谱杀虫作用,因此穆勒获得1948年的诺贝尔奖。后来人们发现,DDT在自然界难降解,可通过食物链在动物体内形成累积性残留,给人体健康和生态环境造成不利影响,因此DDT被逐渐禁用,有人甚至认为这是一个发错的诺贝尔奖。
习近平总书记指出,大自然是人类赖以生存发展的基本条件。尊重自然、顺应自然、保护自然,是全面建设社会主义现代化国家的内在要求。必须牢固树立和践行绿水青山就是金山银山的理念,站在人与自然和谐共生的高度谋划发展。
课堂小结
卤代烃在有机合成、医学领域、材料生产等方面的应用
卤代烃的物理性质,(气味、颜色、状态、密度、沸点、溶解性等)
RMgX+CH2CH2O(环氧乙烷)→R CH2CH2O MgX
了解化学家
格氏试剂的主要作用是延长碳链,而格利雅获得成功也经历了一定的坎坷。
格利雅从来就没有认真读过书,离家出走来到里昂,本想入里昂大学就读,没有知识基础的他只好一切从头开始。路易·波尔韦教授很同情他的遭遇,花了两年的时间帮助他补习功课,经过辅导和他自己的刻苦努力,格利雅进入了里昂大学插班读书。他深知得到读书的机会来之不易,眼前只有一条路就是努力,经过他的刻苦求学,格利雅发现了格氏试剂而被授予博士学位,因此,获得了1912年的诺贝尔化学奖。
离家出走8年之后,格利雅实现了出走时留下的诺言。离开家乡时,他是一个人人讨厌的纨绔子弟,而8年之后他已成为杰出的化学家了。
