苏教版高中化学必修第一册专题1物质的分类及计量1.2物质的化学计量课件(共14张PPT)
文档属性
| 名称 | 苏教版高中化学必修第一册专题1物质的分类及计量1.2物质的化学计量课件(共14张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 3.4MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-23 09:44:48 | ||
图片预览





文档简介
(共14张PPT)
物质的量
较大的物体
以个体计量
以集合体计量
较小的物体
新的量词
包、袋、斤、打……
1粒米、1颗盐是最小的物质吗?
分子、原子、质子、中子、电子等
物质的量
把微小的物质扩大倍数形成一定数目的集合体
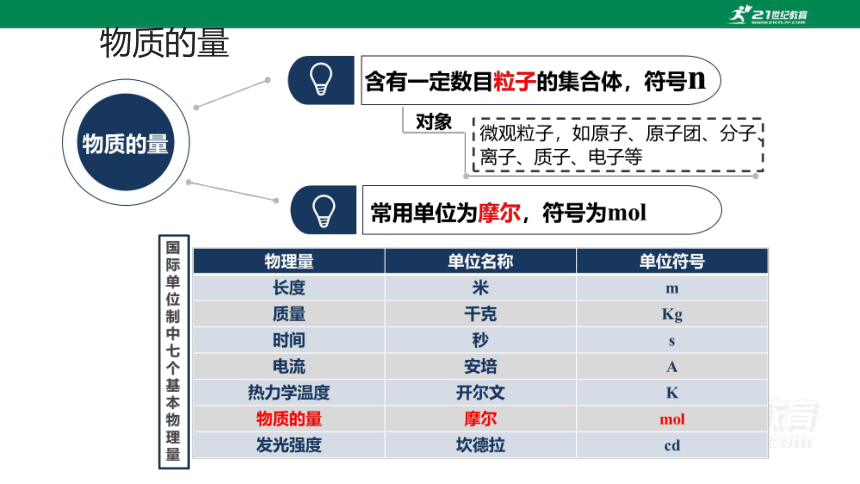
物质的量
物质的量
判断正误,并说明理由。
① 1 mol 氢
② 1mol CO2
③ 1mol大米
错误。没有指出是分子、原子或离子
正确。
错误。大米不是微观粒子
物质的量
使用物质的量注意事项:
① 物质的量这四个字是一个整体,是一个专用名词,不得简化或增添任何字。
③ 物质的量计量的是粒子的集合体,不是单个粒子。
② 物质的量只适用于微观粒子,使用摩作单位时,所指粒子必须指明粒子的种类,如原子、分子、离子等,且粒子的种类一般都要用化学符号表示。
物质的量
1打
1 mol
12个
同0.012千克12C中所含的碳原子的数目相同
1 mol 任何粒子的集合体都含有约6.02×1023 个粒子
一个碳原子的质量: 1.99×10-23克,12克/ 1.99×10-23克≈6.02×1023
物质的量
0.012 kg12C中所含的原子数称为阿伏加德罗常数,符号为NA, NA≈ 6.02×1023 mol-1 。
1 mol O2中约含6.02×1023个氧分子
1 mol Cu中约含6.02×1023个铜原子
1 mol H2SO4中约含6.02×1023个硫酸分子
1 mol NaOH中约含6.02×1023个Na+ 和 6.02×1023个OH-
n mol某种微粒集合体中所含微粒数约为 n×6.02×1023
物质的量
物质的量
1
2.408×1023个H2的物质的量是 。
2
3.01×1023个NH3中含 mol 氨分子, mol 氢原子。
3
1 mol 氦气中有 个 氦原子。
4
a mol Na2CO3中含有 b mol个 氧原子,则阿伏伽德罗常数可以表示为 。
5
含有相同原子总数的NH3和CH4的分子数之比为 ,其中H原子的物质的量之比为 。
0.4 mol
5:4
15:16
0.5
1.5
NA
摩尔质量
假如每颗米的质量都一样,现知道每10000颗米的质量都为5公斤.那么要取10000颗米时,采用数还是用称的方法?
O Al H2 H2O
一个分子或原子的质量 2.657×10-23g 4.485×10-23g 3.294×10-24g 2.990×10-23g
物质的量 1 mol 1 mol 1 mol 1 mol
相对分子或原子质量 16 27 2 18
1 mol物质
的质量 16g 27g 2g 18g
摩尔质量
摩尔质量:单位物质的量(即1mol)的物质所具有的质量叫做该 物质的摩尔质量。符号:M,单位:g · mol-1
粒子符号 相对分子或原子质量 1个分子或原子的质量 1摩尔物质的质量
H2O 2.990×10-23g
Al 4.485×10-23g
C 1.993×10-23g
Fe 9.032×10-23g
H2SO4 1.628×10-22g
18
27
12
56
98
18g
27g
12g
56g
98g
1 mol 任何粒子或物质的质量以g为单位时,其数值都与该粒子的相对原子质量或相对分子质量相等
物质的量
摩尔质量
1、24.5gH2SO4的物质的量是多少?
2、 1.50molNa2CO3的质量是多少?
3、相对原子质量:Fe:56 O:16 H:1
铁的摩尔质量是 ,即1molFe___g; 2molFe______g;
一块质量是28g的铁,这块铁中有 mol铁原子。
水的式量是___,摩尔质量是___________;
2mol的水是 克;90g水是_____mol
n(H2SO4)= ────── = ──────
m(H2SO4)
M(H2SO4)
24.5g
98g.mol-1
=0.25mol
m(Na2CO3)= =1.5mol×106g.mol-1=159g
n(Na2CO3)×M(Na2CO3)
56g/mol
56
112
36
0.5
18g/mol
5
18
物质的量
较大的物体
以个体计量
以集合体计量
较小的物体
新的量词
包、袋、斤、打……
1粒米、1颗盐是最小的物质吗?
分子、原子、质子、中子、电子等
物质的量
把微小的物质扩大倍数形成一定数目的集合体
物质的量
物质的量
判断正误,并说明理由。
① 1 mol 氢
② 1mol CO2
③ 1mol大米
错误。没有指出是分子、原子或离子
正确。
错误。大米不是微观粒子
物质的量
使用物质的量注意事项:
① 物质的量这四个字是一个整体,是一个专用名词,不得简化或增添任何字。
③ 物质的量计量的是粒子的集合体,不是单个粒子。
② 物质的量只适用于微观粒子,使用摩作单位时,所指粒子必须指明粒子的种类,如原子、分子、离子等,且粒子的种类一般都要用化学符号表示。
物质的量
1打
1 mol
12个
同0.012千克12C中所含的碳原子的数目相同
1 mol 任何粒子的集合体都含有约6.02×1023 个粒子
一个碳原子的质量: 1.99×10-23克,12克/ 1.99×10-23克≈6.02×1023
物质的量
0.012 kg12C中所含的原子数称为阿伏加德罗常数,符号为NA, NA≈ 6.02×1023 mol-1 。
1 mol O2中约含6.02×1023个氧分子
1 mol Cu中约含6.02×1023个铜原子
1 mol H2SO4中约含6.02×1023个硫酸分子
1 mol NaOH中约含6.02×1023个Na+ 和 6.02×1023个OH-
n mol某种微粒集合体中所含微粒数约为 n×6.02×1023
物质的量
物质的量
1
2.408×1023个H2的物质的量是 。
2
3.01×1023个NH3中含 mol 氨分子, mol 氢原子。
3
1 mol 氦气中有 个 氦原子。
4
a mol Na2CO3中含有 b mol个 氧原子,则阿伏伽德罗常数可以表示为 。
5
含有相同原子总数的NH3和CH4的分子数之比为 ,其中H原子的物质的量之比为 。
0.4 mol
5:4
15:16
0.5
1.5
NA
摩尔质量
假如每颗米的质量都一样,现知道每10000颗米的质量都为5公斤.那么要取10000颗米时,采用数还是用称的方法?
O Al H2 H2O
一个分子或原子的质量 2.657×10-23g 4.485×10-23g 3.294×10-24g 2.990×10-23g
物质的量 1 mol 1 mol 1 mol 1 mol
相对分子或原子质量 16 27 2 18
1 mol物质
的质量 16g 27g 2g 18g
摩尔质量
摩尔质量:单位物质的量(即1mol)的物质所具有的质量叫做该 物质的摩尔质量。符号:M,单位:g · mol-1
粒子符号 相对分子或原子质量 1个分子或原子的质量 1摩尔物质的质量
H2O 2.990×10-23g
Al 4.485×10-23g
C 1.993×10-23g
Fe 9.032×10-23g
H2SO4 1.628×10-22g
18
27
12
56
98
18g
27g
12g
56g
98g
1 mol 任何粒子或物质的质量以g为单位时,其数值都与该粒子的相对原子质量或相对分子质量相等
物质的量
摩尔质量
1、24.5gH2SO4的物质的量是多少?
2、 1.50molNa2CO3的质量是多少?
3、相对原子质量:Fe:56 O:16 H:1
铁的摩尔质量是 ,即1molFe___g; 2molFe______g;
一块质量是28g的铁,这块铁中有 mol铁原子。
水的式量是___,摩尔质量是___________;
2mol的水是 克;90g水是_____mol
n(H2SO4)= ────── = ──────
m(H2SO4)
M(H2SO4)
24.5g
98g.mol-1
=0.25mol
m(Na2CO3)= =1.5mol×106g.mol-1=159g
n(Na2CO3)×M(Na2CO3)
56g/mol
56
112
36
0.5
18g/mol
5
18
