苏科版 初中物理 八年级下册 第十章 从粒子到宇宙 10.3 探究更小的微粒 课件(25页)
文档属性
| 名称 | 苏科版 初中物理 八年级下册 第十章 从粒子到宇宙 10.3 探究更小的微粒 课件(25页) |

|
|
| 格式 | pptx | ||
| 文件大小 | 8.1MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 苏科版 | ||
| 科目 | 物理 | ||
| 更新时间 | 2025-04-24 00:00:00 | ||
图片预览






文档简介
(共25张PPT)
第十章 从粒子到宇宙
第3节 探索更小的微粒
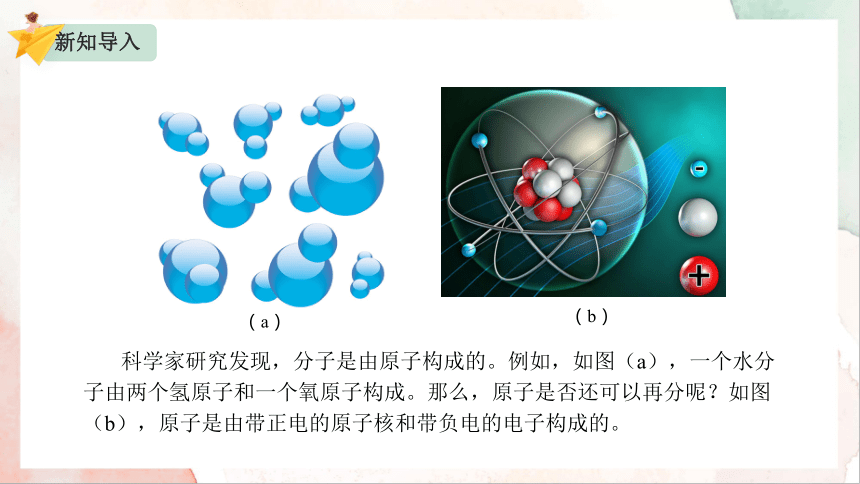
科学家研究发现,分子是由原子构成的。例如,如图(a),一个水分子由两个氢原子和一个氧原子构成。那么,原子是否还可以再分呢?如图(b),原子是由带正电的原子核和带负电的电子构成的。
(a)
(b)
新知导入
1.知道分子是由原子构成的。
2.知道原子的核式结构模型。
3.知道摩擦起电的原因及其实质。
4.了解微观粒子的层次结构和尺度的数量级。
学习目标
1803年9月,道尔顿利用当时已掌握的一些分析数据,计算出了第一批原子量。1803年10月21日,在曼彻斯特的“文学和哲学学会”上,道尔顿第一次阐述了他关于原子论以及原子量计算的见解,其要点:
约翰·道尔顿
(1766—1844年),英国化学家、物理学家。原子理论的提出者。
1. 道尔顿的原子论模型
化学元素由不可分的微粒——原子构成,原子在一切化学变化中是不可再分的最小单位。同种元素的原子性质和质量都相同,不同元素原子的性质和质量各不相同,原子质量是元素基本特征之一。
学习目标
01 原子的核式结构模型
(1)汤姆孙发现电子
1897 年,英国物理学家汤姆孙(1856—1940)在研究阴极射线时发现了电子——人类发现的第一个比原子小的粒子。电子带负电,是原子的构成部分之一。它的发现打破了原子不可再分的传统观念,激发了人们探索原子内部结构的热情。
由于电子是带负电的,而原子又是中性的,因此物理学家推断出在原子中还存在带正电荷的其它物质。
汤姆孙
英国物理学家,电子的发现者。于1906年获得诺贝尔物理学奖。
2. 汤姆孙的原子模型
(2)汤姆孙的“葡萄干蛋糕模型”
1903年汤姆孙提出了一个原子结构模型,人们把它叫做“葡萄干蛋糕”模型。 翻译为“枣糕模型”或“西瓜模型”或“汤姆生模型”。汤姆孙模型认为:
此模型有一定意义,但不能解释后来的α 粒子散射实验,后来被卢瑟福的有核模型所取代。
正电荷均匀分布在整个原子球体中,带负电的电子散布在原子中,这些电子分布在对称的位置上。
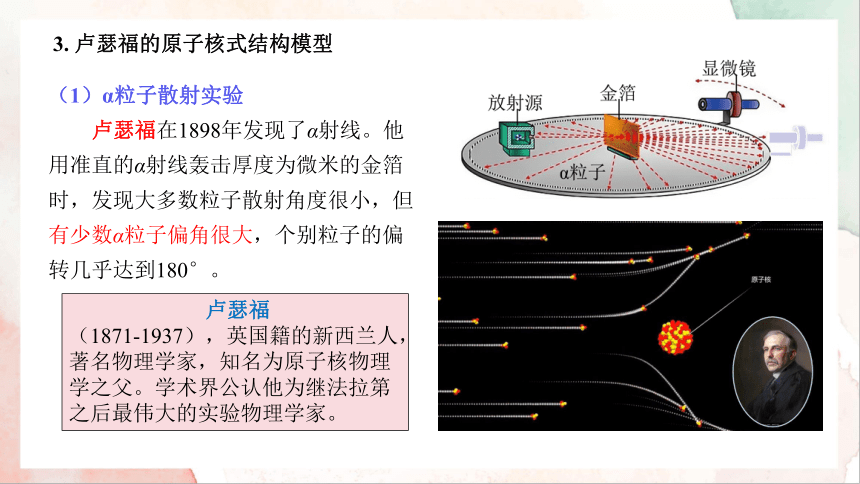
(1)α粒子散射实验
卢瑟福在1898年发现了α射线。他用准直的α射线轰击厚度为微米的金箔时,发现大多数粒子散射角度很小,但有少数α粒子偏角很大,个别粒子的偏转几乎达到180°。
3. 卢瑟福的原子核式结构模型
卢瑟福
(1871-1937),英国籍的新西兰人,著名物理学家,知名为原子核物理学之父。学术界公认他为继法拉第之后最伟大的实验物理学家。
(2) α 粒子散射实验结论
根据实验进行推导:当α粒子穿过原子时,电子对α粒子运动的影响很小,影响α粒子运动的主要是另一种带正电的“粒子”,即原子核。因为绝大多数的α粒子穿过原子时离核较远,受到的斥力很小,运动方向几乎没有改变,只有极少数α粒子可能与核十分接近,受到较大的斥力,才会发生大角度的偏转。
实验结论:
原子中绝大部分是空的;α 粒子前进时撞在一个体积很小而质量又比它大很多的微粒上(原子核)。
原子核
电子
原 子
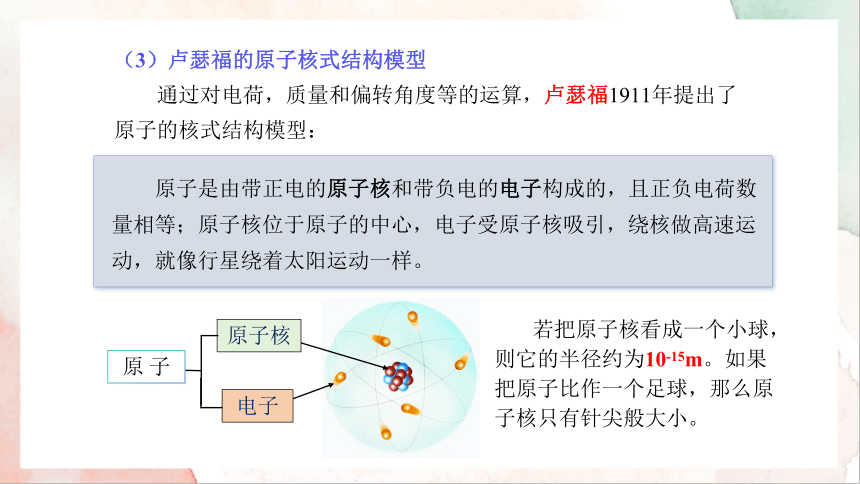
(3)卢瑟福的原子核式结构模型
通过对电荷,质量和偏转角度等的运算,卢瑟福1911年提出了原子的核式结构模型:
原子是由带正电的原子核和带负电的电子构成的,且正负电荷数量相等;原子核位于原子的中心,电子受原子核吸引,绕核做高速运动,就像行星绕着太阳运动一样。
若把原子核看成一个小球,则它的半径约为10-15m。如果把原子比作一个足球,那么原子核只有针尖般大小。
4. 摩擦起电的原因
(1)电子转移观点
由原子的核式结构模型进一步推理可知:因为原子核很小且质量很大,而电子运动的空间很大且质量很小,所以移动或改变原子核非常困难,移动或改变电子比较容易。人们认为静电现象都是由于电子转移而形成的,这种观点称为电子转移观点。 应用电子转移观点,可以解释原子带电、物体带电和摩擦起电现象。
(2)原子带电成为离子
一个中性的原子,如果失去一个或几个电子,就会使核内正电荷总数大于核外负电荷总数,则该原子将带正电,例如氢离子、钠离子。如果得到一个或几个电子,就会使核内正电荷总数小于核外负电荷总数,则该原子将带负电,例如氧离子、氯离子。
(3)物体带电成为带电体
一个中性的物体,如果失去若干电子,则该物体将带正电,如果得到若干电子,则该物体将带负电。
带正电荷
带负电荷
(4)摩擦起电的本质
束缚能力弱
的失去电子
束缚能力强
的得到电子
不同物质的原
子核束缚电子
的本领不同
摩擦起电不是创造了电荷,只是电荷从一个物体转移到另一个物体,使正、负电荷分开。
摩擦起电的本质:电子的转移。
摩擦时
1. 原子核
(1)质子的发现
质子
原子核
1919年,卢瑟福用速度是20000km/s的“子弹”—α 粒子去轰击氮、氟、钾等元素的原子核时,发现在原子核中还存在一种带正电的质量比电子大很多的微粒——质子。
质子所带正电荷的数量=电子所带负电荷的数量
原子核还能再分吗?随着历史的发展,人们对原子内部结构的研究逐步深入。
02 微观粒子探索进展
原子核
中子
詹姆斯·查德威克 (1891-1974),英国物理学家,于1935年获得诺贝尔物理学奖。
(2)中子的发现
中子的概念是由英国物理学家卢瑟福提出,中子的存在是1932年英国物理学家詹姆斯·查德威克用镭的α-射线轰击铍原子时的实验中证实的。科学家在实验中进一步发现中子的质量与质子相同、但是不带电。
原子核
中子
质子
(3)原子核的组成及带电情况
中子
质子
原子核是由质子和中子构成的,质子带正电,中子不带电。质子和中子统称为核子。
原 子
原子核
电 子
中子
质子
不带电
不带电
+
+
-
(4)原子的组成及带电情况
中子
质子
电子
原子的直径:约10-10米
原子核的直径:约10-15米
形象来说,就是地球和乒乓球的比例, 大约一比一千亿。 原子核极小,它的直径在10-16m~10-14m之间,体积只占原子体积的几千亿分之一,在这极小的原子核里却集中了99.95%以上原子的质量。
(5)原子与原子核的大小比较
默里·盖尔曼
(1929—2019),生于美国纽约的一个犹太家庭,物理学家,提出了质子和中子是由三个夸克组成的,并因此获得诺贝尔物理学奖。
(6)夸克
质子和中子还能再分吗?随着人们对原子内部结构的研究逐步深入,物理学家默里·盖尔曼提出了质子和中子还可以再分。
质子和中子是分别由三个夸克组成的。
电子<10-18m
核子由
夸克组成
质子
中子
粒子 分子 原子 原子核 核子
大小
原子核由质子
和中子组成
2. 总结:不同微观粒子的层次结构示意图
10-10~10-5m
10-10m
10-15~10-14m
10-15m
水分子(每个小球表示 一个原子)
1909 年,卢瑟福和他的学生利用一束高速运动的带正电的 α 粒子(由两个质子和两个中子构成)轰击很薄的金箔,获得了极有价值的实验现象和数据。1911 年,卢瑟福根据上述 α 粒子散射实验的结果提出了著名的原子核式结构模型。该实验也启发了人们用更高能量的粒子作为“炮弹”来探索微观世界的奥秘。
我们把能使带电粒子加速到很高能量的装置称为加速器。20 世 纪 30 年代,美国物理学家劳伦斯发明了回旋加速器。1988 年,我 国建成了北京正负电子对撞机。这是当时世界八大高能加速器之一, 也是我国继导弹、原子弹、氢弹、人造卫星、核潜艇之后的又一伟大科技成就。
生活 物理 社会 加速器及其应用
下图所示的高能同步辐射光源直线加速器由中国科学院高 能物理研究所承担建造。它在先进材料、航空航天、能源、环保以 及生物工程等方面发挥了重要作用。
加速器在生产、生活中同样有着非常重要的作用,如用于癌症的治疗、工业探伤、食品的防腐保鲜、复合材料的生产以及医疗用 品消毒等。
高能同步辐射光源直线加速器
探索更小的微粒
原子
模型
原子结构
①汤姆孙发现电子,提出原子的葡萄干蛋糕模型.
②卢瑟福通过α粒子实验,发现质子,提出核式结构模型。
③詹姆斯·查德威克通过实验证实中子的存在.
④默里·盖尔曼发现质子和中子分别由三个夸克组成的。
⑤原子的三种模型: 道尔顿模型;汤姆生模型;卢瑟福的核式结构模型.
原子核
电子(带负电)
质子(带正电)—夸克。
中子(不带电)—夸克。
课堂小结
1.刮大风时尘埃在空中飞舞,对于尘埃,下列说法正确的是( )
A.它和一个分子差不多大小
B.可以借助光学显微镜观察到尘埃分子
C.它的直径大约为10-10m
D.它是由许多分子构成的
D
课堂练习
2. 关于卢瑟福提出的原子结构的核式模型,下列说法中正确的是( )
A. 原子是由原子核和中子组成的
B. 原子是由原子核和核外电子组成的
C. 原子是由质子和中子组成的
D. 原子的质量几乎集中在原子核外
B
3.大千世界,从宏观到微观,从天体到原子,似乎都有那么多惊人的相同规律。如图所示,是太阳系模拟图,行星们在各自的固定轨道上围绕恒星太阳运转,这与 (选填“汤姆逊”或“卢瑟福”)建立的原子核式结构模型十分
相似,其中原子核相当于太阳,绕核运动的 就相当于行星。
卢瑟福
电子
第十章 从粒子到宇宙
第3节 探索更小的微粒
科学家研究发现,分子是由原子构成的。例如,如图(a),一个水分子由两个氢原子和一个氧原子构成。那么,原子是否还可以再分呢?如图(b),原子是由带正电的原子核和带负电的电子构成的。
(a)
(b)
新知导入
1.知道分子是由原子构成的。
2.知道原子的核式结构模型。
3.知道摩擦起电的原因及其实质。
4.了解微观粒子的层次结构和尺度的数量级。
学习目标
1803年9月,道尔顿利用当时已掌握的一些分析数据,计算出了第一批原子量。1803年10月21日,在曼彻斯特的“文学和哲学学会”上,道尔顿第一次阐述了他关于原子论以及原子量计算的见解,其要点:
约翰·道尔顿
(1766—1844年),英国化学家、物理学家。原子理论的提出者。
1. 道尔顿的原子论模型
化学元素由不可分的微粒——原子构成,原子在一切化学变化中是不可再分的最小单位。同种元素的原子性质和质量都相同,不同元素原子的性质和质量各不相同,原子质量是元素基本特征之一。
学习目标
01 原子的核式结构模型
(1)汤姆孙发现电子
1897 年,英国物理学家汤姆孙(1856—1940)在研究阴极射线时发现了电子——人类发现的第一个比原子小的粒子。电子带负电,是原子的构成部分之一。它的发现打破了原子不可再分的传统观念,激发了人们探索原子内部结构的热情。
由于电子是带负电的,而原子又是中性的,因此物理学家推断出在原子中还存在带正电荷的其它物质。
汤姆孙
英国物理学家,电子的发现者。于1906年获得诺贝尔物理学奖。
2. 汤姆孙的原子模型
(2)汤姆孙的“葡萄干蛋糕模型”
1903年汤姆孙提出了一个原子结构模型,人们把它叫做“葡萄干蛋糕”模型。 翻译为“枣糕模型”或“西瓜模型”或“汤姆生模型”。汤姆孙模型认为:
此模型有一定意义,但不能解释后来的α 粒子散射实验,后来被卢瑟福的有核模型所取代。
正电荷均匀分布在整个原子球体中,带负电的电子散布在原子中,这些电子分布在对称的位置上。
(1)α粒子散射实验
卢瑟福在1898年发现了α射线。他用准直的α射线轰击厚度为微米的金箔时,发现大多数粒子散射角度很小,但有少数α粒子偏角很大,个别粒子的偏转几乎达到180°。
3. 卢瑟福的原子核式结构模型
卢瑟福
(1871-1937),英国籍的新西兰人,著名物理学家,知名为原子核物理学之父。学术界公认他为继法拉第之后最伟大的实验物理学家。
(2) α 粒子散射实验结论
根据实验进行推导:当α粒子穿过原子时,电子对α粒子运动的影响很小,影响α粒子运动的主要是另一种带正电的“粒子”,即原子核。因为绝大多数的α粒子穿过原子时离核较远,受到的斥力很小,运动方向几乎没有改变,只有极少数α粒子可能与核十分接近,受到较大的斥力,才会发生大角度的偏转。
实验结论:
原子中绝大部分是空的;α 粒子前进时撞在一个体积很小而质量又比它大很多的微粒上(原子核)。
原子核
电子
原 子
(3)卢瑟福的原子核式结构模型
通过对电荷,质量和偏转角度等的运算,卢瑟福1911年提出了原子的核式结构模型:
原子是由带正电的原子核和带负电的电子构成的,且正负电荷数量相等;原子核位于原子的中心,电子受原子核吸引,绕核做高速运动,就像行星绕着太阳运动一样。
若把原子核看成一个小球,则它的半径约为10-15m。如果把原子比作一个足球,那么原子核只有针尖般大小。
4. 摩擦起电的原因
(1)电子转移观点
由原子的核式结构模型进一步推理可知:因为原子核很小且质量很大,而电子运动的空间很大且质量很小,所以移动或改变原子核非常困难,移动或改变电子比较容易。人们认为静电现象都是由于电子转移而形成的,这种观点称为电子转移观点。 应用电子转移观点,可以解释原子带电、物体带电和摩擦起电现象。
(2)原子带电成为离子
一个中性的原子,如果失去一个或几个电子,就会使核内正电荷总数大于核外负电荷总数,则该原子将带正电,例如氢离子、钠离子。如果得到一个或几个电子,就会使核内正电荷总数小于核外负电荷总数,则该原子将带负电,例如氧离子、氯离子。
(3)物体带电成为带电体
一个中性的物体,如果失去若干电子,则该物体将带正电,如果得到若干电子,则该物体将带负电。
带正电荷
带负电荷
(4)摩擦起电的本质
束缚能力弱
的失去电子
束缚能力强
的得到电子
不同物质的原
子核束缚电子
的本领不同
摩擦起电不是创造了电荷,只是电荷从一个物体转移到另一个物体,使正、负电荷分开。
摩擦起电的本质:电子的转移。
摩擦时
1. 原子核
(1)质子的发现
质子
原子核
1919年,卢瑟福用速度是20000km/s的“子弹”—α 粒子去轰击氮、氟、钾等元素的原子核时,发现在原子核中还存在一种带正电的质量比电子大很多的微粒——质子。
质子所带正电荷的数量=电子所带负电荷的数量
原子核还能再分吗?随着历史的发展,人们对原子内部结构的研究逐步深入。
02 微观粒子探索进展
原子核
中子
詹姆斯·查德威克 (1891-1974),英国物理学家,于1935年获得诺贝尔物理学奖。
(2)中子的发现
中子的概念是由英国物理学家卢瑟福提出,中子的存在是1932年英国物理学家詹姆斯·查德威克用镭的α-射线轰击铍原子时的实验中证实的。科学家在实验中进一步发现中子的质量与质子相同、但是不带电。
原子核
中子
质子
(3)原子核的组成及带电情况
中子
质子
原子核是由质子和中子构成的,质子带正电,中子不带电。质子和中子统称为核子。
原 子
原子核
电 子
中子
质子
不带电
不带电
+
+
-
(4)原子的组成及带电情况
中子
质子
电子
原子的直径:约10-10米
原子核的直径:约10-15米
形象来说,就是地球和乒乓球的比例, 大约一比一千亿。 原子核极小,它的直径在10-16m~10-14m之间,体积只占原子体积的几千亿分之一,在这极小的原子核里却集中了99.95%以上原子的质量。
(5)原子与原子核的大小比较
默里·盖尔曼
(1929—2019),生于美国纽约的一个犹太家庭,物理学家,提出了质子和中子是由三个夸克组成的,并因此获得诺贝尔物理学奖。
(6)夸克
质子和中子还能再分吗?随着人们对原子内部结构的研究逐步深入,物理学家默里·盖尔曼提出了质子和中子还可以再分。
质子和中子是分别由三个夸克组成的。
电子<10-18m
核子由
夸克组成
质子
中子
粒子 分子 原子 原子核 核子
大小
原子核由质子
和中子组成
2. 总结:不同微观粒子的层次结构示意图
10-10~10-5m
10-10m
10-15~10-14m
10-15m
水分子(每个小球表示 一个原子)
1909 年,卢瑟福和他的学生利用一束高速运动的带正电的 α 粒子(由两个质子和两个中子构成)轰击很薄的金箔,获得了极有价值的实验现象和数据。1911 年,卢瑟福根据上述 α 粒子散射实验的结果提出了著名的原子核式结构模型。该实验也启发了人们用更高能量的粒子作为“炮弹”来探索微观世界的奥秘。
我们把能使带电粒子加速到很高能量的装置称为加速器。20 世 纪 30 年代,美国物理学家劳伦斯发明了回旋加速器。1988 年,我 国建成了北京正负电子对撞机。这是当时世界八大高能加速器之一, 也是我国继导弹、原子弹、氢弹、人造卫星、核潜艇之后的又一伟大科技成就。
生活 物理 社会 加速器及其应用
下图所示的高能同步辐射光源直线加速器由中国科学院高 能物理研究所承担建造。它在先进材料、航空航天、能源、环保以 及生物工程等方面发挥了重要作用。
加速器在生产、生活中同样有着非常重要的作用,如用于癌症的治疗、工业探伤、食品的防腐保鲜、复合材料的生产以及医疗用 品消毒等。
高能同步辐射光源直线加速器
探索更小的微粒
原子
模型
原子结构
①汤姆孙发现电子,提出原子的葡萄干蛋糕模型.
②卢瑟福通过α粒子实验,发现质子,提出核式结构模型。
③詹姆斯·查德威克通过实验证实中子的存在.
④默里·盖尔曼发现质子和中子分别由三个夸克组成的。
⑤原子的三种模型: 道尔顿模型;汤姆生模型;卢瑟福的核式结构模型.
原子核
电子(带负电)
质子(带正电)—夸克。
中子(不带电)—夸克。
课堂小结
1.刮大风时尘埃在空中飞舞,对于尘埃,下列说法正确的是( )
A.它和一个分子差不多大小
B.可以借助光学显微镜观察到尘埃分子
C.它的直径大约为10-10m
D.它是由许多分子构成的
D
课堂练习
2. 关于卢瑟福提出的原子结构的核式模型,下列说法中正确的是( )
A. 原子是由原子核和中子组成的
B. 原子是由原子核和核外电子组成的
C. 原子是由质子和中子组成的
D. 原子的质量几乎集中在原子核外
B
3.大千世界,从宏观到微观,从天体到原子,似乎都有那么多惊人的相同规律。如图所示,是太阳系模拟图,行星们在各自的固定轨道上围绕恒星太阳运转,这与 (选填“汤姆逊”或“卢瑟福”)建立的原子核式结构模型十分
相似,其中原子核相当于太阳,绕核运动的 就相当于行星。
卢瑟福
电子
