2.2.2 酚 课件(共23张PPT)
文档属性
| 名称 | 2.2.2 酚 课件(共23张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 2.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-22 00:00:00 | ||
图片预览






文档简介
(共23张PPT)
第2章 官能团与有机化学反应 烃的衍生物
第2节 醇和酚
第1课时 酚及其性质
1、认识酚的组成和结构特点、性质、转化关系。
2、了解酚在生产、生活中的重要应用。
3、认识苯酚分子中苯环和羟基之间的相互影响,能通过羟基与芳香烃基的连接方式,认识酚与芳香醇在结构上的差异。
1.能基于官能团、化学键的特点分析和推断酚的化学性质。能描述和分
析醇的重要反应,能书写相应的反应方程式。(宏观辨识与微观探析)
2.通过苯酚与氢氧化钠溶液以及苯酚钠溶液与二氧化碳反应的有关实验,探究苯酚的有关性质,推断其具有弱酸性,并能结合乙醇的结构与性质,进一步认识烃基对羟基活泼性的影响。 (科学探究与创新意识)
阅读课本,了解酚和酚的存在。酚的命名、苯酚及结构、酚的物理性质。
芳香烃分子中苯环上的氢原子被羟基取代后的有机化合物称为酚。如: (邻甲基苯酚)、 (萘酚)。
三、酚
1.酚的概念
2.苯酚的组成和结构特点:
苯酚俗名:石炭酸,是组成最简单的酚,
分子式:C6H6O 结构简式: 官能团:羟基—OH
—OH
酚的命名:
3、苯酚的物理性质
纯净的苯酚是没有颜色、具有特殊的气味的晶体露置在空气中因小部分发生氧化而显粉红色。
熔点:40.9℃;常温时,苯酚在水中溶解度不大,当温度高于65℃时,能跟水互溶,苯酚易溶于乙醇,乙醚等有机溶剂。
苯酚有毒,其浓溶液对皮肤有强烈的腐蚀性。如果不慎沾到皮肤上,应立即用酒精 洗涤。
实验:取少量苯酚加入水中,苯酚不能完全溶解在水中,加热到65℃时,溶液变澄清,停止加热后,溶液重新变浑浊(乳浊液)。
—O—H
⑴苯环对羟基的影响
酸性
⑵羟基对苯环的影响
苯环上的取代反应
苯酚的结构
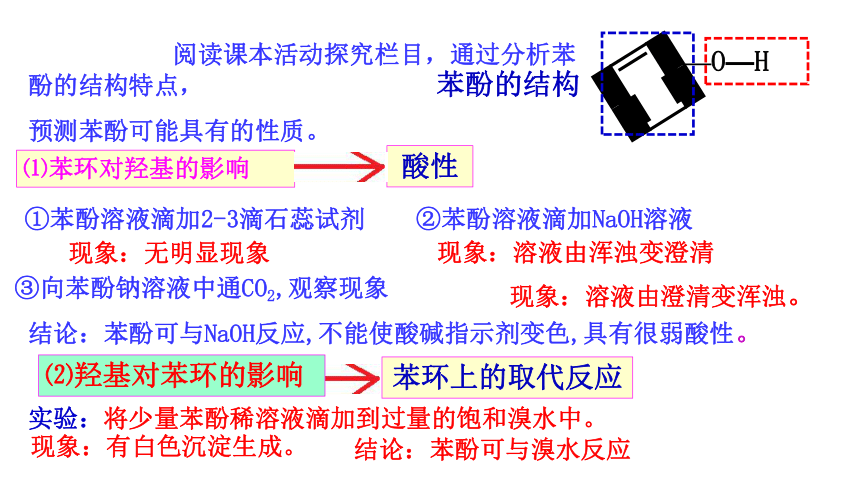
阅读课本活动探究栏目,通过分析苯酚的结构特点,
预测苯酚可能具有的性质。
①苯酚溶液滴加2-3滴石蕊试剂
②苯酚溶液滴加NaOH溶液
现象:无明显现象
现象:溶液由浑浊变澄清
结论:苯酚可与NaOH反应,不能使酸碱指示剂变色,具有很弱酸性。
实验:将少量苯酚稀溶液滴加到过量的饱和溴水中。
现象:有白色沉淀生成。
结论:苯酚可与溴水反应
③向苯酚钠溶液中通CO2,观察现象
现象:溶液由澄清变浑浊。
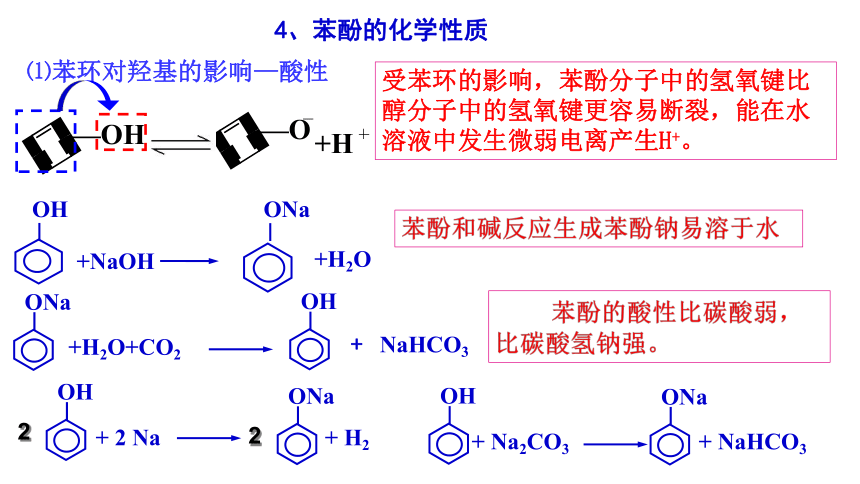
4、苯酚的化学性质
⑴苯环对羟基的影响—酸性
—OH
—O
+H
受苯环的影响,苯酚分子中的氢氧键比醇分子中的氢氧键更容易断裂,能在水溶液中发生微弱电离产生H+。
OH
ONa
+H2O
+NaOH
OH
ONa
+H2O+CO2
+
NaHCO3
OH
ONa
+ 2 Na
+ H2
2
2
OH
ONa
+ Na2CO3
+ NaHCO3
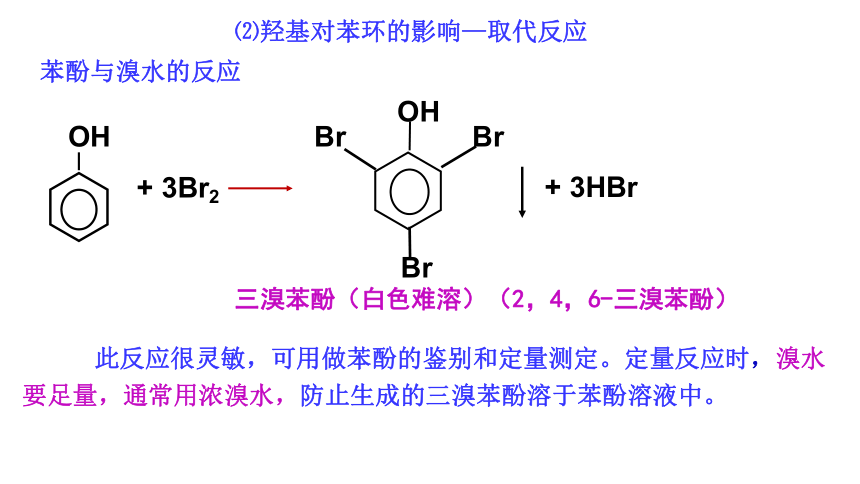
三溴苯酚(白色难溶)(2,4,6-三溴苯酚)
OH
+ 3Br2
+ 3HBr
Br
Br
Br
OH
此反应很灵敏,可用做苯酚的鉴别和定量测定。定量反应时,溴水要足量,通常用浓溴水,防止生成的三溴苯酚溶于苯酚溶液中。
⑵羟基对苯环的影响—取代反应
苯酚与溴水的反应
实验:向盛有少量苯酚溶液的试管中滴加几滴FeCl3 溶液,观察现象。
现象:溶液变成紫色
苯酚与FeCl3溶液能发生显色反应时由于有络合物生成的缘故。此反应常用于酚的鉴别。
+ Fe3+
6
[Fe(C6H5O)6]3-
+ 6 H+
OH
⑶苯酚的显色反应
反应原理:
酚醛树脂:电木,就是苯酚和甲醛聚合反应合成的。
分析反应的断键部位和成键部位,理解反应实质。
由于羟基的影响,使羟基邻对位上的氢原子活化。
⑷苯酚的聚合反应
H+
OH
CH2
n
H
OH+(n-1)H2O
酚醛树脂线路板
5.苯酚的用途
苯酚是重要的有机化工原料,制酚醛树脂、医药(如阿司匹林)、染料等,农药、香料、涂料等;稀溶液用作防腐剂和消毒剂。
1.苯酚的结构简式,掌握芳香醇和酚的区别。
2.苯酚的物理性质:
色、态、味、溶解性、毒性、腐蚀性。
O—H
/或钠
3.苯酚的主要化学性质:
加成反应
酸性
取代反应
显色反应
氧化反应(粉红色)
硝酸
硫酸
1.下列说法中正确的是( )
A.含有羟基的化合物一定属于醇类
B.羟基与链烃基相连的有机物是醇类
C.醇和酚都含有羟基,它们的化学性质相同
D. 与 互为同系物
B
2、分子式为C9H12O的有机物的分子中有一个苯环、一个链烃基,则它属于酚类的结构可能有( )
A. 2种 B. 4种 C. 5种 D. 6种
D
3、下列物质与苯酚互为同系物的是( )
B
4、下列关于苯酚的叙述中,不正确的是( )
A.其水溶液显酸性,俗称石炭酸
B.苯酚暴露在空气中,会因与CO2作用而变成粉红色
C.在水中的溶解度随温度的升高而增大,超过65 ℃可与水混溶
D.其浓溶液对皮肤有强烈的腐蚀性,如果不慎沾在皮肤上,应立即用酒精擦洗
B
① +H2O+CO2―→ +NaHCO3
②2 +H2O+CO2―→ 2 +Na2CO3
③ +NaHCO3―→ +H2CO3
④ +Na2CO3―→ +NaHCO3
5、已知酸性强弱顺序为H2CO3> >HCO3- ,则下列化
学方程式中正确的是 ( )
A.①③ B.②③ C.①④ D.②④
C
6、甲苯中混有少量苯酚,除去苯酚的最佳方法是( )
A.加入足量的NaOH溶液充分振荡后,用分液漏斗分液弃除下层溶液
B.加入溴水,生成三溴苯酚,再过滤除去
C.加水,加热超过70 ℃(苯酚在热水中溶解度很大),然后用分液漏斗振荡分液后,弃除下层溶液
D.将混合物蒸馏(甲苯沸点110 ℃,苯酚沸点182 ℃),可先蒸出甲苯
A
7、下列关于苯酚的叙述,不正确的是( )
A.将苯酚晶体放入少量水中,加热至全部溶解,冷却至50 ℃形成乳浊液
B.苯酚可以和硝酸发生取代反应
C.苯酚易溶于NaOH溶液中
D.苯酚的酸性比碳酸强,比醋酸弱
D
8、只需用一种试剂即可将酒精、苯酚溶液、四氯化碳、己烯、甲苯五种无色液体区分开来,该试剂是( )
A.FeCl3溶液
B.溴水
C.酸性KMnO4溶液
D.金属钠
B
9、分离苯和苯酚的混合物,通常采用的方法是( )
A.振荡混合物,用分液漏斗分离
B.加入NaOH溶液后振荡,用分液漏斗分离;取下层液体通入CO2,待分层后分液
C.加水振荡后用分液漏斗分离
D.加稀盐酸振荡后,用分液漏斗分离
B
(1)性质Ⅰ是________________,操作1是_____、操作2是____。
(2)性质Ⅱ是_______,操作1是____________、操作2是_________。
(3)写出所发生反应的化学方程式:
______________________________________。
______________________________________。
10、如图所示的操作和实验现象,能证明苯酚的两个性质。
在水中的溶解性
加热
冷却
弱酸性
加NaOH溶液
通入CO2
第2章 官能团与有机化学反应 烃的衍生物
第2节 醇和酚
第1课时 酚及其性质
1、认识酚的组成和结构特点、性质、转化关系。
2、了解酚在生产、生活中的重要应用。
3、认识苯酚分子中苯环和羟基之间的相互影响,能通过羟基与芳香烃基的连接方式,认识酚与芳香醇在结构上的差异。
1.能基于官能团、化学键的特点分析和推断酚的化学性质。能描述和分
析醇的重要反应,能书写相应的反应方程式。(宏观辨识与微观探析)
2.通过苯酚与氢氧化钠溶液以及苯酚钠溶液与二氧化碳反应的有关实验,探究苯酚的有关性质,推断其具有弱酸性,并能结合乙醇的结构与性质,进一步认识烃基对羟基活泼性的影响。 (科学探究与创新意识)
阅读课本,了解酚和酚的存在。酚的命名、苯酚及结构、酚的物理性质。
芳香烃分子中苯环上的氢原子被羟基取代后的有机化合物称为酚。如: (邻甲基苯酚)、 (萘酚)。
三、酚
1.酚的概念
2.苯酚的组成和结构特点:
苯酚俗名:石炭酸,是组成最简单的酚,
分子式:C6H6O 结构简式: 官能团:羟基—OH
—OH
酚的命名:
3、苯酚的物理性质
纯净的苯酚是没有颜色、具有特殊的气味的晶体露置在空气中因小部分发生氧化而显粉红色。
熔点:40.9℃;常温时,苯酚在水中溶解度不大,当温度高于65℃时,能跟水互溶,苯酚易溶于乙醇,乙醚等有机溶剂。
苯酚有毒,其浓溶液对皮肤有强烈的腐蚀性。如果不慎沾到皮肤上,应立即用酒精 洗涤。
实验:取少量苯酚加入水中,苯酚不能完全溶解在水中,加热到65℃时,溶液变澄清,停止加热后,溶液重新变浑浊(乳浊液)。
—O—H
⑴苯环对羟基的影响
酸性
⑵羟基对苯环的影响
苯环上的取代反应
苯酚的结构
阅读课本活动探究栏目,通过分析苯酚的结构特点,
预测苯酚可能具有的性质。
①苯酚溶液滴加2-3滴石蕊试剂
②苯酚溶液滴加NaOH溶液
现象:无明显现象
现象:溶液由浑浊变澄清
结论:苯酚可与NaOH反应,不能使酸碱指示剂变色,具有很弱酸性。
实验:将少量苯酚稀溶液滴加到过量的饱和溴水中。
现象:有白色沉淀生成。
结论:苯酚可与溴水反应
③向苯酚钠溶液中通CO2,观察现象
现象:溶液由澄清变浑浊。
4、苯酚的化学性质
⑴苯环对羟基的影响—酸性
—OH
—O
+H
受苯环的影响,苯酚分子中的氢氧键比醇分子中的氢氧键更容易断裂,能在水溶液中发生微弱电离产生H+。
OH
ONa
+H2O
+NaOH
OH
ONa
+H2O+CO2
+
NaHCO3
OH
ONa
+ 2 Na
+ H2
2
2
OH
ONa
+ Na2CO3
+ NaHCO3
三溴苯酚(白色难溶)(2,4,6-三溴苯酚)
OH
+ 3Br2
+ 3HBr
Br
Br
Br
OH
此反应很灵敏,可用做苯酚的鉴别和定量测定。定量反应时,溴水要足量,通常用浓溴水,防止生成的三溴苯酚溶于苯酚溶液中。
⑵羟基对苯环的影响—取代反应
苯酚与溴水的反应
实验:向盛有少量苯酚溶液的试管中滴加几滴FeCl3 溶液,观察现象。
现象:溶液变成紫色
苯酚与FeCl3溶液能发生显色反应时由于有络合物生成的缘故。此反应常用于酚的鉴别。
+ Fe3+
6
[Fe(C6H5O)6]3-
+ 6 H+
OH
⑶苯酚的显色反应
反应原理:
酚醛树脂:电木,就是苯酚和甲醛聚合反应合成的。
分析反应的断键部位和成键部位,理解反应实质。
由于羟基的影响,使羟基邻对位上的氢原子活化。
⑷苯酚的聚合反应
H+
OH
CH2
n
H
OH+(n-1)H2O
酚醛树脂线路板
5.苯酚的用途
苯酚是重要的有机化工原料,制酚醛树脂、医药(如阿司匹林)、染料等,农药、香料、涂料等;稀溶液用作防腐剂和消毒剂。
1.苯酚的结构简式,掌握芳香醇和酚的区别。
2.苯酚的物理性质:
色、态、味、溶解性、毒性、腐蚀性。
O—H
/或钠
3.苯酚的主要化学性质:
加成反应
酸性
取代反应
显色反应
氧化反应(粉红色)
硝酸
硫酸
1.下列说法中正确的是( )
A.含有羟基的化合物一定属于醇类
B.羟基与链烃基相连的有机物是醇类
C.醇和酚都含有羟基,它们的化学性质相同
D. 与 互为同系物
B
2、分子式为C9H12O的有机物的分子中有一个苯环、一个链烃基,则它属于酚类的结构可能有( )
A. 2种 B. 4种 C. 5种 D. 6种
D
3、下列物质与苯酚互为同系物的是( )
B
4、下列关于苯酚的叙述中,不正确的是( )
A.其水溶液显酸性,俗称石炭酸
B.苯酚暴露在空气中,会因与CO2作用而变成粉红色
C.在水中的溶解度随温度的升高而增大,超过65 ℃可与水混溶
D.其浓溶液对皮肤有强烈的腐蚀性,如果不慎沾在皮肤上,应立即用酒精擦洗
B
① +H2O+CO2―→ +NaHCO3
②2 +H2O+CO2―→ 2 +Na2CO3
③ +NaHCO3―→ +H2CO3
④ +Na2CO3―→ +NaHCO3
5、已知酸性强弱顺序为H2CO3> >HCO3- ,则下列化
学方程式中正确的是 ( )
A.①③ B.②③ C.①④ D.②④
C
6、甲苯中混有少量苯酚,除去苯酚的最佳方法是( )
A.加入足量的NaOH溶液充分振荡后,用分液漏斗分液弃除下层溶液
B.加入溴水,生成三溴苯酚,再过滤除去
C.加水,加热超过70 ℃(苯酚在热水中溶解度很大),然后用分液漏斗振荡分液后,弃除下层溶液
D.将混合物蒸馏(甲苯沸点110 ℃,苯酚沸点182 ℃),可先蒸出甲苯
A
7、下列关于苯酚的叙述,不正确的是( )
A.将苯酚晶体放入少量水中,加热至全部溶解,冷却至50 ℃形成乳浊液
B.苯酚可以和硝酸发生取代反应
C.苯酚易溶于NaOH溶液中
D.苯酚的酸性比碳酸强,比醋酸弱
D
8、只需用一种试剂即可将酒精、苯酚溶液、四氯化碳、己烯、甲苯五种无色液体区分开来,该试剂是( )
A.FeCl3溶液
B.溴水
C.酸性KMnO4溶液
D.金属钠
B
9、分离苯和苯酚的混合物,通常采用的方法是( )
A.振荡混合物,用分液漏斗分离
B.加入NaOH溶液后振荡,用分液漏斗分离;取下层液体通入CO2,待分层后分液
C.加水振荡后用分液漏斗分离
D.加稀盐酸振荡后,用分液漏斗分离
B
(1)性质Ⅰ是________________,操作1是_____、操作2是____。
(2)性质Ⅱ是_______,操作1是____________、操作2是_________。
(3)写出所发生反应的化学方程式:
______________________________________。
______________________________________。
10、如图所示的操作和实验现象,能证明苯酚的两个性质。
在水中的溶解性
加热
冷却
弱酸性
加NaOH溶液
通入CO2
