1.1 分子动理论的基本观点 第1课时(共21张PPT)课件 2024-2025学年高二物理鲁科版(2019)选择性必修第三册
文档属性
| 名称 | 1.1 分子动理论的基本观点 第1课时(共21张PPT)课件 2024-2025学年高二物理鲁科版(2019)选择性必修第三册 |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 物理 | ||
| 更新时间 | 2025-04-22 00:00:00 | ||
图片预览






文档简介
(共21张PPT)
第一章 分子动理论的基本观点
第1节 分子动理论的基本观点
第1课时
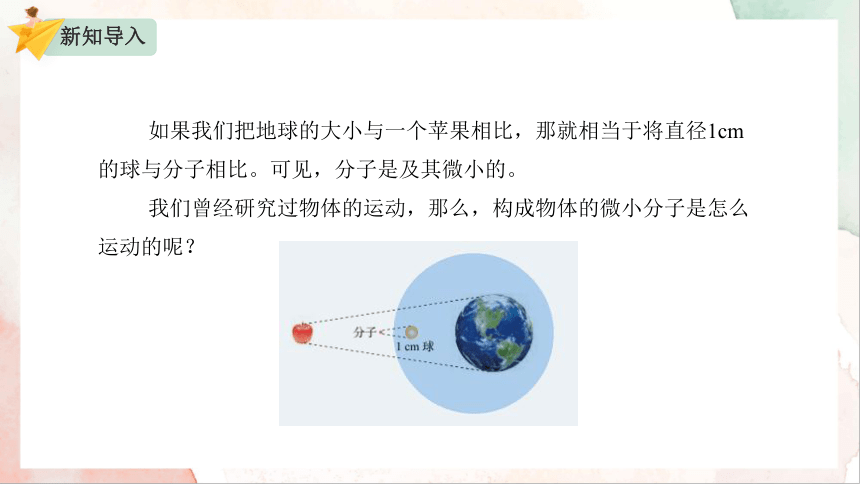
如果我们把地球的大小与一个苹果相比,那就相当于将直径1cm的球与分子相比。可见,分子是及其微小的。
我们曾经研究过物体的运动,那么,构成物体的微小分子是怎么运动的呢?
1.知道物体是由大量分子组成的。
2.知道阿伏伽德罗常数及其意义,会用阿伏伽德罗常数进行计算或估算
3.通过实验了解扩散现象,观察并能解释布朗运动。知道影响布朗运动激烈程度的因素,以及布朗运动产生的原因。
(1)热学中的分子:当探讨分子 、原子或离子等微观粒子的热运动时,通常将它们统称为分子。
知识点一:物体由大量分子组成
1.分子
(2)数值:NA=6.02×1023mol-1。
2.阿伏加德罗常数
1 mol的任何物质都含有相同的粒子数.
是微观世界的一个重要常数,是联系微观物理量和宏观物理量的桥梁.
(3)意义:
(1)定义:
3.有关计算:
(1)已知物质的摩尔质量Mmol,可求出分子质量m0:
(其中,Vmol 为摩尔体积, 为物质的密度)
(2)已知物质的量(摩尔数)n,可求出物体所含分子的数目N.
(3)已知物质的摩尔体积Vmol ,可求出分子的体积 V0
(只适用于固体、液体)
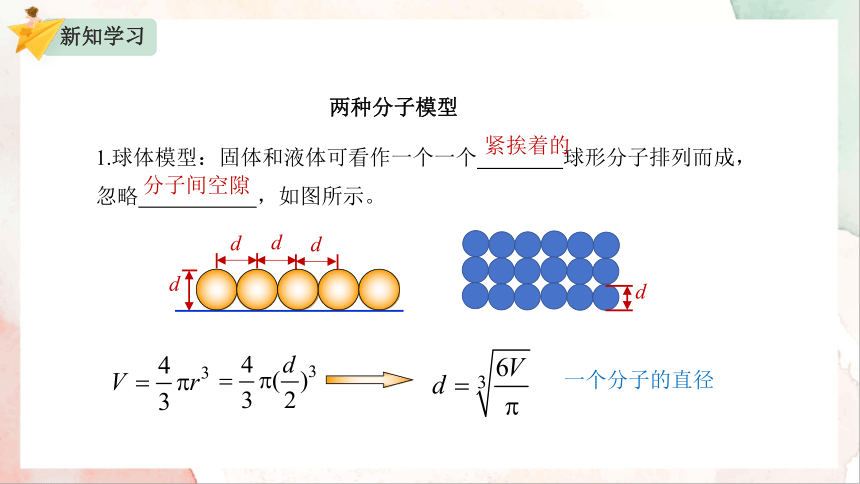
1.球体模型:固体和液体可看作一个一个 球形分子排列而成,忽略 ,如图所示。
两种分子模型
紧挨着的
分子间空隙
d
d
d
d
一个分子的直径
d
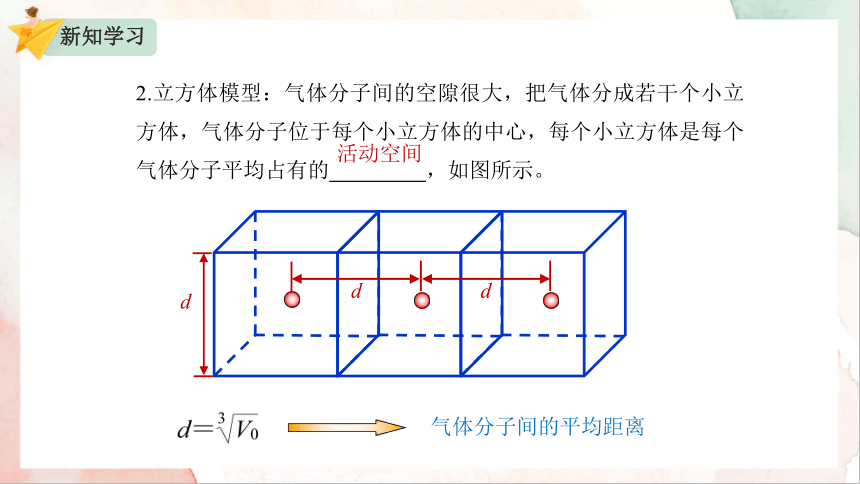
2.立方体模型:气体分子间的空隙很大,把气体分成若干个小立方体,气体分子位于每个小立方体的中心,每个小立方体是每个气体分子平均占有的 ,如图所示。
d
d
d
气体分子间的平均距离
活动空间
知识点二:分子永不停息地做无规则运动
当在树下你走过时,为什么能够闻到沁人心脾的花香呢
(1)定义:不同的物质互相接触时,会发生彼此进入对方的现象,叫做扩散现象.
1.扩散现象
(2)固体、液体、气体都存在这样的现象。
酱油的色素分子
扩散到蛋清中
墨水扩散
扩散快慢与温度有关,温度越高,扩散越快
演 示
用显微镜观察炭粒的运动
取1滴用水稀释过的墨汁,滴在载玻片上,盖上盖玻片,
放在高倍显微镜下观察小炭粒的运动情况。
可以看到悬浮在液体中的小炭粒在不停地做无规则运动。
2. 布朗运动
(1)定义:悬浮在液体(或气体)中的固体微粒永不停息的无规则运动叫做布朗运动。
在显微镜下追踪一个小炭粒的运动,每隔30s把炭粒的位置记录下来,然后用直线把这些位置接时间顺序依次连接起来,就得到类似图所示的微粒运动的位置连线。 可以看出,微粒的运动是无规则的。
实际上,就是在短短的30s内,微粒的运动也是极不规则的。
微粒越小,在某一瞬间跟它相撞的液体分子数就越少,撞击作用的不平衡性就表现的越明显,因而布朗运动就越明显。
(2)布朗运动产生的原因
大量液体分子不停地做无规则运动时,对悬浮在其中的微粒撞击作用不平衡。
点击播放
我们无法直接看见分子的无规则运动。悬浮微粒的无规则运动并不是分子的运动,但是微粒运动的无规则性,间接的反映了液体分子的无规则性。
(3)布朗运动和扩散现象的比较
比较对象 布朗运动 扩散现象
产生 条件
影响 因素
现象 本质
联系 固体微粒足够小,悬浮在液体或气体中
两种不同物质相互接触
温度的高低和微粒的大小
温度的高低、物态形式、物质的浓度差
是液体或气体分子无规则运动的反映
是分子的运动
它们都直接或间接证实了分子的无规则运动
3.热运动:
在扩散现象中,我们会发现,温度越高,扩散得越快。观察布朗运动时也会发现,温度越高,悬浮微粒的运动就越明显。这些事实表明,分子的无规则运动与温度有关系,温度越高,这种运动越激烈。因此,我们把分子永不停息的无规则运动叫做热运动。
扩散现象和布朗运动都不是热运动,扩散现象是分子运动的直接证明;布朗运动间接证明了液体分子的无规则运动。
1.把墨汁用水稀释后取出一滴放在显微镜下观察,下列说法中正确的是( )
A. 在显微镜下既能看到水分子也能看到悬浮的小炭粒,且水分子不停地撞击小炭粒
B. 小炭粒在不停地做无规则运动,这就是所说的布朗运动
C. 越大的炭粒,运动越明显
D. 在显微镜下看起来连成一片的液体,实际上是由许许多多的静止不动的水分子组成的
B
2.(多选)关于扩散现象和布朗运动,下列说法正确的是( )
A.温度越高,扩散现象和布朗运动都越明显
B.运动物体中的分子热运动比静止物体中的分子热运动剧烈
C.扩散现象是分子的运动,布朗运动间接反映了分子的运动
D.颗粒越大,布朗运动越剧烈
AC
3.(多选)用M表示液体或固体的摩尔质量,m表示分子质量,ρ表示物质密度,Vmol表示摩尔体积,V0表示分子体积。NA表示阿伏伽德罗常数,下列关系式正确的是( )
BCD
4.阿伏伽德罗常数是NA(mol-1),铜的摩尔质量是μ(kg/mol),铜的密度是ρ(kg/m3),则下列说法不正确的是( )
D
5.已知氧气分子的质量m0=5.3×10-26 kg,标准状况下氧气的密度ρ=1.43 kg/m3,阿伏伽德罗常数NA=6.02×1023 mol-1,求:(计算结果均保留两位有效数字)
(1)氧气的摩尔质量;
(2)标准状况下氧气分子间的平均距离;
(3)标准状况下1 cm3的氧气中含有的氧气分子数。
答案 (1)3.2×10-2 kg/mol (2)3.3×10-9 m (3)2.7×1019个
分子热运动
扩散
分子动理论的基本观点
物体是由大量分子构成的
布朗运动
热运动
第一章 分子动理论的基本观点
第1节 分子动理论的基本观点
第1课时
如果我们把地球的大小与一个苹果相比,那就相当于将直径1cm的球与分子相比。可见,分子是及其微小的。
我们曾经研究过物体的运动,那么,构成物体的微小分子是怎么运动的呢?
1.知道物体是由大量分子组成的。
2.知道阿伏伽德罗常数及其意义,会用阿伏伽德罗常数进行计算或估算
3.通过实验了解扩散现象,观察并能解释布朗运动。知道影响布朗运动激烈程度的因素,以及布朗运动产生的原因。
(1)热学中的分子:当探讨分子 、原子或离子等微观粒子的热运动时,通常将它们统称为分子。
知识点一:物体由大量分子组成
1.分子
(2)数值:NA=6.02×1023mol-1。
2.阿伏加德罗常数
1 mol的任何物质都含有相同的粒子数.
是微观世界的一个重要常数,是联系微观物理量和宏观物理量的桥梁.
(3)意义:
(1)定义:
3.有关计算:
(1)已知物质的摩尔质量Mmol,可求出分子质量m0:
(其中,Vmol 为摩尔体积, 为物质的密度)
(2)已知物质的量(摩尔数)n,可求出物体所含分子的数目N.
(3)已知物质的摩尔体积Vmol ,可求出分子的体积 V0
(只适用于固体、液体)
1.球体模型:固体和液体可看作一个一个 球形分子排列而成,忽略 ,如图所示。
两种分子模型
紧挨着的
分子间空隙
d
d
d
d
一个分子的直径
d
2.立方体模型:气体分子间的空隙很大,把气体分成若干个小立方体,气体分子位于每个小立方体的中心,每个小立方体是每个气体分子平均占有的 ,如图所示。
d
d
d
气体分子间的平均距离
活动空间
知识点二:分子永不停息地做无规则运动
当在树下你走过时,为什么能够闻到沁人心脾的花香呢
(1)定义:不同的物质互相接触时,会发生彼此进入对方的现象,叫做扩散现象.
1.扩散现象
(2)固体、液体、气体都存在这样的现象。
酱油的色素分子
扩散到蛋清中
墨水扩散
扩散快慢与温度有关,温度越高,扩散越快
演 示
用显微镜观察炭粒的运动
取1滴用水稀释过的墨汁,滴在载玻片上,盖上盖玻片,
放在高倍显微镜下观察小炭粒的运动情况。
可以看到悬浮在液体中的小炭粒在不停地做无规则运动。
2. 布朗运动
(1)定义:悬浮在液体(或气体)中的固体微粒永不停息的无规则运动叫做布朗运动。
在显微镜下追踪一个小炭粒的运动,每隔30s把炭粒的位置记录下来,然后用直线把这些位置接时间顺序依次连接起来,就得到类似图所示的微粒运动的位置连线。 可以看出,微粒的运动是无规则的。
实际上,就是在短短的30s内,微粒的运动也是极不规则的。
微粒越小,在某一瞬间跟它相撞的液体分子数就越少,撞击作用的不平衡性就表现的越明显,因而布朗运动就越明显。
(2)布朗运动产生的原因
大量液体分子不停地做无规则运动时,对悬浮在其中的微粒撞击作用不平衡。
点击播放
我们无法直接看见分子的无规则运动。悬浮微粒的无规则运动并不是分子的运动,但是微粒运动的无规则性,间接的反映了液体分子的无规则性。
(3)布朗运动和扩散现象的比较
比较对象 布朗运动 扩散现象
产生 条件
影响 因素
现象 本质
联系 固体微粒足够小,悬浮在液体或气体中
两种不同物质相互接触
温度的高低和微粒的大小
温度的高低、物态形式、物质的浓度差
是液体或气体分子无规则运动的反映
是分子的运动
它们都直接或间接证实了分子的无规则运动
3.热运动:
在扩散现象中,我们会发现,温度越高,扩散得越快。观察布朗运动时也会发现,温度越高,悬浮微粒的运动就越明显。这些事实表明,分子的无规则运动与温度有关系,温度越高,这种运动越激烈。因此,我们把分子永不停息的无规则运动叫做热运动。
扩散现象和布朗运动都不是热运动,扩散现象是分子运动的直接证明;布朗运动间接证明了液体分子的无规则运动。
1.把墨汁用水稀释后取出一滴放在显微镜下观察,下列说法中正确的是( )
A. 在显微镜下既能看到水分子也能看到悬浮的小炭粒,且水分子不停地撞击小炭粒
B. 小炭粒在不停地做无规则运动,这就是所说的布朗运动
C. 越大的炭粒,运动越明显
D. 在显微镜下看起来连成一片的液体,实际上是由许许多多的静止不动的水分子组成的
B
2.(多选)关于扩散现象和布朗运动,下列说法正确的是( )
A.温度越高,扩散现象和布朗运动都越明显
B.运动物体中的分子热运动比静止物体中的分子热运动剧烈
C.扩散现象是分子的运动,布朗运动间接反映了分子的运动
D.颗粒越大,布朗运动越剧烈
AC
3.(多选)用M表示液体或固体的摩尔质量,m表示分子质量,ρ表示物质密度,Vmol表示摩尔体积,V0表示分子体积。NA表示阿伏伽德罗常数,下列关系式正确的是( )
BCD
4.阿伏伽德罗常数是NA(mol-1),铜的摩尔质量是μ(kg/mol),铜的密度是ρ(kg/m3),则下列说法不正确的是( )
D
5.已知氧气分子的质量m0=5.3×10-26 kg,标准状况下氧气的密度ρ=1.43 kg/m3,阿伏伽德罗常数NA=6.02×1023 mol-1,求:(计算结果均保留两位有效数字)
(1)氧气的摩尔质量;
(2)标准状况下氧气分子间的平均距离;
(3)标准状况下1 cm3的氧气中含有的氧气分子数。
答案 (1)3.2×10-2 kg/mol (2)3.3×10-9 m (3)2.7×1019个
分子热运动
扩散
分子动理论的基本观点
物体是由大量分子构成的
布朗运动
热运动
同课章节目录
- 第1章 分子动理论与气体实验定律
- 第1节 分子动理论的基本观点
- 第2节 科学测量:用油膜法估测油酸分子的大小
- 第3节 气体分子速率分布的统计规律
- 第4节 科学探究:气体压强与体积的关系
- 第5节 气体实验定律
- 第2章 固体与液体
- 第1节 固体类型及微观结构
- 第2节 表面张力和毛细现象
- 第3节 材料及其应用
- 第3章 热力学定律
- 第1节 热力学第一定律
- 第2节 能量的转化与守恒
- 第3节 热力学第二定律
- 第4节 熵——系统无序程度的量度
- 第4章 原子结构
- 第1节 电子的发现与汤姆孙原子模型
- 第2节 原子的核式结构模型
- 第3节 光谱与氢原子光谱
- 第4节 玻尔原子模型
- 第5章 原子核与核能
- 第1节 认识原子核
- 第2节 原子核衰变及半衰期
- 第3节 核力与核能
- 第4节 核裂变和核聚变
- 第5节 核能的利用与环境保护
- 第6章 波粒二象性
- 第1节 光电效应及其解释
- 第2节 实物粒子的波粒二象性
