实验活动1 乙酸乙酯的制备与性质(17张) 2024-2025学年高二化学人教版(2019)选择性必修3
文档属性
| 名称 | 实验活动1 乙酸乙酯的制备与性质(17张) 2024-2025学年高二化学人教版(2019)选择性必修3 |

|
|
| 格式 | pptx | ||
| 文件大小 | 2.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-23 00:00:00 | ||
图片预览





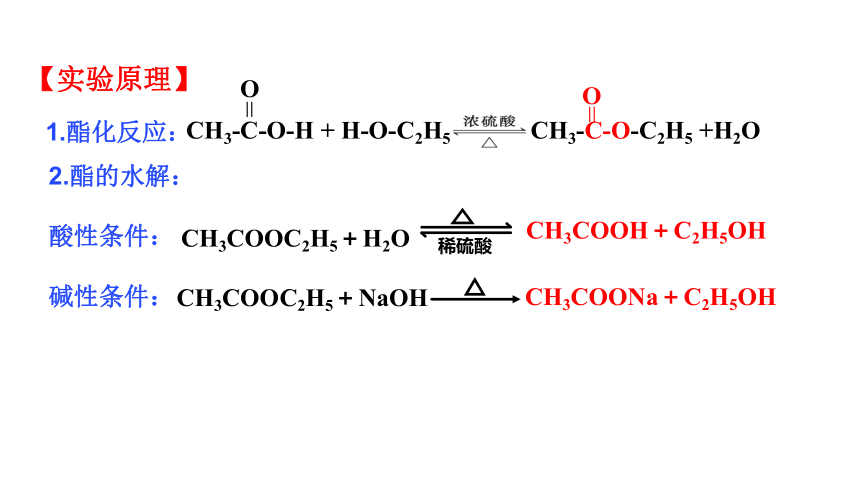

文档简介
(共17张PPT)
实验活动1:乙酸乙酯的制备与性质
第三章 烃的衍生物
厨师烧鱼时常加醋并加点酒,鱼的味道就变得香醇,特别鲜美。为什么呢?
1.了解示踪原子法在酯化反应反应机理分析中的应用。(科学探究与创新意识)
2.能通过实验探究乙酸乙酯在中性、酸性和碱性溶液及不同温度下的水解速率,分析并根据化学平衡移动原理解释原因。(科学探究与创新意识)
1.学习制备乙酸乙酯的方法。
2.加深对酯化反应和酯的水解的认识。
体会课堂探究的乐趣,
汲取新知识的营养,
让我们一起 吧!
进
走
课
堂
【实验仪器】
试管、试管夹、烧杯、量筒、胶头滴管、玻璃导管、乳胶管、橡胶塞、铁架台、酒精灯、火柴、秒表、碎瓷片。
【实验药品】
乙醇、乙酸、浓硫酸、饱和Na2CO3溶液、蒸馏水、3mol/LH2SO4溶液、6mol/LNaOH溶液。
【实验原理】
1.酯化反应:
CH3-C-O-H + H-O-C2H5 CH3-C-O-C2H5 +H2O
=
O
O
=
2.酯的水解:
酸性条件:
碱性条件:
CH3COOH+C2H5OH
CH3COOC2H5+H2O
稀硫酸
CH3COONa+C2H5OH
CH3COOC2H5+NaOH
【实验步骤】
1.乙酸乙酯的制备
实验步骤 实验现象
(1)在一支试管中加入2 mL乙醇,然后边振荡试管边慢慢加入0.5 mL浓硫酸和2 mL乙酸,再加入几片碎瓷片。在另一支试管中加入3 mL饱和Na2CO3溶液。
(2)用小火加热试管里的混合物,将产生的蒸气经导管通到饱和Na2CO3溶液的上方约0.5 cm处,注意观察试管内的变化。反应一段时间后,取下盛有Na2CO3溶液的试管,并停止加热
(3)振荡盛有Na2CO3溶液的试管,静置。待溶液分层后,观察上层的油状液体,并注意闻气味
饱和碳酸钠溶液的液面上有无色透明的难溶于水的油状液体产生
可闻到香味
【思考与讨论】
1.在乙酸乙酯的制备实验中,试剂添加顺序如何?加入碎瓷片的作用是什么?为什么不用大火加热而用小火加热?
【提示】在试管中加入乙醇,然后边振荡边加慢慢加入浓硫酸,最后加入乙酸。
碎瓷片的作用是防止暴沸;大火加热,乙醇、乙酸容易挥发,利用率减小。
2.(1)在乙酸乙酯的制备实验中,导管不能插入饱和Na2CO3溶液的原因是什么?
(2)浓硫酸和Na2CO3的作用是什么?
(3)吸收乙酸乙酯能否用NaOH溶液代替Na2CO3溶液?为什么?
【提示】(1)防止倒吸。
(2)浓硫酸的作用是催化剂和吸水剂;Na2CO3的作用是吸收乙醇、中和乙酸,降低酯的溶解度。
(3)否,乙酸乙酯在NaOH溶液中可以水解。
实验步骤 (1)
(2) 振荡均匀后,把三支试管都放入70~80 ℃的水浴里加热
实验现象 A中液体仍然分层,气味不消失;
B中液体酯层逐渐 ,气味渐渐 ;
C中液体酯层和气味消失的比B____
实验结论 乙酸乙酯在酸性和碱性条件下均发生水解,在碱性条件下水解的_____
消失
消失
快
更快
实验步骤 实验现象
(1) (2)振荡均匀后,把三支试管都放入70~80 ℃的水浴里加热
实验结论 A中液体仍然分层,气味不消失;
B中液体酯层逐渐消失,气味渐渐消失;
C中液体酯层和气味消失的比B快
乙酸乙酯在酸性和碱性条件下均发生水解,在碱性条件下水解的最快。
2.乙酸乙酯的水解
【思考与讨论】
3.通过乙酸乙酯的水解实验,你得出什么结论?
【提示】乙酸乙酯水解需要酸性或碱性条件,碱性条件水解速率大且完全。
4.乙酸乙酯的水解实验,除了通过乙酸乙酯气味消失的快慢来比较酯的水解速率外,还有什么方法可用来比较乙酸乙酯在不同条件下水解速率的差异?
【提示】间隔相同时间内测量并比较剩余乙酸乙酯层的高度。
5.乙酸乙酯在酸性和碱性条件下水解速率和程度不同的原因是什么
【提示】如果是在酸性环境中,乙酸乙酯水解会产生乙酸和乙醇的反应是可逆的,产物不断堆积,水解就会受到抑制,速度就慢了;
如果在碱性环境中,这个反应不是可逆的,因为产生的产物乙酸和碱反应,因此反应可以不断进行下去。
酯化反应 水解
反应关系 催化剂 浓H2SO4 稀H2SO4或NaOH溶液
催化剂的其他作用 吸水,提高乙酸和乙醇的转化率 NaOH中和酯水解生成的乙酸,提高酯的水解率
反应类型 酯化反应,取代反应 水解反应,取代反应
酯化反应和酯水解反应的比较
1. 1-丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度为115~125℃,反应装置如图所示,下列对该实验的描述错误的是( )
A.不能用水浴加热
B.长玻璃管起冷凝回流作用
C.提纯乙酸丁酯需要经过水、NaOH溶液洗涤
D.加入过量乙酸可以提高1 丁醇的转化率
C
2.某羧酸酯的分子式为C18H26O5,1 mol该酯完全水解可得到1 mol羧酸和2 mol乙醇,该羧酸的分子式为( )
A.C14H18O5 B.C14H16O4
C.C16H22O5 D.C16H20O5
A
实验活动1:乙酸乙酯的制备与性质
第三章 烃的衍生物
厨师烧鱼时常加醋并加点酒,鱼的味道就变得香醇,特别鲜美。为什么呢?
1.了解示踪原子法在酯化反应反应机理分析中的应用。(科学探究与创新意识)
2.能通过实验探究乙酸乙酯在中性、酸性和碱性溶液及不同温度下的水解速率,分析并根据化学平衡移动原理解释原因。(科学探究与创新意识)
1.学习制备乙酸乙酯的方法。
2.加深对酯化反应和酯的水解的认识。
体会课堂探究的乐趣,
汲取新知识的营养,
让我们一起 吧!
进
走
课
堂
【实验仪器】
试管、试管夹、烧杯、量筒、胶头滴管、玻璃导管、乳胶管、橡胶塞、铁架台、酒精灯、火柴、秒表、碎瓷片。
【实验药品】
乙醇、乙酸、浓硫酸、饱和Na2CO3溶液、蒸馏水、3mol/LH2SO4溶液、6mol/LNaOH溶液。
【实验原理】
1.酯化反应:
CH3-C-O-H + H-O-C2H5 CH3-C-O-C2H5 +H2O
=
O
O
=
2.酯的水解:
酸性条件:
碱性条件:
CH3COOH+C2H5OH
CH3COOC2H5+H2O
稀硫酸
CH3COONa+C2H5OH
CH3COOC2H5+NaOH
【实验步骤】
1.乙酸乙酯的制备
实验步骤 实验现象
(1)在一支试管中加入2 mL乙醇,然后边振荡试管边慢慢加入0.5 mL浓硫酸和2 mL乙酸,再加入几片碎瓷片。在另一支试管中加入3 mL饱和Na2CO3溶液。
(2)用小火加热试管里的混合物,将产生的蒸气经导管通到饱和Na2CO3溶液的上方约0.5 cm处,注意观察试管内的变化。反应一段时间后,取下盛有Na2CO3溶液的试管,并停止加热
(3)振荡盛有Na2CO3溶液的试管,静置。待溶液分层后,观察上层的油状液体,并注意闻气味
饱和碳酸钠溶液的液面上有无色透明的难溶于水的油状液体产生
可闻到香味
【思考与讨论】
1.在乙酸乙酯的制备实验中,试剂添加顺序如何?加入碎瓷片的作用是什么?为什么不用大火加热而用小火加热?
【提示】在试管中加入乙醇,然后边振荡边加慢慢加入浓硫酸,最后加入乙酸。
碎瓷片的作用是防止暴沸;大火加热,乙醇、乙酸容易挥发,利用率减小。
2.(1)在乙酸乙酯的制备实验中,导管不能插入饱和Na2CO3溶液的原因是什么?
(2)浓硫酸和Na2CO3的作用是什么?
(3)吸收乙酸乙酯能否用NaOH溶液代替Na2CO3溶液?为什么?
【提示】(1)防止倒吸。
(2)浓硫酸的作用是催化剂和吸水剂;Na2CO3的作用是吸收乙醇、中和乙酸,降低酯的溶解度。
(3)否,乙酸乙酯在NaOH溶液中可以水解。
实验步骤 (1)
(2) 振荡均匀后,把三支试管都放入70~80 ℃的水浴里加热
实验现象 A中液体仍然分层,气味不消失;
B中液体酯层逐渐 ,气味渐渐 ;
C中液体酯层和气味消失的比B____
实验结论 乙酸乙酯在酸性和碱性条件下均发生水解,在碱性条件下水解的_____
消失
消失
快
更快
实验步骤 实验现象
(1) (2)振荡均匀后,把三支试管都放入70~80 ℃的水浴里加热
实验结论 A中液体仍然分层,气味不消失;
B中液体酯层逐渐消失,气味渐渐消失;
C中液体酯层和气味消失的比B快
乙酸乙酯在酸性和碱性条件下均发生水解,在碱性条件下水解的最快。
2.乙酸乙酯的水解
【思考与讨论】
3.通过乙酸乙酯的水解实验,你得出什么结论?
【提示】乙酸乙酯水解需要酸性或碱性条件,碱性条件水解速率大且完全。
4.乙酸乙酯的水解实验,除了通过乙酸乙酯气味消失的快慢来比较酯的水解速率外,还有什么方法可用来比较乙酸乙酯在不同条件下水解速率的差异?
【提示】间隔相同时间内测量并比较剩余乙酸乙酯层的高度。
5.乙酸乙酯在酸性和碱性条件下水解速率和程度不同的原因是什么
【提示】如果是在酸性环境中,乙酸乙酯水解会产生乙酸和乙醇的反应是可逆的,产物不断堆积,水解就会受到抑制,速度就慢了;
如果在碱性环境中,这个反应不是可逆的,因为产生的产物乙酸和碱反应,因此反应可以不断进行下去。
酯化反应 水解
反应关系 催化剂 浓H2SO4 稀H2SO4或NaOH溶液
催化剂的其他作用 吸水,提高乙酸和乙醇的转化率 NaOH中和酯水解生成的乙酸,提高酯的水解率
反应类型 酯化反应,取代反应 水解反应,取代反应
酯化反应和酯水解反应的比较
1. 1-丁醇和乙酸在浓硫酸作用下,通过酯化反应制得乙酸丁酯,反应温度为115~125℃,反应装置如图所示,下列对该实验的描述错误的是( )
A.不能用水浴加热
B.长玻璃管起冷凝回流作用
C.提纯乙酸丁酯需要经过水、NaOH溶液洗涤
D.加入过量乙酸可以提高1 丁醇的转化率
C
2.某羧酸酯的分子式为C18H26O5,1 mol该酯完全水解可得到1 mol羧酸和2 mol乙醇,该羧酸的分子式为( )
A.C14H18O5 B.C14H16O4
C.C16H22O5 D.C16H20O5
A
