第3章测评--2025鲁科版化学必修第二册同步练习题(含答案)
文档属性
| 名称 | 第3章测评--2025鲁科版化学必修第二册同步练习题(含答案) |  | |
| 格式 | docx | ||
| 文件大小 | 730.1KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-24 09:28:04 | ||
图片预览




文档简介
中小学教育资源及组卷应用平台
2025鲁科版化学必修第二册
第3章测评
一、选择题(本题包括10个小题,每小题2分,共20分。每小题只有一个选项符合题意)
1.下列说法正确的是( )
A.糖类、油脂、蛋白质均可以水解
B.葡萄糖和蔗糖不互为同分异构体,但互为同系物
C.等质量的乙烯、甲烷分别充分燃烧,甲烷消耗氧气的量多
D.在加热、甲醛、饱和(NH4)2SO4溶液、X射线作用下,蛋白质都会发生变性
2.(2024福建福州延安中学第二学期高一期中质量检测)下列化学用语表达正确的是( )
A.甲烷空间填充模型:
B.乙烯的结构简式:CH2CH2
C.CCl4的电子式:ClCl
D.苯的球棍模型:
3.设NA为阿伏加德罗常数的值,下列说法正确的是 ( )
A.17 g —OH(羟基)中含有的电子数为7NA
B.标准状况下,11.2 L乙醇中含H—O键数目为0.5NA
C.常温常压下,1 mol甲烷和乙烯的混合物完全燃烧,产生的CO2分子数目为1.5NA
D.1 mol甲烷与1 mol氯气光照条件下充分反应产生的HCl分子数目为1NA
4.(2024河北沧州运东四校高一下学期期中)下列关于煤和石油的说法错误的是( )
A.煤和石油均是混合物,属于传统能源
B.石油裂化和裂解的主要目的都是得到重要产品乙烯
C.新型煤化工以生产清洁能源和可替代石油化工的产品为主
D.煤化工和石油化工均可以制得汽油
5.下列叙述错误的是( )
A.1 mol CH2CH2先与HCl发生加成反应,再与Cl2发生取代反应,最多消耗Cl2 2.5 mol
B.实验室中可用如图所示方法除去CH3CH3气体中的CH2CH2气体
C.实验室中可用酸性KMnO4溶液鉴别CH3CH3气体和CH2CH2气体
D.工业上可利用CH2CH2与HCl的加成反应制得纯净的CH3CH2Cl
6.(2024山东烟台第一中学高一检测)用括号内的试剂和分离方法除去下列物质中的少量杂质,不正确的是 ( )
A.乙酸乙酯中混有乙酸(饱和Na2CO3溶液,分液)
B.乙醇中混有乙酸(NaOH溶液,蒸馏)
C.甲烷中混有乙烯(溴的四氯化碳溶液,分液)
D.溴苯中混有溴(NaOH溶液,分液)
7.(2024河南周口恒大中学高一月考)酯化反应是酸与醇反应生成酯和水的反应,如乙酸与乙醇在浓硫酸催化作用下生成乙酸乙酯和水的反应就是酯化反应。下列关于酯化反应的说法正确的是( )
A.属于中和反应
B.属于取代反应
C.酸分子中去氢原子
D.醇分子中去羟基
8.有机物X为合成光刻胶的一种中间体,其结构简式如图所示。下列有关说法中正确的是( )
A.2 mol该物质能与足量Na反应生成22.4 L H2
B.1 mol该物质中含有4 mol碳碳双键
C.在一定条件下该物质能合成有机高分子化合物
D.该物质能使溴水褪色,但不能使酸性高锰酸钾溶液褪色
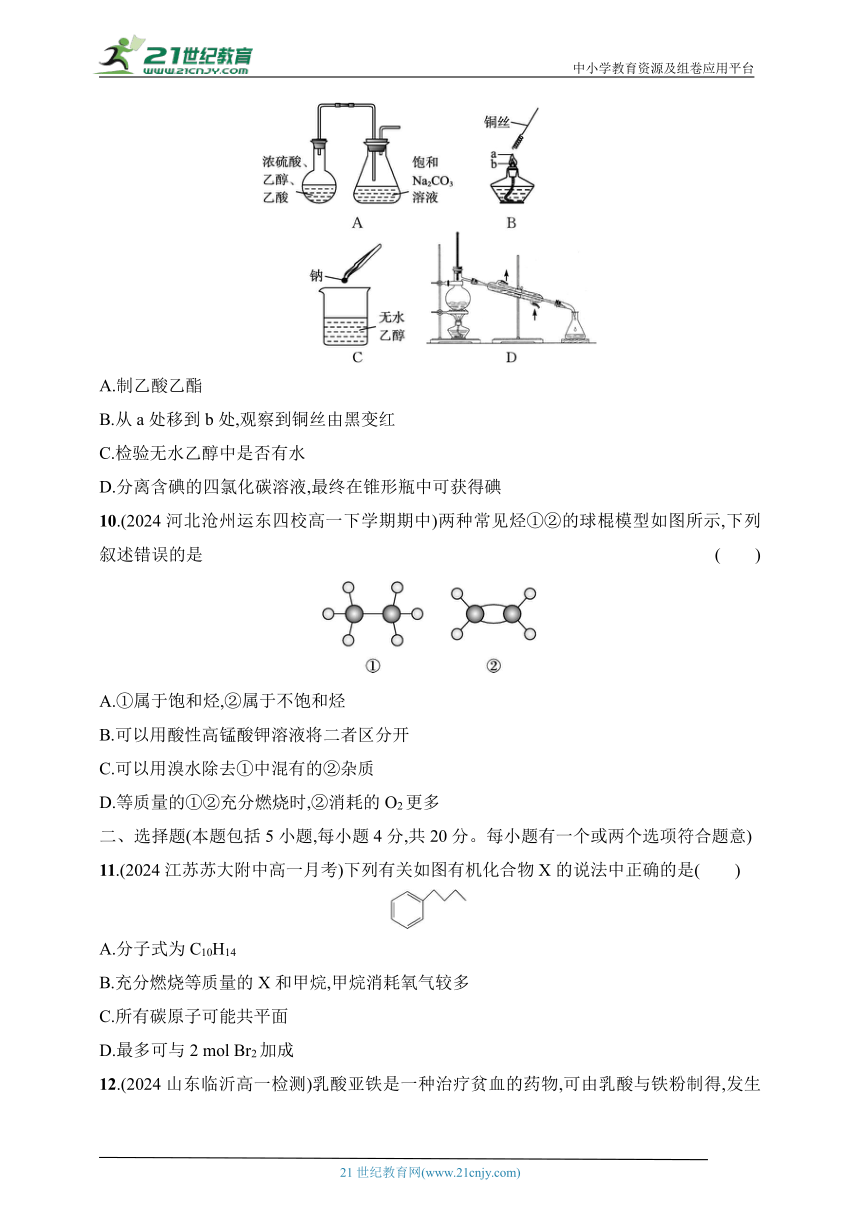
9.(2024山东菏泽高一检测)下列实验能达到预期目的的是( )
A.制乙酸乙酯
B.从a处移到b处,观察到铜丝由黑变红
C.检验无水乙醇中是否有水
D.分离含碘的四氯化碳溶液,最终在锥形瓶中可获得碘
10.(2024河北沧州运东四校高一下学期期中)两种常见烃①②的球棍模型如图所示,下列叙述错误的是 ( )
A.①属于饱和烃,②属于不饱和烃
B.可以用酸性高锰酸钾溶液将二者区分开
C.可以用溴水除去①中混有的②杂质
D.等质量的①②充分燃烧时,②消耗的O2更多
二、选择题(本题包括5小题,每小题4分,共20分。每小题有一个或两个选项符合题意)
11.(2024江苏苏大附中高一月考)下列有关如图有机化合物X的说法中正确的是( )
A.分子式为C10H14
B.充分燃烧等质量的X和甲烷,甲烷消耗氧气较多
C.所有碳原子可能共平面
D.最多可与2 mol Br2加成
12.(2024山东临沂高一检测)乳酸亚铁是一种治疗贫血的药物,可由乳酸与铁粉制得,发生反应的化学方程式如下:+Fe+X。下列说法错误的是 ( )
A.乳酸在一定条件下可生成六元环酯
B.乳酸与乳酸亚铁均具有良好的水溶性
C.X分子中只含有非极性键,该反应中乳酸既表现出酸性又表现出氧化性
D.1 mol乳酸与足量Na或Na2CO3反应均产生1 mol气体
13.制备乙酸乙酯的绿色合成路线之一为
下列说法不正确的是( )
A.M的分子式为C6H10O6
B.N的结构简式为CH3COOH
C.④的反应类型属于取代反应
D.淀粉与纤维素互为同分异构体
14.富马酸亚铁是一种用于治疗缺铁性贫血的药物。富马酸亚铁的制备反应如图所示,下列说法不正确的是( )
A.丁烯二酸与足量乙醇发生酯化反应可以生成C8H12O4
B.b的结构简式为NaOOCHCCHCOONa,难溶于水
C.富马酸亚铁易被氧化变质,应密封保存
D.富马酸亚铁与足量溴水反应时,仅发生碳碳双键与溴水的加成反应
15.已知醛基(—CHO)可被氧化成羧基(—COOH),已知气态烃A的密度是相同状况下氢气密度的14倍,有机物A~E能发生如图所示一系列变化,则下列说法错误的是( )
A.A分子中所有原子均在同一平面内
B.B分子的同分异构体有1种
C.C的水溶液又称福尔马林,具有杀菌、防腐性能
D.等物质的量的B、D与足量钠反应生成气体的量相等
三、非选择题(本题包括5小题,共60分)
16.(12分)(2024福建福州延安中学第二学期高一期中质检)回答下列问题。
(1)下列各组物质中,互为同位素的是 (填序号,下同);互为同素异形体的是 ;互为同系物的是 ;互为同分异构体的是 ;属于同一种物质的是 。
H和H;②CH4和CH3CH2CH3;
③和;④石墨和金刚石;
⑤正丁烷(CH3CH2CH2CH3)和异丁烷()
(2)乙烯水合法也是一种制备乙醇的方法,用该方法制备乙醇时,乙烯和水发生了 反应(填反应类型)。反应的化学方程式: 。
17.(12分)0.2 mol某烃A在氧气中充分燃烧后,生成化合物B、C各1.2 mol。
(1)烃A的分子式是 。
(2)若取一定量的烃A充分燃烧后,生成B、C各3 mol,则有 g的A参加了反应,燃烧时消耗标准状况下的氧气 L。
(3)若烃A不能使溴水褪色,但在一定条件下能与氯气发生取代反应,其一氯代物只有一种,则烃A的结构简式是 。
(4)若烃A能使溴水褪色,在催化剂作用下与H2发生加成反应后生成,则A的结构简式为 。
(5)若烃A能使溴水褪色,且分子中所有碳原子共平面,则A的结构简式为 。
(6)比A少2个碳原子的A的烯烃的同系物的同分异构体共有 种。
18.(12分)A是气态烃,标准状况下气体密度为1.25 g·L-1,G是高分子化合物,如图所示是与A有关的转化。
回答下列问题。
(1)F的结构式为 。
(2)已知A也可以与D在催化剂作用下生成E,写出该反应的化学方程式: 。
(3)写出与D互为同分异构体,且含醛基()的物质I的结构简式: 。
(4)写出H→B的化学方程式: 。
(5)下列说法正确的是 (填字母)。
A.46 g B与足量钠反应可以得到11.2 L氢气(在0 ℃、101 kPa的条件下)
B.B可用作燃料,缓解化石燃料的危机
C.可用碳酸钠溶液鉴别B、D、E三种有机化合物
D.G可与溴水因发生加成反应而使溴水褪色
19.(12分)有机化合物的世界缤纷多彩,根据题目信息回答下列问题。
(1)1 mol苯乙烯()最多能与 mol H2发生加成反应,该反应的产物与氯气在光照条件下反应,其一氯代物有 种。
(2)苯乙烯生成高聚物D的化学方程式为 。
(3)苯乙烯与水反应生成的C中含有甲基,则C的结构简式为 。
(4)某种燃料电池的工作原理示意图如图所示,a、b均为惰性电极。
假设使用的“燃料”是二甲醚(CH3OCH3),则a极的电极反应式为 。
20.(12分)某制糖厂以甘蔗为原料制糖,同时得到大量的甘蔗渣,对甘蔗渣进行综合利用不仅可以提高综合效益,而且还能防止环境污染,生产流程如下:
已知石油裂解已成为生产H的主要方法,E为乙醇催化氧化的产物,G是具有果香味的液体,试回答下列问题。
(1)F中所含官能团的名称是 。
(2)G的结构简式为 。
(3)写出D→E的化学方程式,并注明反应类型: ,
。
(4)F→G的反应装置如图所示。
①图中球形干燥管的作用是 。
②试管Ⅱ中加有饱和Na2CO3溶液,其作用是 。
③分子结构中具有一个羟基的化合物M 10 g,与F反应生成有机产物11.85 g,并回收了未反应的M 1.3 g,则M的相对分子质量为 。
第3章测评
1.C 解析 糖类中的单糖不能发生水解反应,而糖类中的其他糖、油脂、蛋白质均可以水解,A错误;葡萄糖的分子式为C6H12O6,蔗糖的分子式为C12H22O11,分子式不同,不互为同分异构体,结构也不相似,组成上也不是相差CH2的整数倍,故不互为同系物,B错误;由于CH4中氢元素的质量分数高于乙烯中氢元素的质量分数,故等质量的乙烯、甲烷分别充分燃烧,甲烷消耗氧气的量多,C正确;在加热、甲醛、X射线作用下,蛋白质都会发生变性,而加入饱和(NH4)2SO4溶液,则是蛋白质发生盐析,D错误。
2.A 解析 甲烷空间填充模型:,A正确;乙烯的结构简式:CH2CH2,B错误;CCl4的电子式:,C错误;是苯的空间填充模型,D错误。
3.D 解析 17 g —OH(羟基)中含有的电子数为(8+1)NA=9NA,故A错误;标准状况下,乙醇呈液态,不能用气体摩尔体积计算其物质的量,故B错误;常温常压下,1 mol甲烷和乙烯的混合物完全燃烧,产生的CO2分子数目为1NA到2NA之间,故C错误;1 mol甲烷含4 mol H(过量),与1 mol氯气光照条件下充分反应产生的HCl分子数目为1NA,故D正确。
4.B 解析 煤和石油中均含有多种物质,是混合物,属于传统能源,A正确;石油裂化得到的是轻质汽油,裂解得到的是乙烯等气态烃,B错误;新型煤化工以生产清洁能源和可替代石油化工的产品为主,如煤制甲醇、煤制烯烃、煤制天然气、煤制乙二醇和煤制油等,C正确;煤化工和石油化工均可制取汽油,D正确。
5.A 解析 1 mol CH2CH2先与HCl发生加成反应生成1 mol一氯乙烷,分子中含有5 mol H原子,再与Cl2发生取代反应,最多消耗5 mol Cl2,故A错误;乙烷与溴水不反应,乙烯与溴水发生加成反应生成1,2-二溴乙烷,可用溴水除去CH3CH3气体中的CH2CH2气体,故B正确;CH3CH3与酸性高锰酸钾溶液不反应,CH2CH2能被酸性高锰酸钾溶液氧化,乙烯使酸性高锰酸钾溶液褪色,实验室中可用酸性KMnO4溶液鉴别CH3CH3气体和CH2CH2气体,故C正确;CH2CH2与HCl发生加成反应的产物只有CH3CH2Cl,工业上可利用CH2CH2与HCl的加成反应制得纯净的CH3CH2Cl,故D正确。
6.C 解析 用饱和Na2CO3溶液除去乙酸乙酯中的乙酸,然后使用分液的方法分离有机层和水层,A正确;氢氧化钠和乙醇不反应,和乙酸反应生成乙酸钠,然后利用乙醇沸点较低的性质,蒸馏得到乙醇,B正确;乙烯可以与溴反应而进入溶液,甲烷为气体逸出,不需分液,C错误;氢氧化钠不与溴苯反应、与溴反应生成盐溶液,然后使用分液的方法分离有机层和水层,D正确。
7.B 解析 酯化反应是醇与酸的反应,属于取代反应,但不属于中和反应,A错误,B正确;酯化反应中酸分子中去—OH,C错误;酯化反应中醇分子中去—H,D错误。
8.C 解析 羟基能与Na反应生成H2,但未说明标准状况,因此生成H2的体积无法计算,A错误;苯环中没有碳碳双键,1 mol该物质中含有1 mol碳碳双键,B错误;该分子中含有碳碳双键,可以发生加聚反应合成有机高分子化合物,C正确;羟基和碳碳双键均可以使酸性高锰酸钾溶液褪色,D错误。
9.B 解析 制备乙酸乙酯时需要加热,图中无加热装置,实验不能达到预期目的,故A不选;铜丝在外焰a处受热与氧气反应生成黑色的氧化铜,移到内焰b处时,黑色的氧化铜在加热条件下与乙醇蒸气反应生成红色的铜、乙醛和水,则从a处移到b处,观察到铜丝由黑变红,实验能达到预期目的,故B选;乙醇和水均能与金属钠反应生成氢气,无法检验无水乙醇中是否有水,实验不能达到预期目的,可选用无水硫酸铜检验无水乙醇中是否有水,故C不选;碘的沸点高于四氯化碳,且碘易升华,要将碘单质从碘的四氯化碳溶液中提取出来应该用反萃取法,故D不选。
10.D 解析 由题中球棍模型可知,①为乙烷,②为乙烯,据此作答。乙烷属于饱和烃,乙烯属于不饱和烃,A项正确;乙烷不能使酸性高锰酸钾溶液褪色,而乙烯含有碳碳双键,可以被酸性高锰酸钾溶液氧化,从而使酸性高锰酸钾溶液褪色,B项正确;乙烷不能与溴水反应,但乙烯可以与溴水发生加成反应生成油状液体,因此可以用溴水除去乙烷中的乙烯,C项正确;烃(CxHy)在足量的氧气中充分燃烧的化学方程式为CxHy+(x+)O2xCO2+H2O,假设质量都为1 g,则乙烷(C2H6)的物质的量为 mol,由化学方程式可知,消耗O2的物质的量为 mol≈0.116 7 mol,乙烯(C2H4)的物质的量为 mol,消耗O2的物质的量为 mol=0.107 1 mol,所以消耗O2更多的是①乙烷,D项错误。
11.AB 解析 由图可知,分子式为C10H14,A正确。等质量的烃耗氧量由氢原子与碳原子个数比决定,个数比越大耗氧量越多;充分燃烧等质量的X和甲烷,甲烷消耗氧气较多,B正确。分子中含一个正丁基,其所含有的4个碳原子均为饱和碳原子,则所有碳原子不共平面,C错误。分子除苯环外不含不饱和键,不能与溴单质加成,D错误。
12.D 解析 乳酸分子中既含有羟基也含有羧基,在一定条件下可生成六元环酯,其结构简式是
,A正确;乳酸中既含有羟基也含有羧基,乳酸亚铁中含有羟基,二者均具有良好的水溶性,B正确;乳酸与铁反应生成乳酸亚铁和氢气,X应为氢气,含有非极性键,乳酸结构中有羧基,具有酸性,乳酸与铁反应生成氢气,氢元素化合价降低,表现氧化性,C正确;1个乳酸分子中含有1个羟基和1个羧基,1 mol乳酸与足量Na反应生成1 mol H2,乳酸与足量Na2CO3反应时,不生成气体,D错误。
13.AD 解析 淀粉和纤维素水解产物最终为葡萄糖(C6H12O6),A选项错误;葡萄糖在酒化酶作用下发生发酵反应:C6H12O62CH3CH2OH+2CO2↑,乙醇能够转化为乙酸,二者反应生成乙酸乙酯,所以N为乙酸,B选项正确;乙醇与乙酸发生酯化反应(本质是取代反应)生成乙酸乙酯,C选项正确;淀粉和纤维素的分子式都是(C6H10O5)n,但是两者的n值不相同,所以分子式不同,不是同分异构体,D选项错误。
14.BD 解析 HOOCHCCHCOOH与足量乙醇发生酯化反应生成丁烯二酸二乙酯,分子式为C8H12O4,A正确;HOOCHCCHCOOH与碳酸氢钠反应生成
NaOOCHCCHCOONa,易溶于水,B错误;富马酸亚铁中的Fe2+易被氧化,保存时应该密封保存,防止被氧化,C正确;富马酸亚铁与足量溴水反应时,碳碳双键与Br2加成,Fe2+也能被Br2氧化,D错误。
15.C 解析 依题意可得气态烃A的相对分子质量为28,即A为乙烯,由连续催化氧化可知,B为乙醇,C为乙醛,D为乙酸,E为乙酸乙酯。乙烯为平面结构,所有原子在同一平面内,A项正确;B为乙醇,其同分异构体为二甲醚(CH3OCH3),B项正确;1 mol CH3CH2OH和1 mol CH3COOH与足量钠反应,都生成0.5 mol H2,D项正确。
16.答案 (1)① ④ ② ⑤ ③
(2)加成 CH2CH2+H2OCH3CH2OH
解析 (1)质子数相同、中子数不同的同一种元素的不同核素互为同位素H和H互为同位素,答案选①;由同一种元素形成的不同单质互为同素异形体,石墨和金刚石互为同素异形体,答案选④;结构相似,分子式组成相差若干个CH2原子团的有机化合物互为同系物,甲烷和丙烷互为同系物,答案选②;分子式相同,结构不同的化合物互为同分异构体,正丁烷(CH3CH2CH2CH3)和异丁烷()互为同分异构体,答案选⑤;结构和性质完全都相同的是同一种物质,和是同一物质,答案选③。
(2)乙烯水合法制备乙醇的方程式为CH2CH2+H2OCH3CH2OH,根据化学方程式,可知用该方法制备乙醇时,乙烯和水发生加成反应。
17.答案 (1)C6H12 (2)42 100.8
(3) (4)
(5) (6)3
解析 (1)根据0.2 mol烃充分燃烧生成1.2 mol CO2和1.2 mol H2O,所以n(烃)∶n(C)∶n(H)=0.2 mol∶1.2 mol∶2.4 mol=1∶6∶12,所以分子式为C6H12。
(2)由C6H12 + 9O26CO2 +6H2O
1 mol 9 mol 6 mol
n(A) n(O2) 3 mol
得n(A)=0.5 mol,质量为0.5 mol×84 g·mol-1=42 g;n(O2)=4.5 mol,标准状况下的体积为4.5 mol×22.4 L·mol-1=100.8 L。
(3)烃A不能使溴水褪色,说明分子中无碳碳双键,只能是环状烃,一氯代物只有一种,只能是环己烷。
(4)烃A能使溴水褪色,说明A中含有碳碳双键,其加成产物为,则A的结构简式只能为。
(5)因A能使溴水褪色,说明A为烯烃,且所有碳原子共平面,结合乙烯分子共平面,得出A为。
(6)比A少2个碳原子的A的烯烃的同系物为C4H8,其烯烃类的同分异构体可为CH3CHCHCH3、
CH2CH—CH2CH3、,共3种。
18.答案 (1)
(2)CH2CH2+CH3COOHCH3COOCH2CH3
(3)HOCH2CHO或HCOOCH3
(4)CH2OH(CHOH)4CHO2CH3CH2OH+2CO2↑
(5)ABC
解析 由题干已知信息和转化流程图可知,A是气态烃,标准状况下气体密度为1.25 g·L-1,则A的摩尔质量为1.25 g·L-1×22.4 L·mol-1=28 g·mol-1,即A的相对分子质量为28,28÷12=2……4,A的分子式为C2H4,结构简式为
CH2CH2。A在催化剂、加热、加压条件下与H2O发生加成反应生成乙醇,B的结构简式为CH3CH2OH。乙醇催化氧化生成乙醛,C的结构简式为CH3CHO。乙醛催化氧化为乙酸,D的结构简式为CH3COOH。乙醇和乙酸在浓硫酸催化下加热生成乙酸乙酯,E的结构简式为CH3COOCH2CH3。乙烯和Br2的CCl4溶液发生加成反应生成1,2-二溴乙烷,F的结构简式为BrCH2CH2Br。乙烯催化转化为高分子化合物G,G的结构简式为 CH2—CH2 。淀粉在稀硫酸催化下发生水解反应生成葡萄糖,H的结构简式为CH2OH(CHOH)4CHO。葡萄糖在酶的催化作用下转化为酒精即乙醇。
(5)由分析可知,B为CH3CH2OH,46 g B的物质的量为=1 mol,根据反应方程式2CH3CH2OH+2Na2CH3CH2ONa+H2↑可知,与足量钠反应可以得到0.5 mol,即标准状况下0.5 mol×22.4 L·mol-1=11.2 L氢气,A正确;CH3CH2OH可用作燃料,乙醇汽油能够缓解化石燃料的危机,B正确;B、D、E分别为CH3CH2OH、CH3COOH、CH3COOCH2CH3,向三种有机物中加入饱和碳酸钠溶液可以分别观察到形成均一的溶液、产生大量的无色气泡、出现分层,故可用碳酸钠溶液鉴别B、D、E三种有机化合物,C正确;G的结构简式为
,分子中不含碳碳双键等不饱和键,故G不可与溴水因发生加成反应而使溴水褪色,D错误。
19.答案 (1)4 6
(2)n
(3)
(4)CH3OCH3-12e-+16OH-2C+11H2O
解析 在催化剂和加热条件下与足量的H2发生加成反应生成A为;与Br2的CCl4溶液发生加成反应生成B为;结合题干(3)可知在催化剂和加热条件下与H2O发生加成反应生成的C为;在催化剂和加热条件下发生加聚反应生成的高聚物D为。(1)苯环和碳碳双键均可以与氢气发生加成反应,则1 mol苯乙烯()最多能与4 mol H2发生加成反应,生成,有6种类型的氢原子,则与氯气在光照条件下反应,其一氯代物有6种。(2)苯乙烯中含有碳碳双键,通过加聚反应得到高聚物D,其反应的化学方程式为
n。(3)由以上分析可知C的结构简式为。(4)燃料电池中燃料在负极失去电子,发生氧化反应,结合电子移动方向,则a极为二甲醚(CH3OCH3)失去电子在碱性条件下转化为碳酸盐,电极反应式为CH3OCH3-12e-+16OH-2C+11H2O。
20.答案 (1)羧基
(2)CH3COOC2H5(或CH3COOCH2CH3)
(3)2CH3CH2OH+O22CH3CHO+2H2O 氧化反应
(4)①防倒吸 ②溶解乙醇、与乙酸反应、降低乙酸乙酯的溶解度 ③116
解析 (1)F为乙酸,官能团为羧基。(2)G为乙酸乙酯,结构简式为CH3COOC2H5(或CH3COOCH2CH3)。(3)D→E的反应为醇的催化氧化,化学方程式为2CH3CH2OH+O22CH3CHO+2H2O,反应类型为氧化反应。(4)①球形干燥管容积较大,起到防倒吸的作用;②试管Ⅱ中加饱和Na2CO3溶液的作用是溶解乙醇、与乙酸反应、降低乙酸乙酯的溶解度;③设该化合物为ROH,其相对分子质量为x,实际参加反应的M的质量为10 g-1.3 g=8.7 g,则反应的化学方程式可表示为:
ROH+CH3COOHCH3COOR+H2O ΔMr
x x+42 42
8.7 g 11.85 g 11.85 g-
8.7 g
解得x=116。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
2025鲁科版化学必修第二册
第3章测评
一、选择题(本题包括10个小题,每小题2分,共20分。每小题只有一个选项符合题意)
1.下列说法正确的是( )
A.糖类、油脂、蛋白质均可以水解
B.葡萄糖和蔗糖不互为同分异构体,但互为同系物
C.等质量的乙烯、甲烷分别充分燃烧,甲烷消耗氧气的量多
D.在加热、甲醛、饱和(NH4)2SO4溶液、X射线作用下,蛋白质都会发生变性
2.(2024福建福州延安中学第二学期高一期中质量检测)下列化学用语表达正确的是( )
A.甲烷空间填充模型:
B.乙烯的结构简式:CH2CH2
C.CCl4的电子式:ClCl
D.苯的球棍模型:
3.设NA为阿伏加德罗常数的值,下列说法正确的是 ( )
A.17 g —OH(羟基)中含有的电子数为7NA
B.标准状况下,11.2 L乙醇中含H—O键数目为0.5NA
C.常温常压下,1 mol甲烷和乙烯的混合物完全燃烧,产生的CO2分子数目为1.5NA
D.1 mol甲烷与1 mol氯气光照条件下充分反应产生的HCl分子数目为1NA
4.(2024河北沧州运东四校高一下学期期中)下列关于煤和石油的说法错误的是( )
A.煤和石油均是混合物,属于传统能源
B.石油裂化和裂解的主要目的都是得到重要产品乙烯
C.新型煤化工以生产清洁能源和可替代石油化工的产品为主
D.煤化工和石油化工均可以制得汽油
5.下列叙述错误的是( )
A.1 mol CH2CH2先与HCl发生加成反应,再与Cl2发生取代反应,最多消耗Cl2 2.5 mol
B.实验室中可用如图所示方法除去CH3CH3气体中的CH2CH2气体
C.实验室中可用酸性KMnO4溶液鉴别CH3CH3气体和CH2CH2气体
D.工业上可利用CH2CH2与HCl的加成反应制得纯净的CH3CH2Cl
6.(2024山东烟台第一中学高一检测)用括号内的试剂和分离方法除去下列物质中的少量杂质,不正确的是 ( )
A.乙酸乙酯中混有乙酸(饱和Na2CO3溶液,分液)
B.乙醇中混有乙酸(NaOH溶液,蒸馏)
C.甲烷中混有乙烯(溴的四氯化碳溶液,分液)
D.溴苯中混有溴(NaOH溶液,分液)
7.(2024河南周口恒大中学高一月考)酯化反应是酸与醇反应生成酯和水的反应,如乙酸与乙醇在浓硫酸催化作用下生成乙酸乙酯和水的反应就是酯化反应。下列关于酯化反应的说法正确的是( )
A.属于中和反应
B.属于取代反应
C.酸分子中去氢原子
D.醇分子中去羟基
8.有机物X为合成光刻胶的一种中间体,其结构简式如图所示。下列有关说法中正确的是( )
A.2 mol该物质能与足量Na反应生成22.4 L H2
B.1 mol该物质中含有4 mol碳碳双键
C.在一定条件下该物质能合成有机高分子化合物
D.该物质能使溴水褪色,但不能使酸性高锰酸钾溶液褪色
9.(2024山东菏泽高一检测)下列实验能达到预期目的的是( )
A.制乙酸乙酯
B.从a处移到b处,观察到铜丝由黑变红
C.检验无水乙醇中是否有水
D.分离含碘的四氯化碳溶液,最终在锥形瓶中可获得碘
10.(2024河北沧州运东四校高一下学期期中)两种常见烃①②的球棍模型如图所示,下列叙述错误的是 ( )
A.①属于饱和烃,②属于不饱和烃
B.可以用酸性高锰酸钾溶液将二者区分开
C.可以用溴水除去①中混有的②杂质
D.等质量的①②充分燃烧时,②消耗的O2更多
二、选择题(本题包括5小题,每小题4分,共20分。每小题有一个或两个选项符合题意)
11.(2024江苏苏大附中高一月考)下列有关如图有机化合物X的说法中正确的是( )
A.分子式为C10H14
B.充分燃烧等质量的X和甲烷,甲烷消耗氧气较多
C.所有碳原子可能共平面
D.最多可与2 mol Br2加成
12.(2024山东临沂高一检测)乳酸亚铁是一种治疗贫血的药物,可由乳酸与铁粉制得,发生反应的化学方程式如下:+Fe+X。下列说法错误的是 ( )
A.乳酸在一定条件下可生成六元环酯
B.乳酸与乳酸亚铁均具有良好的水溶性
C.X分子中只含有非极性键,该反应中乳酸既表现出酸性又表现出氧化性
D.1 mol乳酸与足量Na或Na2CO3反应均产生1 mol气体
13.制备乙酸乙酯的绿色合成路线之一为
下列说法不正确的是( )
A.M的分子式为C6H10O6
B.N的结构简式为CH3COOH
C.④的反应类型属于取代反应
D.淀粉与纤维素互为同分异构体
14.富马酸亚铁是一种用于治疗缺铁性贫血的药物。富马酸亚铁的制备反应如图所示,下列说法不正确的是( )
A.丁烯二酸与足量乙醇发生酯化反应可以生成C8H12O4
B.b的结构简式为NaOOCHCCHCOONa,难溶于水
C.富马酸亚铁易被氧化变质,应密封保存
D.富马酸亚铁与足量溴水反应时,仅发生碳碳双键与溴水的加成反应
15.已知醛基(—CHO)可被氧化成羧基(—COOH),已知气态烃A的密度是相同状况下氢气密度的14倍,有机物A~E能发生如图所示一系列变化,则下列说法错误的是( )
A.A分子中所有原子均在同一平面内
B.B分子的同分异构体有1种
C.C的水溶液又称福尔马林,具有杀菌、防腐性能
D.等物质的量的B、D与足量钠反应生成气体的量相等
三、非选择题(本题包括5小题,共60分)
16.(12分)(2024福建福州延安中学第二学期高一期中质检)回答下列问题。
(1)下列各组物质中,互为同位素的是 (填序号,下同);互为同素异形体的是 ;互为同系物的是 ;互为同分异构体的是 ;属于同一种物质的是 。
H和H;②CH4和CH3CH2CH3;
③和;④石墨和金刚石;
⑤正丁烷(CH3CH2CH2CH3)和异丁烷()
(2)乙烯水合法也是一种制备乙醇的方法,用该方法制备乙醇时,乙烯和水发生了 反应(填反应类型)。反应的化学方程式: 。
17.(12分)0.2 mol某烃A在氧气中充分燃烧后,生成化合物B、C各1.2 mol。
(1)烃A的分子式是 。
(2)若取一定量的烃A充分燃烧后,生成B、C各3 mol,则有 g的A参加了反应,燃烧时消耗标准状况下的氧气 L。
(3)若烃A不能使溴水褪色,但在一定条件下能与氯气发生取代反应,其一氯代物只有一种,则烃A的结构简式是 。
(4)若烃A能使溴水褪色,在催化剂作用下与H2发生加成反应后生成,则A的结构简式为 。
(5)若烃A能使溴水褪色,且分子中所有碳原子共平面,则A的结构简式为 。
(6)比A少2个碳原子的A的烯烃的同系物的同分异构体共有 种。
18.(12分)A是气态烃,标准状况下气体密度为1.25 g·L-1,G是高分子化合物,如图所示是与A有关的转化。
回答下列问题。
(1)F的结构式为 。
(2)已知A也可以与D在催化剂作用下生成E,写出该反应的化学方程式: 。
(3)写出与D互为同分异构体,且含醛基()的物质I的结构简式: 。
(4)写出H→B的化学方程式: 。
(5)下列说法正确的是 (填字母)。
A.46 g B与足量钠反应可以得到11.2 L氢气(在0 ℃、101 kPa的条件下)
B.B可用作燃料,缓解化石燃料的危机
C.可用碳酸钠溶液鉴别B、D、E三种有机化合物
D.G可与溴水因发生加成反应而使溴水褪色
19.(12分)有机化合物的世界缤纷多彩,根据题目信息回答下列问题。
(1)1 mol苯乙烯()最多能与 mol H2发生加成反应,该反应的产物与氯气在光照条件下反应,其一氯代物有 种。
(2)苯乙烯生成高聚物D的化学方程式为 。
(3)苯乙烯与水反应生成的C中含有甲基,则C的结构简式为 。
(4)某种燃料电池的工作原理示意图如图所示,a、b均为惰性电极。
假设使用的“燃料”是二甲醚(CH3OCH3),则a极的电极反应式为 。
20.(12分)某制糖厂以甘蔗为原料制糖,同时得到大量的甘蔗渣,对甘蔗渣进行综合利用不仅可以提高综合效益,而且还能防止环境污染,生产流程如下:
已知石油裂解已成为生产H的主要方法,E为乙醇催化氧化的产物,G是具有果香味的液体,试回答下列问题。
(1)F中所含官能团的名称是 。
(2)G的结构简式为 。
(3)写出D→E的化学方程式,并注明反应类型: ,
。
(4)F→G的反应装置如图所示。
①图中球形干燥管的作用是 。
②试管Ⅱ中加有饱和Na2CO3溶液,其作用是 。
③分子结构中具有一个羟基的化合物M 10 g,与F反应生成有机产物11.85 g,并回收了未反应的M 1.3 g,则M的相对分子质量为 。
第3章测评
1.C 解析 糖类中的单糖不能发生水解反应,而糖类中的其他糖、油脂、蛋白质均可以水解,A错误;葡萄糖的分子式为C6H12O6,蔗糖的分子式为C12H22O11,分子式不同,不互为同分异构体,结构也不相似,组成上也不是相差CH2的整数倍,故不互为同系物,B错误;由于CH4中氢元素的质量分数高于乙烯中氢元素的质量分数,故等质量的乙烯、甲烷分别充分燃烧,甲烷消耗氧气的量多,C正确;在加热、甲醛、X射线作用下,蛋白质都会发生变性,而加入饱和(NH4)2SO4溶液,则是蛋白质发生盐析,D错误。
2.A 解析 甲烷空间填充模型:,A正确;乙烯的结构简式:CH2CH2,B错误;CCl4的电子式:,C错误;是苯的空间填充模型,D错误。
3.D 解析 17 g —OH(羟基)中含有的电子数为(8+1)NA=9NA,故A错误;标准状况下,乙醇呈液态,不能用气体摩尔体积计算其物质的量,故B错误;常温常压下,1 mol甲烷和乙烯的混合物完全燃烧,产生的CO2分子数目为1NA到2NA之间,故C错误;1 mol甲烷含4 mol H(过量),与1 mol氯气光照条件下充分反应产生的HCl分子数目为1NA,故D正确。
4.B 解析 煤和石油中均含有多种物质,是混合物,属于传统能源,A正确;石油裂化得到的是轻质汽油,裂解得到的是乙烯等气态烃,B错误;新型煤化工以生产清洁能源和可替代石油化工的产品为主,如煤制甲醇、煤制烯烃、煤制天然气、煤制乙二醇和煤制油等,C正确;煤化工和石油化工均可制取汽油,D正确。
5.A 解析 1 mol CH2CH2先与HCl发生加成反应生成1 mol一氯乙烷,分子中含有5 mol H原子,再与Cl2发生取代反应,最多消耗5 mol Cl2,故A错误;乙烷与溴水不反应,乙烯与溴水发生加成反应生成1,2-二溴乙烷,可用溴水除去CH3CH3气体中的CH2CH2气体,故B正确;CH3CH3与酸性高锰酸钾溶液不反应,CH2CH2能被酸性高锰酸钾溶液氧化,乙烯使酸性高锰酸钾溶液褪色,实验室中可用酸性KMnO4溶液鉴别CH3CH3气体和CH2CH2气体,故C正确;CH2CH2与HCl发生加成反应的产物只有CH3CH2Cl,工业上可利用CH2CH2与HCl的加成反应制得纯净的CH3CH2Cl,故D正确。
6.C 解析 用饱和Na2CO3溶液除去乙酸乙酯中的乙酸,然后使用分液的方法分离有机层和水层,A正确;氢氧化钠和乙醇不反应,和乙酸反应生成乙酸钠,然后利用乙醇沸点较低的性质,蒸馏得到乙醇,B正确;乙烯可以与溴反应而进入溶液,甲烷为气体逸出,不需分液,C错误;氢氧化钠不与溴苯反应、与溴反应生成盐溶液,然后使用分液的方法分离有机层和水层,D正确。
7.B 解析 酯化反应是醇与酸的反应,属于取代反应,但不属于中和反应,A错误,B正确;酯化反应中酸分子中去—OH,C错误;酯化反应中醇分子中去—H,D错误。
8.C 解析 羟基能与Na反应生成H2,但未说明标准状况,因此生成H2的体积无法计算,A错误;苯环中没有碳碳双键,1 mol该物质中含有1 mol碳碳双键,B错误;该分子中含有碳碳双键,可以发生加聚反应合成有机高分子化合物,C正确;羟基和碳碳双键均可以使酸性高锰酸钾溶液褪色,D错误。
9.B 解析 制备乙酸乙酯时需要加热,图中无加热装置,实验不能达到预期目的,故A不选;铜丝在外焰a处受热与氧气反应生成黑色的氧化铜,移到内焰b处时,黑色的氧化铜在加热条件下与乙醇蒸气反应生成红色的铜、乙醛和水,则从a处移到b处,观察到铜丝由黑变红,实验能达到预期目的,故B选;乙醇和水均能与金属钠反应生成氢气,无法检验无水乙醇中是否有水,实验不能达到预期目的,可选用无水硫酸铜检验无水乙醇中是否有水,故C不选;碘的沸点高于四氯化碳,且碘易升华,要将碘单质从碘的四氯化碳溶液中提取出来应该用反萃取法,故D不选。
10.D 解析 由题中球棍模型可知,①为乙烷,②为乙烯,据此作答。乙烷属于饱和烃,乙烯属于不饱和烃,A项正确;乙烷不能使酸性高锰酸钾溶液褪色,而乙烯含有碳碳双键,可以被酸性高锰酸钾溶液氧化,从而使酸性高锰酸钾溶液褪色,B项正确;乙烷不能与溴水反应,但乙烯可以与溴水发生加成反应生成油状液体,因此可以用溴水除去乙烷中的乙烯,C项正确;烃(CxHy)在足量的氧气中充分燃烧的化学方程式为CxHy+(x+)O2xCO2+H2O,假设质量都为1 g,则乙烷(C2H6)的物质的量为 mol,由化学方程式可知,消耗O2的物质的量为 mol≈0.116 7 mol,乙烯(C2H4)的物质的量为 mol,消耗O2的物质的量为 mol=0.107 1 mol,所以消耗O2更多的是①乙烷,D项错误。
11.AB 解析 由图可知,分子式为C10H14,A正确。等质量的烃耗氧量由氢原子与碳原子个数比决定,个数比越大耗氧量越多;充分燃烧等质量的X和甲烷,甲烷消耗氧气较多,B正确。分子中含一个正丁基,其所含有的4个碳原子均为饱和碳原子,则所有碳原子不共平面,C错误。分子除苯环外不含不饱和键,不能与溴单质加成,D错误。
12.D 解析 乳酸分子中既含有羟基也含有羧基,在一定条件下可生成六元环酯,其结构简式是
,A正确;乳酸中既含有羟基也含有羧基,乳酸亚铁中含有羟基,二者均具有良好的水溶性,B正确;乳酸与铁反应生成乳酸亚铁和氢气,X应为氢气,含有非极性键,乳酸结构中有羧基,具有酸性,乳酸与铁反应生成氢气,氢元素化合价降低,表现氧化性,C正确;1个乳酸分子中含有1个羟基和1个羧基,1 mol乳酸与足量Na反应生成1 mol H2,乳酸与足量Na2CO3反应时,不生成气体,D错误。
13.AD 解析 淀粉和纤维素水解产物最终为葡萄糖(C6H12O6),A选项错误;葡萄糖在酒化酶作用下发生发酵反应:C6H12O62CH3CH2OH+2CO2↑,乙醇能够转化为乙酸,二者反应生成乙酸乙酯,所以N为乙酸,B选项正确;乙醇与乙酸发生酯化反应(本质是取代反应)生成乙酸乙酯,C选项正确;淀粉和纤维素的分子式都是(C6H10O5)n,但是两者的n值不相同,所以分子式不同,不是同分异构体,D选项错误。
14.BD 解析 HOOCHCCHCOOH与足量乙醇发生酯化反应生成丁烯二酸二乙酯,分子式为C8H12O4,A正确;HOOCHCCHCOOH与碳酸氢钠反应生成
NaOOCHCCHCOONa,易溶于水,B错误;富马酸亚铁中的Fe2+易被氧化,保存时应该密封保存,防止被氧化,C正确;富马酸亚铁与足量溴水反应时,碳碳双键与Br2加成,Fe2+也能被Br2氧化,D错误。
15.C 解析 依题意可得气态烃A的相对分子质量为28,即A为乙烯,由连续催化氧化可知,B为乙醇,C为乙醛,D为乙酸,E为乙酸乙酯。乙烯为平面结构,所有原子在同一平面内,A项正确;B为乙醇,其同分异构体为二甲醚(CH3OCH3),B项正确;1 mol CH3CH2OH和1 mol CH3COOH与足量钠反应,都生成0.5 mol H2,D项正确。
16.答案 (1)① ④ ② ⑤ ③
(2)加成 CH2CH2+H2OCH3CH2OH
解析 (1)质子数相同、中子数不同的同一种元素的不同核素互为同位素H和H互为同位素,答案选①;由同一种元素形成的不同单质互为同素异形体,石墨和金刚石互为同素异形体,答案选④;结构相似,分子式组成相差若干个CH2原子团的有机化合物互为同系物,甲烷和丙烷互为同系物,答案选②;分子式相同,结构不同的化合物互为同分异构体,正丁烷(CH3CH2CH2CH3)和异丁烷()互为同分异构体,答案选⑤;结构和性质完全都相同的是同一种物质,和是同一物质,答案选③。
(2)乙烯水合法制备乙醇的方程式为CH2CH2+H2OCH3CH2OH,根据化学方程式,可知用该方法制备乙醇时,乙烯和水发生加成反应。
17.答案 (1)C6H12 (2)42 100.8
(3) (4)
(5) (6)3
解析 (1)根据0.2 mol烃充分燃烧生成1.2 mol CO2和1.2 mol H2O,所以n(烃)∶n(C)∶n(H)=0.2 mol∶1.2 mol∶2.4 mol=1∶6∶12,所以分子式为C6H12。
(2)由C6H12 + 9O26CO2 +6H2O
1 mol 9 mol 6 mol
n(A) n(O2) 3 mol
得n(A)=0.5 mol,质量为0.5 mol×84 g·mol-1=42 g;n(O2)=4.5 mol,标准状况下的体积为4.5 mol×22.4 L·mol-1=100.8 L。
(3)烃A不能使溴水褪色,说明分子中无碳碳双键,只能是环状烃,一氯代物只有一种,只能是环己烷。
(4)烃A能使溴水褪色,说明A中含有碳碳双键,其加成产物为,则A的结构简式只能为。
(5)因A能使溴水褪色,说明A为烯烃,且所有碳原子共平面,结合乙烯分子共平面,得出A为。
(6)比A少2个碳原子的A的烯烃的同系物为C4H8,其烯烃类的同分异构体可为CH3CHCHCH3、
CH2CH—CH2CH3、,共3种。
18.答案 (1)
(2)CH2CH2+CH3COOHCH3COOCH2CH3
(3)HOCH2CHO或HCOOCH3
(4)CH2OH(CHOH)4CHO2CH3CH2OH+2CO2↑
(5)ABC
解析 由题干已知信息和转化流程图可知,A是气态烃,标准状况下气体密度为1.25 g·L-1,则A的摩尔质量为1.25 g·L-1×22.4 L·mol-1=28 g·mol-1,即A的相对分子质量为28,28÷12=2……4,A的分子式为C2H4,结构简式为
CH2CH2。A在催化剂、加热、加压条件下与H2O发生加成反应生成乙醇,B的结构简式为CH3CH2OH。乙醇催化氧化生成乙醛,C的结构简式为CH3CHO。乙醛催化氧化为乙酸,D的结构简式为CH3COOH。乙醇和乙酸在浓硫酸催化下加热生成乙酸乙酯,E的结构简式为CH3COOCH2CH3。乙烯和Br2的CCl4溶液发生加成反应生成1,2-二溴乙烷,F的结构简式为BrCH2CH2Br。乙烯催化转化为高分子化合物G,G的结构简式为 CH2—CH2 。淀粉在稀硫酸催化下发生水解反应生成葡萄糖,H的结构简式为CH2OH(CHOH)4CHO。葡萄糖在酶的催化作用下转化为酒精即乙醇。
(5)由分析可知,B为CH3CH2OH,46 g B的物质的量为=1 mol,根据反应方程式2CH3CH2OH+2Na2CH3CH2ONa+H2↑可知,与足量钠反应可以得到0.5 mol,即标准状况下0.5 mol×22.4 L·mol-1=11.2 L氢气,A正确;CH3CH2OH可用作燃料,乙醇汽油能够缓解化石燃料的危机,B正确;B、D、E分别为CH3CH2OH、CH3COOH、CH3COOCH2CH3,向三种有机物中加入饱和碳酸钠溶液可以分别观察到形成均一的溶液、产生大量的无色气泡、出现分层,故可用碳酸钠溶液鉴别B、D、E三种有机化合物,C正确;G的结构简式为
,分子中不含碳碳双键等不饱和键,故G不可与溴水因发生加成反应而使溴水褪色,D错误。
19.答案 (1)4 6
(2)n
(3)
(4)CH3OCH3-12e-+16OH-2C+11H2O
解析 在催化剂和加热条件下与足量的H2发生加成反应生成A为;与Br2的CCl4溶液发生加成反应生成B为;结合题干(3)可知在催化剂和加热条件下与H2O发生加成反应生成的C为;在催化剂和加热条件下发生加聚反应生成的高聚物D为。(1)苯环和碳碳双键均可以与氢气发生加成反应,则1 mol苯乙烯()最多能与4 mol H2发生加成反应,生成,有6种类型的氢原子,则与氯气在光照条件下反应,其一氯代物有6种。(2)苯乙烯中含有碳碳双键,通过加聚反应得到高聚物D,其反应的化学方程式为
n。(3)由以上分析可知C的结构简式为。(4)燃料电池中燃料在负极失去电子,发生氧化反应,结合电子移动方向,则a极为二甲醚(CH3OCH3)失去电子在碱性条件下转化为碳酸盐,电极反应式为CH3OCH3-12e-+16OH-2C+11H2O。
20.答案 (1)羧基
(2)CH3COOC2H5(或CH3COOCH2CH3)
(3)2CH3CH2OH+O22CH3CHO+2H2O 氧化反应
(4)①防倒吸 ②溶解乙醇、与乙酸反应、降低乙酸乙酯的溶解度 ③116
解析 (1)F为乙酸,官能团为羧基。(2)G为乙酸乙酯,结构简式为CH3COOC2H5(或CH3COOCH2CH3)。(3)D→E的反应为醇的催化氧化,化学方程式为2CH3CH2OH+O22CH3CHO+2H2O,反应类型为氧化反应。(4)①球形干燥管容积较大,起到防倒吸的作用;②试管Ⅱ中加饱和Na2CO3溶液的作用是溶解乙醇、与乙酸反应、降低乙酸乙酯的溶解度;③设该化合物为ROH,其相对分子质量为x,实际参加反应的M的质量为10 g-1.3 g=8.7 g,则反应的化学方程式可表示为:
ROH+CH3COOHCH3COOR+H2O ΔMr
x x+42 42
8.7 g 11.85 g 11.85 g-
8.7 g
解得x=116。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
