分层作业11 化学反应中能量变化的本质及转化形式--2025鲁科版化学必修第二册同步练习题(含答案)
文档属性
| 名称 | 分层作业11 化学反应中能量变化的本质及转化形式--2025鲁科版化学必修第二册同步练习题(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 579.9KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-24 00:00:00 | ||
图片预览


文档简介
中小学教育资源及组卷应用平台
2025鲁科版化学必修第二册
分层作业11 化学反应中能量变化的本质及转化形式
A级必备知识基础练
以下选择题只有一个选项符合题目要求。
题组1.化学反应的特征——物质变化和能量变化
1.下列对化学反应过程的理解错误的是( )
A.化学反应过程中同时存在物质和能量的变化
B.凡是能量变化一定发生在化学变化中
C.化学反应中同时存在质量守恒和能量守恒
D.能量的释放和吸收以发生变化的物质为基础
2.(2024北京五十五中调研)下列关于化学反应中物质或能量变化的判断正确的是( )
A.加热条件下进行的化学反应一定是吸热反应
B.化学键的断裂和形成是化学反应中能量变化的主要原因
C.一定条件下进行的化学反应,只能将化学能转化为热能和光能
D.将NH4Cl固体与Ba(OH)2·8H2O固体混合并搅拌,反应放出热量
题组2.常见的吸热反应和放热反应
3.(2024江苏常州联盟学校学情调研)下列反应的热量变化与下图相符的是( )
A.C和水蒸气高温反应生成水煤气
B.煅烧石灰石
C.锌和盐酸反应制氢气
D.氢氧化钡晶体和氯化铵晶体研磨放出氨气
4.(2024山东青岛高一期中)下列反应中,既属于氧化还原反应又属于吸热反应的是( )
A.盐酸与小苏打反应
B.铝与稀盐酸反应
C.C与H2O(g)反应
D.S与O2的燃烧反应
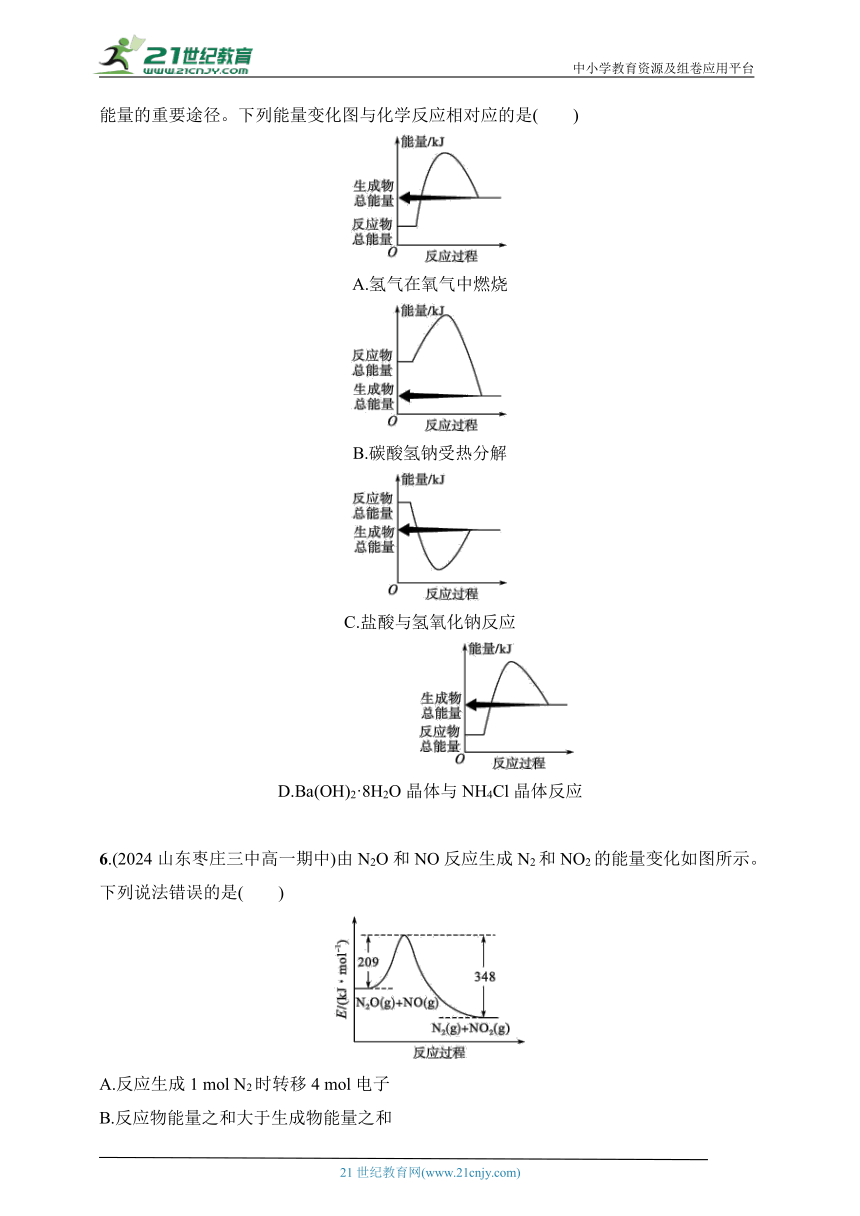
5.(2024甘肃武威高一期中)化学反应在发生物质变化的同时伴随着能量变化,是人类获取能量的重要途径。下列能量变化图与化学反应相对应的是( )
A.氢气在氧气中燃烧
B.碳酸氢钠受热分解
C.盐酸与氢氧化钠反应
D.Ba(OH)2·8H2O晶体与NH4Cl晶体反应
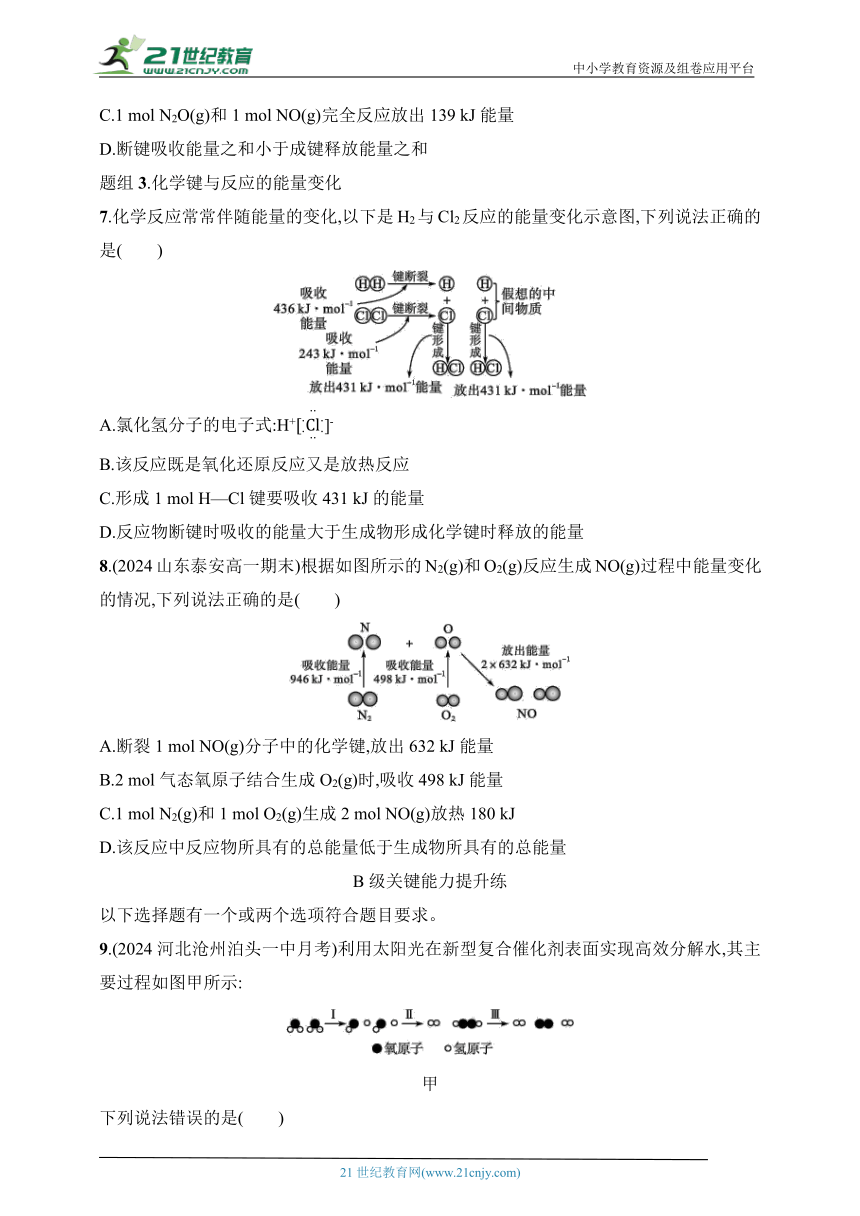
6.(2024山东枣庄三中高一期中)由N2O和NO反应生成N2和NO2的能量变化如图所示。下列说法错误的是( )
A.反应生成1 mol N2时转移4 mol电子
B.反应物能量之和大于生成物能量之和
C.1 mol N2O(g)和1 mol NO(g)完全反应放出139 kJ能量
D.断键吸收能量之和小于成键释放能量之和
题组3.化学键与反应的能量变化
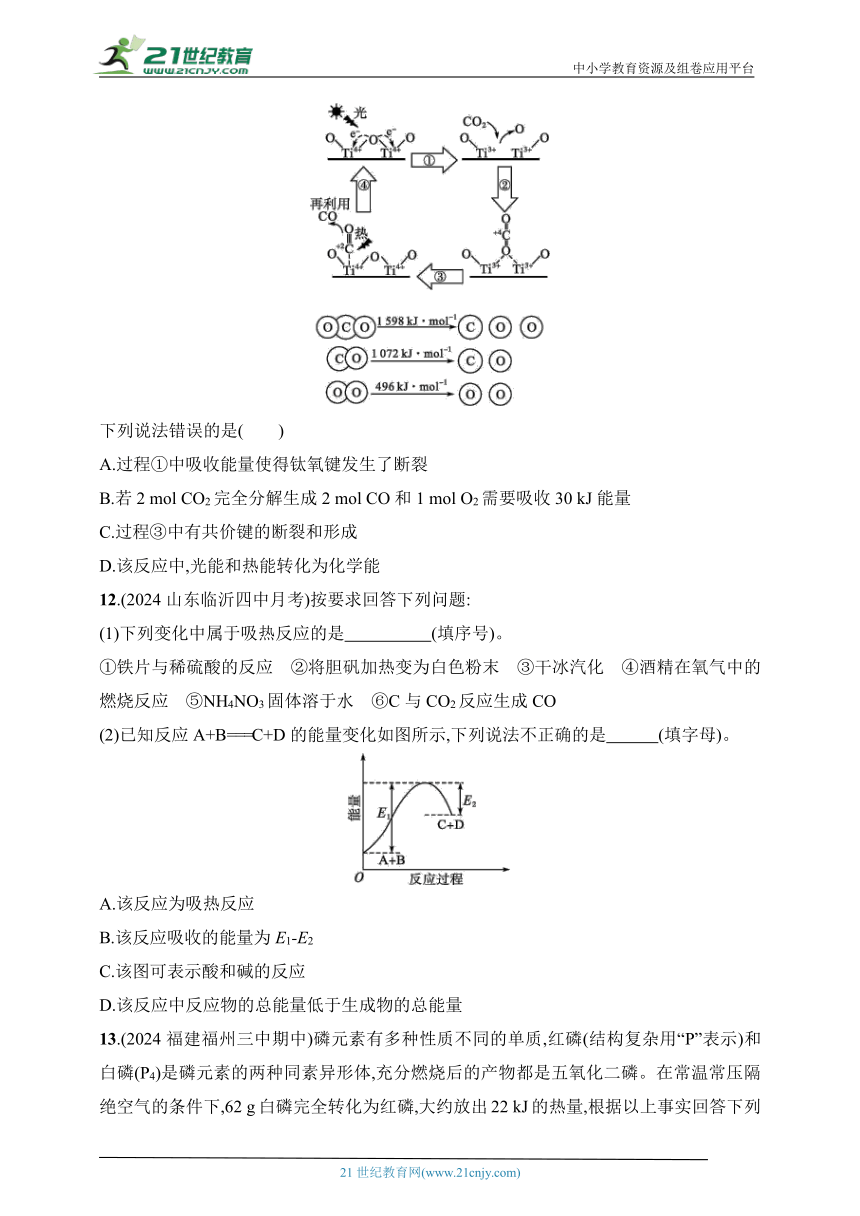
7.化学反应常常伴随能量的变化,以下是H2与Cl2反应的能量变化示意图,下列说法正确的是( )
A.氯化氢分子的电子式:H+]-
B.该反应既是氧化还原反应又是放热反应
C.形成1 mol H—Cl键要吸收431 kJ的能量
D.反应物断键时吸收的能量大于生成物形成化学键时释放的能量
8.(2024山东泰安高一期末)根据如图所示的N2(g)和O2(g)反应生成NO(g)过程中能量变化的情况,下列说法正确的是( )
A.断裂1 mol NO(g)分子中的化学键,放出632 kJ能量
B.2 mol气态氧原子结合生成O2(g)时,吸收498 kJ能量
C.1 mol N2(g)和1 mol O2(g)生成2 mol NO(g)放热180 kJ
D.该反应中反应物所具有的总能量低于生成物所具有的总能量
B级关键能力提升练
以下选择题有一个或两个选项符合题目要求。
9.(2024河北沧州泊头一中月考)利用太阳光在新型复合催化剂表面实现高效分解水,其主要过程如图甲所示:
甲
下列说法错误的是( )
乙
A.过程中实现了光能转化为化学能
B.氢能资源丰富,属于可再生能源
C.过程Ⅰ吸收能量,过程Ⅱ释放能量
D.2H2O2H2↑+O2↑反应的能量变化如上图所示
10.(2024山东聊城高一期中)化学反应A2+B2 ===2AB的能量变化如图所示,则下列说法不正确的是( )
A.该反应是吸热反应
B.断裂1 mol A—A键和1 mol B—B键吸收x kJ的能量
C.断裂2 mol A-B键需要吸收y kJ的能量
D.AB的总能量高于A2和B2的总能量
11.(2024河南郑州高一期中)以TiO2为催化剂的光热化学循环分解CO2的反应,为室温气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示:
下列说法错误的是( )
A.过程①中吸收能量使得钛氧键发生了断裂
B.若2 mol CO2完全分解生成2 mol CO和1 mol O2需要吸收30 kJ能量
C.过程③中有共价键的断裂和形成
D.该反应中,光能和热能转化为化学能
12.(2024山东临沂四中月考)按要求回答下列问题:
(1)下列变化中属于吸热反应的是 (填序号)。
①铁片与稀硫酸的反应 ②将胆矾加热变为白色粉末 ③干冰汽化 ④酒精在氧气中的燃烧反应 ⑤NH4NO3固体溶于水 ⑥C与CO2反应生成CO
(2)已知反应A+B===C+D的能量变化如图所示,下列说法不正确的是 (填字母)。
A.该反应为吸热反应
B.该反应吸收的能量为E1-E2
C.该图可表示酸和碱的反应
D.该反应中反应物的总能量低于生成物的总能量
13.(2024福建福州三中期中)磷元素有多种性质不同的单质,红磷(结构复杂用“P”表示)和白磷(P4)是磷元素的两种同素异形体,充分燃烧后的产物都是五氧化二磷。在常温常压隔绝空气的条件下,62 g白磷完全转化为红磷,大约放出22 kJ的热量,根据以上事实回答下列问题:
(1)白磷与红磷中更稳定的是 (填“红磷”或“白磷”,下同);等质量的红磷和白磷分别完全燃烧,放出热量较多的是 。
(2)如图所示,在锥形瓶内放置装有水的小试管A,若A中发生的反应能使B中a端液面高于b端,则说明A中发生的反应是 (填“吸热反应”或“放热反应”)。
C级学科素养拔高练
14.硅是太阳能电池的重要材料。工业冶炼纯硅的原理为
粗硅冶炼:①SiO2+2CSi(粗)+2CO↑。
精炼硅:②Si+3HClSiHCl3+H2;
③SiHCl3+H2Si+3HCl。
化学反应与能量变化如图所示,回答下列问题:
(1)①是 (填“吸热”或“放热”,下同)反应,②是 反应,③是 反应。
(2)反应②断裂反应物中的化学键所吸收的能量 (填“大于”或“小于”)形成生成物中的化学键所放出的能量。
15.氢气是一种理想的汽车新能源,发展氢能汽车的关键是氢气的制备及储存技术。制备氢气通常有下列方法:
①电解水制氢:2H2O2H2↑+O2↑;
②高温使水分解制氢:2H2O2H2↑+O2↑;
③太阳光催化分解水制氢:2H2O2H2↑+O2↑;
④天然气制氢:CH4+H2OCO+3H2。
(1)最为节能的方法是 (填序号)。
(2)从化学键断裂与形成的角度分析方法①②③反应产生等物质的量的H2,消耗的能量是否相同 (填“相同”或“不同”),理由是
。
(3)破坏1 mol氢气中的化学键需要吸收436 kJ能量,破坏 mol氧气中的化学键需要吸收249 kJ能量,形成水分子中的1 mol H—O键释放463 kJ能量。下图表示氢气和氧气反应过程中能量的变化。
a.请将图中①②的能量变化的数值,填在下边的横线上。
① kJ ② kJ
b.生成27 g水蒸气放出的热量为 kJ。
分层作业11 化学反应中能量变化的本质及转化形式
1.B 解析 化学反应过程中都会伴随着物质变化和能量变化,A正确;化学变化过程中往往伴随着能量的变化,但有能量变化时不一定发生了化学变化,如灯泡通电发光放热,B错误;化学反应的实质是原子的重新组合,符合质量守恒,反应过程中往往伴随着能量的变化,符合能量守恒,C正确;化学反应过程中同时存在物质和能量的变化,且能量的释放和吸收是以发生变化的物质为基础的,二者密不可分,D正确。
2.B 解析 放热反应有的也需要加热才能发生,如煤炭的燃烧,故A错误;化学反应的实质是反应物化学键断裂吸收能量,生成物形成化学键放出能量,反应过程中一定伴随能量变化,故B正确;一定条件下进行的化学反应,可以将化学能转化成光能、热能或电能等,故C错误;将NH4Cl固体与Ba(OH)2·8H2O固体混合并搅拌,反应吸收热量,故D错误。
3.C 解析 题图所示的反应为放热反应。C与水蒸气高温条件下生成水煤气的反应为吸热反应,A错误;煅烧石灰石,石灰石分解生成CaO和CO2,该反应为吸热反应,B错误;锌与盐酸反应制氢气,该反应为放热反应,C正确;氢氧化钡晶体与氯化铵晶体反应生成氨气,该反应为吸热反应,D错误。
4.C 解析 盐酸与小苏打反应属于吸热反应,但不存在元素化合价的变化,属于非氧化还原反应,A不符合题意;铝与稀盐酸反应是氧化还原反应,但是放热反应,B不符合题意;C与H2O(g)反应为吸热反应,且该反应中碳元素和氢元素的化合价发生变化,则属于氧化还原反应,C符合题意;S与O2的燃烧反应属于氧化还原反应,但属于放热反应,D不符合题意。
5.D 解析 氢气在氧气中燃烧为放热反应,反应物的总能量大于生成物的总能量,A中反应与图像不符;碳酸氢钠受热分解为吸热反应,反应物的总能量小于生成物的总能量,B中反应与图像不符;氢氧化钠与盐酸的反应为放热反应,但是断裂化学键需要吸收能量,形成化学键需要放出能量,C中反应与图像不符;Ba(OH)2·8H2O晶体与NH4Cl晶体的反应为吸热反应,反应物的总能量小于生成物的总能量,D中反应与图像相符。
6.A 解析 该反应的化学方程式为N2O+NON2+NO2,生成1 mol N2时转移2 mol电子,故A错误;根据能量变化图,反应物的总能量大于生成物的总能量,此反应属于放热反应,故B正确;根据能量变化图,1 mol N2O(g)和1 mol NO(g)完全反应,放出的能量为348 kJ-209 kJ=139 kJ,故C正确;断键吸收能量,成键释放能量,此反应是放热反应,因此断键吸收能量之和小于成键释放能量之和,故D正确。
7.B 解析 HCl是共价化合物,其电子式为,A错误;根据题图,化学键断裂吸收的能量为679 kJ,形成化学键放出的能量为862 kJ,吸收的能量小于放出的能量,故该反应为放热反应,该反应是有单质参加的化合反应,属于氧化还原反应,B正确;形成1 mol H—Cl键要放出431 kJ的能量,C错误;化学键断裂吸收的能量为679 kJ,形成化学键放出的能量为862 kJ,吸收的能量小于放出的能量,D错误。
8.D 解析 1 mol NO(g)分子中的化学键断裂时需要吸收632 kJ能量,A错误;2 mol 气态氧原子结合生成1 mol O2(g)时需要放出498 kJ能量,B错误;1 mol N2(g)和1 mol O2(g)生成2 mol NO(g)吸热180 kJ,C错误;该反应是吸热反应,所以该反应中反应物所具有的总能量低于生成物所具有的总能量,D正确。
9.D 解析 水分解成氢气和氧气需吸收能量。利用太阳光在新型复合催化剂表面实现高效分解水的过程中实现了光能转化为化学能,A正确;氢能资源丰富,属于可再生能源,B正确;过程Ⅰ为化学键断裂,吸收能量,过程Ⅱ为化学键形成,释放能量,C正确;2H2O2H2↑+O2↑,该反应为吸热反应,图乙所示反应为放热反应,D错误。
10.AD 解析 因为反应物的总能量高于生成物的总能量,故该反应是放热反应,A错误;断裂1 mol A—A键和1 mol B—B键吸收x kJ的能量,B正确;由图可知,断裂2 mol A—B键需要吸收y kJ的能量,C正确;1 mol A2和1 mol B2的总能量高于2 mol AB的总能量,选项没有给出各物质的量,无法比较能量高低,D错误。
11.B 解析 由图可知,过程①中钛氧键发生了断裂,共价键的断裂是吸收能量的过程,A正确;由题给数据可知,2 mol CO2分子中共价键断裂吸收的能量为1 598 kJ×2,生成2 mol CO和1 mol O2时,形成共价键释放的能量为(1 072 kJ×2+496 kJ),则该反应需要吸收的能量为1 598 kJ×2-(1 072 kJ×2+496 kJ)=556 kJ,B错误;由图可知,过程③中有碳氧共价键的断裂和形成,C正确;该反应中,提供光能断裂钛氧键,提供热能断裂钛碳键,从而实现光能和热能向化学能的转变,D正确。
12.答案 (1)②⑥ (2)C
解析 (1)①铁片与稀硫酸的反应为放热反应;②将胆矾加热变为白色粉末,胆矾失去结晶水,为吸热反应;③干冰汽化为物理变化;④酒精在氧气中的燃烧反应为放热反应;⑤NH4NO3固体溶于水是物理变化;⑥C与CO2反应生成CO,反应过程吸收能量,为吸热反应。(2)由图可知,反应物的总能量低于生成物的总能量,该反应为吸热反应,A正确;该反应吸收的能量为E1-E2,B正确;酸碱中和反应为放热反应,题给反应为吸热反应,C错误;由图可知,该反应中反应物的总能量低于生成物的总能量,D正确。
13.答案 (1)红磷 白磷
(2)吸热反应
解析 (1)在常温常压隔绝空气的条件下,62 g白磷完全转化为红磷,大约放出22 kJ的热量,这说明62 g白磷的能量高于62 g红磷的能量,能量越低越稳定,所以白磷与红磷中更稳定的是红磷;白磷的能量高于红磷的能量,所以等质量的红磷和白磷分别完全燃烧,放出热量较多的是白磷。
(2)在锥形瓶内放置装有水的小试管A,若A中发生的反应能使B中a端液面高于b端,说明反应后锥形瓶内压强减小,则说明A中发生的反应是吸热反应。
14.答案 (1)吸热 放热 吸热 (2)小于
15.答案 (1)③
(2)相同 反应①②③中反应物的总能量相等,生成物的总能量也相等,则反应消耗的能量相同
(3)a.①1 370 ②1 852 b.361.5
解析 (1)反应①②④会消耗电能或热能,而反应③是在催化剂作用下,利用取之不尽的太阳能,故反应③是最为节能的方法。
(2)反应①②③都是通过分解H2O获得H2,产生等物质的量的H2时消耗的H2O的物质的量也相等,破坏化学键和形成化学键的量也分别相同,故消耗的能量也相同。
(3)a.①中2 mol H2(g)、1 mol O2(g)生成H、O原子吸收的能量为2×436 kJ+2×249 kJ=1 370 kJ。②中H、O原子生成2 mol H2O(g)释放的能量为4×463 kJ=1 852 kJ。b.生成27 g(物质的量为1.5 mol)水蒸气放出的热量为×(1 852 kJ-1 370 kJ)=361.5 kJ。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
2025鲁科版化学必修第二册
分层作业11 化学反应中能量变化的本质及转化形式
A级必备知识基础练
以下选择题只有一个选项符合题目要求。
题组1.化学反应的特征——物质变化和能量变化
1.下列对化学反应过程的理解错误的是( )
A.化学反应过程中同时存在物质和能量的变化
B.凡是能量变化一定发生在化学变化中
C.化学反应中同时存在质量守恒和能量守恒
D.能量的释放和吸收以发生变化的物质为基础
2.(2024北京五十五中调研)下列关于化学反应中物质或能量变化的判断正确的是( )
A.加热条件下进行的化学反应一定是吸热反应
B.化学键的断裂和形成是化学反应中能量变化的主要原因
C.一定条件下进行的化学反应,只能将化学能转化为热能和光能
D.将NH4Cl固体与Ba(OH)2·8H2O固体混合并搅拌,反应放出热量
题组2.常见的吸热反应和放热反应
3.(2024江苏常州联盟学校学情调研)下列反应的热量变化与下图相符的是( )
A.C和水蒸气高温反应生成水煤气
B.煅烧石灰石
C.锌和盐酸反应制氢气
D.氢氧化钡晶体和氯化铵晶体研磨放出氨气
4.(2024山东青岛高一期中)下列反应中,既属于氧化还原反应又属于吸热反应的是( )
A.盐酸与小苏打反应
B.铝与稀盐酸反应
C.C与H2O(g)反应
D.S与O2的燃烧反应
5.(2024甘肃武威高一期中)化学反应在发生物质变化的同时伴随着能量变化,是人类获取能量的重要途径。下列能量变化图与化学反应相对应的是( )
A.氢气在氧气中燃烧
B.碳酸氢钠受热分解
C.盐酸与氢氧化钠反应
D.Ba(OH)2·8H2O晶体与NH4Cl晶体反应
6.(2024山东枣庄三中高一期中)由N2O和NO反应生成N2和NO2的能量变化如图所示。下列说法错误的是( )
A.反应生成1 mol N2时转移4 mol电子
B.反应物能量之和大于生成物能量之和
C.1 mol N2O(g)和1 mol NO(g)完全反应放出139 kJ能量
D.断键吸收能量之和小于成键释放能量之和
题组3.化学键与反应的能量变化
7.化学反应常常伴随能量的变化,以下是H2与Cl2反应的能量变化示意图,下列说法正确的是( )
A.氯化氢分子的电子式:H+]-
B.该反应既是氧化还原反应又是放热反应
C.形成1 mol H—Cl键要吸收431 kJ的能量
D.反应物断键时吸收的能量大于生成物形成化学键时释放的能量
8.(2024山东泰安高一期末)根据如图所示的N2(g)和O2(g)反应生成NO(g)过程中能量变化的情况,下列说法正确的是( )
A.断裂1 mol NO(g)分子中的化学键,放出632 kJ能量
B.2 mol气态氧原子结合生成O2(g)时,吸收498 kJ能量
C.1 mol N2(g)和1 mol O2(g)生成2 mol NO(g)放热180 kJ
D.该反应中反应物所具有的总能量低于生成物所具有的总能量
B级关键能力提升练
以下选择题有一个或两个选项符合题目要求。
9.(2024河北沧州泊头一中月考)利用太阳光在新型复合催化剂表面实现高效分解水,其主要过程如图甲所示:
甲
下列说法错误的是( )
乙
A.过程中实现了光能转化为化学能
B.氢能资源丰富,属于可再生能源
C.过程Ⅰ吸收能量,过程Ⅱ释放能量
D.2H2O2H2↑+O2↑反应的能量变化如上图所示
10.(2024山东聊城高一期中)化学反应A2+B2 ===2AB的能量变化如图所示,则下列说法不正确的是( )
A.该反应是吸热反应
B.断裂1 mol A—A键和1 mol B—B键吸收x kJ的能量
C.断裂2 mol A-B键需要吸收y kJ的能量
D.AB的总能量高于A2和B2的总能量
11.(2024河南郑州高一期中)以TiO2为催化剂的光热化学循环分解CO2的反应,为室温气体减排提供了一个新途径,该反应的机理及各分子化学键完全断裂时的能量变化如图所示:
下列说法错误的是( )
A.过程①中吸收能量使得钛氧键发生了断裂
B.若2 mol CO2完全分解生成2 mol CO和1 mol O2需要吸收30 kJ能量
C.过程③中有共价键的断裂和形成
D.该反应中,光能和热能转化为化学能
12.(2024山东临沂四中月考)按要求回答下列问题:
(1)下列变化中属于吸热反应的是 (填序号)。
①铁片与稀硫酸的反应 ②将胆矾加热变为白色粉末 ③干冰汽化 ④酒精在氧气中的燃烧反应 ⑤NH4NO3固体溶于水 ⑥C与CO2反应生成CO
(2)已知反应A+B===C+D的能量变化如图所示,下列说法不正确的是 (填字母)。
A.该反应为吸热反应
B.该反应吸收的能量为E1-E2
C.该图可表示酸和碱的反应
D.该反应中反应物的总能量低于生成物的总能量
13.(2024福建福州三中期中)磷元素有多种性质不同的单质,红磷(结构复杂用“P”表示)和白磷(P4)是磷元素的两种同素异形体,充分燃烧后的产物都是五氧化二磷。在常温常压隔绝空气的条件下,62 g白磷完全转化为红磷,大约放出22 kJ的热量,根据以上事实回答下列问题:
(1)白磷与红磷中更稳定的是 (填“红磷”或“白磷”,下同);等质量的红磷和白磷分别完全燃烧,放出热量较多的是 。
(2)如图所示,在锥形瓶内放置装有水的小试管A,若A中发生的反应能使B中a端液面高于b端,则说明A中发生的反应是 (填“吸热反应”或“放热反应”)。
C级学科素养拔高练
14.硅是太阳能电池的重要材料。工业冶炼纯硅的原理为
粗硅冶炼:①SiO2+2CSi(粗)+2CO↑。
精炼硅:②Si+3HClSiHCl3+H2;
③SiHCl3+H2Si+3HCl。
化学反应与能量变化如图所示,回答下列问题:
(1)①是 (填“吸热”或“放热”,下同)反应,②是 反应,③是 反应。
(2)反应②断裂反应物中的化学键所吸收的能量 (填“大于”或“小于”)形成生成物中的化学键所放出的能量。
15.氢气是一种理想的汽车新能源,发展氢能汽车的关键是氢气的制备及储存技术。制备氢气通常有下列方法:
①电解水制氢:2H2O2H2↑+O2↑;
②高温使水分解制氢:2H2O2H2↑+O2↑;
③太阳光催化分解水制氢:2H2O2H2↑+O2↑;
④天然气制氢:CH4+H2OCO+3H2。
(1)最为节能的方法是 (填序号)。
(2)从化学键断裂与形成的角度分析方法①②③反应产生等物质的量的H2,消耗的能量是否相同 (填“相同”或“不同”),理由是
。
(3)破坏1 mol氢气中的化学键需要吸收436 kJ能量,破坏 mol氧气中的化学键需要吸收249 kJ能量,形成水分子中的1 mol H—O键释放463 kJ能量。下图表示氢气和氧气反应过程中能量的变化。
a.请将图中①②的能量变化的数值,填在下边的横线上。
① kJ ② kJ
b.生成27 g水蒸气放出的热量为 kJ。
分层作业11 化学反应中能量变化的本质及转化形式
1.B 解析 化学反应过程中都会伴随着物质变化和能量变化,A正确;化学变化过程中往往伴随着能量的变化,但有能量变化时不一定发生了化学变化,如灯泡通电发光放热,B错误;化学反应的实质是原子的重新组合,符合质量守恒,反应过程中往往伴随着能量的变化,符合能量守恒,C正确;化学反应过程中同时存在物质和能量的变化,且能量的释放和吸收是以发生变化的物质为基础的,二者密不可分,D正确。
2.B 解析 放热反应有的也需要加热才能发生,如煤炭的燃烧,故A错误;化学反应的实质是反应物化学键断裂吸收能量,生成物形成化学键放出能量,反应过程中一定伴随能量变化,故B正确;一定条件下进行的化学反应,可以将化学能转化成光能、热能或电能等,故C错误;将NH4Cl固体与Ba(OH)2·8H2O固体混合并搅拌,反应吸收热量,故D错误。
3.C 解析 题图所示的反应为放热反应。C与水蒸气高温条件下生成水煤气的反应为吸热反应,A错误;煅烧石灰石,石灰石分解生成CaO和CO2,该反应为吸热反应,B错误;锌与盐酸反应制氢气,该反应为放热反应,C正确;氢氧化钡晶体与氯化铵晶体反应生成氨气,该反应为吸热反应,D错误。
4.C 解析 盐酸与小苏打反应属于吸热反应,但不存在元素化合价的变化,属于非氧化还原反应,A不符合题意;铝与稀盐酸反应是氧化还原反应,但是放热反应,B不符合题意;C与H2O(g)反应为吸热反应,且该反应中碳元素和氢元素的化合价发生变化,则属于氧化还原反应,C符合题意;S与O2的燃烧反应属于氧化还原反应,但属于放热反应,D不符合题意。
5.D 解析 氢气在氧气中燃烧为放热反应,反应物的总能量大于生成物的总能量,A中反应与图像不符;碳酸氢钠受热分解为吸热反应,反应物的总能量小于生成物的总能量,B中反应与图像不符;氢氧化钠与盐酸的反应为放热反应,但是断裂化学键需要吸收能量,形成化学键需要放出能量,C中反应与图像不符;Ba(OH)2·8H2O晶体与NH4Cl晶体的反应为吸热反应,反应物的总能量小于生成物的总能量,D中反应与图像相符。
6.A 解析 该反应的化学方程式为N2O+NON2+NO2,生成1 mol N2时转移2 mol电子,故A错误;根据能量变化图,反应物的总能量大于生成物的总能量,此反应属于放热反应,故B正确;根据能量变化图,1 mol N2O(g)和1 mol NO(g)完全反应,放出的能量为348 kJ-209 kJ=139 kJ,故C正确;断键吸收能量,成键释放能量,此反应是放热反应,因此断键吸收能量之和小于成键释放能量之和,故D正确。
7.B 解析 HCl是共价化合物,其电子式为,A错误;根据题图,化学键断裂吸收的能量为679 kJ,形成化学键放出的能量为862 kJ,吸收的能量小于放出的能量,故该反应为放热反应,该反应是有单质参加的化合反应,属于氧化还原反应,B正确;形成1 mol H—Cl键要放出431 kJ的能量,C错误;化学键断裂吸收的能量为679 kJ,形成化学键放出的能量为862 kJ,吸收的能量小于放出的能量,D错误。
8.D 解析 1 mol NO(g)分子中的化学键断裂时需要吸收632 kJ能量,A错误;2 mol 气态氧原子结合生成1 mol O2(g)时需要放出498 kJ能量,B错误;1 mol N2(g)和1 mol O2(g)生成2 mol NO(g)吸热180 kJ,C错误;该反应是吸热反应,所以该反应中反应物所具有的总能量低于生成物所具有的总能量,D正确。
9.D 解析 水分解成氢气和氧气需吸收能量。利用太阳光在新型复合催化剂表面实现高效分解水的过程中实现了光能转化为化学能,A正确;氢能资源丰富,属于可再生能源,B正确;过程Ⅰ为化学键断裂,吸收能量,过程Ⅱ为化学键形成,释放能量,C正确;2H2O2H2↑+O2↑,该反应为吸热反应,图乙所示反应为放热反应,D错误。
10.AD 解析 因为反应物的总能量高于生成物的总能量,故该反应是放热反应,A错误;断裂1 mol A—A键和1 mol B—B键吸收x kJ的能量,B正确;由图可知,断裂2 mol A—B键需要吸收y kJ的能量,C正确;1 mol A2和1 mol B2的总能量高于2 mol AB的总能量,选项没有给出各物质的量,无法比较能量高低,D错误。
11.B 解析 由图可知,过程①中钛氧键发生了断裂,共价键的断裂是吸收能量的过程,A正确;由题给数据可知,2 mol CO2分子中共价键断裂吸收的能量为1 598 kJ×2,生成2 mol CO和1 mol O2时,形成共价键释放的能量为(1 072 kJ×2+496 kJ),则该反应需要吸收的能量为1 598 kJ×2-(1 072 kJ×2+496 kJ)=556 kJ,B错误;由图可知,过程③中有碳氧共价键的断裂和形成,C正确;该反应中,提供光能断裂钛氧键,提供热能断裂钛碳键,从而实现光能和热能向化学能的转变,D正确。
12.答案 (1)②⑥ (2)C
解析 (1)①铁片与稀硫酸的反应为放热反应;②将胆矾加热变为白色粉末,胆矾失去结晶水,为吸热反应;③干冰汽化为物理变化;④酒精在氧气中的燃烧反应为放热反应;⑤NH4NO3固体溶于水是物理变化;⑥C与CO2反应生成CO,反应过程吸收能量,为吸热反应。(2)由图可知,反应物的总能量低于生成物的总能量,该反应为吸热反应,A正确;该反应吸收的能量为E1-E2,B正确;酸碱中和反应为放热反应,题给反应为吸热反应,C错误;由图可知,该反应中反应物的总能量低于生成物的总能量,D正确。
13.答案 (1)红磷 白磷
(2)吸热反应
解析 (1)在常温常压隔绝空气的条件下,62 g白磷完全转化为红磷,大约放出22 kJ的热量,这说明62 g白磷的能量高于62 g红磷的能量,能量越低越稳定,所以白磷与红磷中更稳定的是红磷;白磷的能量高于红磷的能量,所以等质量的红磷和白磷分别完全燃烧,放出热量较多的是白磷。
(2)在锥形瓶内放置装有水的小试管A,若A中发生的反应能使B中a端液面高于b端,说明反应后锥形瓶内压强减小,则说明A中发生的反应是吸热反应。
14.答案 (1)吸热 放热 吸热 (2)小于
15.答案 (1)③
(2)相同 反应①②③中反应物的总能量相等,生成物的总能量也相等,则反应消耗的能量相同
(3)a.①1 370 ②1 852 b.361.5
解析 (1)反应①②④会消耗电能或热能,而反应③是在催化剂作用下,利用取之不尽的太阳能,故反应③是最为节能的方法。
(2)反应①②③都是通过分解H2O获得H2,产生等物质的量的H2时消耗的H2O的物质的量也相等,破坏化学键和形成化学键的量也分别相同,故消耗的能量也相同。
(3)a.①中2 mol H2(g)、1 mol O2(g)生成H、O原子吸收的能量为2×436 kJ+2×249 kJ=1 370 kJ。②中H、O原子生成2 mol H2O(g)释放的能量为4×463 kJ=1 852 kJ。b.生成27 g(物质的量为1.5 mol)水蒸气放出的热量为×(1 852 kJ-1 370 kJ)=361.5 kJ。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
