专题3 从海水中获得的化学物质 分层作业14 氯气的发现与制备--2025苏教版化学必修第一册同步练习题
文档属性
| 名称 | 专题3 从海水中获得的化学物质 分层作业14 氯气的发现与制备--2025苏教版化学必修第一册同步练习题 |

|
|
| 格式 | docx | ||
| 文件大小 | 454.8KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-24 14:15:40 | ||
图片预览

文档简介
中小学教育资源及组卷应用平台
2025苏教版化学必修第一册
分层作业14 氯气的发现与制备
A级必备知识基础练
1.在制氯气时有如下操作,操作顺序正确的是( )
①连接好装置,检查气密性
②缓缓加热,加快反应,使气体均匀逸出
③在圆底烧瓶中加入二氧化锰粉末
④从盛有浓盐酸的分液漏斗中将浓盐酸缓缓滴入烧瓶中
⑤将多余的Cl2用NaOH溶液吸收
⑥用向上排空气法收集氯气
A.①②③④⑤⑥
B.③④②①⑥⑤
C.①④③②⑥⑤
D.①③④②⑥⑤
2.实验室制氯气的尾气中含有较多的氯气,有毒,要吸收这些尾气,下列试剂最适合的是( )
A.饱和石灰水 B.饱和食盐水
C.自来水 D.烧碱溶液
3.下列关于实验室用MnO2制取Cl2的叙述不正确的是( )
A.需用浓盐酸
B.缓慢加热反应
C.充分反应后,HCl无剩余
D.多余氯气常用较浓的碱液吸收
4.根据电解饱和食盐水的化学方程式:2NaCl+2H2OH2↑+Cl2↑+2NaOH,每生成4 mol 的NaOH,下列说法正确的是( )
A.在X极生成2 mol Cl2
B.在X极生成2 mol H2
C.在Y极生成4 mol Cl2
D.NaOH在Y极生成
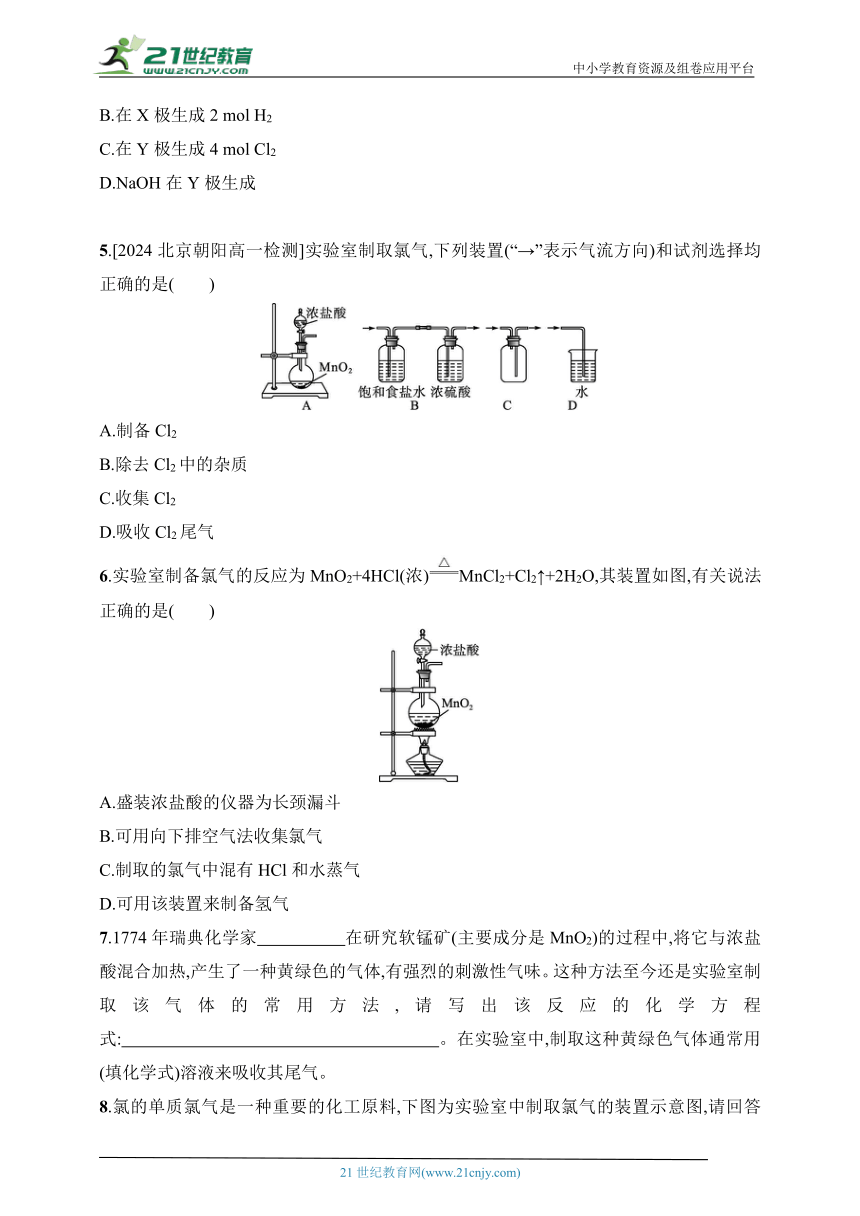
5.[2024北京朝阳高一检测]实验室制取氯气,下列装置(“→”表示气流方向)和试剂选择均正确的是( )
A.制备Cl2
B.除去Cl2中的杂质
C.收集Cl2
D.吸收Cl2尾气
6.实验室制备氯气的反应为MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O,其装置如图,有关说法正确的是( )
A.盛装浓盐酸的仪器为长颈漏斗
B.可用向下排空气法收集氯气
C.制取的氯气中混有HCl和水蒸气
D.可用该装置来制备氢气
7.1774年瑞典化学家 在研究软锰矿(主要成分是MnO2)的过程中,将它与浓盐酸混合加热,产生了一种黄绿色的气体,有强烈的刺激性气味。这种方法至今还是实验室制取该气体的常用方法,请写出该反应的化学方程式: 。在实验室中,制取这种黄绿色气体通常用 (填化学式)溶液来吸收其尾气。
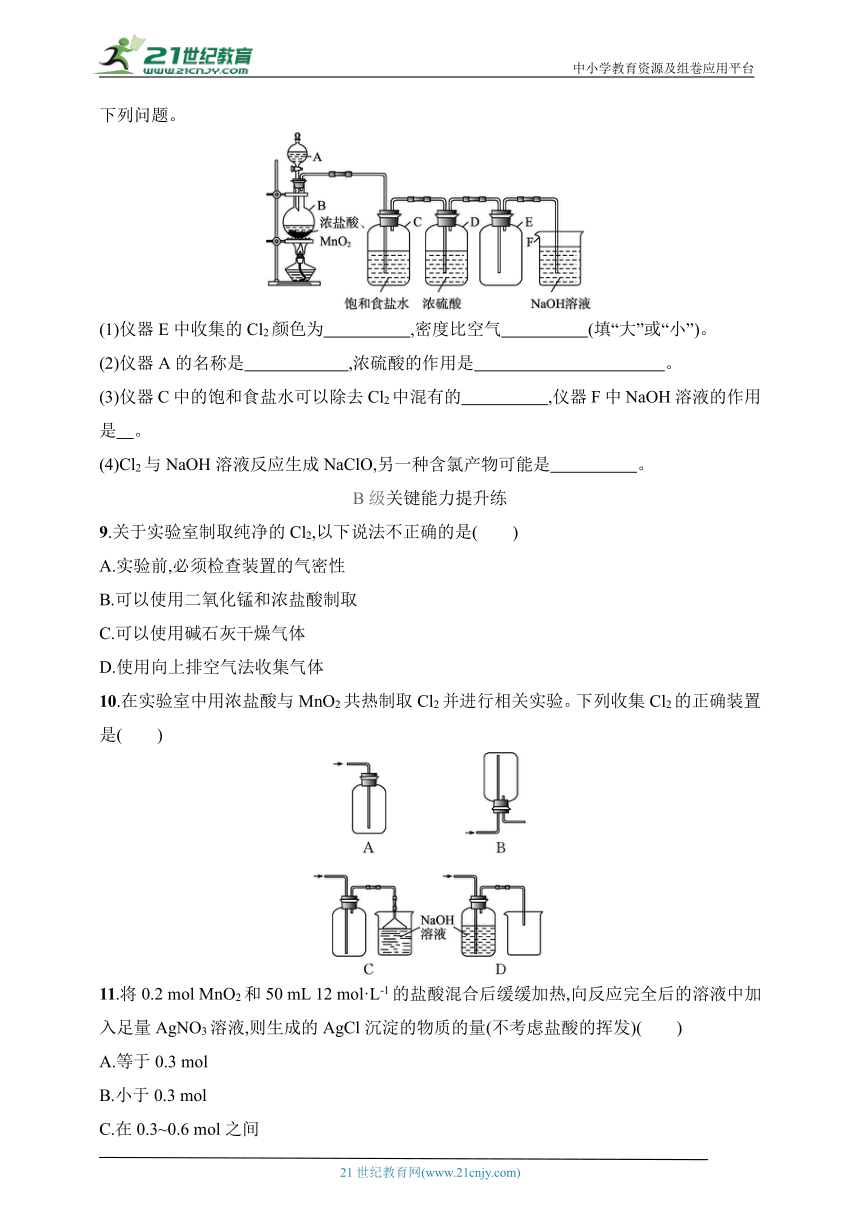
8.氯的单质氯气是一种重要的化工原料,下图为实验室中制取氯气的装置示意图,请回答下列问题。
(1)仪器E中收集的Cl2颜色为 ,密度比空气 (填“大”或“小”)。
(2)仪器A的名称是 ,浓硫酸的作用是 。
(3)仪器C中的饱和食盐水可以除去Cl2中混有的 ,仪器F中NaOH溶液的作用是 。
(4)Cl2与NaOH溶液反应生成NaClO,另一种含氯产物可能是 。
B级关键能力提升练
9.关于实验室制取纯净的Cl2,以下说法不正确的是( )
A.实验前,必须检查装置的气密性
B.可以使用二氧化锰和浓盐酸制取
C.可以使用碱石灰干燥气体
D.使用向上排空气法收集气体
10.在实验室中用浓盐酸与MnO2共热制取Cl2并进行相关实验。下列收集Cl2的正确装置是( )
11.将0.2 mol MnO2和50 mL 12 mol·L-1的盐酸混合后缓缓加热,向反应完全后的溶液中加入足量AgNO3溶液,则生成的AgCl沉淀的物质的量(不考虑盐酸的挥发)( )
A.等于0.3 mol
B.小于0.3 mol
C.在0.3~0.6 mol之间
D.以上结论均不正确
12.下图表示某实验室为制取纯净氯气而设计的装置图,图中A、B是可控制的弹簧铁夹。
(1)烧杯中盛放的液体是 ,其作用是 ,水槽中盛放的液体是 。
(2)简述操作过程(从氯气已经产生开始):在收集氯气之前,应 ;当氯气纯度合乎要求时,应 ;当氯气收集完毕后,应 。
(3)将8.7 g MnO2与含HCl 14.6 g的浓盐酸共热制Cl2,甲同学认为可制得Cl2 7.1 g,乙同学认为制得Cl2的质量小于7.1 g,你认为 (填“甲”或“乙”)同学正确,原因是 。
C级学科素养创新练
13.请用下图所示装置组装一个电解饱和食盐水(电极均为石墨棒)并测定电解时产生的H2的体积和检验Cl2的实验装置(提示:Cl2可与KI反应生成I2,淀粉遇I2变蓝)。
(1)组装装置时,各接口的连接顺序是(填字母代号):A接 、 接 ;B接 、 接 。
(2)证明产物Cl2的实验现象是 。
(3)实验测得产生的氢气体积(已折算成标准状况)为11.2 mL,电解后溶液的体积恰好为50.0 mL,则溶液中NaOH的物质的量浓度为 。
分层作业14 氯气的发现与制备
A级 必备知识基础练
1.D 解析 确定实验室制取气体的操作顺序要注意:①连接好装置后,要先检查装置气密性,后装药品;②装药品的顺序是先加固体,后加液体;③对于有毒的气体,一定要有尾气处理装置。
2.D 解析 Ca(OH)2溶解度较小,用饱和石灰水不能充分吸收氯气。
3.C
4.B 解析 X电极与电源的负极相连,X极生成2 mol H2,A项错误,B项正确;Y电极与电源的正极相连,在Y极生成2 mol Cl2,C项错误;NaOH在X极附近生成,D项错误。
5.B 解析 浓盐酸和二氧化锰反应需加热,A错误;氯气通过饱和食盐水可以去除HCl杂质,且氯气在饱和食盐水中损耗少,B正确;氯气的密度大于空气,收集时用向上排空气法,C错误;氯气有毒,用氢氧化钠溶液吸收尾气,D错误。
6.C 解析 盛装浓盐酸的仪器为分液漏斗,A错误;氯气密度比空气大,应用向上排空气法收集,B错误;加热过程浓盐酸会挥发,有水蒸气产生,C正确;较活泼的金属与酸反应制备氢气不需要加热,D错误。
7.答案 舍勒 MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O NaOH(或KOH)
8.答案 (1)黄绿色 大
(2)分液漏斗 干燥氯气
(3)氯化氢气体(或HCl) 吸收尾气
(4)NaCl
B级 关键能力提升练
9.C
10.C 解析 A中装置集气瓶用单孔橡胶塞塞紧,只能进气,不能排气,瓶内压强增大到一定程度,可能将橡胶塞弹出,A项错误;因为Cl2密度比空气的密度大,用B中装置收集Cl2应短管进气,B项错误;C中装置既能收集Cl2,又能进行尾气处理且防倒吸,C项正确;由于Cl2能和NaOH溶液反应,所以D中装置不能收集到Cl2,D项错误。
11.C 解析 由题意可知n(HCl)=0.6 mol,根据化学方程式MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O可判断出MnO2过量。若0.6 mol HCl完全反应,反应后的溶液中存在0.3 mol Cl-,加入足量AgNO3溶液生成0.3 mol AgCl。但随着反应的进行,盐酸的浓度减小,而稀盐酸与MnO2不反应,所以实际消耗的Cl-的物质的量小于0.3 mol,即反应后溶液中存在的Cl-的物质的量大于0.3 mol,故加入足量AgNO3溶液产生AgCl的物质的量大于0.3 mol、小于0.6 mol,C项正确。
12.答案 (1)NaOH溶液 吸收多余的Cl2 饱和食盐水
(2)打开B夹,关闭A夹 打开A夹,关闭B夹 关闭A夹,打开B夹
(3)乙 ①浓盐酸易挥发;②随着反应进行,浓盐酸浓度会降低,稀盐酸不能与MnO2继续反应
解析 用饱和食盐水可洗去Cl2中混有的HCl,又可减少Cl2损失,可用排饱和食盐水法收集Cl2。处理制Cl2的尾气用强碱溶液。由于浓盐酸易挥发,稀盐酸不能与MnO2反应,故用浓盐酸与MnO2共热制Cl2时HCl不能完全反应。
C级 学科素养创新练
13.答案 (1)G F H D E C
(2)淀粉碘化钾溶液变蓝 (3)0.02 mol·L-1
解析 (1)用石墨棒作电极电解饱和食盐水时,在与电源正极相连接的电极上产生氯气,在与电源负极相连接的电极上产生氢气和氢氧化钠,即A端生成氢气,B端生成氯气。则A接储气瓶的G→F,把水排入量筒内,用量筒中的水的体积确定产生H2的体积;B接洗气瓶的D→E,生成的Cl2在洗气瓶中使淀粉碘化钾溶液变蓝,E→C,多余的Cl2用NaOH溶液吸收。(2)Cl2可与KI反应生成I2,淀粉遇I2变蓝色。(3)氢气物质的量为=0.000 5 mol,由2NaCl+2H2O2NaOH+Cl2↑+H2↑,可知n(NaOH)=2n(H2)=0.001 mol,则c(NaOH)==0.02 mol·L-1。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
2025苏教版化学必修第一册
分层作业14 氯气的发现与制备
A级必备知识基础练
1.在制氯气时有如下操作,操作顺序正确的是( )
①连接好装置,检查气密性
②缓缓加热,加快反应,使气体均匀逸出
③在圆底烧瓶中加入二氧化锰粉末
④从盛有浓盐酸的分液漏斗中将浓盐酸缓缓滴入烧瓶中
⑤将多余的Cl2用NaOH溶液吸收
⑥用向上排空气法收集氯气
A.①②③④⑤⑥
B.③④②①⑥⑤
C.①④③②⑥⑤
D.①③④②⑥⑤
2.实验室制氯气的尾气中含有较多的氯气,有毒,要吸收这些尾气,下列试剂最适合的是( )
A.饱和石灰水 B.饱和食盐水
C.自来水 D.烧碱溶液
3.下列关于实验室用MnO2制取Cl2的叙述不正确的是( )
A.需用浓盐酸
B.缓慢加热反应
C.充分反应后,HCl无剩余
D.多余氯气常用较浓的碱液吸收
4.根据电解饱和食盐水的化学方程式:2NaCl+2H2OH2↑+Cl2↑+2NaOH,每生成4 mol 的NaOH,下列说法正确的是( )
A.在X极生成2 mol Cl2
B.在X极生成2 mol H2
C.在Y极生成4 mol Cl2
D.NaOH在Y极生成
5.[2024北京朝阳高一检测]实验室制取氯气,下列装置(“→”表示气流方向)和试剂选择均正确的是( )
A.制备Cl2
B.除去Cl2中的杂质
C.收集Cl2
D.吸收Cl2尾气
6.实验室制备氯气的反应为MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O,其装置如图,有关说法正确的是( )
A.盛装浓盐酸的仪器为长颈漏斗
B.可用向下排空气法收集氯气
C.制取的氯气中混有HCl和水蒸气
D.可用该装置来制备氢气
7.1774年瑞典化学家 在研究软锰矿(主要成分是MnO2)的过程中,将它与浓盐酸混合加热,产生了一种黄绿色的气体,有强烈的刺激性气味。这种方法至今还是实验室制取该气体的常用方法,请写出该反应的化学方程式: 。在实验室中,制取这种黄绿色气体通常用 (填化学式)溶液来吸收其尾气。
8.氯的单质氯气是一种重要的化工原料,下图为实验室中制取氯气的装置示意图,请回答下列问题。
(1)仪器E中收集的Cl2颜色为 ,密度比空气 (填“大”或“小”)。
(2)仪器A的名称是 ,浓硫酸的作用是 。
(3)仪器C中的饱和食盐水可以除去Cl2中混有的 ,仪器F中NaOH溶液的作用是 。
(4)Cl2与NaOH溶液反应生成NaClO,另一种含氯产物可能是 。
B级关键能力提升练
9.关于实验室制取纯净的Cl2,以下说法不正确的是( )
A.实验前,必须检查装置的气密性
B.可以使用二氧化锰和浓盐酸制取
C.可以使用碱石灰干燥气体
D.使用向上排空气法收集气体
10.在实验室中用浓盐酸与MnO2共热制取Cl2并进行相关实验。下列收集Cl2的正确装置是( )
11.将0.2 mol MnO2和50 mL 12 mol·L-1的盐酸混合后缓缓加热,向反应完全后的溶液中加入足量AgNO3溶液,则生成的AgCl沉淀的物质的量(不考虑盐酸的挥发)( )
A.等于0.3 mol
B.小于0.3 mol
C.在0.3~0.6 mol之间
D.以上结论均不正确
12.下图表示某实验室为制取纯净氯气而设计的装置图,图中A、B是可控制的弹簧铁夹。
(1)烧杯中盛放的液体是 ,其作用是 ,水槽中盛放的液体是 。
(2)简述操作过程(从氯气已经产生开始):在收集氯气之前,应 ;当氯气纯度合乎要求时,应 ;当氯气收集完毕后,应 。
(3)将8.7 g MnO2与含HCl 14.6 g的浓盐酸共热制Cl2,甲同学认为可制得Cl2 7.1 g,乙同学认为制得Cl2的质量小于7.1 g,你认为 (填“甲”或“乙”)同学正确,原因是 。
C级学科素养创新练
13.请用下图所示装置组装一个电解饱和食盐水(电极均为石墨棒)并测定电解时产生的H2的体积和检验Cl2的实验装置(提示:Cl2可与KI反应生成I2,淀粉遇I2变蓝)。
(1)组装装置时,各接口的连接顺序是(填字母代号):A接 、 接 ;B接 、 接 。
(2)证明产物Cl2的实验现象是 。
(3)实验测得产生的氢气体积(已折算成标准状况)为11.2 mL,电解后溶液的体积恰好为50.0 mL,则溶液中NaOH的物质的量浓度为 。
分层作业14 氯气的发现与制备
A级 必备知识基础练
1.D 解析 确定实验室制取气体的操作顺序要注意:①连接好装置后,要先检查装置气密性,后装药品;②装药品的顺序是先加固体,后加液体;③对于有毒的气体,一定要有尾气处理装置。
2.D 解析 Ca(OH)2溶解度较小,用饱和石灰水不能充分吸收氯气。
3.C
4.B 解析 X电极与电源的负极相连,X极生成2 mol H2,A项错误,B项正确;Y电极与电源的正极相连,在Y极生成2 mol Cl2,C项错误;NaOH在X极附近生成,D项错误。
5.B 解析 浓盐酸和二氧化锰反应需加热,A错误;氯气通过饱和食盐水可以去除HCl杂质,且氯气在饱和食盐水中损耗少,B正确;氯气的密度大于空气,收集时用向上排空气法,C错误;氯气有毒,用氢氧化钠溶液吸收尾气,D错误。
6.C 解析 盛装浓盐酸的仪器为分液漏斗,A错误;氯气密度比空气大,应用向上排空气法收集,B错误;加热过程浓盐酸会挥发,有水蒸气产生,C正确;较活泼的金属与酸反应制备氢气不需要加热,D错误。
7.答案 舍勒 MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O NaOH(或KOH)
8.答案 (1)黄绿色 大
(2)分液漏斗 干燥氯气
(3)氯化氢气体(或HCl) 吸收尾气
(4)NaCl
B级 关键能力提升练
9.C
10.C 解析 A中装置集气瓶用单孔橡胶塞塞紧,只能进气,不能排气,瓶内压强增大到一定程度,可能将橡胶塞弹出,A项错误;因为Cl2密度比空气的密度大,用B中装置收集Cl2应短管进气,B项错误;C中装置既能收集Cl2,又能进行尾气处理且防倒吸,C项正确;由于Cl2能和NaOH溶液反应,所以D中装置不能收集到Cl2,D项错误。
11.C 解析 由题意可知n(HCl)=0.6 mol,根据化学方程式MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O可判断出MnO2过量。若0.6 mol HCl完全反应,反应后的溶液中存在0.3 mol Cl-,加入足量AgNO3溶液生成0.3 mol AgCl。但随着反应的进行,盐酸的浓度减小,而稀盐酸与MnO2不反应,所以实际消耗的Cl-的物质的量小于0.3 mol,即反应后溶液中存在的Cl-的物质的量大于0.3 mol,故加入足量AgNO3溶液产生AgCl的物质的量大于0.3 mol、小于0.6 mol,C项正确。
12.答案 (1)NaOH溶液 吸收多余的Cl2 饱和食盐水
(2)打开B夹,关闭A夹 打开A夹,关闭B夹 关闭A夹,打开B夹
(3)乙 ①浓盐酸易挥发;②随着反应进行,浓盐酸浓度会降低,稀盐酸不能与MnO2继续反应
解析 用饱和食盐水可洗去Cl2中混有的HCl,又可减少Cl2损失,可用排饱和食盐水法收集Cl2。处理制Cl2的尾气用强碱溶液。由于浓盐酸易挥发,稀盐酸不能与MnO2反应,故用浓盐酸与MnO2共热制Cl2时HCl不能完全反应。
C级 学科素养创新练
13.答案 (1)G F H D E C
(2)淀粉碘化钾溶液变蓝 (3)0.02 mol·L-1
解析 (1)用石墨棒作电极电解饱和食盐水时,在与电源正极相连接的电极上产生氯气,在与电源负极相连接的电极上产生氢气和氢氧化钠,即A端生成氢气,B端生成氯气。则A接储气瓶的G→F,把水排入量筒内,用量筒中的水的体积确定产生H2的体积;B接洗气瓶的D→E,生成的Cl2在洗气瓶中使淀粉碘化钾溶液变蓝,E→C,多余的Cl2用NaOH溶液吸收。(2)Cl2可与KI反应生成I2,淀粉遇I2变蓝色。(3)氢气物质的量为=0.000 5 mol,由2NaCl+2H2O2NaOH+Cl2↑+H2↑,可知n(NaOH)=2n(H2)=0.001 mol,则c(NaOH)==0.02 mol·L-1。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
