专题3 从海水中获得的化学物质 分层作业15 氯气的性质及应用--2025苏教版化学必修第一册同步练习题(含答案)
文档属性
| 名称 | 专题3 从海水中获得的化学物质 分层作业15 氯气的性质及应用--2025苏教版化学必修第一册同步练习题(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 433.1KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-24 00:00:00 | ||
图片预览

文档简介
中小学教育资源及组卷应用平台
2025苏教版化学必修第一册
分层作业15 氯气的性质及应用
A级必备知识基础练
1.下列物质中同时含有氯气分子(Cl2)和氯离子(Cl-)的是( )
A.液氯 B.新制氯水
C.CaCl2溶液 D.KClO3溶液
2.下列关于氯气的叙述中,不正确的是( )
A.氯气是一种有毒的气体
B.氯气、氯水、液氯是同一种物质
C.氯气与水的反应是可逆反应
D.氯气是一种黄绿色、有刺激性气味的气体
3.关于氯及其化合物,下列说法正确的是( )
A.工业上用氯气和石灰乳制备漂白粉,漂白粉是纯净物
B.检验Cl2中是否混有HCl气体的方法是将气体通入硝酸银溶液
C.Cl2在化学反应中其元素化合价既能升高又能降低
D.铁粉在Cl2中燃烧制得FeCl2
4.下列说法不正确的是( )
①钠、氢气都能在氯气中燃烧生成白色烟雾
②铜丝在氯气中燃烧,生成蓝绿色的氯化铜
③液氯就是氯气的水溶液,它能使干燥的有色布条褪色
④久置的氯水,因氯气几乎完全挥发掉,剩下的就是水
A.仅③ B.仅②和③
C.仅①和④ D.①②③④
5.向含酚酞的氢氧化钠溶液中慢慢滴加氯水,滴到一定量时,红色突然褪去。某同学为探究该实验现象产生的原因,进行了如下操作,不正确的是( )
A.预测原因:氯水中的酸与氢氧化钠溶液发生中和反应,将氢氧化钠消耗完所致
B.实验设计:往褪色后的溶液中继续滴加氢氧化钠溶液,观察溶液是否重新变红
C.解释现象:往褪色后的溶液中滴加氢氧化钠溶液后不变红,说明不是中和反应所致
D.反思评价:溶液褪色的原因可能是氯水中的氯分子具有漂白性
6.下列化学反应中,有两种盐生成的是( )
①氯气和铜反应 ②氯气和氢氧化钠溶液反应
③氯化钠溶液和硝酸银溶液反应 ④氯气和水反应
A.③④ B.②③
C.①②③ D.②④
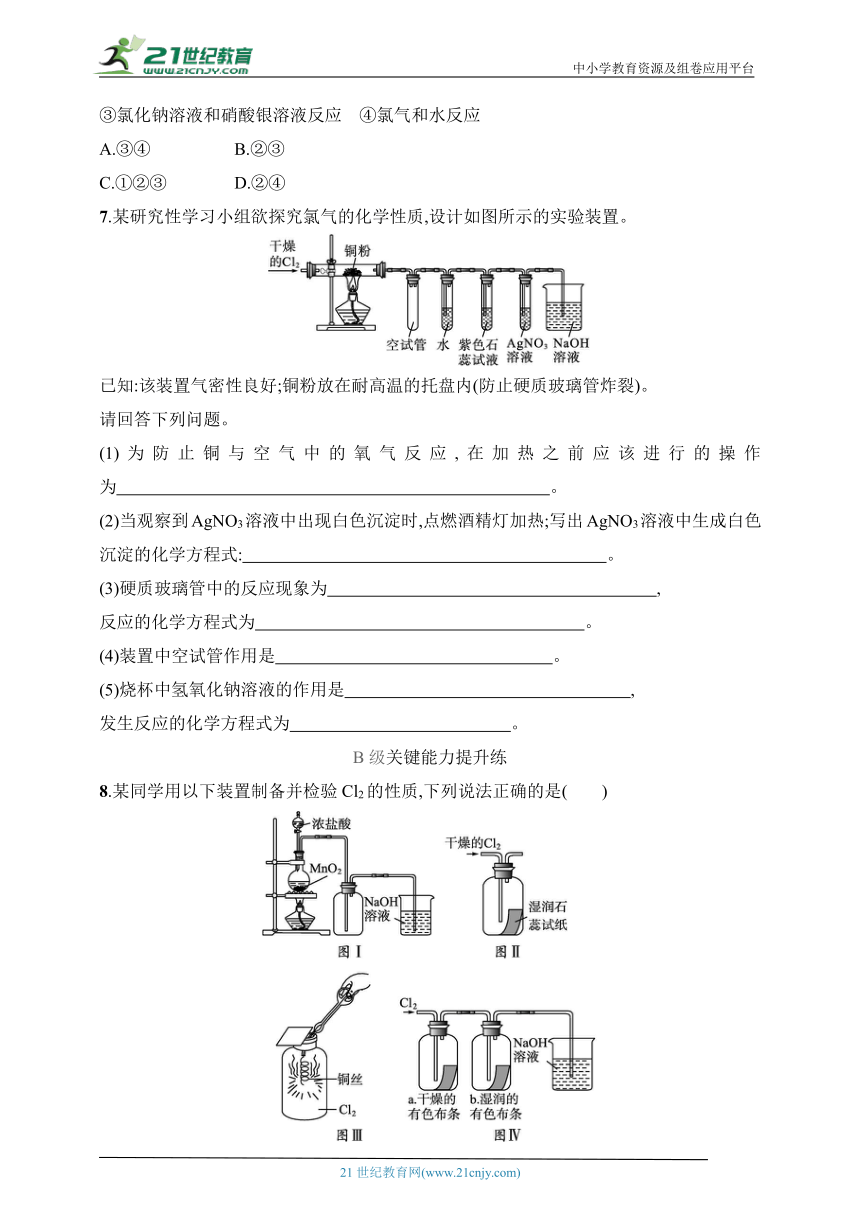
7.某研究性学习小组欲探究氯气的化学性质,设计如图所示的实验装置。
已知:该装置气密性良好;铜粉放在耐高温的托盘内(防止硬质玻璃管炸裂)。
请回答下列问题。
(1)为防止铜与空气中的氧气反应,在加热之前应该进行的操作为 。
(2)当观察到AgNO3溶液中出现白色沉淀时,点燃酒精灯加热;写出AgNO3溶液中生成白色沉淀的化学方程式: 。
(3)硬质玻璃管中的反应现象为 ,
反应的化学方程式为 。
(4)装置中空试管作用是 。
(5)烧杯中氢氧化钠溶液的作用是 ,
发生反应的化学方程式为 。
B级关键能力提升练
8.某同学用以下装置制备并检验Cl2的性质,下列说法正确的是( )
A.图Ⅰ:若MnO2过量,则浓盐酸可全部消耗完
B.图Ⅱ:湿润石蕊试纸变红色
C.图Ⅲ:产生白色的烟
D.图Ⅳ:干燥的有色布条不褪色
9.“84”消毒液是常用的消毒剂,下列有关“84”消毒液的叙述不正确的是( )
A.“84”消毒液的有效成分是次氯酸钠
B.使用时向“84”消毒液中加入少量醋酸,其消毒能力更强
C.“84”消毒液可适用于皮毛制品及钢铁制品的消毒
D.“84”消毒液、医用酒精均可用于消毒
10.新制氯水的成分复杂,但饱和氯水久置后,成分发生变化,下列粒子①Cl2 ②H2O ③Cl-
④HClO ⑤H+,因饱和氯水久置于空气中而减少的是( )
A.仅有①②③ B.仅有①④
C.仅有②④ D.仅有①②④
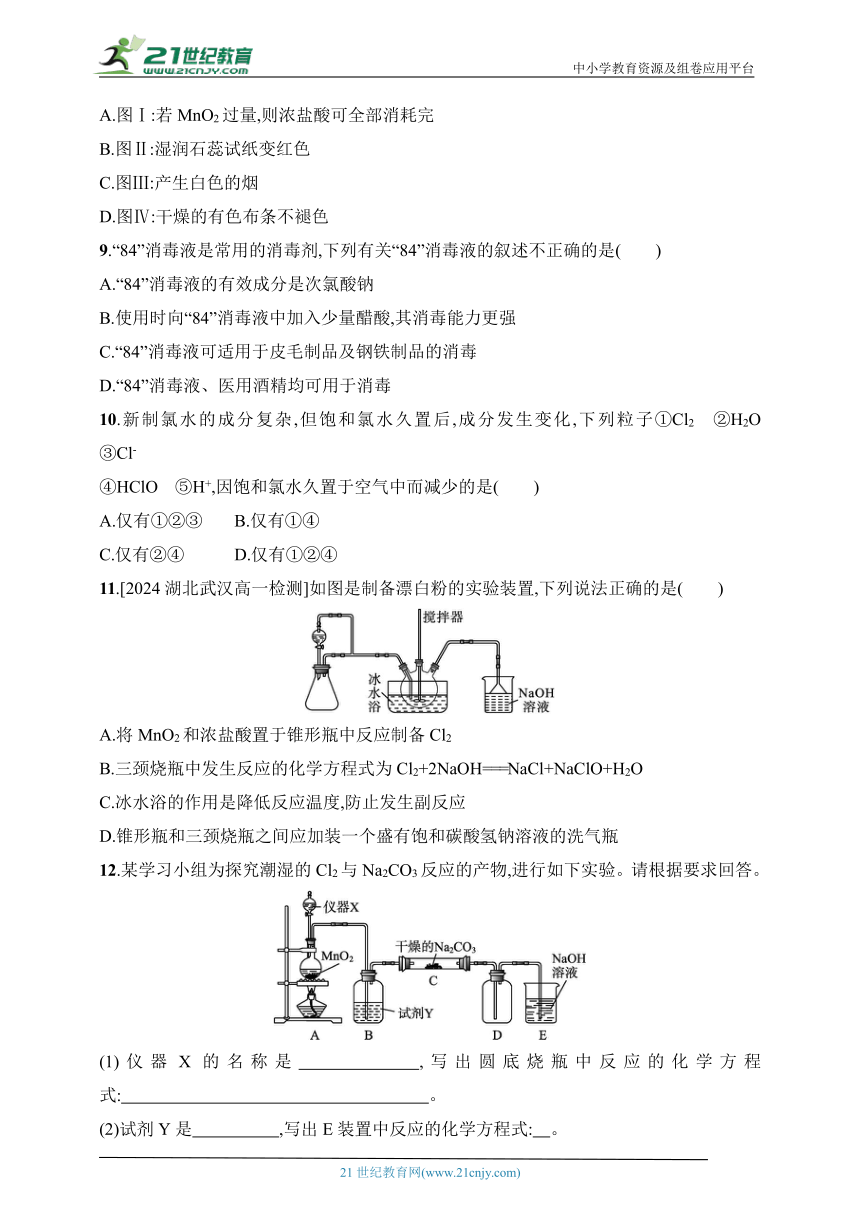
11.[2024湖北武汉高一检测]如图是制备漂白粉的实验装置,下列说法正确的是( )
A.将MnO2和浓盐酸置于锥形瓶中反应制备Cl2
B.三颈烧瓶中发生反应的化学方程式为Cl2+2NaOH===NaCl+NaClO+H2O
C.冰水浴的作用是降低反应温度,防止发生副反应
D.锥形瓶和三颈烧瓶之间应加装一个盛有饱和碳酸氢钠溶液的洗气瓶
12.某学习小组为探究潮湿的Cl2与Na2CO3反应的产物,进行如下实验。请根据要求回答。
(1)仪器X的名称是 ,写出圆底烧瓶中反应的化学方程式: 。
(2)试剂Y是 ,写出E装置中反应的化学方程式: 。
(3)装置C中Cl2与Na2CO3以等物质的量反应,且生成的气体产物仅为Cl2O,固体产物有两种,其中之一是NaHCO3,另一产物的化学式是 。
(4)NaHCO3溶液显 (填“酸”或“碱”)性。
C级学科素养创新练
13.漂白粉和明矾是政府抗震救灾的必需物资。请按要求回答下列问题:
(1)漂白粉是一种 (填“纯净物”或“混合物”),有效成分的化学式为 。
(2)工业上制备漂白粉的化学方程式为 。
(3)漂白粉溶于水有杀菌消毒作用,其原理是(用化学方程式表示) 。
(4)家庭中使用漂白粉时,为了增强漂白能力,可加入的少量物质是 (填字母)。
A.食醋
B.食盐
C.烧碱
D.纯碱
(5)某同学在探究漂白粉溶液的性质时,在漂白粉溶液中加入几滴无色酚酞溶液,发现溶液呈红色,随后溶液迅速褪色,说明漂白粉溶液呈 性,并具有 性。
(6)明矾是无色晶体,其化学式为KAl(SO4)2·12H2O,是一种常用的净水剂。证明其溶液中含有硫酸根离子的方法为 。
分层作业15 氯气的性质及应用
A级 必备知识基础练
1.B 2.B
3.C 解析 氯气和石灰乳反应生成氯化钙、次氯酸钙,故漂白粉不是纯净物,故A错误;Cl2和HCl的溶液都能与硝酸银反应生成沉淀,则将混合气体通入硝酸银溶液无法检验是否含有HCl,故B错误;氯气中Cl元素的化合价为0价,为中间价态,Cl原子既能失去电子也能得到电子,所以Cl2在化学反应中其元素化合价既能升高又能降低,故C正确;铁粉和氯气反应生成氯化铁,故D错误。
4.D 解析 ①Na在Cl2中燃烧生成白烟,无雾产生;氢气在氯气中燃烧后生成白雾,无烟产生。②CuCl2为棕黄色固体。③液氯为液态的氯气单质,为纯净物,不能使干燥的有色布条褪色。④久置的氯水因HClO分解而变为稀盐酸。
5.D 解析 碱溶液能使酚酞变红色,若氯水中的酸与氢氧化钠溶液发生中和反应,将氢氧化钠消耗完,则酚酞褪色,A正确;若酚酞褪色由氢氧化钠消耗完所致,则溶液褪色后酚酞仍然存在,往褪色后的溶液中继续滴加氢氧化钠溶液,溶液将重新变红,B正确;往褪色后的溶液中滴加氢氧化钠溶液后不变红,说明褪色后溶液中酚酞已经不存在,说明不是中和反应所致,C正确;溶液褪色的原因可能是氯水中的次氯酸具有漂白性,氯气不具有漂白性,D不正确。
6.B 解析 氯气和铜反应生成氯化铜,氯气和氢氧化钠溶液反应生成NaCl和NaClO两种盐,氯化钠溶液和硝酸银溶液反应生成氯化银和硝酸钠两种盐,氯气和水反应生成盐酸和次氯酸两种酸,所以选B。
7.答案 (1)通入氯气排尽装置中的空气
(2)Cl2+H2OHCl+HClO、HCl+AgNO3AgCl↓+HNO3
(3)剧烈反应,产生棕黄色的烟 Cu+Cl2 CuCl2
(4)防止右侧试管中的水倒吸入硬质玻璃管中,使硬质玻璃管炸裂
(5)吸收尾气中的氯气,防止污染空气 Cl2+2NaOHNaCl+NaClO+H2O
B级 关键能力提升练
8.D 解析 若MnO2过量,浓盐酸随着反应进行,浓度减小到一定程度,变为稀盐酸,不再与二氧化锰继续反应,故盐酸不能全部消耗,A错误;Cl2使湿润石蕊试纸先变红后褪色,B错误;铜在氯气中燃烧生成CuCl2,产生棕黄色烟,C错误;湿润的有色布条能褪色,是因为氯气与水反应生成HCl和次氯酸,次氯酸具有漂白性,使有色布条褪色,而氯气没有漂白性,不能使干燥的有色布条褪色,D正确。
9.C 解析 “84”消毒液的有效成分是次氯酸钠,A正确;使用时向“84”消毒液中加入少量醋酸,醋酸和次氯酸根离子反应生成次氯酸,使消毒能力更强,B正确;“84”消毒液具有强氧化性,不适用于皮毛制品消毒,C错误;“84”消毒液和医用酒精均可用于消毒,D正确。
10.D 解析 Cl2与水反应:Cl2+H2OHClO+HCl,新制氯水中含有三种分子(Cl2、H2O、HClO)和四种离子(H+、Cl-、ClO-及少量OH-);次氯酸不稳定,受热易分解,HClO分解导致了Cl2的不断反应,最后变成了HCl溶液,同时会有水参与反应,所以减少的是①Cl2、②H2O、④HClO。
11.C 解析 MnO2和浓盐酸反应制备Cl2需加热,A错误;漂白粉的成分中含有Ca(ClO)2和CaCl2,应由Cl2和Ca(OH)2制备,B错误;该反应放热,为避免发生副反应,需用冰水浴降低温度,C正确;饱和碳酸氢钠溶液能吸收Cl2,同时有二氧化碳产生,应用饱和氯化钠溶液吸收Cl2中的HCl,D错误。
12.答案 (1)分液漏斗 MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O
(2)饱和NaCl溶液 Cl2+2NaOHNaCl+NaClO+H2O
(3)NaCl (4)碱
C级 学科素养创新练
13.答案 (1)混合物 Ca(ClO)2
(2)2Cl2+2Ca(OH)2===CaCl2+Ca(ClO)2+2H2O
(3)Ca(ClO)2+CO2+H2O===CaCO3↓+2HClO
(4)A (5)碱 漂白
(6)先加入盐酸酸化,如无现象,再加入氯化钡溶液,如生成白色沉淀,可证明含有硫酸根离子
解析 (1)漂白粉的主要成分是氯化钙、次氯酸钙,其有效成分为次氯酸钙,为混合物。(2)漂白粉是用Cl2与石灰乳反应制取的,反应的化学方程式为2Cl2+2Ca(OH)2CaCl2+Ca(ClO)2+2H2O。(3)次氯酸钙能吸收空气中的水和二氧化碳,生成的次氯酸具有杀菌消毒作用,漂白粉生效的反应原理用化学方程式表示为Ca(ClO)2+CO2+H2OCaCO3↓+2HClO。(4)为增强漂白粉的漂白能力,可用酸与次氯酸钙反应生成次氯酸,食醋中含有醋酸,故A符合。(5)在漂白粉溶液中加入几滴无色酚酞溶液,发现溶液呈红色,随后溶液迅速褪色,说明漂白粉溶液呈碱性,且具有漂白性。(6)检验硫酸根离子,可先加入盐酸酸化,如无现象,再加入氯化钡溶液,如生成白色沉淀,可证明含有硫酸根离子。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
2025苏教版化学必修第一册
分层作业15 氯气的性质及应用
A级必备知识基础练
1.下列物质中同时含有氯气分子(Cl2)和氯离子(Cl-)的是( )
A.液氯 B.新制氯水
C.CaCl2溶液 D.KClO3溶液
2.下列关于氯气的叙述中,不正确的是( )
A.氯气是一种有毒的气体
B.氯气、氯水、液氯是同一种物质
C.氯气与水的反应是可逆反应
D.氯气是一种黄绿色、有刺激性气味的气体
3.关于氯及其化合物,下列说法正确的是( )
A.工业上用氯气和石灰乳制备漂白粉,漂白粉是纯净物
B.检验Cl2中是否混有HCl气体的方法是将气体通入硝酸银溶液
C.Cl2在化学反应中其元素化合价既能升高又能降低
D.铁粉在Cl2中燃烧制得FeCl2
4.下列说法不正确的是( )
①钠、氢气都能在氯气中燃烧生成白色烟雾
②铜丝在氯气中燃烧,生成蓝绿色的氯化铜
③液氯就是氯气的水溶液,它能使干燥的有色布条褪色
④久置的氯水,因氯气几乎完全挥发掉,剩下的就是水
A.仅③ B.仅②和③
C.仅①和④ D.①②③④
5.向含酚酞的氢氧化钠溶液中慢慢滴加氯水,滴到一定量时,红色突然褪去。某同学为探究该实验现象产生的原因,进行了如下操作,不正确的是( )
A.预测原因:氯水中的酸与氢氧化钠溶液发生中和反应,将氢氧化钠消耗完所致
B.实验设计:往褪色后的溶液中继续滴加氢氧化钠溶液,观察溶液是否重新变红
C.解释现象:往褪色后的溶液中滴加氢氧化钠溶液后不变红,说明不是中和反应所致
D.反思评价:溶液褪色的原因可能是氯水中的氯分子具有漂白性
6.下列化学反应中,有两种盐生成的是( )
①氯气和铜反应 ②氯气和氢氧化钠溶液反应
③氯化钠溶液和硝酸银溶液反应 ④氯气和水反应
A.③④ B.②③
C.①②③ D.②④
7.某研究性学习小组欲探究氯气的化学性质,设计如图所示的实验装置。
已知:该装置气密性良好;铜粉放在耐高温的托盘内(防止硬质玻璃管炸裂)。
请回答下列问题。
(1)为防止铜与空气中的氧气反应,在加热之前应该进行的操作为 。
(2)当观察到AgNO3溶液中出现白色沉淀时,点燃酒精灯加热;写出AgNO3溶液中生成白色沉淀的化学方程式: 。
(3)硬质玻璃管中的反应现象为 ,
反应的化学方程式为 。
(4)装置中空试管作用是 。
(5)烧杯中氢氧化钠溶液的作用是 ,
发生反应的化学方程式为 。
B级关键能力提升练
8.某同学用以下装置制备并检验Cl2的性质,下列说法正确的是( )
A.图Ⅰ:若MnO2过量,则浓盐酸可全部消耗完
B.图Ⅱ:湿润石蕊试纸变红色
C.图Ⅲ:产生白色的烟
D.图Ⅳ:干燥的有色布条不褪色
9.“84”消毒液是常用的消毒剂,下列有关“84”消毒液的叙述不正确的是( )
A.“84”消毒液的有效成分是次氯酸钠
B.使用时向“84”消毒液中加入少量醋酸,其消毒能力更强
C.“84”消毒液可适用于皮毛制品及钢铁制品的消毒
D.“84”消毒液、医用酒精均可用于消毒
10.新制氯水的成分复杂,但饱和氯水久置后,成分发生变化,下列粒子①Cl2 ②H2O ③Cl-
④HClO ⑤H+,因饱和氯水久置于空气中而减少的是( )
A.仅有①②③ B.仅有①④
C.仅有②④ D.仅有①②④
11.[2024湖北武汉高一检测]如图是制备漂白粉的实验装置,下列说法正确的是( )
A.将MnO2和浓盐酸置于锥形瓶中反应制备Cl2
B.三颈烧瓶中发生反应的化学方程式为Cl2+2NaOH===NaCl+NaClO+H2O
C.冰水浴的作用是降低反应温度,防止发生副反应
D.锥形瓶和三颈烧瓶之间应加装一个盛有饱和碳酸氢钠溶液的洗气瓶
12.某学习小组为探究潮湿的Cl2与Na2CO3反应的产物,进行如下实验。请根据要求回答。
(1)仪器X的名称是 ,写出圆底烧瓶中反应的化学方程式: 。
(2)试剂Y是 ,写出E装置中反应的化学方程式: 。
(3)装置C中Cl2与Na2CO3以等物质的量反应,且生成的气体产物仅为Cl2O,固体产物有两种,其中之一是NaHCO3,另一产物的化学式是 。
(4)NaHCO3溶液显 (填“酸”或“碱”)性。
C级学科素养创新练
13.漂白粉和明矾是政府抗震救灾的必需物资。请按要求回答下列问题:
(1)漂白粉是一种 (填“纯净物”或“混合物”),有效成分的化学式为 。
(2)工业上制备漂白粉的化学方程式为 。
(3)漂白粉溶于水有杀菌消毒作用,其原理是(用化学方程式表示) 。
(4)家庭中使用漂白粉时,为了增强漂白能力,可加入的少量物质是 (填字母)。
A.食醋
B.食盐
C.烧碱
D.纯碱
(5)某同学在探究漂白粉溶液的性质时,在漂白粉溶液中加入几滴无色酚酞溶液,发现溶液呈红色,随后溶液迅速褪色,说明漂白粉溶液呈 性,并具有 性。
(6)明矾是无色晶体,其化学式为KAl(SO4)2·12H2O,是一种常用的净水剂。证明其溶液中含有硫酸根离子的方法为 。
分层作业15 氯气的性质及应用
A级 必备知识基础练
1.B 2.B
3.C 解析 氯气和石灰乳反应生成氯化钙、次氯酸钙,故漂白粉不是纯净物,故A错误;Cl2和HCl的溶液都能与硝酸银反应生成沉淀,则将混合气体通入硝酸银溶液无法检验是否含有HCl,故B错误;氯气中Cl元素的化合价为0价,为中间价态,Cl原子既能失去电子也能得到电子,所以Cl2在化学反应中其元素化合价既能升高又能降低,故C正确;铁粉和氯气反应生成氯化铁,故D错误。
4.D 解析 ①Na在Cl2中燃烧生成白烟,无雾产生;氢气在氯气中燃烧后生成白雾,无烟产生。②CuCl2为棕黄色固体。③液氯为液态的氯气单质,为纯净物,不能使干燥的有色布条褪色。④久置的氯水因HClO分解而变为稀盐酸。
5.D 解析 碱溶液能使酚酞变红色,若氯水中的酸与氢氧化钠溶液发生中和反应,将氢氧化钠消耗完,则酚酞褪色,A正确;若酚酞褪色由氢氧化钠消耗完所致,则溶液褪色后酚酞仍然存在,往褪色后的溶液中继续滴加氢氧化钠溶液,溶液将重新变红,B正确;往褪色后的溶液中滴加氢氧化钠溶液后不变红,说明褪色后溶液中酚酞已经不存在,说明不是中和反应所致,C正确;溶液褪色的原因可能是氯水中的次氯酸具有漂白性,氯气不具有漂白性,D不正确。
6.B 解析 氯气和铜反应生成氯化铜,氯气和氢氧化钠溶液反应生成NaCl和NaClO两种盐,氯化钠溶液和硝酸银溶液反应生成氯化银和硝酸钠两种盐,氯气和水反应生成盐酸和次氯酸两种酸,所以选B。
7.答案 (1)通入氯气排尽装置中的空气
(2)Cl2+H2OHCl+HClO、HCl+AgNO3AgCl↓+HNO3
(3)剧烈反应,产生棕黄色的烟 Cu+Cl2 CuCl2
(4)防止右侧试管中的水倒吸入硬质玻璃管中,使硬质玻璃管炸裂
(5)吸收尾气中的氯气,防止污染空气 Cl2+2NaOHNaCl+NaClO+H2O
B级 关键能力提升练
8.D 解析 若MnO2过量,浓盐酸随着反应进行,浓度减小到一定程度,变为稀盐酸,不再与二氧化锰继续反应,故盐酸不能全部消耗,A错误;Cl2使湿润石蕊试纸先变红后褪色,B错误;铜在氯气中燃烧生成CuCl2,产生棕黄色烟,C错误;湿润的有色布条能褪色,是因为氯气与水反应生成HCl和次氯酸,次氯酸具有漂白性,使有色布条褪色,而氯气没有漂白性,不能使干燥的有色布条褪色,D正确。
9.C 解析 “84”消毒液的有效成分是次氯酸钠,A正确;使用时向“84”消毒液中加入少量醋酸,醋酸和次氯酸根离子反应生成次氯酸,使消毒能力更强,B正确;“84”消毒液具有强氧化性,不适用于皮毛制品消毒,C错误;“84”消毒液和医用酒精均可用于消毒,D正确。
10.D 解析 Cl2与水反应:Cl2+H2OHClO+HCl,新制氯水中含有三种分子(Cl2、H2O、HClO)和四种离子(H+、Cl-、ClO-及少量OH-);次氯酸不稳定,受热易分解,HClO分解导致了Cl2的不断反应,最后变成了HCl溶液,同时会有水参与反应,所以减少的是①Cl2、②H2O、④HClO。
11.C 解析 MnO2和浓盐酸反应制备Cl2需加热,A错误;漂白粉的成分中含有Ca(ClO)2和CaCl2,应由Cl2和Ca(OH)2制备,B错误;该反应放热,为避免发生副反应,需用冰水浴降低温度,C正确;饱和碳酸氢钠溶液能吸收Cl2,同时有二氧化碳产生,应用饱和氯化钠溶液吸收Cl2中的HCl,D错误。
12.答案 (1)分液漏斗 MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O
(2)饱和NaCl溶液 Cl2+2NaOHNaCl+NaClO+H2O
(3)NaCl (4)碱
C级 学科素养创新练
13.答案 (1)混合物 Ca(ClO)2
(2)2Cl2+2Ca(OH)2===CaCl2+Ca(ClO)2+2H2O
(3)Ca(ClO)2+CO2+H2O===CaCO3↓+2HClO
(4)A (5)碱 漂白
(6)先加入盐酸酸化,如无现象,再加入氯化钡溶液,如生成白色沉淀,可证明含有硫酸根离子
解析 (1)漂白粉的主要成分是氯化钙、次氯酸钙,其有效成分为次氯酸钙,为混合物。(2)漂白粉是用Cl2与石灰乳反应制取的,反应的化学方程式为2Cl2+2Ca(OH)2CaCl2+Ca(ClO)2+2H2O。(3)次氯酸钙能吸收空气中的水和二氧化碳,生成的次氯酸具有杀菌消毒作用,漂白粉生效的反应原理用化学方程式表示为Ca(ClO)2+CO2+H2OCaCO3↓+2HClO。(4)为增强漂白粉的漂白能力,可用酸与次氯酸钙反应生成次氯酸,食醋中含有醋酸,故A符合。(5)在漂白粉溶液中加入几滴无色酚酞溶液,发现溶液呈红色,随后溶液迅速褪色,说明漂白粉溶液呈碱性,且具有漂白性。(6)检验硫酸根离子,可先加入盐酸酸化,如无现象,再加入氯化钡溶液,如生成白色沉淀,可证明含有硫酸根离子。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
