鲁教版九年级化学下册7.1.2酸的化学性质课件
文档属性
| 名称 | 鲁教版九年级化学下册7.1.2酸的化学性质课件 |

|
|
| 格式 | ppt | ||
| 文件大小 | 18.5MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-24 00:00:00 | ||
图片预览







文档简介
(共20张PPT)
第七章 认识酸和碱
7.1.2酸的化学性质
情 境 导 入
7.1.2酸的化学性质
在焊接金属钢板之前,首先要用少量稀盐酸来擦拭金属表面,你能解释其中的道理吗?
金属表面会生锈,不及时除去,会影响焊接的牢固程度。因此,可以使用稀盐酸来除去金属表面的锈。
情 境 导 入
前面学习过哪些有盐酸参与的化学反应?
CaCO3+2HCl=CaCl2+CO2↑ +H2O
盐酸有哪些化学性质呢?
新 课 探 究
在两支试管中分别加入少量稀盐酸,然后分别滴入几滴紫色石蕊试液和无色酚酞试液,观察现象。
滴加石蕊
滴加酚酞
紫色石蕊遇酸变______
红
不变色
无色酚酞遇酸_ _
1.酸与指示剂的作用
7.1.2酸的化学性质
新课探究
情境导入
课堂小结
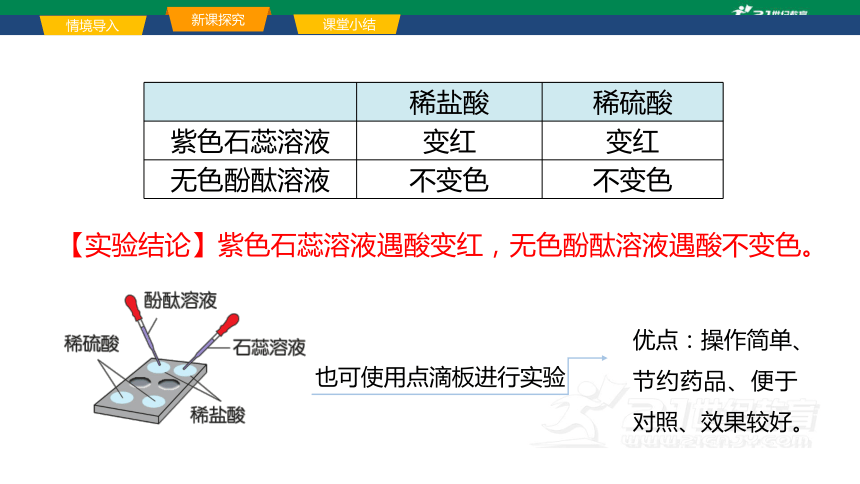
稀盐酸 稀硫酸
紫色石蕊溶液 变红 变红
无色酚酞溶液 不变色 不变色
【实验结论】紫色石蕊溶液遇酸变红,无色酚酞溶液遇酸不变色。
也可使用点滴板进行实验
优点:操作简单、节约药品、便于对照、效果较好。
单击此处添加标题文本内容
新课探究
情境导入
课堂小结
向盛有生锈铁钉的试管中加入少量稀盐酸,观察现象;待铁锈除尽后再加入少量稀盐酸,观察现象。
常温下,盐酸能与铁锈[主要成分为氧化铁(Fe2O3)]
发生反应,还能与除锈后的铁钉发生反应,化学
方程式分别为:
Fe2O3 + 6HCl =2FeCl3 + 3H2O
(氯化铁)
Fe + 2HCl =FeCl2 + H2 ↑
(氯化亚铁)
2.盐酸与生锈铁钉反应
单击此处添加标题文本内容
新课探究
情境导入
课堂小结
现 象 _____色粉末消失,无色溶液变为_____色
化学方程式 + HCl
+ H2SO4
H2SO4 + CuO = CuSO4 + H2O
蓝
2HCl + CuO = CuCl2 + H2O
黑
拓展:氧化铜与稀硫酸反应
单击此处添加标题文本内容
新课探究
情境导入
课堂小结
3.硫酸与盐酸性质的比较
若用稀硫酸代替稀盐酸,重复实验,你观察到了哪些现象?
1. 请写出有关反应的化学方程式。
Fe+H2SO4=FeSO4 +H2 ↑
Fe2O3 + 3H2SO4 =Fe2(SO4)3 + 3H2O
2. 某实验小组的同学得出了这样的结论:酸具有相似的化学性质。请帮助他们总结一下酸有哪些相似的化学性质。
单击此处添加标题文本内容
新课探究
情境导入
课堂小结
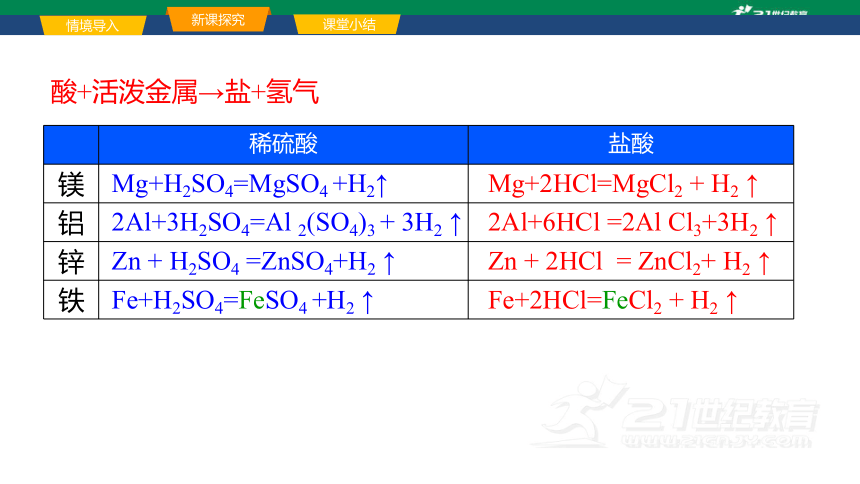
稀硫酸 盐酸
镁
铝
锌
铁
Mg+H2SO4=MgSO4 +H2↑
Mg+2HCl=MgCl2 + H2 ↑
Zn + H2SO4 =ZnSO4+H2 ↑
Zn + 2HCl = ZnCl2+ H2 ↑
Fe+H2SO4=FeSO4 +H2 ↑
Fe+2HCl=FeCl2 + H2 ↑
2Al+3H2SO4=Al 2(SO4)3 + 3H2 ↑
2Al+6HCl =2Al Cl3+3H2 ↑
酸+活泼金属→盐+氢气
单击此处添加标题文本内容
新课探究
情境导入
课堂小结
现象及化学方程式
现 象 铁锈____,无色溶液变为___色
铁锈+盐酸
铁锈+硫酸
用途
Fe2O3 + 6HCl = 2FeCl3 + 3H2O
Fe2O3 + 3H2SO4 = Fe2(SO4)3 + 3H2O
消失
金属表面除锈
黄
Fe3+
酸+金属氧化物→盐+水
【讨论】用盐酸除铁锈时,能否将铁钉长时间浸没在稀盐酸中?
不能,因为稀盐酸能够与铁钉反应。
单击此处添加标题文本内容
新课探究
情境导入
课堂小结
为什么酸具有相似的化学性质呢?那是因为它们在溶于水时,都解离出了共同的阳离子——氢离子,正是由于氢离子的存在,导致它们具有一些相似的化学性质。
HCl 和 H2SO4 在水中解离出 H+ 和酸根阴离子
(1)能使紫色石蕊试液变红色;
(2)能与某些金属氧化物反应,生成水;
(3)能与某些金属反应,生成氢气。
单击此处添加标题文本内容
新课探究
情境导入
课堂小结
盐酸和硫酸为什么有这些相似的化学性质
HCl在水中会解离出H+和Cl-
H2SO4在水中会解离出H+和SO42-
交流与讨论
HCl和H2SO4在水中解离出离子
都能解离出H+,所以化学性质相似。
单击此处添加标题文本内容
新课探究
情境导入
课堂小结
当然,由于不同的酸溶于水时解离出的酸根阴离子不同,其性质也存在差异。例如,硫酸能与氯化钡(BaCl2)反应,生成白色的硫酸钡(BaSO4)沉淀,而盐酸不与氯化钡发生反应。
BaCl2 + H2SO4 =BaSO4 ↓ + 2HCl
像 BaCl2、FeCl3、BaSO4、CaCO3 等均是由金属
阳离子和酸根阴离子构成的化合物,化学上把这类
化合物称为盐。
单击此处添加标题文本内容
新课探究
情境导入
课堂小结
4.常见酸的主要用途
课 堂 小 结
3.酸+金属氧化物=_______(用途: )
红
盐+氢气
酸的化学性质
金属表面除锈
盐+水
不变色
紫色石蕊溶液遇酸变 ,无色酚酞溶液遇酸 。
1.酸与指示剂的作用
2.酸+金属=__________
Fe2O3 + 6HCl = 2FeCl3 + 3H2O
Fe2O3 + 3H2SO4 = Fe2(SO4)3 + 3H2O
7.1.2酸的化学性质
单击此处添加标题文本内容
新课探究
情境导入
课堂小结
1.下图是物质X溶于水中发生解离的微观示意图,其中能说明X是一种酸的是( )
C
单击此处添加标题文本内容
新课探究
情境导入
课堂小结
2.(2023 滨州)下列有关实验现象的描述,正确的是( )
A.打开盛浓硫酸的试剂瓶,瓶口会形成白雾
B.铁与稀硫酸反应时有气泡产生,形成黄色溶液
C.将铜片放入稀硫酸中,铜片逐渐消失,形成蓝色溶液
D.用稀硫酸除铁锈时,铁锈逐渐溶解,形成黄色溶液
D
新课探究
情境导入
课堂小结
3.(2024 南明区校级二模)同学们以稀硫酸为例,依据酸的不同性质绘制了如下思维导图,下列说法正确的是( )
A.过程①所选的试剂是无色酚酞溶液
B.过程②的化学方程式为CuO+H2SO4═CuSO4+H2O
C.过程③所选的物质可以是铜单质
D.过程④的原理可用于金属除锈
D
单击此处添加标题文本内容
新课探究
情境导入
课堂小结
4.(2024 沙依巴克区三模)轻松除垢,清新空气。使用洁厕灵你可以轻松拥有一个干净、清新的卫生间,让你的生活更加舒适和健康。请根据如表所示的标签内容回答下列问题。
(1)标签上写有“勿用于大理石的清洁”,其原因是 。(写化学方程式)
名称:洁厕灵
功能:有效清除污垢、除异味
有效成分:HCl
注意事项:勿用于大理石的清洁
CaCO3+2HCl=CaCl2+CO2↑ +H2O
单击此处添加标题文本内容
新课探究
情境导入
课堂小结
(2)用湿布蘸取少量“洁厕灵”擦拭生锈的剪刀,可清除表面的铁锈,使其光亮如新,反应的化学方程式是 。白醋、稀硫酸也能发生类似的反应,因为白醋、稀硫酸、盐酸中都含有 (填离子符号)。
(3)烧水的铝壶中常结有一层水垢,用适量的稀盐酸可以除去它。但盐酸的用量过多,会损坏铝壶,原因是 。
Fe2O3+6HCl═2FeCl3+3H2O
H+
盐酸能和铝反应生成氯化铝和氢气
第七章 认识酸和碱
7.1.2酸的化学性质
情 境 导 入
7.1.2酸的化学性质
在焊接金属钢板之前,首先要用少量稀盐酸来擦拭金属表面,你能解释其中的道理吗?
金属表面会生锈,不及时除去,会影响焊接的牢固程度。因此,可以使用稀盐酸来除去金属表面的锈。
情 境 导 入
前面学习过哪些有盐酸参与的化学反应?
CaCO3+2HCl=CaCl2+CO2↑ +H2O
盐酸有哪些化学性质呢?
新 课 探 究
在两支试管中分别加入少量稀盐酸,然后分别滴入几滴紫色石蕊试液和无色酚酞试液,观察现象。
滴加石蕊
滴加酚酞
紫色石蕊遇酸变______
红
不变色
无色酚酞遇酸_ _
1.酸与指示剂的作用
7.1.2酸的化学性质
新课探究
情境导入
课堂小结
稀盐酸 稀硫酸
紫色石蕊溶液 变红 变红
无色酚酞溶液 不变色 不变色
【实验结论】紫色石蕊溶液遇酸变红,无色酚酞溶液遇酸不变色。
也可使用点滴板进行实验
优点:操作简单、节约药品、便于对照、效果较好。
单击此处添加标题文本内容
新课探究
情境导入
课堂小结
向盛有生锈铁钉的试管中加入少量稀盐酸,观察现象;待铁锈除尽后再加入少量稀盐酸,观察现象。
常温下,盐酸能与铁锈[主要成分为氧化铁(Fe2O3)]
发生反应,还能与除锈后的铁钉发生反应,化学
方程式分别为:
Fe2O3 + 6HCl =2FeCl3 + 3H2O
(氯化铁)
Fe + 2HCl =FeCl2 + H2 ↑
(氯化亚铁)
2.盐酸与生锈铁钉反应
单击此处添加标题文本内容
新课探究
情境导入
课堂小结
现 象 _____色粉末消失,无色溶液变为_____色
化学方程式 + HCl
+ H2SO4
H2SO4 + CuO = CuSO4 + H2O
蓝
2HCl + CuO = CuCl2 + H2O
黑
拓展:氧化铜与稀硫酸反应
单击此处添加标题文本内容
新课探究
情境导入
课堂小结
3.硫酸与盐酸性质的比较
若用稀硫酸代替稀盐酸,重复实验,你观察到了哪些现象?
1. 请写出有关反应的化学方程式。
Fe+H2SO4=FeSO4 +H2 ↑
Fe2O3 + 3H2SO4 =Fe2(SO4)3 + 3H2O
2. 某实验小组的同学得出了这样的结论:酸具有相似的化学性质。请帮助他们总结一下酸有哪些相似的化学性质。
单击此处添加标题文本内容
新课探究
情境导入
课堂小结
稀硫酸 盐酸
镁
铝
锌
铁
Mg+H2SO4=MgSO4 +H2↑
Mg+2HCl=MgCl2 + H2 ↑
Zn + H2SO4 =ZnSO4+H2 ↑
Zn + 2HCl = ZnCl2+ H2 ↑
Fe+H2SO4=FeSO4 +H2 ↑
Fe+2HCl=FeCl2 + H2 ↑
2Al+3H2SO4=Al 2(SO4)3 + 3H2 ↑
2Al+6HCl =2Al Cl3+3H2 ↑
酸+活泼金属→盐+氢气
单击此处添加标题文本内容
新课探究
情境导入
课堂小结
现象及化学方程式
现 象 铁锈____,无色溶液变为___色
铁锈+盐酸
铁锈+硫酸
用途
Fe2O3 + 6HCl = 2FeCl3 + 3H2O
Fe2O3 + 3H2SO4 = Fe2(SO4)3 + 3H2O
消失
金属表面除锈
黄
Fe3+
酸+金属氧化物→盐+水
【讨论】用盐酸除铁锈时,能否将铁钉长时间浸没在稀盐酸中?
不能,因为稀盐酸能够与铁钉反应。
单击此处添加标题文本内容
新课探究
情境导入
课堂小结
为什么酸具有相似的化学性质呢?那是因为它们在溶于水时,都解离出了共同的阳离子——氢离子,正是由于氢离子的存在,导致它们具有一些相似的化学性质。
HCl 和 H2SO4 在水中解离出 H+ 和酸根阴离子
(1)能使紫色石蕊试液变红色;
(2)能与某些金属氧化物反应,生成水;
(3)能与某些金属反应,生成氢气。
单击此处添加标题文本内容
新课探究
情境导入
课堂小结
盐酸和硫酸为什么有这些相似的化学性质
HCl在水中会解离出H+和Cl-
H2SO4在水中会解离出H+和SO42-
交流与讨论
HCl和H2SO4在水中解离出离子
都能解离出H+,所以化学性质相似。
单击此处添加标题文本内容
新课探究
情境导入
课堂小结
当然,由于不同的酸溶于水时解离出的酸根阴离子不同,其性质也存在差异。例如,硫酸能与氯化钡(BaCl2)反应,生成白色的硫酸钡(BaSO4)沉淀,而盐酸不与氯化钡发生反应。
BaCl2 + H2SO4 =BaSO4 ↓ + 2HCl
像 BaCl2、FeCl3、BaSO4、CaCO3 等均是由金属
阳离子和酸根阴离子构成的化合物,化学上把这类
化合物称为盐。
单击此处添加标题文本内容
新课探究
情境导入
课堂小结
4.常见酸的主要用途
课 堂 小 结
3.酸+金属氧化物=_______(用途: )
红
盐+氢气
酸的化学性质
金属表面除锈
盐+水
不变色
紫色石蕊溶液遇酸变 ,无色酚酞溶液遇酸 。
1.酸与指示剂的作用
2.酸+金属=__________
Fe2O3 + 6HCl = 2FeCl3 + 3H2O
Fe2O3 + 3H2SO4 = Fe2(SO4)3 + 3H2O
7.1.2酸的化学性质
单击此处添加标题文本内容
新课探究
情境导入
课堂小结
1.下图是物质X溶于水中发生解离的微观示意图,其中能说明X是一种酸的是( )
C
单击此处添加标题文本内容
新课探究
情境导入
课堂小结
2.(2023 滨州)下列有关实验现象的描述,正确的是( )
A.打开盛浓硫酸的试剂瓶,瓶口会形成白雾
B.铁与稀硫酸反应时有气泡产生,形成黄色溶液
C.将铜片放入稀硫酸中,铜片逐渐消失,形成蓝色溶液
D.用稀硫酸除铁锈时,铁锈逐渐溶解,形成黄色溶液
D
新课探究
情境导入
课堂小结
3.(2024 南明区校级二模)同学们以稀硫酸为例,依据酸的不同性质绘制了如下思维导图,下列说法正确的是( )
A.过程①所选的试剂是无色酚酞溶液
B.过程②的化学方程式为CuO+H2SO4═CuSO4+H2O
C.过程③所选的物质可以是铜单质
D.过程④的原理可用于金属除锈
D
单击此处添加标题文本内容
新课探究
情境导入
课堂小结
4.(2024 沙依巴克区三模)轻松除垢,清新空气。使用洁厕灵你可以轻松拥有一个干净、清新的卫生间,让你的生活更加舒适和健康。请根据如表所示的标签内容回答下列问题。
(1)标签上写有“勿用于大理石的清洁”,其原因是 。(写化学方程式)
名称:洁厕灵
功能:有效清除污垢、除异味
有效成分:HCl
注意事项:勿用于大理石的清洁
CaCO3+2HCl=CaCl2+CO2↑ +H2O
单击此处添加标题文本内容
新课探究
情境导入
课堂小结
(2)用湿布蘸取少量“洁厕灵”擦拭生锈的剪刀,可清除表面的铁锈,使其光亮如新,反应的化学方程式是 。白醋、稀硫酸也能发生类似的反应,因为白醋、稀硫酸、盐酸中都含有 (填离子符号)。
(3)烧水的铝壶中常结有一层水垢,用适量的稀盐酸可以除去它。但盐酸的用量过多,会损坏铝壶,原因是 。
Fe2O3+6HCl═2FeCl3+3H2O
H+
盐酸能和铝反应生成氯化铝和氢气
同课章节目录
