必修第二册 3.3 饮食中的有机化合物-乙酸(共18张PPT)
文档属性
| 名称 | 必修第二册 3.3 饮食中的有机化合物-乙酸(共18张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 6.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-24 00:00:00 | ||
图片预览





文档简介
(共18张PPT)
鲁科版高中化学高一必修第二册
第3章 重要的有机化合物
第3节 饮食中的有机化合物
---乙酸
【学习目标·核心素养】
1、了解乙酸的组成和结构特点
2、掌握乙酸的主要化学性质:酸性、酯化反应
3、变化观念与平衡思想:
通过对乙酸的学习,体会有机反应和无机反应条件、试剂、生成物等差异,深化“结构决定性质”“性质反映结构”“性质决定用途”等学科观念。
1
乙酸的结构
2
乙酸的物理性质
3
乙酸的化学性质
主要任务
分子式:C2H4O2
结构简式:CH3COOH
H
H
O
结构式:H C C O H
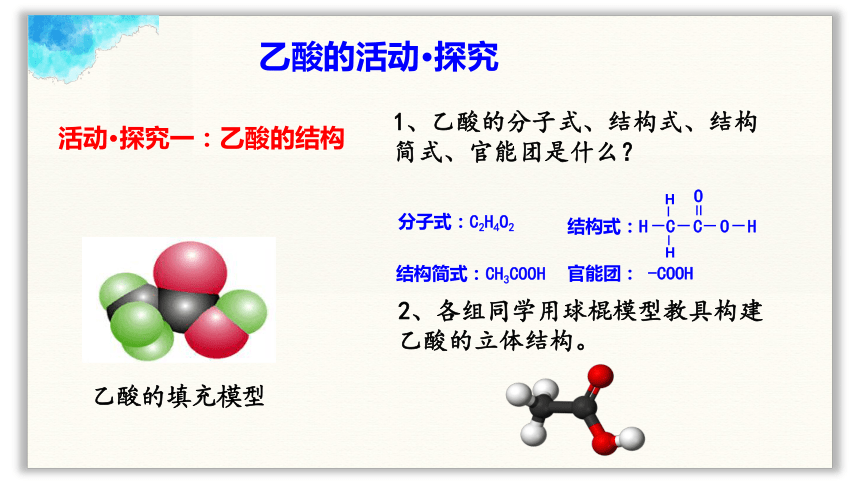
1、乙酸的分子式、结构式、结构简式、官能团是什么?
2、各组同学用球棍模型教具构建乙酸的立体结构。
乙酸的活动·探究
活动·探究一:乙酸的结构
乙酸的填充模型
官能团: -COOH
乙酸的活动·探究
活动·探究二:乙酸的物理性质
请同学们仔细观察桌子上的乙酸,自主归纳总结乙酸的物理性质。
颜 色 :
气 味 :
状 态 :
溶 解 性:
熔 点 :
沸 点 :
无色
强烈刺激性气味
液体
117.90C
16.60C
易溶于水和酒精
当温度低于16.60C时,乙酸就凝结成像冰一样的晶体,所以无水乙酸又称冰醋酸
【想一想】
如何从试剂瓶中取出冰醋酸晶体
用热毛巾捂或浸入温水中或放入>16.6℃的环境中
乙酸的活动·探究
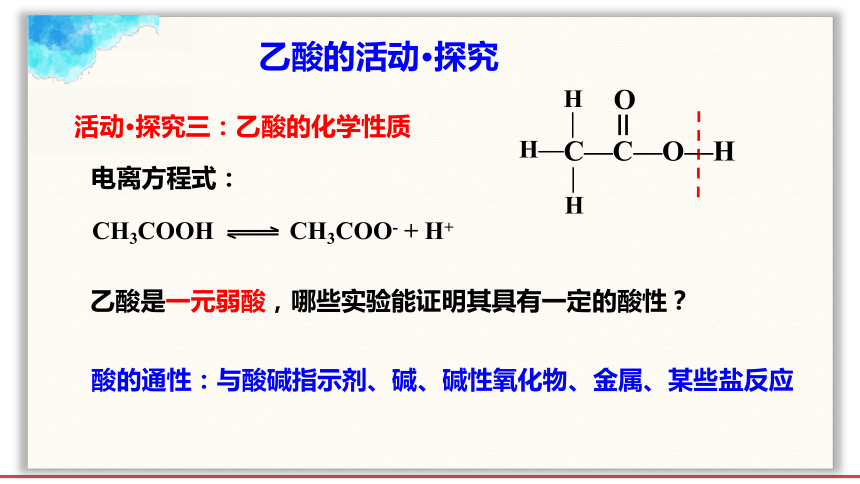
活动·探究三:乙酸的化学性质
CH3COOH CH3COO- + H+
电离方程式:
乙酸是一元弱酸,哪些实验能证明其具有一定的酸性?
酸的通性:与酸碱指示剂、碱、碱性氧化物、金属、某些盐反应
H
O
C—C—O—H
H—
—
H
—
乙酸的活动·探究
活动·探究三:乙酸的化学性质
请你根据现有的化学药品,设计实验方案,证明乙酸具有一定的酸性?
药品:锌粒、NaOH溶液、Na2CO3溶液、碳酸钙、
乙酸溶液、酚酞溶液、石蕊溶液。
1、酸性
②与活泼金属Zn反应
①酸碱指示剂
③与碱NaOH反应
④与碱性氧化物Na2O反应
⑤与某些盐CaCO3反应
Zn +2CH3COOH
(CH3COO)2Zn +H2
NaOH + CH3COOH
CH3COONa + H2O
Na2O+ 2CH3COOH
2CH3COONa + H2O
CaCO3 + 2CH3COOH
(CH3COO)2Ca+H2O+ CO2
家庭中常用食醋浸泡有水垢[主要成分是CaCO3和Mg(OH)2 ]暖瓶或水壶?
活动·探究三:乙酸的化学性质
能使紫色石蕊试液变红。
酸性: CH3COOH>H2CO3
乙酸的活动·探究
活动·探究三:乙酸的化学性质
厨师烧鱼、做排骨时常加醋并加点酒,这样鱼、肉的味道就变得无腥、香醇,特别鲜美,为什么?
俗话说“酒越陈越香”,为什么?
活动·探究三:乙酸的化学性质
在试管里先加入3mL乙醇和2mL乙酸的混合物,然后一边摇动试管一边慢慢地加入2mL浓硫酸,加入2-3块碎瓷片。如图,用酒精灯小心均匀的加热试管3-5min。将生成的气体经导管通到饱和Na2CO3溶液的液面上。
乙酸、乙醇、
浓硫酸的混合物
饱和Na2CO3溶液
【观察现象】
分层,饱和碳酸钠溶液的液面上有无色透明的不溶于水的油状液体,并可闻到香味。
活动·探究三:乙酸的化学性质
酒越陈越香:
CH3CH2OH
CH3CHO
CH3COOH
氧化
氧化
酯化反应
CH3-C-O-CH2-CH3
O
(乙酸乙酯)
在浓硫酸存在、加热的条件下,乙酸和乙醇发生反应,生成无色、透明、不溶于水、有香味的油状液体。该油状液体是乙酸乙酯。
实验结论:
释疑解惑
猜想一
猜想二
CH3-C-O-H H-O-CH2-CH3
O
活动·探究三:乙酸的化学性质
18
18
O O
CH3—C—OH+H—O—C2H5 CH3—C—O—C2H5 + H2O
浓H2SO4
△
活动·探究三:乙酸的化学性质
乙酸乙酯
反应原理:
羧酸脱羟基,醇脱羟基上的氢原子
酸跟醇起作用,生成酯和水的反应。
它是可逆的反应。
2、酯化反应:
① 药品混合:
②浓硫酸的作用:
③碎瓷片:
先加入乙醇再加乙酸,最后浓硫酸
催化剂和吸水剂
防止暴沸
④饱和碳酸钠的作用:
中和乙酸,溶解乙醇,降低乙酸乙酯的溶解度,便于酯的分层析出
⑤长导管的作用:
⑥导管末端在液面以上:
导气,冷凝
防止倒吸
·重要的化学试剂;是制药、染料、农药工业的重要原料;可用于制造醋酸纤维素等。
·在日常生活中也有广泛的用途。
【用途】
【随堂演练·知识落实】
1、关于乙酸的下列说法中不正确的是 ( )
A.乙酸易溶于水和乙醇
B.无水乙酸又称冰醋酸,它是纯净物
C.乙酸是一种重要的有机酸,是有刺激性气味的液体
D.乙酸分子里有四个氢原子,所以不是一元酸
D
2、大理石可以用作墙面、地面和厨房桌面,其主要成份是碳酸钙、食醋不慎滴在大理石桌面上,会使其失去光泽,变得粗糙,下列能正确解释此现象的是( )
A、食醋中的水使碳酸钙溶解
B.食醋中的醋酸将碳酸钙氧化
C.食醋中的醋酸与碳酸钙反应并放出大量的二氧化碳
D.食醋中的醋酸与碳酸钙发生了取代反应
C
3.除去乙酸乙酯中含有的乙酸,最好的处理和操作是( )
A.蒸馏
B.水洗后分液
C.用过量饱和碳酸钠溶液洗涤后分液
D.用过量氢氧化钠溶液洗涤后分液
C
课堂小结
是一种重要的化工原料
在日常生活中也有广泛的用途
O
CH3—C—O—H
小结:
酸 性
酯化反应
鲁科版高中化学高一必修第二册
第3章 重要的有机化合物
第3节 饮食中的有机化合物
---乙酸
【学习目标·核心素养】
1、了解乙酸的组成和结构特点
2、掌握乙酸的主要化学性质:酸性、酯化反应
3、变化观念与平衡思想:
通过对乙酸的学习,体会有机反应和无机反应条件、试剂、生成物等差异,深化“结构决定性质”“性质反映结构”“性质决定用途”等学科观念。
1
乙酸的结构
2
乙酸的物理性质
3
乙酸的化学性质
主要任务
分子式:C2H4O2
结构简式:CH3COOH
H
H
O
结构式:H C C O H
1、乙酸的分子式、结构式、结构简式、官能团是什么?
2、各组同学用球棍模型教具构建乙酸的立体结构。
乙酸的活动·探究
活动·探究一:乙酸的结构
乙酸的填充模型
官能团: -COOH
乙酸的活动·探究
活动·探究二:乙酸的物理性质
请同学们仔细观察桌子上的乙酸,自主归纳总结乙酸的物理性质。
颜 色 :
气 味 :
状 态 :
溶 解 性:
熔 点 :
沸 点 :
无色
强烈刺激性气味
液体
117.90C
16.60C
易溶于水和酒精
当温度低于16.60C时,乙酸就凝结成像冰一样的晶体,所以无水乙酸又称冰醋酸
【想一想】
如何从试剂瓶中取出冰醋酸晶体
用热毛巾捂或浸入温水中或放入>16.6℃的环境中
乙酸的活动·探究
活动·探究三:乙酸的化学性质
CH3COOH CH3COO- + H+
电离方程式:
乙酸是一元弱酸,哪些实验能证明其具有一定的酸性?
酸的通性:与酸碱指示剂、碱、碱性氧化物、金属、某些盐反应
H
O
C—C—O—H
H—
—
H
—
乙酸的活动·探究
活动·探究三:乙酸的化学性质
请你根据现有的化学药品,设计实验方案,证明乙酸具有一定的酸性?
药品:锌粒、NaOH溶液、Na2CO3溶液、碳酸钙、
乙酸溶液、酚酞溶液、石蕊溶液。
1、酸性
②与活泼金属Zn反应
①酸碱指示剂
③与碱NaOH反应
④与碱性氧化物Na2O反应
⑤与某些盐CaCO3反应
Zn +2CH3COOH
(CH3COO)2Zn +H2
NaOH + CH3COOH
CH3COONa + H2O
Na2O+ 2CH3COOH
2CH3COONa + H2O
CaCO3 + 2CH3COOH
(CH3COO)2Ca+H2O+ CO2
家庭中常用食醋浸泡有水垢[主要成分是CaCO3和Mg(OH)2 ]暖瓶或水壶?
活动·探究三:乙酸的化学性质
能使紫色石蕊试液变红。
酸性: CH3COOH>H2CO3
乙酸的活动·探究
活动·探究三:乙酸的化学性质
厨师烧鱼、做排骨时常加醋并加点酒,这样鱼、肉的味道就变得无腥、香醇,特别鲜美,为什么?
俗话说“酒越陈越香”,为什么?
活动·探究三:乙酸的化学性质
在试管里先加入3mL乙醇和2mL乙酸的混合物,然后一边摇动试管一边慢慢地加入2mL浓硫酸,加入2-3块碎瓷片。如图,用酒精灯小心均匀的加热试管3-5min。将生成的气体经导管通到饱和Na2CO3溶液的液面上。
乙酸、乙醇、
浓硫酸的混合物
饱和Na2CO3溶液
【观察现象】
分层,饱和碳酸钠溶液的液面上有无色透明的不溶于水的油状液体,并可闻到香味。
活动·探究三:乙酸的化学性质
酒越陈越香:
CH3CH2OH
CH3CHO
CH3COOH
氧化
氧化
酯化反应
CH3-C-O-CH2-CH3
O
(乙酸乙酯)
在浓硫酸存在、加热的条件下,乙酸和乙醇发生反应,生成无色、透明、不溶于水、有香味的油状液体。该油状液体是乙酸乙酯。
实验结论:
释疑解惑
猜想一
猜想二
CH3-C-O-H H-O-CH2-CH3
O
活动·探究三:乙酸的化学性质
18
18
O O
CH3—C—OH+H—O—C2H5 CH3—C—O—C2H5 + H2O
浓H2SO4
△
活动·探究三:乙酸的化学性质
乙酸乙酯
反应原理:
羧酸脱羟基,醇脱羟基上的氢原子
酸跟醇起作用,生成酯和水的反应。
它是可逆的反应。
2、酯化反应:
① 药品混合:
②浓硫酸的作用:
③碎瓷片:
先加入乙醇再加乙酸,最后浓硫酸
催化剂和吸水剂
防止暴沸
④饱和碳酸钠的作用:
中和乙酸,溶解乙醇,降低乙酸乙酯的溶解度,便于酯的分层析出
⑤长导管的作用:
⑥导管末端在液面以上:
导气,冷凝
防止倒吸
·重要的化学试剂;是制药、染料、农药工业的重要原料;可用于制造醋酸纤维素等。
·在日常生活中也有广泛的用途。
【用途】
【随堂演练·知识落实】
1、关于乙酸的下列说法中不正确的是 ( )
A.乙酸易溶于水和乙醇
B.无水乙酸又称冰醋酸,它是纯净物
C.乙酸是一种重要的有机酸,是有刺激性气味的液体
D.乙酸分子里有四个氢原子,所以不是一元酸
D
2、大理石可以用作墙面、地面和厨房桌面,其主要成份是碳酸钙、食醋不慎滴在大理石桌面上,会使其失去光泽,变得粗糙,下列能正确解释此现象的是( )
A、食醋中的水使碳酸钙溶解
B.食醋中的醋酸将碳酸钙氧化
C.食醋中的醋酸与碳酸钙反应并放出大量的二氧化碳
D.食醋中的醋酸与碳酸钙发生了取代反应
C
3.除去乙酸乙酯中含有的乙酸,最好的处理和操作是( )
A.蒸馏
B.水洗后分液
C.用过量饱和碳酸钠溶液洗涤后分液
D.用过量氢氧化钠溶液洗涤后分液
C
课堂小结
是一种重要的化工原料
在日常生活中也有广泛的用途
O
CH3—C—O—H
小结:
酸 性
酯化反应
