专题7 氮与社会可持续发展 分层作业10 铵盐的性质--2025苏教版化学必修第二册同步练习题(含答案)
文档属性
| 名称 | 专题7 氮与社会可持续发展 分层作业10 铵盐的性质--2025苏教版化学必修第二册同步练习题(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 618.8KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-27 18:35:19 | ||
图片预览


文档简介
中小学教育资源及组卷应用平台
2025苏教版化学必修第二册
分层作业10 铵盐的性质
A级必备知识基础练
1.下列物质不需要保存在棕色试剂瓶里的是( )
A.氨水 B.硝酸
C.硫酸铵 D.次氯酸
2.大型影剧院容纳的人数众多,防火安全非常重要。用浓氯化铵溶液处理过的舞台幕布不易着火,其原因是( )
A.幕布的着火点升高
B.幕布的质量增加
C.氯化铵分解吸收热量,降低了温度
D.氯化铵分解产生的气体不易燃烧
3.实验室制备干燥的氨气所需的药品是( )
A.NH4Cl稀溶液、NaOH稀溶液、碱石灰
B.饱和氨水、NaOH固体、五氧化二磷固体
C.NaOH溶液、NH4Cl晶体、浓硫酸
D.NH4Cl固体、Ca(OH)2固体、碱石灰
4.实验室可以按如图所示的装置干燥、收集气体M,多余的气体可用水吸收,则M是( )
A.NH3 B.NO
C.Cl2 D.NO2
5.已知氨气极易溶于水,难溶于有机溶剂CCl4。下列不适合做氨气的尾气吸收装置的是( )
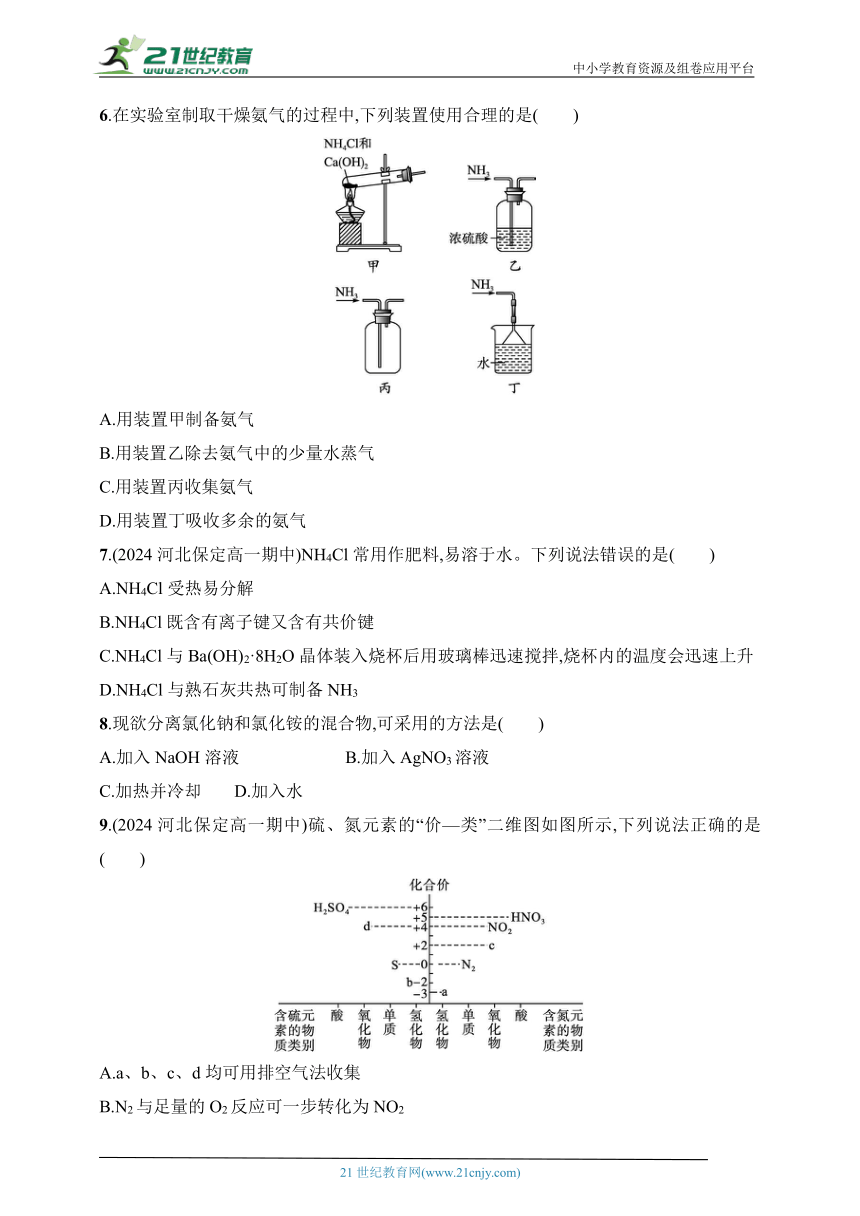
6.在实验室制取干燥氨气的过程中,下列装置使用合理的是( )
A.用装置甲制备氨气
B.用装置乙除去氨气中的少量水蒸气
C.用装置丙收集氨气
D.用装置丁吸收多余的氨气
7.(2024河北保定高一期中)NH4Cl常用作肥料,易溶于水。下列说法错误的是( )
A.NH4Cl受热易分解
B.NH4Cl既含有离子键又含有共价键
C.NH4Cl与Ba(OH)2·8H2O晶体装入烧杯后用玻璃棒迅速搅拌,烧杯内的温度会迅速上升
D.NH4Cl与熟石灰共热可制备NH3
8.现欲分离氯化钠和氯化铵的混合物,可采用的方法是( )
A.加入NaOH溶液 B.加入AgNO3溶液
C.加热并冷却 D.加入水
9.(2024河北保定高一期中)硫、氮元素的“价—类”二维图如图所示,下列说法正确的是( )
A.a、b、c、d均可用排空气法收集
B.N2与足量的O2反应可一步转化为NO2
C.稀硝酸和稀硫酸能分别与锌发生置换反应
D.a能使湿润的红色石蕊试纸变蓝
10.为探究氨气的溶解性,某兴趣小组按如图所示装置进行实验(f为止水夹),请回答下列问题:
(1)要得到干燥的氨气可选用 (填字母)作干燥剂。
A.碱石灰 B.浓硫酸
C.浓硝酸 D.氢氧化钠溶液
(2)用如图装置进行喷泉实验,烧瓶中已装满干燥氨气(标准状况),引发水向上喷的操作是 。
11.已知A、B、C、D为气体,其中A呈黄绿色,D极易溶于水,且D形成的溶液可使酚酞变红。它们之间的转化关系如图所示:
(1)将B点燃,把导管伸入盛满A气体的集气瓶中,可以观察到的实验现象是 。
(2)实验室可用如图所示装置收集D,下列叙述正确的是 (填序号)。
①D气体不能用排水法收集
②干燥管里盛有碱石灰
③图中的a为浸有稀硫酸的棉花
(3)检验E中阳离子的方法是:取少量E置于试管中,加水溶解, 。
B级关键能力提升练
12.下列由相关实验现象所推出的结论正确的是( )
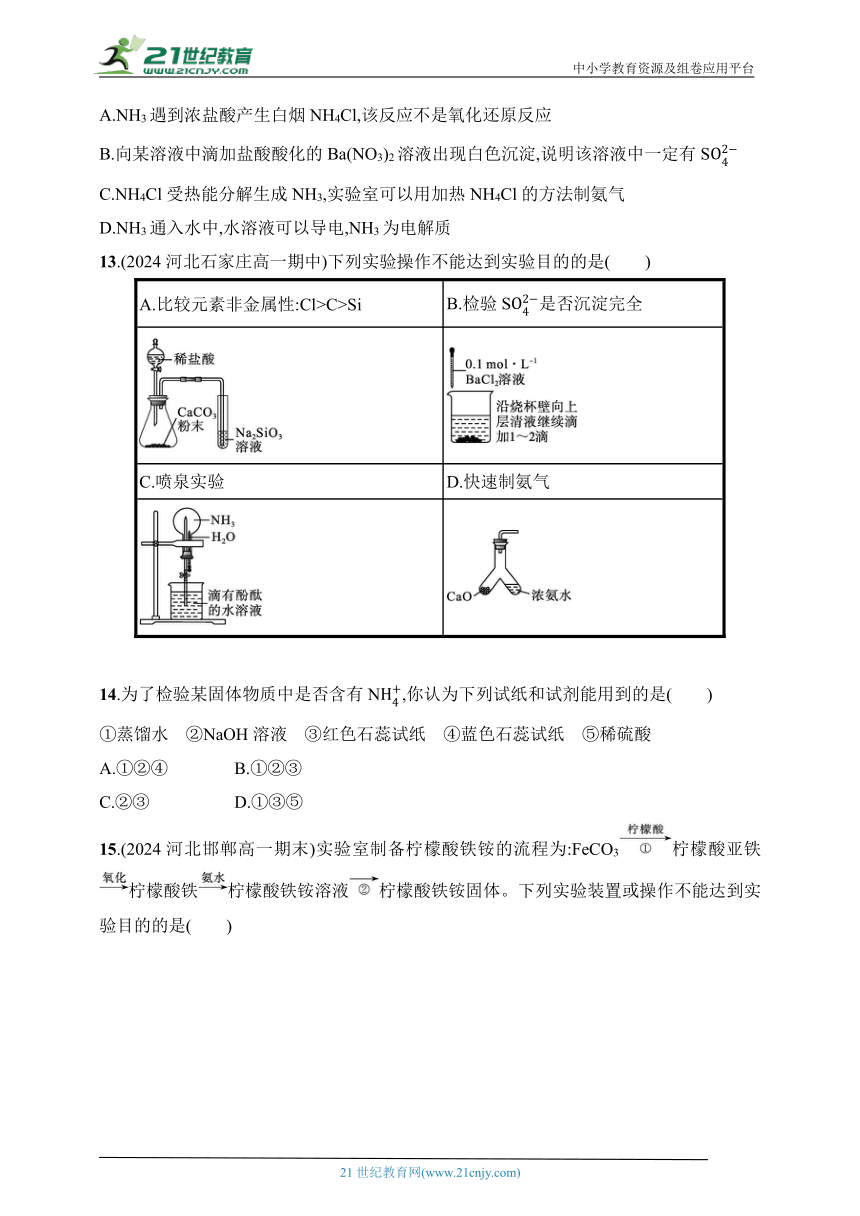
A.NH3遇到浓盐酸产生白烟NH4Cl,该反应不是氧化还原反应
B.向某溶液中滴加盐酸酸化的Ba(NO3)2溶液出现白色沉淀,说明该溶液中一定有S
C.NH4Cl受热能分解生成NH3,实验室可以用加热NH4Cl的方法制氨气
D.NH3通入水中,水溶液可以导电,NH3为电解质
13.(2024河北石家庄高一期中)下列实验操作不能达到实验目的的是( )
A.比较元素非金属性:Cl>C>Si B.检验S是否沉淀完全
C.喷泉实验 D.快速制氨气
14.为了检验某固体物质中是否含有N,你认为下列试纸和试剂能用到的是( )
①蒸馏水 ②NaOH溶液 ③红色石蕊试纸 ④蓝色石蕊试纸 ⑤稀硫酸
A.①②④ B.①②③
C.②③ D.①③⑤
15.(2024河北邯郸高一期末)实验室制备柠檬酸铁铵的流程为:FeCO3柠檬酸亚铁柠檬酸铁柠檬酸铁铵溶液柠檬酸铁铵固体。下列实验装置或操作不能达到实验目的的是( )
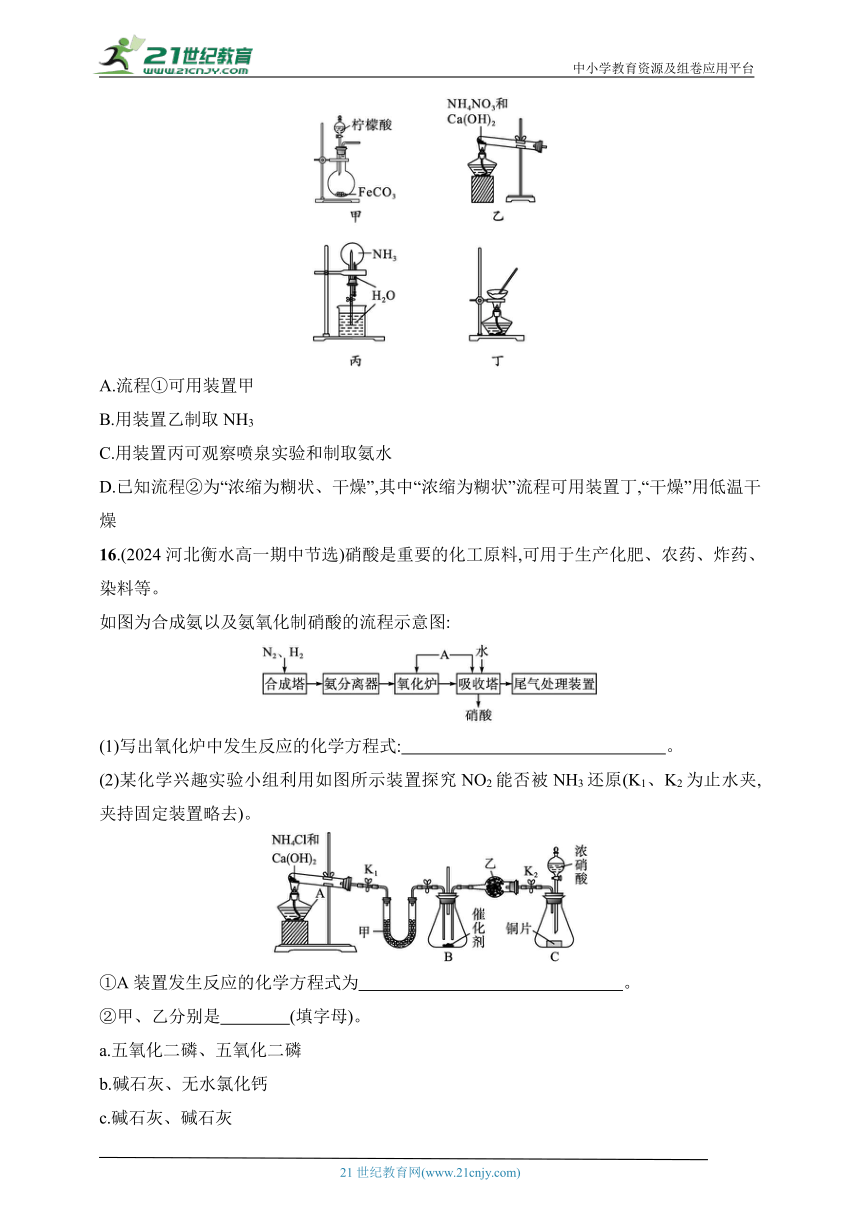
A.流程①可用装置甲
B.用装置乙制取NH3
C.用装置丙可观察喷泉实验和制取氨水
D.已知流程②为“浓缩为糊状、干燥”,其中“浓缩为糊状”流程可用装置丁,“干燥”用低温干燥
16.(2024河北衡水高一期中节选)硝酸是重要的化工原料,可用于生产化肥、农药、炸药、染料等。
如图为合成氨以及氨氧化制硝酸的流程示意图:
(1)写出氧化炉中发生反应的化学方程式: 。
(2)某化学兴趣实验小组利用如图所示装置探究NO2能否被NH3还原(K1、K2为止水夹,夹持固定装置略去)。
①A装置发生反应的化学方程式为 。
②甲、乙分别是 (填字母)。
a.五氧化二磷、五氧化二磷
b.碱石灰、无水氯化钙
c.碱石灰、碱石灰
③若NO2能够被NH3还原为N2,反应中氧化剂和还原剂物质的量之比为 。
④此实验装置存在一个明显的缺陷是 。
17.硫酸铵是一种无机物,化学式为(NH4)2SO4,白色颗粒,无气味,受热易分解。某化学研究小组拟探究其在400 ℃时的分解产物,实验装置如图所示(部分夹持装置已略去)。
回答下列问题:
(1)仪器a的名称是 。
(2)先关闭止水夹n,打开止水夹m,400 ℃加热装置C,装置E中品红溶液褪色,证明分解产物中含有 (填化学式),品红溶液褪色说明其具有 。然后打开止水夹n,关闭止水夹m,装置A中的现象是 ,说明分解产物中含有氨气,碱石灰的作用是 ,400 ℃加热装置C至(NH4)2SO4完全分解无残留物,停止加热,进一步研究发现,气体产物中有N2生成。
(3)装置D内稀盐酸吸收的气体是 (填化学式)。
(4)检验装置F内溶液中有S、无S的实验操作和现象是 。
(5)(NH4)2SO4在400 ℃分解的化学方程式是 。
C级学科素养拔高练
18.某化学兴趣小组利用如图装置制取氨气并探究氨气的有关性质。
(1)装置A中烧瓶内试剂可选用 (填字母)。
a.碱石灰 b.浓硫酸 c.生石灰 d.五氧化二磷 e.烧碱固体
(2)若探究氨气的还原性,需要打开K1、K3,K2处导管连接制取纯净、干燥氯气的装置。
①用二氧化锰与浓盐酸制取氯气,生成的气体必须通过盛有 试剂的洗气瓶。
②D中氨气与氯气反应产生白烟,同时生成一种无色无味的气体,该反应的化学方程式为 。
③从K3处导管逸出的气体中含有少量Cl2,则C装置中应盛放 (填化学式)溶液,反应的离子方程式为 。
分层作业10 铵盐的性质
1.C 氨水易挥发且不稳定,需要低温避光保存,需要保存在棕色试剂瓶里;硝酸见光易分解,需要保存在棕色试剂瓶里;硫酸铵见光不分解,不需要保存在棕色试剂瓶里;次氯酸见光会分解,需要保存在棕色试剂瓶里。
2.C 3.D
4.A 解析 由题意可知,该气体的密度小于空气,易溶于水。
5.C 解析 NH3极易溶于水,若用C项中的装置做NH3的尾气处理装置,则容易发生倒吸,NH3难溶于CCl4,故A装置可防倒吸,B项和D项装置原理相似,都可以防倒吸。
6.D 解析 利用NH4Cl固体和Ca(OH)2固体加热制取NH3时,试管口要略低于试管底部,A错误;NH3与浓硫酸发生反应生成(NH4)2SO4,B错误;NH3的密度小于空气的密度,应采用向下排空气法收集NH3,要从短导管通入NH3,C错误;NH3极易溶于水,装置丁既能吸收多余的NH3,又能防止倒吸,D正确。
7.C 解析 氯化铵是铵盐,受热易分解,A正确;NH4Cl中铵根离子和氯离子间为离子键,铵根离子内氮原子和氢原子间是共价键,故既含有离子键又含有共价键,B正确;NH4Cl与Ba(OH)2·8H2O晶体在室温下的反应是吸热反应,两者装入烧杯后用玻璃棒迅速搅拌,烧杯内的温度会迅速下降,C不正确;NH4Cl与熟石灰[Ca(OH)2]共热是实验室制备氨气的方法,D正确。
8.C 解析 加入NaOH溶液可以除去其中的NH4Cl,但却不能达到分离的目的;AgNO3溶液与NaCl和NH4Cl均反应生成AgCl沉淀,因此不能将二者分离;两种物质均易溶于水,加入水也不能将二者分离;因NH4Cl受热分解为NH3和HCl气体,NH3和HCl气体遇冷又会生成NH4Cl,但NaCl受热不分解,所以用加热并冷却的方法可以使二者分离。故选C。
9.D 解析 由图可知,a为NH3,b为H2S,c为NO,d为SO2。NO能被O2氧化产生红棕色NO2,不可用排空气法收集,A错误;N2与足量的O2反应生成NO,不可一步转化为NO2,B错误;单质锌可与稀硝酸反应生成硝酸锌、水和一氧化氮等,不是置换反应,C错误;NH3为碱性气体,能使湿润的红色石蕊试纸变蓝,D正确。
10.答案 (1)A (2)打开止水夹f,挤出胶头滴管中的液体
解析 (1)浓硝酸和氢氧化钠溶液不能用作干燥剂,浓硫酸可以和氨气反应,实验室可选用碱石灰来干燥氨气。(2)将胶头滴管中的少量液体挤入烧瓶,氨气极易溶于水,使瓶内压强迅速减小,在大气压的作用下,烧杯中的液体会顺利进入烧瓶,形成喷泉。
11.答案 (1)安静燃烧,发出苍白色火焰,瓶口有白雾
(2)①②③
(3)加入浓NaOH溶液,加热,生成无色、有刺激性气味的气体,用湿润的红色石蕊试纸靠近试管口处,若试纸变为蓝色,证明E中有N,否则,则不含N(答案合理即可)
解析 根据气体A呈黄绿色,气体D极易溶于水且形成的溶液可使酚酞变红,推知A为Cl2,D为NH3;根据气体B能在气体A(Cl2)中燃烧,推知B为H2;联系框图中各物质间的转化关系,进一步推知C为HCl,E为NH4Cl。
12.A 解析 NH3遇到浓盐酸产生白烟NH4Cl,该反应没有元素化合价变化,不是氧化还原反应,A正确;向某溶液中滴加盐酸酸化的Ba(NO3)2溶液出现白色沉淀,也可能是氯化银沉淀,或者是酸性条件下亚硫酸根离子被硝酸根离子氧化生成硫酸根离子而形成硫酸钡沉淀,不能说明该溶液中一定有S,B错误;NH4Cl受热能分解生成氨气和氯化氢,在管口遇冷很快又化合生成氯化铵,不能用于实验室制氨气,C错误;NH3通入水中,与水反应生成NH3·H2O,NH3·H2O电离出铵根离子和氢氧根离子,故水溶液可以导电,而NH3为非电解质,D错误。
13.A 解析 挥发出的HCl气体也能与硅酸钠反应生成硅酸,不能比较C和Si的非金属性,A错误;继续向烧杯的清液中滴加氯化钡溶液,若不产生沉淀,说明S沉淀完全,B正确;氨气极易溶于水,内外形成压强差,液体被压入烧瓶中,形成喷泉,C正确;浓氨水与氧化钙混合,氧化钙与水反应放出大量的热,加速一水合氨的分解以制氨气,D正确。
14.B 解析 固体加蒸馏水溶解,再加入NaOH溶液后,加热,若含有N,则N+OH-NH3↑+H2O,NH3能使湿润(用到蒸馏水)的红色石蕊试纸变蓝。故选B。
15.B 解析 柠檬酸能与FeCO3反应生成柠檬酸亚铁和CO2,CO2能够排除装置中的空气,防止氧化Fe2+,故流程①可用装置甲,A不合题意;由于NH4NO3受热易分解,甚至发生爆炸,故不能用NH4NO3和Ca(OH)2共热制备NH3,应该用NH4Cl和Ca(OH)2共热制备NH3,B符合题意;氨气极易溶于水,能够用装置丙观察喷泉实验和制取氨水,C不合题意;已知流程②为“浓缩为糊状、干燥”,其中“浓缩为糊状”流程可用装置丁即蒸发浓缩,由于柠檬酸铁铵属于铵盐,受热易分解,故“干燥”用低温干燥,D不合题意。
16.答案 (1)4NH3+5O24NO+6H2O
(2)①2NH4Cl+Ca(OH)2CaCl2+2NH3↑+2H2O ②b ③3∶4 ④缺少尾气处理装置
解析 (2)②甲用于干燥氨气,乙用于干燥NO2。五氧化二磷能与氨气反应,不能用其干燥氨气,a错误;碱石灰不与氨气反应,能干燥氨气,无水氯化钙不与NO2反应,能干燥NO2,b正确;碱石灰与NO2反应,不能用碱石灰干燥NO2,c错误。③NO2与NH3反应生成N2和水,该反应中NO2得电子为氧化剂,NH3失电子为还原剂,根据得失电子守恒,氧化剂和还原剂的物质的量之比为3∶4。④从实验装置可知,该实验装置缺少尾气处理装置,多余的氨气和NO2没有被处理直接排入空气中。
17.答案 (1)干燥管(或球形干燥管)
(2)SO2 漂白性 试纸变蓝 除去NH3中的SO2和H2O
(3)NH3
(4)取少量装置F内溶液于试管中,滴加足量的BaCl2溶液,生成白色沉淀;加入足量稀盐酸后沉淀完全溶解,并放出无色具有刺激性气味的气体
(5)3SO44NH3↑+N2↑+3SO2↑+6H2O↑
解析 (1)由题干实验装置图可知,仪器a的名称是球形干燥管或干燥管。(2)先关闭止水夹n,打开止水夹m,400 ℃加热装置C,SO2具有漂白性,能够漂白品红等有色物质,装置E中品红溶液褪色,证明分解产物中含有SO2,品红溶液褪色说明其具有漂白性;NH3溶于水呈碱性,则NH3遇到湿润的红色石蕊试纸将其变为蓝色,然后打开止水夹n,关闭止水夹m,装置A中的现象是试纸变蓝,说明分解产物中含有氨气,碱石灰的作用是除去NH3中的SO2和H2O。(3)由(2)中分析可知,分解产物为SO2、N2、NH3和H2O,故装置D内稀盐酸吸收的气体是NH3。(4)利用BaSO3不溶于水而溶于稀盐酸、BaSO4既不溶于水也不溶于稀盐酸的特性可知,检验装置F内溶液中有S、无S的实验操作和现象是取少量装置F内溶液于试管中,滴加足量的BaCl2溶液,生成白色沉淀;加入足量稀盐酸后沉淀完全溶解,并放出无色具有刺激性气味的气体。(5)由上述分析可知,分解产物为SO2、N2、NH3和H2O,则该分解反应的化学方程式为3SO44NH3↑+N2↑+3SO2↑+6H2O↑。
18.答案 (1)ace (2)①饱和食盐水、浓硫酸 ②3Cl2+8NH36NH4Cl+N2 ③NaOH(合理即可) Cl2+2OH-Cl-+ClO-+H2O
解析 (1)升高温度能促进NH3·H2O分解生成氨气,为促进NH3·H2O分解,则烧瓶中加入的物质遇氨水后能放出大量的热,且和氨水不反应。碱石灰遇水放出大量的热,且和氨水不反应,故a选;浓硫酸和氨水反应,故b不选;生石灰遇水放出大量的热,且和氨水不反应,故c选;五氧化二磷与氨水反应,故d不选;烧碱固体遇水放出大量的热,且和氨水不反应,故e选。(2)①用浓盐酸和二氧化锰制取的氯气中含有氯化氢气体和水蒸气,为防止干扰实验,氯气在进入烧瓶前,应该分别用饱和食盐水和浓硫酸除去氯化氢气体和水蒸气。②根据得失电子守恒知,D中生成的无色无味的气体是氮气,所以该反应的化学方程式为3Cl2+8NH36NH4Cl+N2。③可以用氢氧化钠溶液除去氯气,反应的离子方程式为Cl2+2OH-Cl-+ClO-+H2O。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
2025苏教版化学必修第二册
分层作业10 铵盐的性质
A级必备知识基础练
1.下列物质不需要保存在棕色试剂瓶里的是( )
A.氨水 B.硝酸
C.硫酸铵 D.次氯酸
2.大型影剧院容纳的人数众多,防火安全非常重要。用浓氯化铵溶液处理过的舞台幕布不易着火,其原因是( )
A.幕布的着火点升高
B.幕布的质量增加
C.氯化铵分解吸收热量,降低了温度
D.氯化铵分解产生的气体不易燃烧
3.实验室制备干燥的氨气所需的药品是( )
A.NH4Cl稀溶液、NaOH稀溶液、碱石灰
B.饱和氨水、NaOH固体、五氧化二磷固体
C.NaOH溶液、NH4Cl晶体、浓硫酸
D.NH4Cl固体、Ca(OH)2固体、碱石灰
4.实验室可以按如图所示的装置干燥、收集气体M,多余的气体可用水吸收,则M是( )
A.NH3 B.NO
C.Cl2 D.NO2
5.已知氨气极易溶于水,难溶于有机溶剂CCl4。下列不适合做氨气的尾气吸收装置的是( )
6.在实验室制取干燥氨气的过程中,下列装置使用合理的是( )
A.用装置甲制备氨气
B.用装置乙除去氨气中的少量水蒸气
C.用装置丙收集氨气
D.用装置丁吸收多余的氨气
7.(2024河北保定高一期中)NH4Cl常用作肥料,易溶于水。下列说法错误的是( )
A.NH4Cl受热易分解
B.NH4Cl既含有离子键又含有共价键
C.NH4Cl与Ba(OH)2·8H2O晶体装入烧杯后用玻璃棒迅速搅拌,烧杯内的温度会迅速上升
D.NH4Cl与熟石灰共热可制备NH3
8.现欲分离氯化钠和氯化铵的混合物,可采用的方法是( )
A.加入NaOH溶液 B.加入AgNO3溶液
C.加热并冷却 D.加入水
9.(2024河北保定高一期中)硫、氮元素的“价—类”二维图如图所示,下列说法正确的是( )
A.a、b、c、d均可用排空气法收集
B.N2与足量的O2反应可一步转化为NO2
C.稀硝酸和稀硫酸能分别与锌发生置换反应
D.a能使湿润的红色石蕊试纸变蓝
10.为探究氨气的溶解性,某兴趣小组按如图所示装置进行实验(f为止水夹),请回答下列问题:
(1)要得到干燥的氨气可选用 (填字母)作干燥剂。
A.碱石灰 B.浓硫酸
C.浓硝酸 D.氢氧化钠溶液
(2)用如图装置进行喷泉实验,烧瓶中已装满干燥氨气(标准状况),引发水向上喷的操作是 。
11.已知A、B、C、D为气体,其中A呈黄绿色,D极易溶于水,且D形成的溶液可使酚酞变红。它们之间的转化关系如图所示:
(1)将B点燃,把导管伸入盛满A气体的集气瓶中,可以观察到的实验现象是 。
(2)实验室可用如图所示装置收集D,下列叙述正确的是 (填序号)。
①D气体不能用排水法收集
②干燥管里盛有碱石灰
③图中的a为浸有稀硫酸的棉花
(3)检验E中阳离子的方法是:取少量E置于试管中,加水溶解, 。
B级关键能力提升练
12.下列由相关实验现象所推出的结论正确的是( )
A.NH3遇到浓盐酸产生白烟NH4Cl,该反应不是氧化还原反应
B.向某溶液中滴加盐酸酸化的Ba(NO3)2溶液出现白色沉淀,说明该溶液中一定有S
C.NH4Cl受热能分解生成NH3,实验室可以用加热NH4Cl的方法制氨气
D.NH3通入水中,水溶液可以导电,NH3为电解质
13.(2024河北石家庄高一期中)下列实验操作不能达到实验目的的是( )
A.比较元素非金属性:Cl>C>Si B.检验S是否沉淀完全
C.喷泉实验 D.快速制氨气
14.为了检验某固体物质中是否含有N,你认为下列试纸和试剂能用到的是( )
①蒸馏水 ②NaOH溶液 ③红色石蕊试纸 ④蓝色石蕊试纸 ⑤稀硫酸
A.①②④ B.①②③
C.②③ D.①③⑤
15.(2024河北邯郸高一期末)实验室制备柠檬酸铁铵的流程为:FeCO3柠檬酸亚铁柠檬酸铁柠檬酸铁铵溶液柠檬酸铁铵固体。下列实验装置或操作不能达到实验目的的是( )
A.流程①可用装置甲
B.用装置乙制取NH3
C.用装置丙可观察喷泉实验和制取氨水
D.已知流程②为“浓缩为糊状、干燥”,其中“浓缩为糊状”流程可用装置丁,“干燥”用低温干燥
16.(2024河北衡水高一期中节选)硝酸是重要的化工原料,可用于生产化肥、农药、炸药、染料等。
如图为合成氨以及氨氧化制硝酸的流程示意图:
(1)写出氧化炉中发生反应的化学方程式: 。
(2)某化学兴趣实验小组利用如图所示装置探究NO2能否被NH3还原(K1、K2为止水夹,夹持固定装置略去)。
①A装置发生反应的化学方程式为 。
②甲、乙分别是 (填字母)。
a.五氧化二磷、五氧化二磷
b.碱石灰、无水氯化钙
c.碱石灰、碱石灰
③若NO2能够被NH3还原为N2,反应中氧化剂和还原剂物质的量之比为 。
④此实验装置存在一个明显的缺陷是 。
17.硫酸铵是一种无机物,化学式为(NH4)2SO4,白色颗粒,无气味,受热易分解。某化学研究小组拟探究其在400 ℃时的分解产物,实验装置如图所示(部分夹持装置已略去)。
回答下列问题:
(1)仪器a的名称是 。
(2)先关闭止水夹n,打开止水夹m,400 ℃加热装置C,装置E中品红溶液褪色,证明分解产物中含有 (填化学式),品红溶液褪色说明其具有 。然后打开止水夹n,关闭止水夹m,装置A中的现象是 ,说明分解产物中含有氨气,碱石灰的作用是 ,400 ℃加热装置C至(NH4)2SO4完全分解无残留物,停止加热,进一步研究发现,气体产物中有N2生成。
(3)装置D内稀盐酸吸收的气体是 (填化学式)。
(4)检验装置F内溶液中有S、无S的实验操作和现象是 。
(5)(NH4)2SO4在400 ℃分解的化学方程式是 。
C级学科素养拔高练
18.某化学兴趣小组利用如图装置制取氨气并探究氨气的有关性质。
(1)装置A中烧瓶内试剂可选用 (填字母)。
a.碱石灰 b.浓硫酸 c.生石灰 d.五氧化二磷 e.烧碱固体
(2)若探究氨气的还原性,需要打开K1、K3,K2处导管连接制取纯净、干燥氯气的装置。
①用二氧化锰与浓盐酸制取氯气,生成的气体必须通过盛有 试剂的洗气瓶。
②D中氨气与氯气反应产生白烟,同时生成一种无色无味的气体,该反应的化学方程式为 。
③从K3处导管逸出的气体中含有少量Cl2,则C装置中应盛放 (填化学式)溶液,反应的离子方程式为 。
分层作业10 铵盐的性质
1.C 氨水易挥发且不稳定,需要低温避光保存,需要保存在棕色试剂瓶里;硝酸见光易分解,需要保存在棕色试剂瓶里;硫酸铵见光不分解,不需要保存在棕色试剂瓶里;次氯酸见光会分解,需要保存在棕色试剂瓶里。
2.C 3.D
4.A 解析 由题意可知,该气体的密度小于空气,易溶于水。
5.C 解析 NH3极易溶于水,若用C项中的装置做NH3的尾气处理装置,则容易发生倒吸,NH3难溶于CCl4,故A装置可防倒吸,B项和D项装置原理相似,都可以防倒吸。
6.D 解析 利用NH4Cl固体和Ca(OH)2固体加热制取NH3时,试管口要略低于试管底部,A错误;NH3与浓硫酸发生反应生成(NH4)2SO4,B错误;NH3的密度小于空气的密度,应采用向下排空气法收集NH3,要从短导管通入NH3,C错误;NH3极易溶于水,装置丁既能吸收多余的NH3,又能防止倒吸,D正确。
7.C 解析 氯化铵是铵盐,受热易分解,A正确;NH4Cl中铵根离子和氯离子间为离子键,铵根离子内氮原子和氢原子间是共价键,故既含有离子键又含有共价键,B正确;NH4Cl与Ba(OH)2·8H2O晶体在室温下的反应是吸热反应,两者装入烧杯后用玻璃棒迅速搅拌,烧杯内的温度会迅速下降,C不正确;NH4Cl与熟石灰[Ca(OH)2]共热是实验室制备氨气的方法,D正确。
8.C 解析 加入NaOH溶液可以除去其中的NH4Cl,但却不能达到分离的目的;AgNO3溶液与NaCl和NH4Cl均反应生成AgCl沉淀,因此不能将二者分离;两种物质均易溶于水,加入水也不能将二者分离;因NH4Cl受热分解为NH3和HCl气体,NH3和HCl气体遇冷又会生成NH4Cl,但NaCl受热不分解,所以用加热并冷却的方法可以使二者分离。故选C。
9.D 解析 由图可知,a为NH3,b为H2S,c为NO,d为SO2。NO能被O2氧化产生红棕色NO2,不可用排空气法收集,A错误;N2与足量的O2反应生成NO,不可一步转化为NO2,B错误;单质锌可与稀硝酸反应生成硝酸锌、水和一氧化氮等,不是置换反应,C错误;NH3为碱性气体,能使湿润的红色石蕊试纸变蓝,D正确。
10.答案 (1)A (2)打开止水夹f,挤出胶头滴管中的液体
解析 (1)浓硝酸和氢氧化钠溶液不能用作干燥剂,浓硫酸可以和氨气反应,实验室可选用碱石灰来干燥氨气。(2)将胶头滴管中的少量液体挤入烧瓶,氨气极易溶于水,使瓶内压强迅速减小,在大气压的作用下,烧杯中的液体会顺利进入烧瓶,形成喷泉。
11.答案 (1)安静燃烧,发出苍白色火焰,瓶口有白雾
(2)①②③
(3)加入浓NaOH溶液,加热,生成无色、有刺激性气味的气体,用湿润的红色石蕊试纸靠近试管口处,若试纸变为蓝色,证明E中有N,否则,则不含N(答案合理即可)
解析 根据气体A呈黄绿色,气体D极易溶于水且形成的溶液可使酚酞变红,推知A为Cl2,D为NH3;根据气体B能在气体A(Cl2)中燃烧,推知B为H2;联系框图中各物质间的转化关系,进一步推知C为HCl,E为NH4Cl。
12.A 解析 NH3遇到浓盐酸产生白烟NH4Cl,该反应没有元素化合价变化,不是氧化还原反应,A正确;向某溶液中滴加盐酸酸化的Ba(NO3)2溶液出现白色沉淀,也可能是氯化银沉淀,或者是酸性条件下亚硫酸根离子被硝酸根离子氧化生成硫酸根离子而形成硫酸钡沉淀,不能说明该溶液中一定有S,B错误;NH4Cl受热能分解生成氨气和氯化氢,在管口遇冷很快又化合生成氯化铵,不能用于实验室制氨气,C错误;NH3通入水中,与水反应生成NH3·H2O,NH3·H2O电离出铵根离子和氢氧根离子,故水溶液可以导电,而NH3为非电解质,D错误。
13.A 解析 挥发出的HCl气体也能与硅酸钠反应生成硅酸,不能比较C和Si的非金属性,A错误;继续向烧杯的清液中滴加氯化钡溶液,若不产生沉淀,说明S沉淀完全,B正确;氨气极易溶于水,内外形成压强差,液体被压入烧瓶中,形成喷泉,C正确;浓氨水与氧化钙混合,氧化钙与水反应放出大量的热,加速一水合氨的分解以制氨气,D正确。
14.B 解析 固体加蒸馏水溶解,再加入NaOH溶液后,加热,若含有N,则N+OH-NH3↑+H2O,NH3能使湿润(用到蒸馏水)的红色石蕊试纸变蓝。故选B。
15.B 解析 柠檬酸能与FeCO3反应生成柠檬酸亚铁和CO2,CO2能够排除装置中的空气,防止氧化Fe2+,故流程①可用装置甲,A不合题意;由于NH4NO3受热易分解,甚至发生爆炸,故不能用NH4NO3和Ca(OH)2共热制备NH3,应该用NH4Cl和Ca(OH)2共热制备NH3,B符合题意;氨气极易溶于水,能够用装置丙观察喷泉实验和制取氨水,C不合题意;已知流程②为“浓缩为糊状、干燥”,其中“浓缩为糊状”流程可用装置丁即蒸发浓缩,由于柠檬酸铁铵属于铵盐,受热易分解,故“干燥”用低温干燥,D不合题意。
16.答案 (1)4NH3+5O24NO+6H2O
(2)①2NH4Cl+Ca(OH)2CaCl2+2NH3↑+2H2O ②b ③3∶4 ④缺少尾气处理装置
解析 (2)②甲用于干燥氨气,乙用于干燥NO2。五氧化二磷能与氨气反应,不能用其干燥氨气,a错误;碱石灰不与氨气反应,能干燥氨气,无水氯化钙不与NO2反应,能干燥NO2,b正确;碱石灰与NO2反应,不能用碱石灰干燥NO2,c错误。③NO2与NH3反应生成N2和水,该反应中NO2得电子为氧化剂,NH3失电子为还原剂,根据得失电子守恒,氧化剂和还原剂的物质的量之比为3∶4。④从实验装置可知,该实验装置缺少尾气处理装置,多余的氨气和NO2没有被处理直接排入空气中。
17.答案 (1)干燥管(或球形干燥管)
(2)SO2 漂白性 试纸变蓝 除去NH3中的SO2和H2O
(3)NH3
(4)取少量装置F内溶液于试管中,滴加足量的BaCl2溶液,生成白色沉淀;加入足量稀盐酸后沉淀完全溶解,并放出无色具有刺激性气味的气体
(5)3SO44NH3↑+N2↑+3SO2↑+6H2O↑
解析 (1)由题干实验装置图可知,仪器a的名称是球形干燥管或干燥管。(2)先关闭止水夹n,打开止水夹m,400 ℃加热装置C,SO2具有漂白性,能够漂白品红等有色物质,装置E中品红溶液褪色,证明分解产物中含有SO2,品红溶液褪色说明其具有漂白性;NH3溶于水呈碱性,则NH3遇到湿润的红色石蕊试纸将其变为蓝色,然后打开止水夹n,关闭止水夹m,装置A中的现象是试纸变蓝,说明分解产物中含有氨气,碱石灰的作用是除去NH3中的SO2和H2O。(3)由(2)中分析可知,分解产物为SO2、N2、NH3和H2O,故装置D内稀盐酸吸收的气体是NH3。(4)利用BaSO3不溶于水而溶于稀盐酸、BaSO4既不溶于水也不溶于稀盐酸的特性可知,检验装置F内溶液中有S、无S的实验操作和现象是取少量装置F内溶液于试管中,滴加足量的BaCl2溶液,生成白色沉淀;加入足量稀盐酸后沉淀完全溶解,并放出无色具有刺激性气味的气体。(5)由上述分析可知,分解产物为SO2、N2、NH3和H2O,则该分解反应的化学方程式为3SO44NH3↑+N2↑+3SO2↑+6H2O↑。
18.答案 (1)ace (2)①饱和食盐水、浓硫酸 ②3Cl2+8NH36NH4Cl+N2 ③NaOH(合理即可) Cl2+2OH-Cl-+ClO-+H2O
解析 (1)升高温度能促进NH3·H2O分解生成氨气,为促进NH3·H2O分解,则烧瓶中加入的物质遇氨水后能放出大量的热,且和氨水不反应。碱石灰遇水放出大量的热,且和氨水不反应,故a选;浓硫酸和氨水反应,故b不选;生石灰遇水放出大量的热,且和氨水不反应,故c选;五氧化二磷与氨水反应,故d不选;烧碱固体遇水放出大量的热,且和氨水不反应,故e选。(2)①用浓盐酸和二氧化锰制取的氯气中含有氯化氢气体和水蒸气,为防止干扰实验,氯气在进入烧瓶前,应该分别用饱和食盐水和浓硫酸除去氯化氢气体和水蒸气。②根据得失电子守恒知,D中生成的无色无味的气体是氮气,所以该反应的化学方程式为3Cl2+8NH36NH4Cl+N2。③可以用氢氧化钠溶液除去氯气,反应的离子方程式为Cl2+2OH-Cl-+ClO-+H2O。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
