专题8 有机化合物的获得与应用 分层作业16 乙酸--2025苏教版化学必修第二册同步练习题(含答案)
文档属性
| 名称 | 专题8 有机化合物的获得与应用 分层作业16 乙酸--2025苏教版化学必修第二册同步练习题(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 562.4KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-27 00:00:00 | ||
图片预览



文档简介
中小学教育资源及组卷应用平台
2025苏教版化学必修第二册
分层作业16 乙酸
A级必备知识基础练
1.下列有关乙酸的物理性质的叙述不正确的是( )
A.食醋的颜色(红棕色)就是乙酸的颜色
B.乙酸的熔点比水高,很容易变成固体
C.乙酸俗称冰醋酸
D.乙酸和乙醇可以互溶,故不能用分液法分离
2.乙酸是生活中常见的一种有机物,下列关于乙酸的说法正确的是( )
A.乙酸的官能团为—OH
B.乙酸的酸性比碳酸弱
C.乙酸能够与金属钠反应产生氢气
D.乙酸能使紫色的石蕊溶液变蓝
3.酒精和醋酸是生活中的常用品,下列方法不能将二者鉴别开的是( )
A.闻气味
B.分别用来浸泡水壶中的水垢看是否溶解
C.分别滴加NaOH溶液
D.分别滴加紫色石蕊溶液
4.(2024河北衡水高一期中)乙酸和乙醇是生活中常见的两种有机物,下列关于乙酸和乙醇的说法不正确的是( )
A.乙醇可以使酸性高锰酸钾溶液褪色
B.75%(体积分数)的乙醇溶液常用于医疗消毒
C.氢氧化钠能和乙酸、乙醇反应,且都属于取代反应
D.乙醇和乙酸在一定条件下能反应生成乙酸乙酯,该反应属于取代反应
5.某有机物的空间填充模型如图所示,其中白球表示氢原子,黑球表示碳原子,灰球表示氧原子,则下列关于这种有机物的描述不正确的是( )
A.俗称醋酸
B.可以发生取代反应
C.分子中所有原子不可能在同一平面
D.一定条件下可与乙醇反应,反应时该有机物断裂O—H
6.除去括号内杂质所用试剂和方法正确的是( )
选项 物质 所用试剂 方法
A 乙醇(乙酸) 氢氧化钠溶液 分液
B 乙烷(乙烯) 酸性高锰酸钾溶液 洗气
C 乙酸乙酯(乙酸) 饱和碳酸钠溶液 蒸馏
D 乙醇(水) 生石灰 蒸馏
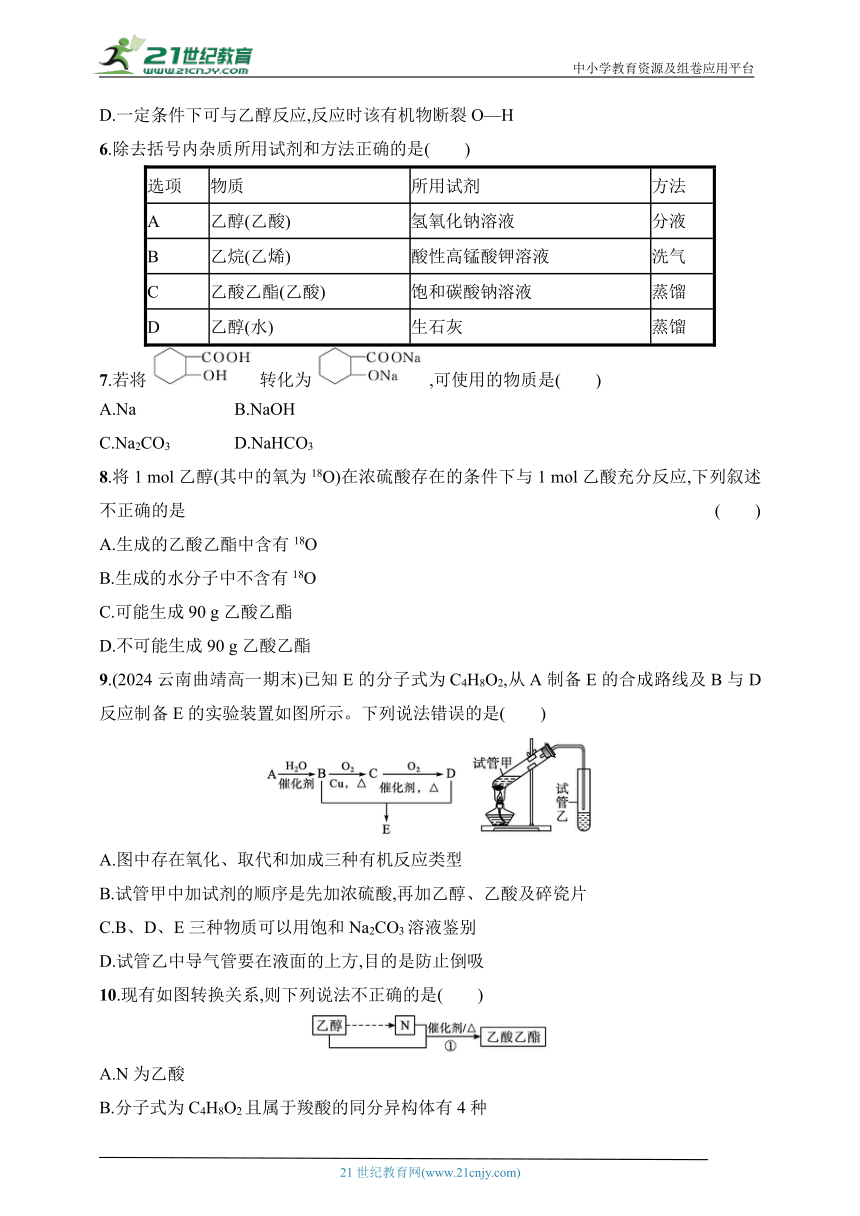
7.若将转化为,可使用的物质是( )
A.Na B.NaOH
C.Na2CO3 D.NaHCO3
8.将1 mol乙醇(其中的氧为18O)在浓硫酸存在的条件下与1 mol乙酸充分反应,下列叙述不正确的是 ( )
A.生成的乙酸乙酯中含有18O
B.生成的水分子中不含有18O
C.可能生成90 g乙酸乙酯
D.不可能生成90 g乙酸乙酯
9.(2024云南曲靖高一期末)已知E的分子式为C4H8O2,从A制备E的合成路线及B与D反应制备E的实验装置如图所示。下列说法错误的是( )
A.图中存在氧化、取代和加成三种有机反应类型
B.试管甲中加试剂的顺序是先加浓硫酸,再加乙醇、乙酸及碎瓷片
C.B、D、E三种物质可以用饱和Na2CO3溶液鉴别
D.试管乙中导气管要在液面的上方,目的是防止倒吸
10.现有如图转换关系,则下列说法不正确的是( )
A.N为乙酸
B.分子式为C4H8O2且属于羧酸的同分异构体有4种
C.过程①如果加热一段时间后发现忘记加碎瓷片,应该停止加热,待冷却后补加
D.可用饱和碳酸钠溶液来除掉乙酸乙酯中混有的乙酸
11.烃A的产量能衡量一个国家石油化工发展水平,F的碳原子数为D的两倍,以A、D为原料合成F和高分子化合物E,其合成路线如图所示:
(1)A的结构式为 ;B中决定性质的重要原子团的名称为 。
(2)写出反应的化学方程式及反应类型:
① ;
反应类型 。
② ;
反应类型 。
(3)实验室怎样区分B和D
。
12.A、B两种液态有机化合物均由碳、氢、氧三种元素组成,物质A能溶于水,它的相对分子质量是60,分子中有8个原子,其中氧原子数与碳原子数相等,且A与Na2CO3溶液混合时产生气体。B分子中有9个原子,分子内所有原子的核电荷数之和为26,且B只能与钠反应放出氢气,不能与Na2CO3溶液反应。请回答下列问题:
(1)A的结构简式为 ,B的结构简式为 。
(2)写出A与Na2CO3溶液反应的化学方程式: 。
(3)写出B与Na反应的化学方程式: 。
B级关键能力提升练
13.下列关于乙酸的说法中,正确的有( )
①乙酸分子里有四个氢原子,所以它不是一元酸
②乙酸乙酯中残留的乙酸,有效的处理方法是用过量饱和碳酸钠溶液洗涤后分液
③1 mol乙酸与足量乙醇在浓硫酸作用下加热可生成88 g乙酸乙酯
④乙酸是一种重要的有机酸,常温下乙酸是有刺激性气味的液体
⑤乙酸能够与金属钠反应产生氢气
⑥乙酸的酸性比碳酸弱
⑦食醋中含有乙酸,乙酸可由乙醇氧化得到
⑧乙酸易溶于水和乙醇,其水溶液能导电
A.3种 B.6种 C.4种 D.5种
14.有机化合物甲、乙的键线式如图。下列说法错误的是( )
甲 乙
A.甲、乙互称为同分异构体
B.与甲为同一种物质
C.甲能与金属钠反应生成氢气,而乙不能
D.甲、乙都能使酸性KMnO4溶液褪色
15.分子式为C5H10O2并能与饱和NaHCO3溶液反应放出气体的有机化合物有(不含立体异构)( )
A.3种 B.4种 C.5种 D.6种
16.分支酸可用于生化研究,其结构简式如图。下列关于分枝酸的叙述正确的是( )
A.分子中含有2种官能团
B.可与乙醇、乙酸反应,且反应类型相同
C.1 mol分支酸最多可与3 mol NaOH发生中和反应
D.可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
17.(2024河北邢台高一期末)乙酸乙酯样品中混有乙酸和乙醇,某兴趣小组设计如下方案分离与提纯该样品。
下列叙述错误的是( )
A.步骤1中,试剂1为NaOH溶液
B.步骤1得到的乙酸乙酯不溶于水
C.步骤2中,采用蒸馏操作
D.步骤3中,硫酸不能用盐酸替代
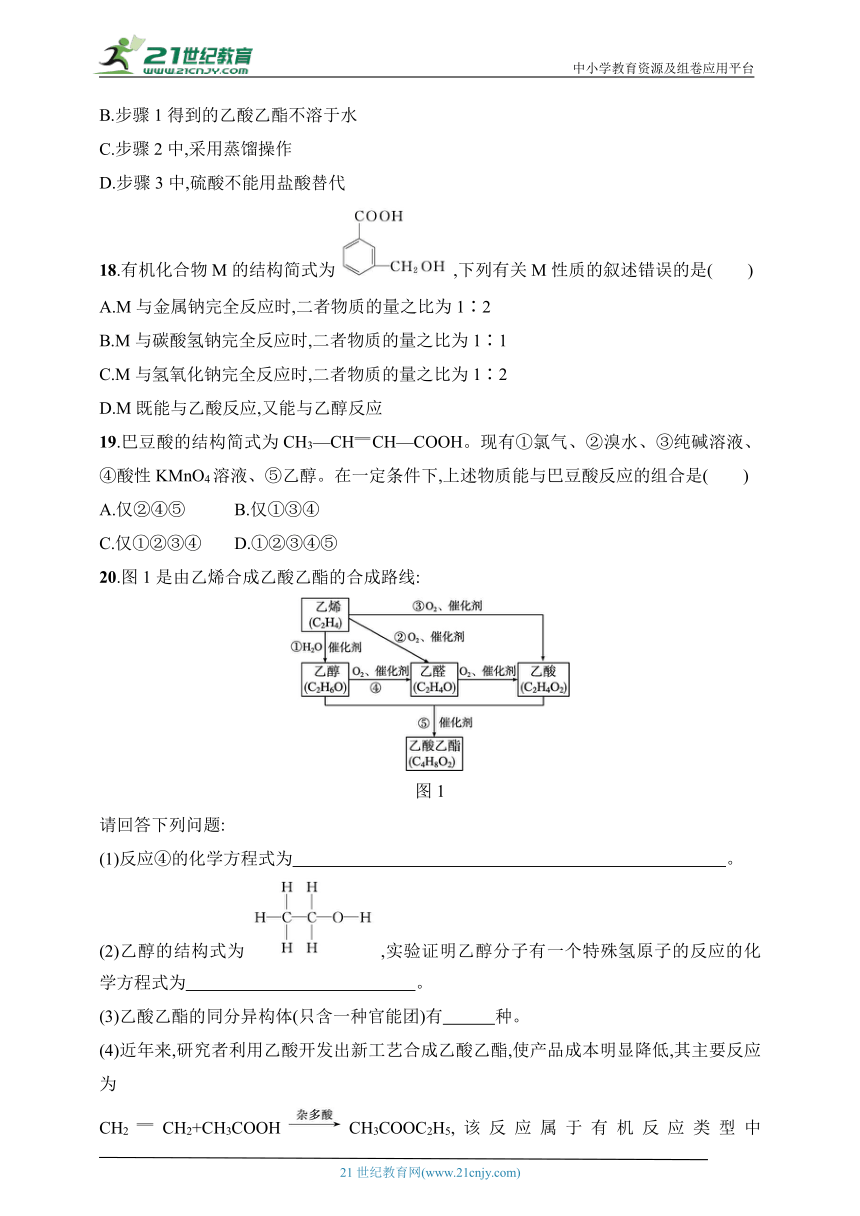
18.有机化合物M的结构简式为,下列有关M性质的叙述错误的是( )
A.M与金属钠完全反应时,二者物质的量之比为1∶2
B.M与碳酸氢钠完全反应时,二者物质的量之比为1∶1
C.M与氢氧化钠完全反应时,二者物质的量之比为1∶2
D.M既能与乙酸反应,又能与乙醇反应
19.巴豆酸的结构简式为CH3—CHCH—COOH。现有①氯气、②溴水、③纯碱溶液、④酸性KMnO4溶液、⑤乙醇。在一定条件下,上述物质能与巴豆酸反应的组合是( )
A.仅②④⑤ B.仅①③④
C.仅①②③④ D.①②③④⑤
20.图1是由乙烯合成乙酸乙酯的合成路线:
图1
请回答下列问题:
(1)反应④的化学方程式为 。
(2)乙醇的结构式为,实验证明乙醇分子有一个特殊氢原子的反应的化学方程式为 。
(3)乙酸乙酯的同分异构体(只含一种官能团)有 种。
(4)近年来,研究者利用乙酸开发出新工艺合成乙酸乙酯,使产品成本明显降低,其主要反应为
CH2CH2+CH3COOHCH3COOC2H5,该反应属于有机反应类型中的 。
(5)实验室用如图2装置制备乙酸乙酯:试管中碎瓷片的作用是 ;
导管a的作用是导气和 ;试管b内饱和Na2CO3溶液的作用一方面是除去乙酸乙酯中混有的乙酸和乙醇,另一方面是 。
图2
21.(2024广西百色高一期末)丙烯酸乙酯天然存在于菠萝等水果中,是一种合成香料,可以用乙烯、丙烯等石油化工产品为原料进行合成,合成线路如下:
(1)由乙烯生成有机物A的化学方程式为 。
(2)乙烯、丙烯的关系是 。
A.同分异构体 B.同系物
C.同位素 D.同素异形体
(3)有机物B的结构简式为 ;官能团的名称是 。
(4)丙烯与氯化氢发生加成反应生成两种同分异构体,结构简式为 。
(5)A与B反应生成丙烯酸乙酯的化学方程式为 。
C级学科素养拔高练
22.酸牛奶中含有乳酸,其结构简式为。在病房、手术室、实验室等场所中采用乳酸蒸气消毒,可有效杀灭空气中的细菌;乳酸聚合得到的聚乳酸抽成丝纺成线,是良好的手术缝线,缝口愈合后不用拆线,能自动降解成乳酸被人体吸收,无不良后果。
试回答下列问题:
(1)乳酸分子中含有的官能团名称为 。
(2)写出乳酸跟少量碳酸钠反应的化学方程式: 。
(3)乳酸在浓硫酸存在下,两分子相互反应,生成链状物质的结构简式为 ;两分子相互反应,生成环状物质的结构简式为 。
分层作业16 乙酸
1.A 2.C
3.C 解析 NaOH溶液与乙醇互溶,NaOH溶液与乙酸反应无明显现象,答案选C。
4.C 解析 乙醇是非电解质,不能与氢氧化钠溶液反应,乙酸溶液与氢氧化钠溶液的反应属于中和反应,不属于取代反应,故C错误。
5.D 解析 由该有机物的空间填充模型可知,其结构简式为CH3COOH,俗称醋酸,A正确;含有—COOH,可与醇发生酯化反应,属于取代反应,B正确;分子中含有—CH3,所有原子不可能在同一平面,C正确;与乙醇发生酯化反应时,乙酸脱去羟基,断裂C—O,D错误。
6.D
7.A 解析 —COOH和—OH均与Na发生置换反应,可实现转化,A正确;—OH与NaOH、Na2CO3、NaHCO3均不反应,B、C、D错误。
8.C 解析 酯化反应的实质是“酸脱羟基醇脱氢”,
+H2O,所以生成的水中不可能有18O;生成酯的相对分子质量为90,由于酯化反应是可逆反应,不能进行到底,因此实际上不可能得到90 g乙酸乙酯。
9.B 解析 由转化关系和E的分子式为C4H8O2可知,A为乙烯,与水发生加成反应生成B(乙醇),乙醇氧化生成C(乙醛),乙醛氧化生成D(乙酸),B与D发生酯化反应生成E,故A正确;浓硫酸与其他液体混合时会放出大量的热,所以应先加入碎瓷片、酒精、浓硫酸,再慢慢加入乙酸,故B错误;B、D、E三种物质可以用饱和Na2CO3溶液鉴别,现象分别为溶解、溶解产生气泡、分为上下两层,故C正确;如果导气管伸入饱和碳酸钠溶液液面以下,可能引起倒吸,试管乙中导气管要在液面的上方,目的是防止倒吸,故D正确。
10.B 解析 乙醇与N反应生成乙酸乙酯,则N为乙酸,A正确;分子式为C4H8O2且属于羧酸的同分异构体有2种:CH3CH2CH2COOH和,B错误;过程①如果加热一段时间后发现忘记加碎瓷片,应该立即停止加热,待冷却后补加,防止暴沸,C正确;乙酸与碳酸钠反应生成乙酸钠而被除去,D正确。
11.答案 (1) 羟基
(2)①2CH3CH2OH+O22CH3CHO+2H2O 氧化反应
②CH3COOH+CH3CH2OHCH3COOCH2CH3+H2O 酯化反应(或取代反应)
(3)分别取少量待测液于试管中,滴加少量石蕊溶液,若溶液变红,则所取待测液为乙酸,另一种为乙醇(或其他合理方法)
解析 衡量一个国家石油化工发展水平的是乙烯的产量,根据框图,B为乙醇,C为乙醛,F为某酸乙酯。因为F中碳原子数为D的两倍,所以D为乙酸。
12.答案 (1)CH3COOH CH3CH2OH
(2)2CH3COOH+Na2CO32CH3COONa+CO2↑+H2O
(3)2CH3CH2OH+2Na2CH3CH2ONa+H2↑
解析 A是能溶于水且能与Na2CO3反应、分子组成中有C、H、O的有机化合物,可能是羧酸,分子中的氧原子及碳原子数只能都为2(根据碳原子数与氧原子数相同,相对分子质量为60),可推知A为CH3COOH。B物质分子中所有原子的核电荷数之和为26,因为C、H、O三种元素的原子核电荷数分别是6、1、8,B分子中有9个原子,只能跟钠反应放出氢气,所以B分子中只能有1个氧原子,分子中碳原子数必小于3。经分析,只有C2H6O符合题意,结合性质可以确定B为CH3CH2OH。
13.D 解析 ①乙酸的结构简式为CH3COOH,虽然乙酸分子中有4个氢原子,但乙酸只能电离出一个氢原子,因此乙酸属于一元酸,故①错误;②乙酸乙酯是不溶于水的液体,密度小于水,乙酸乙酯中混有乙酸,常用饱和碳酸钠溶液处理,碳酸钠能吸收乙酸,同时降低乙酸乙酯在溶液中的溶解度使之析出,然后采用分液方法进行分离,故②正确;③乙酸与乙醇发生酯化反应,该反应为可逆反应,不能完全进行到底,因此1 mol乙酸与足量的乙醇反应,生成乙酸乙酯的质量小于88 g,故③错误;④乙酸是一种有机酸,常温下乙酸是具有强烈刺激性气味的液体,故④正确;⑤乙酸能与金属钠反应生成乙酸钠和氢气,故⑤正确;⑥乙酸的酸性强于碳酸,故⑥错误;⑦食醋中含有乙酸,乙酸可以由乙醇经过氧化得到,故⑦正确;⑧乙酸易溶于水和乙醇,乙酸属于电解质,其水溶液能导电,故⑧正确。综上所述,正确的是②④⑤⑦⑧。
14.B 解析 甲、乙分子式相同,结构不同,互称为同分异构体,故A正确;甲的结构简式为,的结构简式为,甲为羧酸,为酯,二者互称为同分异构体,不是同一种物质,故B错误;甲含有羧基,能和钠反应,乙不含羧基或羟基,乙不能和钠反应,故C正确;碳碳双键能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,甲、乙都含有碳碳双键,所以都能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,故D正确。
15.B 解析 分子式为C5H10O2并能与饱和NaHCO3溶液反应放出气体的有机化合物属于羧酸,其官能团为—COOH,将该有机化合物看作C4H9—COOH,而丁基(C4H9—)有4种不同的结构,分别为CH3CH2CH2CH2—、(CH3)2CHCH2—、(CH3)3C—、,从而推知该有机化合物有4种不同的分子结构。
16.B 解析 分子中含有羧基、碳碳双键、羟基等不止2种官能团,A错误;分支酸分子中含有的羧基、羟基可分别与乙醇、乙酸发生酯化反应,B正确;分子中只有羧基可与NaOH反应,故1 mol分支酸最多可与2 mol NaOH发生中和反应,C错误;使溴的四氯化碳溶液褪色是因为碳碳双键与Br2发生了加成反应,使酸性高锰酸钾溶液褪色是因为发生了氧化反应,D错误。
17.A 解析 由分离提纯路线可知,试剂1为饱和碳酸钠溶液,乙酸能与碳酸钠反应生成易溶于水的乙酸钠,经步骤1分液得到乙酸乙酯和溶液1(乙醇、乙酸钠和过量的饱和碳酸钠溶液);步骤2为蒸馏,得到乙醇和溶液2(碳酸钠和乙酸钠溶液);加入硫酸酸化,经过步骤3蒸馏得到乙酸。由分析可知,步骤1中加入试剂1为饱和碳酸钠溶液,氢氧化钠会与乙酸乙酯反应,试剂1不能为氢氧化钠溶液,A错误;乙酸乙酯不溶于水,B正确;溶液1含乙醇、乙酸钠、碳酸钠,乙醇沸点低,采用蒸馏可分离出乙醇,C正确;步骤3中加入的硫酸与乙酸钠反应生成乙酸,然后将生成的乙酸蒸馏出来,盐酸是挥发性酸,则乙酸中会混有杂质,不能用盐酸代替硫酸,D正确。
18.C 解析 M与Na完全反应时,1 mol—COOH、1 mol —OH各消耗1 mol Na,A项正确;1 mol—COOH只与1 mol NaHCO3反应,B项正确;1 mol—COOH消耗1 mol NaOH,—OH不与NaOH反应,C项错误;M中既含—OH,又含有—COOH,所以既能与乙酸反应,又能与乙醇反应,D项正确。
19.D 解析 巴豆酸分子中含有和—COOH,碳碳双键可与氯气、溴发生加成反应,可被酸性高锰酸钾溶液氧化;羧基可与纯碱溶液反应放出CO2,可与乙醇发生酯化反应,因此①②③④⑤均正确。
20.答案 (1)2CH3CH2OH+O22CH3CHO+2H2O
(2)2CH3CH2OH+2Na2CH3CH2ONa+H2↑
(3)5 (4)加成反应
(5)防止液体暴沸 冷凝回流 降低乙酸乙酯的溶解度
解析 (1)乙醇分子中含有羟基,在Cu作催化剂、加热条件下发生氧化反应,产生乙醛和水,反应的化学方程式是2CH3CH2OH+O22CH3CHO+2H2O。
(2)实验证明乙醇分子有一个特殊氢原子的反应的化学方程式为2CH3CH2OH+2Na2CH3CH2ONa+H2↑。
(3)乙酸乙酯分子式是C4H8O2,它的同分异构体中只含有一种官能团的物质有酯、羧酸;属于酯类的有HCOOCH2CH2CH3、HCOOCH(CH3)2、
CH3CH2COOCH3;羧酸有CH3CH2CH2COOH、
(CH3)2CHCOOH,因此共有5种同分异构体。
(4)乙烯与乙酸反应生成乙酸乙酯为加成反应。
(5)试管中碎瓷片的作用是防止液体暴沸;导管a的作用是导气和冷凝回流;试管b内饱和Na2CO3溶液的作用的另一方面是降低乙酸乙酯的溶解度。
21.答案 (1)CH2CH2+H2OCH3CH2OH
(2)B (3)CH2CHCOOH 碳碳双键、羧基
(4)ClCH2—CH2—CH3、CH3—CHCl—CH3
(5)CH2CHCOOH+CH3CH2OHCH2CHCOOCH2CH3+H2O
解析 根据丙烯酸乙酯逆推,A和B反应生成丙烯酸乙酯的反应类型是酯化反应,反应物为乙醇和丙烯酸,结合题目所给的初始物质的结构简式可知,有机物A为CH3CH2OH,有机物B为CH2CHCOOH,乙烯与水发生加成反应生成乙醇,丙烯发生氧化反应生成丙烯酸。(3)有机物B是丙烯酸
(CH2CHCOOH),其官能团名称为碳碳双键、羧基。(4)丙烯与氯化氢发生加成反应,得到的两种同分异构体为
ClCH2—CH2—CH3、CH3—CHCl—CH3。(5)A与B的反应是酯化反应,化学方程式为CH2CHCOOH+CH3CH2OHCH2CHCOOCH2CH3+H2O。
22.答案 (1)羟基、羧基
(2)+Na2CO32+CO2↑+H2O
(3)
解析 (1)乳酸中含有—OH和—COOH两种官能团。
(2)乳酸分子中的羧基与少量碳酸钠反应,放出二氧化碳。
(3)乳酸分子中的—OH和—COOH能发生酯化反应,当两分子乳酸发生酯化反应只生成一分子水时,其结构为链状;当两分子乳酸发生酯化反应生成两分子水时,其结构为环状。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
2025苏教版化学必修第二册
分层作业16 乙酸
A级必备知识基础练
1.下列有关乙酸的物理性质的叙述不正确的是( )
A.食醋的颜色(红棕色)就是乙酸的颜色
B.乙酸的熔点比水高,很容易变成固体
C.乙酸俗称冰醋酸
D.乙酸和乙醇可以互溶,故不能用分液法分离
2.乙酸是生活中常见的一种有机物,下列关于乙酸的说法正确的是( )
A.乙酸的官能团为—OH
B.乙酸的酸性比碳酸弱
C.乙酸能够与金属钠反应产生氢气
D.乙酸能使紫色的石蕊溶液变蓝
3.酒精和醋酸是生活中的常用品,下列方法不能将二者鉴别开的是( )
A.闻气味
B.分别用来浸泡水壶中的水垢看是否溶解
C.分别滴加NaOH溶液
D.分别滴加紫色石蕊溶液
4.(2024河北衡水高一期中)乙酸和乙醇是生活中常见的两种有机物,下列关于乙酸和乙醇的说法不正确的是( )
A.乙醇可以使酸性高锰酸钾溶液褪色
B.75%(体积分数)的乙醇溶液常用于医疗消毒
C.氢氧化钠能和乙酸、乙醇反应,且都属于取代反应
D.乙醇和乙酸在一定条件下能反应生成乙酸乙酯,该反应属于取代反应
5.某有机物的空间填充模型如图所示,其中白球表示氢原子,黑球表示碳原子,灰球表示氧原子,则下列关于这种有机物的描述不正确的是( )
A.俗称醋酸
B.可以发生取代反应
C.分子中所有原子不可能在同一平面
D.一定条件下可与乙醇反应,反应时该有机物断裂O—H
6.除去括号内杂质所用试剂和方法正确的是( )
选项 物质 所用试剂 方法
A 乙醇(乙酸) 氢氧化钠溶液 分液
B 乙烷(乙烯) 酸性高锰酸钾溶液 洗气
C 乙酸乙酯(乙酸) 饱和碳酸钠溶液 蒸馏
D 乙醇(水) 生石灰 蒸馏
7.若将转化为,可使用的物质是( )
A.Na B.NaOH
C.Na2CO3 D.NaHCO3
8.将1 mol乙醇(其中的氧为18O)在浓硫酸存在的条件下与1 mol乙酸充分反应,下列叙述不正确的是 ( )
A.生成的乙酸乙酯中含有18O
B.生成的水分子中不含有18O
C.可能生成90 g乙酸乙酯
D.不可能生成90 g乙酸乙酯
9.(2024云南曲靖高一期末)已知E的分子式为C4H8O2,从A制备E的合成路线及B与D反应制备E的实验装置如图所示。下列说法错误的是( )
A.图中存在氧化、取代和加成三种有机反应类型
B.试管甲中加试剂的顺序是先加浓硫酸,再加乙醇、乙酸及碎瓷片
C.B、D、E三种物质可以用饱和Na2CO3溶液鉴别
D.试管乙中导气管要在液面的上方,目的是防止倒吸
10.现有如图转换关系,则下列说法不正确的是( )
A.N为乙酸
B.分子式为C4H8O2且属于羧酸的同分异构体有4种
C.过程①如果加热一段时间后发现忘记加碎瓷片,应该停止加热,待冷却后补加
D.可用饱和碳酸钠溶液来除掉乙酸乙酯中混有的乙酸
11.烃A的产量能衡量一个国家石油化工发展水平,F的碳原子数为D的两倍,以A、D为原料合成F和高分子化合物E,其合成路线如图所示:
(1)A的结构式为 ;B中决定性质的重要原子团的名称为 。
(2)写出反应的化学方程式及反应类型:
① ;
反应类型 。
② ;
反应类型 。
(3)实验室怎样区分B和D
。
12.A、B两种液态有机化合物均由碳、氢、氧三种元素组成,物质A能溶于水,它的相对分子质量是60,分子中有8个原子,其中氧原子数与碳原子数相等,且A与Na2CO3溶液混合时产生气体。B分子中有9个原子,分子内所有原子的核电荷数之和为26,且B只能与钠反应放出氢气,不能与Na2CO3溶液反应。请回答下列问题:
(1)A的结构简式为 ,B的结构简式为 。
(2)写出A与Na2CO3溶液反应的化学方程式: 。
(3)写出B与Na反应的化学方程式: 。
B级关键能力提升练
13.下列关于乙酸的说法中,正确的有( )
①乙酸分子里有四个氢原子,所以它不是一元酸
②乙酸乙酯中残留的乙酸,有效的处理方法是用过量饱和碳酸钠溶液洗涤后分液
③1 mol乙酸与足量乙醇在浓硫酸作用下加热可生成88 g乙酸乙酯
④乙酸是一种重要的有机酸,常温下乙酸是有刺激性气味的液体
⑤乙酸能够与金属钠反应产生氢气
⑥乙酸的酸性比碳酸弱
⑦食醋中含有乙酸,乙酸可由乙醇氧化得到
⑧乙酸易溶于水和乙醇,其水溶液能导电
A.3种 B.6种 C.4种 D.5种
14.有机化合物甲、乙的键线式如图。下列说法错误的是( )
甲 乙
A.甲、乙互称为同分异构体
B.与甲为同一种物质
C.甲能与金属钠反应生成氢气,而乙不能
D.甲、乙都能使酸性KMnO4溶液褪色
15.分子式为C5H10O2并能与饱和NaHCO3溶液反应放出气体的有机化合物有(不含立体异构)( )
A.3种 B.4种 C.5种 D.6种
16.分支酸可用于生化研究,其结构简式如图。下列关于分枝酸的叙述正确的是( )
A.分子中含有2种官能团
B.可与乙醇、乙酸反应,且反应类型相同
C.1 mol分支酸最多可与3 mol NaOH发生中和反应
D.可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
17.(2024河北邢台高一期末)乙酸乙酯样品中混有乙酸和乙醇,某兴趣小组设计如下方案分离与提纯该样品。
下列叙述错误的是( )
A.步骤1中,试剂1为NaOH溶液
B.步骤1得到的乙酸乙酯不溶于水
C.步骤2中,采用蒸馏操作
D.步骤3中,硫酸不能用盐酸替代
18.有机化合物M的结构简式为,下列有关M性质的叙述错误的是( )
A.M与金属钠完全反应时,二者物质的量之比为1∶2
B.M与碳酸氢钠完全反应时,二者物质的量之比为1∶1
C.M与氢氧化钠完全反应时,二者物质的量之比为1∶2
D.M既能与乙酸反应,又能与乙醇反应
19.巴豆酸的结构简式为CH3—CHCH—COOH。现有①氯气、②溴水、③纯碱溶液、④酸性KMnO4溶液、⑤乙醇。在一定条件下,上述物质能与巴豆酸反应的组合是( )
A.仅②④⑤ B.仅①③④
C.仅①②③④ D.①②③④⑤
20.图1是由乙烯合成乙酸乙酯的合成路线:
图1
请回答下列问题:
(1)反应④的化学方程式为 。
(2)乙醇的结构式为,实验证明乙醇分子有一个特殊氢原子的反应的化学方程式为 。
(3)乙酸乙酯的同分异构体(只含一种官能团)有 种。
(4)近年来,研究者利用乙酸开发出新工艺合成乙酸乙酯,使产品成本明显降低,其主要反应为
CH2CH2+CH3COOHCH3COOC2H5,该反应属于有机反应类型中的 。
(5)实验室用如图2装置制备乙酸乙酯:试管中碎瓷片的作用是 ;
导管a的作用是导气和 ;试管b内饱和Na2CO3溶液的作用一方面是除去乙酸乙酯中混有的乙酸和乙醇,另一方面是 。
图2
21.(2024广西百色高一期末)丙烯酸乙酯天然存在于菠萝等水果中,是一种合成香料,可以用乙烯、丙烯等石油化工产品为原料进行合成,合成线路如下:
(1)由乙烯生成有机物A的化学方程式为 。
(2)乙烯、丙烯的关系是 。
A.同分异构体 B.同系物
C.同位素 D.同素异形体
(3)有机物B的结构简式为 ;官能团的名称是 。
(4)丙烯与氯化氢发生加成反应生成两种同分异构体,结构简式为 。
(5)A与B反应生成丙烯酸乙酯的化学方程式为 。
C级学科素养拔高练
22.酸牛奶中含有乳酸,其结构简式为。在病房、手术室、实验室等场所中采用乳酸蒸气消毒,可有效杀灭空气中的细菌;乳酸聚合得到的聚乳酸抽成丝纺成线,是良好的手术缝线,缝口愈合后不用拆线,能自动降解成乳酸被人体吸收,无不良后果。
试回答下列问题:
(1)乳酸分子中含有的官能团名称为 。
(2)写出乳酸跟少量碳酸钠反应的化学方程式: 。
(3)乳酸在浓硫酸存在下,两分子相互反应,生成链状物质的结构简式为 ;两分子相互反应,生成环状物质的结构简式为 。
分层作业16 乙酸
1.A 2.C
3.C 解析 NaOH溶液与乙醇互溶,NaOH溶液与乙酸反应无明显现象,答案选C。
4.C 解析 乙醇是非电解质,不能与氢氧化钠溶液反应,乙酸溶液与氢氧化钠溶液的反应属于中和反应,不属于取代反应,故C错误。
5.D 解析 由该有机物的空间填充模型可知,其结构简式为CH3COOH,俗称醋酸,A正确;含有—COOH,可与醇发生酯化反应,属于取代反应,B正确;分子中含有—CH3,所有原子不可能在同一平面,C正确;与乙醇发生酯化反应时,乙酸脱去羟基,断裂C—O,D错误。
6.D
7.A 解析 —COOH和—OH均与Na发生置换反应,可实现转化,A正确;—OH与NaOH、Na2CO3、NaHCO3均不反应,B、C、D错误。
8.C 解析 酯化反应的实质是“酸脱羟基醇脱氢”,
+H2O,所以生成的水中不可能有18O;生成酯的相对分子质量为90,由于酯化反应是可逆反应,不能进行到底,因此实际上不可能得到90 g乙酸乙酯。
9.B 解析 由转化关系和E的分子式为C4H8O2可知,A为乙烯,与水发生加成反应生成B(乙醇),乙醇氧化生成C(乙醛),乙醛氧化生成D(乙酸),B与D发生酯化反应生成E,故A正确;浓硫酸与其他液体混合时会放出大量的热,所以应先加入碎瓷片、酒精、浓硫酸,再慢慢加入乙酸,故B错误;B、D、E三种物质可以用饱和Na2CO3溶液鉴别,现象分别为溶解、溶解产生气泡、分为上下两层,故C正确;如果导气管伸入饱和碳酸钠溶液液面以下,可能引起倒吸,试管乙中导气管要在液面的上方,目的是防止倒吸,故D正确。
10.B 解析 乙醇与N反应生成乙酸乙酯,则N为乙酸,A正确;分子式为C4H8O2且属于羧酸的同分异构体有2种:CH3CH2CH2COOH和,B错误;过程①如果加热一段时间后发现忘记加碎瓷片,应该立即停止加热,待冷却后补加,防止暴沸,C正确;乙酸与碳酸钠反应生成乙酸钠而被除去,D正确。
11.答案 (1) 羟基
(2)①2CH3CH2OH+O22CH3CHO+2H2O 氧化反应
②CH3COOH+CH3CH2OHCH3COOCH2CH3+H2O 酯化反应(或取代反应)
(3)分别取少量待测液于试管中,滴加少量石蕊溶液,若溶液变红,则所取待测液为乙酸,另一种为乙醇(或其他合理方法)
解析 衡量一个国家石油化工发展水平的是乙烯的产量,根据框图,B为乙醇,C为乙醛,F为某酸乙酯。因为F中碳原子数为D的两倍,所以D为乙酸。
12.答案 (1)CH3COOH CH3CH2OH
(2)2CH3COOH+Na2CO32CH3COONa+CO2↑+H2O
(3)2CH3CH2OH+2Na2CH3CH2ONa+H2↑
解析 A是能溶于水且能与Na2CO3反应、分子组成中有C、H、O的有机化合物,可能是羧酸,分子中的氧原子及碳原子数只能都为2(根据碳原子数与氧原子数相同,相对分子质量为60),可推知A为CH3COOH。B物质分子中所有原子的核电荷数之和为26,因为C、H、O三种元素的原子核电荷数分别是6、1、8,B分子中有9个原子,只能跟钠反应放出氢气,所以B分子中只能有1个氧原子,分子中碳原子数必小于3。经分析,只有C2H6O符合题意,结合性质可以确定B为CH3CH2OH。
13.D 解析 ①乙酸的结构简式为CH3COOH,虽然乙酸分子中有4个氢原子,但乙酸只能电离出一个氢原子,因此乙酸属于一元酸,故①错误;②乙酸乙酯是不溶于水的液体,密度小于水,乙酸乙酯中混有乙酸,常用饱和碳酸钠溶液处理,碳酸钠能吸收乙酸,同时降低乙酸乙酯在溶液中的溶解度使之析出,然后采用分液方法进行分离,故②正确;③乙酸与乙醇发生酯化反应,该反应为可逆反应,不能完全进行到底,因此1 mol乙酸与足量的乙醇反应,生成乙酸乙酯的质量小于88 g,故③错误;④乙酸是一种有机酸,常温下乙酸是具有强烈刺激性气味的液体,故④正确;⑤乙酸能与金属钠反应生成乙酸钠和氢气,故⑤正确;⑥乙酸的酸性强于碳酸,故⑥错误;⑦食醋中含有乙酸,乙酸可以由乙醇经过氧化得到,故⑦正确;⑧乙酸易溶于水和乙醇,乙酸属于电解质,其水溶液能导电,故⑧正确。综上所述,正确的是②④⑤⑦⑧。
14.B 解析 甲、乙分子式相同,结构不同,互称为同分异构体,故A正确;甲的结构简式为,的结构简式为,甲为羧酸,为酯,二者互称为同分异构体,不是同一种物质,故B错误;甲含有羧基,能和钠反应,乙不含羧基或羟基,乙不能和钠反应,故C正确;碳碳双键能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,甲、乙都含有碳碳双键,所以都能被酸性高锰酸钾溶液氧化而使酸性高锰酸钾溶液褪色,故D正确。
15.B 解析 分子式为C5H10O2并能与饱和NaHCO3溶液反应放出气体的有机化合物属于羧酸,其官能团为—COOH,将该有机化合物看作C4H9—COOH,而丁基(C4H9—)有4种不同的结构,分别为CH3CH2CH2CH2—、(CH3)2CHCH2—、(CH3)3C—、,从而推知该有机化合物有4种不同的分子结构。
16.B 解析 分子中含有羧基、碳碳双键、羟基等不止2种官能团,A错误;分支酸分子中含有的羧基、羟基可分别与乙醇、乙酸发生酯化反应,B正确;分子中只有羧基可与NaOH反应,故1 mol分支酸最多可与2 mol NaOH发生中和反应,C错误;使溴的四氯化碳溶液褪色是因为碳碳双键与Br2发生了加成反应,使酸性高锰酸钾溶液褪色是因为发生了氧化反应,D错误。
17.A 解析 由分离提纯路线可知,试剂1为饱和碳酸钠溶液,乙酸能与碳酸钠反应生成易溶于水的乙酸钠,经步骤1分液得到乙酸乙酯和溶液1(乙醇、乙酸钠和过量的饱和碳酸钠溶液);步骤2为蒸馏,得到乙醇和溶液2(碳酸钠和乙酸钠溶液);加入硫酸酸化,经过步骤3蒸馏得到乙酸。由分析可知,步骤1中加入试剂1为饱和碳酸钠溶液,氢氧化钠会与乙酸乙酯反应,试剂1不能为氢氧化钠溶液,A错误;乙酸乙酯不溶于水,B正确;溶液1含乙醇、乙酸钠、碳酸钠,乙醇沸点低,采用蒸馏可分离出乙醇,C正确;步骤3中加入的硫酸与乙酸钠反应生成乙酸,然后将生成的乙酸蒸馏出来,盐酸是挥发性酸,则乙酸中会混有杂质,不能用盐酸代替硫酸,D正确。
18.C 解析 M与Na完全反应时,1 mol—COOH、1 mol —OH各消耗1 mol Na,A项正确;1 mol—COOH只与1 mol NaHCO3反应,B项正确;1 mol—COOH消耗1 mol NaOH,—OH不与NaOH反应,C项错误;M中既含—OH,又含有—COOH,所以既能与乙酸反应,又能与乙醇反应,D项正确。
19.D 解析 巴豆酸分子中含有和—COOH,碳碳双键可与氯气、溴发生加成反应,可被酸性高锰酸钾溶液氧化;羧基可与纯碱溶液反应放出CO2,可与乙醇发生酯化反应,因此①②③④⑤均正确。
20.答案 (1)2CH3CH2OH+O22CH3CHO+2H2O
(2)2CH3CH2OH+2Na2CH3CH2ONa+H2↑
(3)5 (4)加成反应
(5)防止液体暴沸 冷凝回流 降低乙酸乙酯的溶解度
解析 (1)乙醇分子中含有羟基,在Cu作催化剂、加热条件下发生氧化反应,产生乙醛和水,反应的化学方程式是2CH3CH2OH+O22CH3CHO+2H2O。
(2)实验证明乙醇分子有一个特殊氢原子的反应的化学方程式为2CH3CH2OH+2Na2CH3CH2ONa+H2↑。
(3)乙酸乙酯分子式是C4H8O2,它的同分异构体中只含有一种官能团的物质有酯、羧酸;属于酯类的有HCOOCH2CH2CH3、HCOOCH(CH3)2、
CH3CH2COOCH3;羧酸有CH3CH2CH2COOH、
(CH3)2CHCOOH,因此共有5种同分异构体。
(4)乙烯与乙酸反应生成乙酸乙酯为加成反应。
(5)试管中碎瓷片的作用是防止液体暴沸;导管a的作用是导气和冷凝回流;试管b内饱和Na2CO3溶液的作用的另一方面是降低乙酸乙酯的溶解度。
21.答案 (1)CH2CH2+H2OCH3CH2OH
(2)B (3)CH2CHCOOH 碳碳双键、羧基
(4)ClCH2—CH2—CH3、CH3—CHCl—CH3
(5)CH2CHCOOH+CH3CH2OHCH2CHCOOCH2CH3+H2O
解析 根据丙烯酸乙酯逆推,A和B反应生成丙烯酸乙酯的反应类型是酯化反应,反应物为乙醇和丙烯酸,结合题目所给的初始物质的结构简式可知,有机物A为CH3CH2OH,有机物B为CH2CHCOOH,乙烯与水发生加成反应生成乙醇,丙烯发生氧化反应生成丙烯酸。(3)有机物B是丙烯酸
(CH2CHCOOH),其官能团名称为碳碳双键、羧基。(4)丙烯与氯化氢发生加成反应,得到的两种同分异构体为
ClCH2—CH2—CH3、CH3—CHCl—CH3。(5)A与B的反应是酯化反应,化学方程式为CH2CHCOOH+CH3CH2OHCH2CHCOOCH2CH3+H2O。
22.答案 (1)羟基、羧基
(2)+Na2CO32+CO2↑+H2O
(3)
解析 (1)乳酸中含有—OH和—COOH两种官能团。
(2)乳酸分子中的羧基与少量碳酸钠反应,放出二氧化碳。
(3)乳酸分子中的—OH和—COOH能发生酯化反应,当两分子乳酸发生酯化反应只生成一分子水时,其结构为链状;当两分子乳酸发生酯化反应生成两分子水时,其结构为环状。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
