北京门头沟中学2025年高二化学复习课件:1.2 研究有机化合物的一般方法 课件(共29张PPT)
文档属性
| 名称 | 北京门头沟中学2025年高二化学复习课件:1.2 研究有机化合物的一般方法 课件(共29张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 2.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-27 00:00:00 | ||
图片预览







文档简介
(共29张PPT)
2025年高二化学复习
人教版 选择性必修3
第二节 研究有机化合物的一般方法
课时1 分离、提纯
Contents
目录
知识点突破
01
实战分析
02
知识点突破
01
有机物分离和提纯的常用方法
知识点
1.混合物分离、提纯的原则
(1)不能引入新杂质;(2)提纯后的物质成分不变;
(3)实验过程和操作方法简单易行;(4)节约试剂。
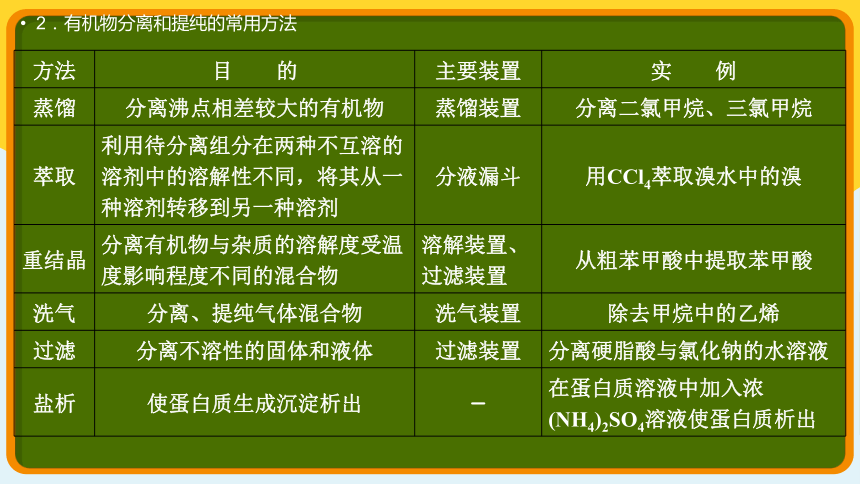
2.有机物分离和提纯的常用方法
方法 目 的 主要装置 实 例
蒸馏 分离沸点相差较大的有机物 蒸馏装置 分离二氯甲烷、三氯甲烷
萃取 利用待分离组分在两种不互溶的溶剂中的溶解性不同,将其从一种溶剂转移到另一种溶剂 分液漏斗 用CCl4萃取溴水中的溴
重结晶 分离有机物与杂质的溶解度受温度影响程度不同的混合物 溶解装置、过滤装置 从粗苯甲酸中提取苯甲酸
洗气 分离、提纯气体混合物 洗气装置 除去甲烷中的乙烯
过滤 分离不溶性的固体和液体 过滤装置 分离硬脂酸与氯化钠的水溶液
盐析 使蛋白质生成沉淀析出 — 在蛋白质溶液中加入浓(NH4)2SO4溶液使蛋白质析出
对多组分混合物的分离、提纯,一般还需要加入其他试剂,加入的试剂一般只和杂质反应(或者只和非杂质反应,而杂质却不反应),如分离硝基苯与混酸(加入NaOH溶液)、乙酸乙酯与乙酸(加入饱和Na2CO3溶液)、甲烷和乙烯(用溴水)等。
判断:下列说法正确的打“√”,不正确的打“×”。
(1)溴和戊烷可用分液漏斗分离。(×)
(2)蒸馏是分离、提纯液态有机物的常用方法。(√)
(3)重结晶的首要工作是选择适当的溶剂。(√)
(4)萃取包括液 - 液萃取和固 - 液萃取。(√)
(5)用蒸馏法分离苯和溴苯。(√)
(6)用重结晶方法提纯苯甲酸。(√)
(7)可用苯将溴从溴苯中萃取出来。(×)
实战分析
02
除去下列物质中所含少量杂质(括号内为杂质),所选用的试剂和分离方法能达到实验目的的是(D)
选项 混 合 物 试 剂 分 离 方 法
A 甲烷(乙烯) 酸性高锰酸钾溶液 洗气
B 乙醇(水) 浓硫酸 蒸馏
C 溴苯(苯) 液溴和铁粉 过滤
D 四氯化碳(碘) 氢氧化钠溶液 分液
[解析] 利用物质性质的差异性来除杂。A选项中乙烯被高锰酸钾氧化生成二氧化碳气体,引入新杂质;B选项中乙醇会被浓硫酸碳化;C选项中过量的溴会溶解在溴苯中,引入新杂质;D选项中碘能与氢氧化钠溶液反应,所以静置后出现分层现象,分液就可以得到四氯化碳,D项正确。
中医典籍《肘后备急方》所载治疗疟疾的方法“青蒿一握,以水二升渍,绞取汁,尽服之”,对屠呦呦团队研发治疗疟疾的特效药——青蒿素有巨大的启示作用。屠呦呦在对比实验中发现古法疗效低下,她设计的提取青蒿素的工艺可以简化成如下流程:
根据上述信息分析,下列判断或叙述中,肯定错误的是(C)
A.从天然植物中提取有效成分治疗疾病是药物研发的重要途径
B.将青蒿粉碎可以提高有效成分的提取率
C.青蒿素易溶于水和乙醚
D.操作1是过滤,操作2是蒸馏
[解析] 从天然植物中提取有效成分治疗疾病是药物研发的重要途径,例如中草药,故A项正确;将青蒿粉碎可以增大与萃取剂的接触面积,提高有效成分的提取率,故B项正确;青蒿素易溶于乙醚,可以用乙醚来萃取,题干中有“青蒿一握,以水二升渍,绞取汁”“古法疗效低下”,推测青蒿素不易溶于水,结合青蒿素结构中亲水基团很少,说明青蒿素不易溶于水,故C项错误;根据图中工艺,操作1是过滤,操作2是蒸馏,故D项正确。
课时2 确定实验式、分子式、分子结构
Contents
目录
知识点突破
01
实战分析
02
知识点突破
01
有机物分子式的确定方法
知识一
1.确定有机物化学式的一般步骤:
2.组成元素的判断:运用燃烧法,确定元素的种类。若生成CO2,则说明含有碳元素;若生成H2O,则说明含有氢元素。但是氧元素可能来自氧气,故无法判断。此时应定量地运用题目中交代的数据进行判断。
设有机物燃烧后CO2中碳元素的质量为m(C),H2O中氢元素的质量为m(H)。
m(有机物)>m(C)+m(H)→有机物中含有氧元素
m(有机物)=m(C)+m(H)→有机物中不含氧元素
3.分子式的确定:
(1)物质的量关系法:由密度或其他条件→求摩尔质量→求1 mol分子中所含各元素原子的物质的量→求分子式。
(2)最简式法:先利用有机物中各元素的质量分数求出有机物的最简式,再结合有机物的相对分子质量求得分子式。例如:
(3)燃烧法:若题目直接给出有机物及燃烧产物的质量,可根据有机物燃烧的化学方程式或差量法求出分子式。
有机物结构式的确定流程
知识二
判断 下列说法正确的打“√”,不正确的打“×”。
(1)从核磁共振氢谱图上可以推知有机物分子中有几种不同类型的氢原子及它们的相对数目。(√)
(2)红外光谱是用高能电子流等轰击样品分子,使分子失去电子变成分子离子或碎片离子。(×)
(3)质谱法具有快速、微量、精确的特点。(√)
(4)通过红外光谱图可以初步判断有机物所含的官能团。(√)
(5)某有机物在氧气中充分燃烧,生成的水蒸气和CO2的物质的量之比为1∶1,由此可得出结论:分子中碳、氢原子个数比为2∶1。(×)
实战分析
02
某化合物的结构式(键线式)及球棍模型如下:
[解析] 根据该物质的核磁共振氢谱图判断,H原子有8种,A项错误;该物质中不含苯环,所以不是芳香族化合物,B项错误;根据该物质的球棍模型判断Et为乙基,C项错误;根据球棍模型可知,该物质的分子式是C9H12O4,D项正确。
该有机物分子的核磁共振氢谱图如图。下列关于该有机物的叙述正确的是( )
A.该有机物不同化学环境的氢原子有6种
B.该有机物属于芳香族化合物
C.键线式中的Et代表的基团为—CH3
D.该有机物的分子式为C9H12O4
D
为测定某有机化合物A的结构,进行如下实验。
Ⅰ.分子式的测定
图1 图2
[解析] (1) 5.4 g水的物质的量为0.3 mol,8.8 g二氧化碳的物质的量为0.2 mol,消耗氧气6.72 L(标准状况),物质的量为0.3 mol,根据原子守恒,有机物A含有0.2 mol C、0.6 mol H和0.1 mol O,则C、H、O的最简整数比为2∶6∶1,实验式为C2H6O。(2) 根据质谱图,可知A的相对分子质量为46,分子式为C2H6O。(3) 根据有机化合物的成键特点,分子中不含不饱和键,可能的结构简式为CH3CH2OH、H3C—O—CH3。(4) 根据核磁共振氢谱,分子中共含有3种氢原子,则有机物A的结构简式为CH3CH2OH,含有的官能团为羟基。
THANK YOU
2025年高二化学复习
人教版 选择性必修3
第二节 研究有机化合物的一般方法
课时1 分离、提纯
Contents
目录
知识点突破
01
实战分析
02
知识点突破
01
有机物分离和提纯的常用方法
知识点
1.混合物分离、提纯的原则
(1)不能引入新杂质;(2)提纯后的物质成分不变;
(3)实验过程和操作方法简单易行;(4)节约试剂。
2.有机物分离和提纯的常用方法
方法 目 的 主要装置 实 例
蒸馏 分离沸点相差较大的有机物 蒸馏装置 分离二氯甲烷、三氯甲烷
萃取 利用待分离组分在两种不互溶的溶剂中的溶解性不同,将其从一种溶剂转移到另一种溶剂 分液漏斗 用CCl4萃取溴水中的溴
重结晶 分离有机物与杂质的溶解度受温度影响程度不同的混合物 溶解装置、过滤装置 从粗苯甲酸中提取苯甲酸
洗气 分离、提纯气体混合物 洗气装置 除去甲烷中的乙烯
过滤 分离不溶性的固体和液体 过滤装置 分离硬脂酸与氯化钠的水溶液
盐析 使蛋白质生成沉淀析出 — 在蛋白质溶液中加入浓(NH4)2SO4溶液使蛋白质析出
对多组分混合物的分离、提纯,一般还需要加入其他试剂,加入的试剂一般只和杂质反应(或者只和非杂质反应,而杂质却不反应),如分离硝基苯与混酸(加入NaOH溶液)、乙酸乙酯与乙酸(加入饱和Na2CO3溶液)、甲烷和乙烯(用溴水)等。
判断:下列说法正确的打“√”,不正确的打“×”。
(1)溴和戊烷可用分液漏斗分离。(×)
(2)蒸馏是分离、提纯液态有机物的常用方法。(√)
(3)重结晶的首要工作是选择适当的溶剂。(√)
(4)萃取包括液 - 液萃取和固 - 液萃取。(√)
(5)用蒸馏法分离苯和溴苯。(√)
(6)用重结晶方法提纯苯甲酸。(√)
(7)可用苯将溴从溴苯中萃取出来。(×)
实战分析
02
除去下列物质中所含少量杂质(括号内为杂质),所选用的试剂和分离方法能达到实验目的的是(D)
选项 混 合 物 试 剂 分 离 方 法
A 甲烷(乙烯) 酸性高锰酸钾溶液 洗气
B 乙醇(水) 浓硫酸 蒸馏
C 溴苯(苯) 液溴和铁粉 过滤
D 四氯化碳(碘) 氢氧化钠溶液 分液
[解析] 利用物质性质的差异性来除杂。A选项中乙烯被高锰酸钾氧化生成二氧化碳气体,引入新杂质;B选项中乙醇会被浓硫酸碳化;C选项中过量的溴会溶解在溴苯中,引入新杂质;D选项中碘能与氢氧化钠溶液反应,所以静置后出现分层现象,分液就可以得到四氯化碳,D项正确。
中医典籍《肘后备急方》所载治疗疟疾的方法“青蒿一握,以水二升渍,绞取汁,尽服之”,对屠呦呦团队研发治疗疟疾的特效药——青蒿素有巨大的启示作用。屠呦呦在对比实验中发现古法疗效低下,她设计的提取青蒿素的工艺可以简化成如下流程:
根据上述信息分析,下列判断或叙述中,肯定错误的是(C)
A.从天然植物中提取有效成分治疗疾病是药物研发的重要途径
B.将青蒿粉碎可以提高有效成分的提取率
C.青蒿素易溶于水和乙醚
D.操作1是过滤,操作2是蒸馏
[解析] 从天然植物中提取有效成分治疗疾病是药物研发的重要途径,例如中草药,故A项正确;将青蒿粉碎可以增大与萃取剂的接触面积,提高有效成分的提取率,故B项正确;青蒿素易溶于乙醚,可以用乙醚来萃取,题干中有“青蒿一握,以水二升渍,绞取汁”“古法疗效低下”,推测青蒿素不易溶于水,结合青蒿素结构中亲水基团很少,说明青蒿素不易溶于水,故C项错误;根据图中工艺,操作1是过滤,操作2是蒸馏,故D项正确。
课时2 确定实验式、分子式、分子结构
Contents
目录
知识点突破
01
实战分析
02
知识点突破
01
有机物分子式的确定方法
知识一
1.确定有机物化学式的一般步骤:
2.组成元素的判断:运用燃烧法,确定元素的种类。若生成CO2,则说明含有碳元素;若生成H2O,则说明含有氢元素。但是氧元素可能来自氧气,故无法判断。此时应定量地运用题目中交代的数据进行判断。
设有机物燃烧后CO2中碳元素的质量为m(C),H2O中氢元素的质量为m(H)。
m(有机物)>m(C)+m(H)→有机物中含有氧元素
m(有机物)=m(C)+m(H)→有机物中不含氧元素
3.分子式的确定:
(1)物质的量关系法:由密度或其他条件→求摩尔质量→求1 mol分子中所含各元素原子的物质的量→求分子式。
(2)最简式法:先利用有机物中各元素的质量分数求出有机物的最简式,再结合有机物的相对分子质量求得分子式。例如:
(3)燃烧法:若题目直接给出有机物及燃烧产物的质量,可根据有机物燃烧的化学方程式或差量法求出分子式。
有机物结构式的确定流程
知识二
判断 下列说法正确的打“√”,不正确的打“×”。
(1)从核磁共振氢谱图上可以推知有机物分子中有几种不同类型的氢原子及它们的相对数目。(√)
(2)红外光谱是用高能电子流等轰击样品分子,使分子失去电子变成分子离子或碎片离子。(×)
(3)质谱法具有快速、微量、精确的特点。(√)
(4)通过红外光谱图可以初步判断有机物所含的官能团。(√)
(5)某有机物在氧气中充分燃烧,生成的水蒸气和CO2的物质的量之比为1∶1,由此可得出结论:分子中碳、氢原子个数比为2∶1。(×)
实战分析
02
某化合物的结构式(键线式)及球棍模型如下:
[解析] 根据该物质的核磁共振氢谱图判断,H原子有8种,A项错误;该物质中不含苯环,所以不是芳香族化合物,B项错误;根据该物质的球棍模型判断Et为乙基,C项错误;根据球棍模型可知,该物质的分子式是C9H12O4,D项正确。
该有机物分子的核磁共振氢谱图如图。下列关于该有机物的叙述正确的是( )
A.该有机物不同化学环境的氢原子有6种
B.该有机物属于芳香族化合物
C.键线式中的Et代表的基团为—CH3
D.该有机物的分子式为C9H12O4
D
为测定某有机化合物A的结构,进行如下实验。
Ⅰ.分子式的测定
图1 图2
[解析] (1) 5.4 g水的物质的量为0.3 mol,8.8 g二氧化碳的物质的量为0.2 mol,消耗氧气6.72 L(标准状况),物质的量为0.3 mol,根据原子守恒,有机物A含有0.2 mol C、0.6 mol H和0.1 mol O,则C、H、O的最简整数比为2∶6∶1,实验式为C2H6O。(2) 根据质谱图,可知A的相对分子质量为46,分子式为C2H6O。(3) 根据有机化合物的成键特点,分子中不含不饱和键,可能的结构简式为CH3CH2OH、H3C—O—CH3。(4) 根据核磁共振氢谱,分子中共含有3种氢原子,则有机物A的结构简式为CH3CH2OH,含有的官能团为羟基。
THANK YOU
