第30讲 有机物推断与合成 学案(含答案)2026届高三化学一轮总复习
文档属性
| 名称 | 第30讲 有机物推断与合成 学案(含答案)2026届高三化学一轮总复习 |

|
|
| 格式 | doc | ||
| 文件大小 | 8.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-28 00:00:00 | ||
图片预览




文档简介
第30讲 有机物推断与合成
复习要求 1. 认识有机合成的关键是碳骨架的构建和官能团的转化。2. 能综合应用有关知识完成有机化合物推断、官能团检验、有机合成路线设计等任务。3. 能参与环境保护等与有机化合物性质应用相关的社会性议题的讨论,并做出有科学依据的判断、评价和决策。
知识体系
考点一 有机推断
一、 常见官能团性质总结
官能团(或其他基团) 常见的特征反应及其性质
烷烃基 取代反应:在光照条件下与卤素单质反应
碳碳双键、碳碳三键 (1)加成反应:使________________________________褪色 (2)氧化反应:能使______________褪色
苯环 (1)取代反应:①在FeBr3催化下与液溴反应;②在浓硫酸催化下与浓硝酸反应(2)加成反应:在一定条件下与H2反应注意:苯与溴水、酸性高锰酸钾溶液都不反应
碳卤键(卤代烃) (1)水解反应:卤代烃在NaOH水溶液中加热生成醇(2)消去反应:(部分)卤代烃与NaOH醇溶液共热生成不饱和烃
醇羟基 (1)与活泼金属(Na)反应放出H2(2)催化氧化:在铜或银催化下被氧化成醛基或酮羰基(3)与羧酸发生酯化反应生成酯
酚羟基 (1)弱酸性:能与NaOH溶液反应(2)显色反应:遇FeCl3溶液显紫色(3)取代反应:与浓溴水反应生成白色沉淀
醛基 (1)氧化反应:①与银氨溶液反应产生光亮的银镜;②与新制的Cu(OH)2共热产生砖红色沉淀(2)还原反应:与H2加成生成醇
羧基 (1)使紫色石蕊溶液变红(2)与NaHCO3溶液反应产生CO2(3)与醇羟基发生酯化反应
酯基 水解反应:①酸性条件下水解生成羧酸和醇;②碱性条件下水解生成羧酸盐和醇
酰胺基 在强酸、强碱条件下均能发生水解反应
硝基
【思维拓展】
二、 有机推断的突破口
1. 根据分子式,利用不饱和度(Ω)推断可能含有的官能团
2. 根据特征现象推断官能团
反应现象 思考方向
溴水褪色 可能含有碳碳双键、碳碳三键或酚羟基、醛基等
酸性高锰酸钾溶液褪色 可能含有碳碳双键、碳碳三键、醛基、酚羟基或有机物为苯的同系物等
遇氯化铁溶液显紫色 含有酚羟基
生成银镜或砖红色沉淀 含有醛基或甲酸酯基
与钠反应产生H2 可能含有羟基或羧基
加入碳酸氢钠溶液产生CO2 含有羧基
加入浓溴水产生白色沉淀 含有酚羟基
3. 根据反应条件推断有机反应类型和官能团
反应条件 可能的反应
浓硫酸,△ ①醇的消去;②酯化反应;③苯环的硝化;④醇分子间脱水
NaOH/水,△ ①卤代烃的水解;②酯的水解
NaOH/醇,△ 卤代烃的消去
X2(如Cl2、Br2)/FeX3 苯环的卤代
X2(如Cl2、Br2)/光照 烷基的卤代
O3或KMnO4/H+ 氧化反应
Fe/HCl 硝基被还原为氨基
H2,催化剂、△ ①醛被还原为醇;②酮被还原为醇
LiAlH4 酯被还原为醇
4. 根据相对分子质量变化确定官能团的衍变和官能团个数
(1)RCOOHRCOOC2H5,羧酸与乙醇发生酯化反应,若含一个羧基,则产物的相对分子质量与RCOOH相比增加28,若含两个羧基,则产物的相对分子质量与RCOOH相比增加56。
(2)ROHCH3COOR,醇与乙酸发生酯化反应,若含一个羟基,则产物的相对分子质量与ROH相比增加42,若含两个羟基,则产物的相对分子质量与ROH相比增加84。
5. 根据题目给予的新信息推断陌生反应
观察新信息化学方程式的反应条件,找出题干合成线路图中相同条件,推出此转化过程发生的反应类型,同时也能确定反应物中参与反应的官能团及对应产物。
三、 典型有机物的性质及转化关系
1. 重要烃的性质及转化
2. 重要烃的衍生物之间的转化关系
【易错辨析】
1. 乙烯的聚合反应,可以使碳链减短。( )
2. 烯烃与酸性KMnO4溶液的反应,可以使碳链减短。( )
3. 卤代烃与NaCN的取代反应,可以使碳链减短。( )
4. 已知:。由苯乙烯制备有机材料中间体G的一种合成路线如图所示。X的结构简式为。( )
5. A→B过程中有一种分子式为C8H10O2的副产物生成,该副产物的结构简式为。( )
类型1 依据结构差异,推断断键位置
1. 吡贝地尔可用于治疗帕金森病,对于控制帕金森病的震颤、运动迟缓、肌张力增高有一定的作用。另外对于不宁腿综合征也有治疗效果。其部分合成路线如图:
A,
物质A的结构简式为________________。
类型2 依据特征条件,推断反应规律
2. (2024·江阴一模)化合物H是一种用于合成药物的中间体,其部分合成路线流程图如下:
已知:。H的分子式为C18H18O3,结构中含有三个六元环,其结构简式为________________。
3. (2024·南通如皋高三一模)一种药物中间体G的部分合成路线如下:
已知:RCH===CHR′RCOOH+R′COOH
转化①除物质B外,还有另一含苯环的有机产物生成。则A的结构简式为________________。
类型3 根据反应类型推断结构简式
4. (2024·宝应高三上期末)化合物G是一种重要的药物中间体,其部分人工合成路线如下:
B→C中经历BXYC的过程,写出中间体Y的结构简式:________________。
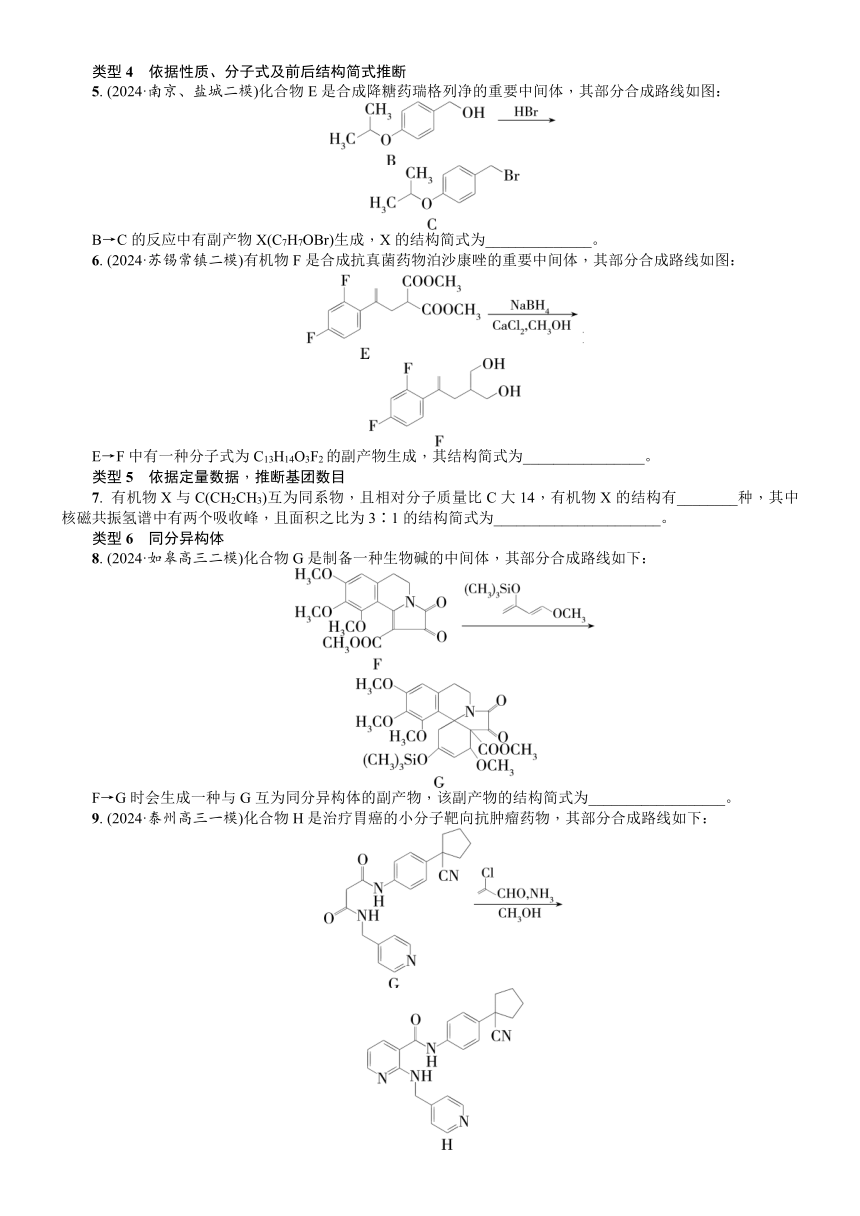
类型4 依据性质、分子式及前后结构简式推断
5. (2024·南京、盐城二模)化合物E是合成降糖药瑞格列净的重要中间体,其部分合成路线如图:
B→C的反应中有副产物X(C7H7OBr)生成,X的结构简式为______________。
6. (2024·苏锡常镇二模)有机物F是合成抗真菌药物泊沙康唑的重要中间体,其部分合成路线如图:
E→F中有一种分子式为C13H14O3F2的副产物生成,其结构简式为________________。
类型5 依据定量数据,推断基团数目
7. 有机物X与C(CH2CH3)互为同系物,且相对分子质量比C大14,有机物X的结构有________种,其中核磁共振氢谱中有两个吸收峰,且面积之比为3∶1的结构简式为______________________。
类型6 同分异构体
8. (2024·如皋高三二模)化合物G是制备一种生物碱的中间体,其部分合成路线如下:
F→G时会生成一种与G互为同分异构体的副产物,该副产物的结构简式为__________________。
9. (2024·泰州高三一模)化合物H是治疗胃癌的小分子靶向抗肿瘤药物,其部分合成路线如下:
G→H的反应中有一种与H互为同分异构体的副产物生成,其结构简式为______________________________。
考点二 有机合成路线设计
一、 有机合成的基本思路
二、 官能团的转化
1. 用衍变关系引入官能团,如:
卤代烃伯醇(R—CH2OH)醛(R—CHO)羧酸(R—COOH)
2. 通过不同反应,增加官能团的个数,如:
3. 通过不同反应,改变官能团的位置,如:
三、 有机合成中常见官能团的引入
官能团 引入方法
碳卤键(—X) ①烃、酚的取代;②不饱和烃与HX、X2(X代表卤素原子,下同)的加成;③醇与氢卤酸(HX)的取代
羟基(—OH) ①烯烃与水的加成;②醛、酮与氢气的加成;③卤代烃在碱性条件下的水解;④酯的水解;⑤葡萄糖发酵产生乙醇
①某些醇或卤代烃的消去;②炔烃不完全加成;③烷烃的裂化
①醇的催化氧化;②连在同一个碳上的两个羟基脱水;③寡糖或多糖水解可引入醛基;④含碳碳三键的物质与水的加成
羧基(—COOH) ①醛基的氧化;②酯、酰胺、肽、蛋白质、羧酸盐的水解
—CHO 含有—CH2OH结构的醇催化氧化
COO— 酯化反应
苯环上引入不同的官能团 ①卤代:X2和FeX3;②硝化:浓硝酸和浓硫酸共热;③烃基氧化;④先卤代后水解
四、 有机合成中官能团的消除
官能团 消除官能团的常用方法
—OH ①________反应;②________反应;③________反应
—X(卤素原子) ①________反应;②________反应
碳碳双键(或碳碳三键) ________反应
—CHO ①________反应;②________反应
________反应
—COOH ①与盐或碱反应;②________反应
________反应
五、 有机合成中官能团的保护和恢复
官能团 被保护的官能团性质 保护和恢复方法(举例)
碳碳双键 易与卤素单质加成,易被O2、臭氧、酸性KMnO4溶液等氧化
醇羟基 易被酸性KMnO4溶液氧化 成酯保护,再水解、酸化,重新转化为醇羟基
酚羟基 易被O2、酸性KMnO4溶液、浓硝酸等氧化
续表
醛基(或羰基) ①醛基易被氧化;②醛基(或羰基)易被还原
羧基 除了能与羟基酯化,还能与其他官能团反应 成酯保护,再水解、酸化,重新转化为羧基
氨基 易被氧化
【易错辨析】
1.可发生催化氧化反应引入羧基。( )
2. 可发生消去反应引入碳碳双键。( )
3. CH3CH2Br可发生取代反应引入羟基。( )
4. 如果以乙烯为原料,经过加成反应、取代反应可制得乙二醇。( )
5. 与CH2===CH2可发生加成反应引入环。(
)
1. 写出用乙醇为原料制备2 丁烯醛的合成路线(其他试剂任选)。
2. (2024·湖南卷)化合物H是一种具有生物活性的苯并呋喃衍生物,合成路线如下(部分条件忽略,溶剂未写出):
A B C D E F G H
依据以上流程信息,结合所学知识,设计以和Cl2CHOCH3为原料合成CHHO?COO?H的路线(HCN等无机试剂任选)。
3. (2025·天一中学模拟)酮基布洛芬片是用于治疗各种关节炎、强直性脊柱炎引起的关节肿痛以及痛经、牙痛、术后痛和癌性痛等的非处方药。其合成路线如图所示:
以乙烷和碳酸二甲酯()为原料(无机试剂任选),设计制备异丁酸的一种合成路线。
4. (2022·浙江1月选考)化合物H是一种具有多种生物活性的天然化合物。某课题组设计的合成路线如图(部分反应条件已省略):
已知:R1BrR1MgBr
+
以化合物苯乙炔()、溴苯和环氧乙烷()为原料,设计的合成路线(用流程图表示,无机试剂、有机溶剂任选)。
5. (2024·苏州高三上期末)二氢荆芥内酯(H)可用作驱虫剂,其人工合成路线如下:
写出以CH3CH===CH2和为原料制备的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程示例见本题题干)。
6. (2024·南京、盐城高三二模)F是一种治疗心脑血管疾病药物的中间体,其合成路线如下(—C6H5表示苯基):
已知:CH3COOHCH3COCl,写出以和为原料制备的合成路线(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
考点三 有机合成综合
一、 成环反应
举例 反应类型
成环烃 +2Na―→+2NaCl 取代反应
成环醚 ________反应
成环状酯 ________反应
双烯合成反应(Diels Alder反应) ; 由共轭双烯烃与烯烃或炔烃(或其衍生物)进行1,4 加成,生成环状化合物的反应称为双烯合成反应(该反应是合成六元环的常用方法)
二、 增长碳链的反应
举例 说明
醛、酮的加成反应 先加成后消去:具有α H的醛(或酮),在催化剂作用下,α H加成到羰基氧上,生成β 羟基醛(或酮),然后脱水生成α,β 不饱和醛(或酮)
续表
三、 缩短碳链的反应(烯烃或炔烃的氧化)
四、 胺的取代反应
五、 还原反应
六、 氧化反应
举例 说明
醇被氧化为醛 2RCH2OH+O2__________________ 伯醇可被催化氧化为醛
醇被氧化为酮 仲醇可被氧化为酮
氧化生成苯甲酸 苯环上含有CH结构的有机物均可被酸性KMnO4溶液氧化为苯甲酸
考点四 常考有机信息
Diels Alder反应
二、 双烯成环(或烯与炔)
三、 羟醛缩合反应
四、 烯烃的氧化反应
1. 烯烃被臭氧氧化
2. 烯烃被酸性高锰酸钾溶液氧化
五、 醛、酮与格氏试剂(RMgX)加成合成醇
六、 环氧烷的开环加成
七、 官能团的保护与恢复
有关α H的反应
举例 及时巩固
烯烃 CH3—CH===CH2+Cl2ClCH2—CH===CH2+HCl CH3CH2CH===CH2+Cl2____________________+HCl
续表
苯环侧链
羧酸 CH3COOHCH2BrCOOH
酮
酯
酮、酯
类型1 成环反应
1. (2024·苏锡常镇高三一模)以胍盐离子液体(GIL)为催化剂合成化合物G的路线如下:
(1)化合物G中sp、sp2杂化的碳原子数目之比为____________。
(2)B→D过程中还可能经历B→X→D,其中物质X与C互为同分异构体,X的结构简式为____________________________。
(3)E→F的反应过程中加入KOH溶液可以提高F的产率,其原因是___________________________________。
(4)写出同时满足下列条件的C的一种同分异构体的结构简式:________________________________________。
能发生水解反应,生成两种产物均含苯环,且两种产物中核磁共振氢谱分别为2个峰和4个峰。
(5)已知:①RCNRCOOH;②RCNRCH2NH2。
写出以CH3CHO、和CH3CN为原料制备的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
2. 天然产物F具有抗肿瘤、镇痉等生物活性,可通过以下路线合成:
(1)化合物C中含有的含氧官能团名称为____________________。
(2)E→F的反应类型为____________________。
(3)D→E中有一种副产品(分子式C14H14O3)生成,该副产品的结构简式为____________________。
(4)C的一种同分异构体同时满足以下条件,写出该同分异构体的结构简式:____________________。
a. 能与FeCl3溶液发生显色反应;
b. 碱性条件下水解生成两种产物,酸化后分子中均只有2种不同化学环境的氢。
(5)写出以和COOCH3为原料制备的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
3. (2024·连云港高三三模)洛索洛芬钠(G)是一种抗炎镇痛药物,其一种合成路线如下:
(1)B分子中碳原子的杂化方式为____________。
(2)C中所含官能团名称为________________。
(3)B→C的反应需经历B→X→C的过程。X的分子式为C10H12O3,B→X的反应类型为____________。
(4)D的一种同分异构体同时满足下列条件,写出该同分异构体的结构式:____________________。
①含有苯环。
②能水解,且一定条件下彻底完全水解后的产物都只含有两种不同化学环境的氢原子。
(5)写出以CH3CH2OH、为原料制备的合成路线流程图(涉及题干中条件任用、无机试剂任用,合成路线流程图示例见本题题干)。
4. (2024·南京、盐城高三上一模)匹唑派(G)是一种新型精神类药品,其合成路线之一如下:
已知:Boc—结构简式为。
回答下列问题:
(1)C分子中采取sp3杂化的碳原子数目是______________。
(2)D→E过程中____________(填“能”或者“不能”)用KOH替换K2CO3。
(3)E→F过程中还生成一种分子式为C3H6O3的酯类产物,该产物的结构简式为______________。
(4)C的一种同分异构体同时满足下列条件,该同分异构体的结构简式为______________________________________________________。
①分子中含有两个苯环和一个硝基;②分子中不同化学环境的氢原子个数比是1∶2∶2∶1。
已知:
写出以苯为原料制备的合成路线流程图(无机试剂和流程中的有机试剂任用,合成路线流程图示例见本题题干)。
类型2 开环反应
5. (2024·南京、盐城高三一模)索拉非尼(H)可用于肝癌的治疗,其一种合成路线如下:
(1)欲确定CH3OH中存在C—O和O—H化学键,可采取的仪器分析方法为__________(填字母)。
A. 原子发射光谱 B. 核磁共振氢谱 C. 质谱 D. 红外光谱
(2)C在酸性条件下不稳定,B→C的反应中应控制的投料比不低于__________。
(3)D的熔点比邻硝基苯酚的__________(填“高”或“低”或“无法确定”)。
(4)F的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式______________________。分子中所有碳原子轨道杂化类型相同;1 mol该物质完全水解最多消耗3 mol NaOH,水解产物之一的分子中不同化学环境的氢原子个数比为2∶1。
(5)G的分子式为C8H3ClF3NO,其结构简式为__________________________。
(6)请设计以和为原料制备的合成路线(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
类型3 增长碳链
6. (2024·苏锡常镇四市二调)化合物G是合成抗肿瘤化合物氯化两面针碱的中间体,其合成路线如下:
(1)G分子中含氧官能团的名称为____________。
(2)B→C的反应类型为____________。
(3)A的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:______________________。
①分子能发生银镜反应、水解反应,且能与FeCl3溶液发生显色反应;②分子中含有四种不同化学环境的氢原子。
(4)化合物F的分子式为C19H18O5,F的结构简式为__________________________________。
(5)已知:①卤代烃与肼在碱性条件下易生成胺和腈(R—CN);
②。
写出以为原料制备的合成路线流程图(无机试剂、有机溶剂任用,合成路线流程图示例见本题题干)。
7. (2024·苏州高三调研)有机物Ⅰ是一种药物合成的中间体,其合成路线如下:
(1)B→C的反应类型为__________。
(2)流程中设计E→F的目的是__________________________________________________________。
(3)A→B得到的产物若不经提纯,依据B到E的合成路线会生成一种与E互为同分异构体的副产物X,X的结构简式为________________。
(4)B的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:______________________。
①有手性碳原子,与FeCl3溶液发生显色反应且能使Br2的CCl4溶液褪色;
②碱性条件下水解后酸化生成两种有机产物,产物之一分子中只有两种不同化学环境的氢原子。
(5)写出以苯、甲苯、CH3CHMgBrCH3为原料制备的合成路线流程图(无机试剂和有机溶剂任用,合成路线示例见本题题干)。
类型4 缩短碳链——双键的氧化
8. (2024·泰州中学高三上期初)有机物F是一种新型大环芳酰胺的合成原料,可通过以下方法合成:
(1)A中采用sp2杂化方式的碳原子有__________个。
(2)D→E的反应类型为____________。
(3)若B直接硝化,最后主要产物的结构简式为________________________________。
(4)写出一种符合下列条件的B的同分异构体的结构简式:_________________________________________。
①能与FeCl3溶液发生显色反应;
②分子中含有2个苯环,共有3种不同化学环境的氢原子。
(5)已知:RCOOH+,写出以CH3CH2OH、CH3CH2CH2NH2和为原料制备的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
类型5 α H的取代反应
9. (2023·江苏卷)化合物I是鞘氨醇激酶抑制剂,其合成路线如下:
(1)化合物A的酸性比环己醇的__________(填“强”或“弱”或“无差别”)。
(2)B的分子式为C2H3OCl,可由乙酸与SOCl2反应合成,B的结构简式为____________。
(3)A→C中加入(C2H5)3N是为了消耗反应中产生的__________(填化学式)。
(4)写出同时满足下列条件的C的一种同分异构体的结构简式:________________________________。
碱性条件水解后酸化生成两种产物,产物之一的分子中碳原子轨道杂化类型相同且室温下不能使2%酸性KMnO4溶液褪色;加热条件下,铜催化另一产物与氧气反应,所得有机产物的核磁共振氢谱中只有1个峰。
(5)G的分子式为C8H8Br2,F→H的反应类型为______________。
(6)写出以、和CH2===CH2为原料制备的合成路线流图(须用NBS和AIBN,无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
类型6 官能团的保护和恢复
10. 汉黄芩素具有抗氧化、抗病毒等多种药理活性,其一种合成路线如下:
已知:BnBr的结构简式为。
(1)A―→B中除生成B外,该反应中所得另一有机产物的结构简式为__________________________。
(2)D―→E的反应有HI生成。PinBH的结构简式为____________________________。
(3)F―→G的反应中所用DMS易水解生成H2SO4,故合成反应须在无水环境中进行。DMS的结构简式:,其水解的化学方程式为____________________________________________。
(4)A的一种同分异构体同时满足下列条件,该同分异构体的结构简式为________________________。
①苯环上只有一个取代基,能发生银镜反应;
②能发生水解反应,且水解产物之一能与FeCl3溶液发生显色反应;
③分子中有5种不同化学环境的氢原子。
(5)写出以和BnBr为原料制备的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。
素 养 评 估
1. (2022·江苏卷)化合物G可用于药用多肽的结构修饰,其人工合成路线如下:
(1)A分子中碳原子的杂化轨道类型为__________。
(2)B→C的反应类型为__________。
(3)D的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:__________________________。
①分子中含有4种不同化学环境的氢原子;②碱性条件水解,酸化后得2种产物,其中一种含苯环且有2种含氧官能团,2种产物均能被银氨溶液氧化。
(4)F的分子式为C12H17NO2,其结构简式为____________。
(5)已知:(R和R′表示烃基或氢,R″表示烃基);
写出以和CH3MgBr为原料制备的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
2. (2025·扬州中学校考模拟预测)六羰基钼催化剂对于间位取代苯衍生物的合成至关重要,一种化合物H的合成路线如下:
(1)有机物G中的官能团名称为______________。
(2)有机物F的分子式为C10H10,则其结构简式为______________。
(3)D和乙二醇(HOCH2CH2OH)以物质的量之比为2∶1完全酯化的产物有多种同分异构体,其中一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:______________________________________。
①分子中含有3种不同化学环境的氢原子;
②能发生银镜反应;
③能发生水解反应,且1 mol该分子水解时消耗4 mol NaOH。
(4)D→E的过程为先发生加成反应,再发生消去反应,其反应机理如下:
试描述“加成反应”的历程:________________________________________________________________。
________________________________________________________________________
(5)写出以苯乙烯、苯甲酸、为原料制备的合成路线流程图(无机试剂和有机溶剂任用,合成路线示例见本题题干)。
3. (2025·靖江市统考模拟)呫吨酮衍生物是治疗糖尿病的有效药,某呫吨酮衍生物的合成路线如下。
A(C9H10O4)B C D E F eq \o(――→,\s\up7())G
已知:Ⅰ. PhOH+PhCH2ClPhOCH2PhPhOH
Ⅱ. Ph—为苯基:
(1)B→C的反应类型为__________。
(2)A→B过程的目的是______________。
(3)F中sp2杂化的碳原子数为________。
(4)G的一种同系物(比其相对分子质量大14)的同分异构体同时满足下列条件,写出该同分异构体的结构简式:__________________________。
①能发生银镜反应,能使FeCl3溶液显色;
②酸性条件下,水解产物只有两种,且含两个苯环的产物中存在三种不同化学环境的氢。
(5)写出以、为原料制备的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
4. (2025·江苏各地模拟优选)化合物F是合成某种祛痰止咳药的重要中间体,其合成路线如下:
(1)A中与苯环相连的官能团名称为____________。
(2)D→E的过程中,涉及的反应类型:加成反应、__________,实验室中常用于鉴别C、D的试剂为____________________。
(3)的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:________________________。
①分子中有一个含氮五元环;②核磁共振氢谱显示分子中有5种不同化学环境的氢原子;③红外光谱显示分子中无甲基。
(4)已知:易被氧化(R为H或烃基)。设计以和为原料制备的合成路线流程图(无机试剂和有机溶剂任用,合成路线示例见本题题干)。
第30讲 有机物推断与合成
考点一 有机推断
一、 溴水或溴的四氯化碳溶液 酸性KMnO4溶液
【易错辨析】
1. × 2. √ 3. × 4. √ 5. √
命题突破
1. OHCl
解析:由B的结构简式,可推出A的结构简式为:OHCl。
2.
解析:H的分子式为C18H18O3,结构中含有三个六元环,其结构简式为。
3.
解析:根据B的结构可知B中有8个C原子,则反应①的另一种含有苯环的有机产物含7个C原子,且有羧基,应为苯甲酸,结合已知,可以推出A的结构简式为:。
4.
解析:由B→C反应经历可知,B还原生成,和—CHO加成生成X为,X发生消去反应生成Y为,Y发生加成得到C,故答案为。
5.
解析:根据B的结构,B与HBr反应有副产物C7H7OBr产生,可推知X的结构是。
6.
解析:E发生还原反应生成F,酯基均变为羟基,F的分子式为C12H14O2F2,副产物的分子式为C13H14O3F2,对比可知副产物中还有一个酯基并未被还原为羟基,结构简式为:。
7. 8
解析:C为CH2CH3,有机物X与C互为同系物,且相对分子质量比C大14,①当X存在和—CH2CH2CH3或—CH(CH3)2基团时有2种结构;②当X存在苯环和—CH3、—CH2CH3基团时,存在邻间对3种结构;③当X存在苯环和—CH3、—CH3、—CH3基团时,有3种结构;有机物X的结构有2+3+3=8种,其中核磁共振氢谱中有两个吸收峰,且面积之比为3∶1的结构简式为H3CCH3CH3。
8.
解析:F→G本质为Diels Alder反应或双烯合成,含共轭二烯结构的含硅反应物与F五元环中的碳碳双键进行1,4 加成,生成六元环状化合物,即G,由于该含硅反应物中碳碳双键不对称,则F→G时会生成一种与G互为同分异构体的副产物,该副产物的结构简式为。
9.
解析:G→H的反应中有一种与H互为同分异构体的副产物生成,根据断键方式分析可以选择在不同的酮羰基上发生反应,其一得到H,另一得到其结构简式为。
考点二 有机合成路线设计
知识归纳
四、 消去 氧化 酯化 消去 水解 加成 还原 氧化 加成 酯化 水解
【易错辨析】
1. × 2. √ 3. √ 4. √ 5. √
命题突破
1.
解析:先把乙醇氧化为乙醛,然后2分子乙醛在氢氧化钠稀溶液中生成CH3CH—CH2CHOOH,最后CH3CH—CH2CHOOH脱水生成2 丁烯醛。
2.
3.
4.
5.
解析:以CH3CH===CH2和为原料制备,制备流程图可以为。
6.
考点三 有机合成综合
知识归纳
一、 取代 取代
三、 (酮)羰基 醛基 (酮)羰基 羧基
四、 RNHR′+HBr
六、 2RCHO+2H2O
考点四 常考有机信息
知识归纳
一、
二、
三、
四、 1.
2.
五、 CHCH3OMgCl CHCH3OH CCH3OMgClCH3CH2CH2CH3 CCH3OHCH3CH2CH2CH3 CH3CH2CHO
六、
八、
命题突破
1. (1)1∶9 (2)
(3)中和消去反应生成的HCN,降低HCN浓度促进反应正向进行
(4
(5)
解析:A与苯甲醛先在GIL下反应,产物在加热的条件下生成生成B,对比B、C、D的结构可知,B碳碳双键与NCCN加成生成C,C中碳氧双键与NCCN加成生成D,D在GIL下成环生成E,E发生消去反应生成F,同时有HCN生成,KOH中和生成的HCN,使平衡正向进行,提高F产率,F加热生成G。
(1)化合物G中sp杂化的C原子是—CN中的C,数目为2,苯环上的C均为sp2杂化,共18个,化合物G中sp、sp2杂化的碳原子数目之比为1∶9;
(2)对比B、C、D的结构可知,B碳碳双键与NCCN加成生成C,C中碳氧双键与NCCN加成生成D,B→D过程中还可能经历B→X→D,B中碳氧双键先与NCCN加成生成X,X中的碳碳双键再与NCCN加成生成D,X的结构为:;
(3)E发生消去反应生成F,同时有HCN生成,加入KOH溶液,中和生成的HCN,降低HCN浓度促进反应正向进行;
(4)C的同分异构体能发生水解反应,说明水解基团为肽键,生成两种产物均含苯环,说明结构为R1—CONH—R2,且R1和R2均含有苯环,两种产物中核磁共振氢谱分别为2个峰和4个峰,即等效氢的数目分别为2、4,符合条件的结构为:H2NNHCOCCHCH3CCH或H2NNHCOCHCCH3CHC;
(5)与CH3CHO先在GIL下反应,产物在加热的条件下生成
2. (1)(酮)羰基、酯基 (2)还原反应 (3)
(4)、
(5)
解析:A和X发生取代反应生成B,B加热后生成C,C发生氧化反应生成D,D与CH3I在NaH作用下发生反应生成E,E还原生成F。
(1)C的结构简式为,含有的含氧官能团名称为(酮)羰基、酯基;
(2)根据E和F的结构简式分析,羰基转化为羟基,反应过程中得到了H,则E→F的反应类型为还原反应;
(3)由E的结构简式知,E分子式为C15H16O3,副产物(分子式为C14H14O3)比E少1个CH2,则与E相比,生成E时有2个甲基取代了2个H,而生成副产物时只有1个甲基取代了H,故副产物的结构简式:;
(4)C的结构简式为,C的一种同分异构体同时满足:a.能与FeCl3溶液发生显色反应,则含有酚羟基;b.碱性条件下水解生成两种产物,酸化后分子中均只有2种不同化学环境的氢则高度对称,符合条件的同分异构体有OHOCCOC—C(CH3)3、;
(5)以和COOCH3为原料制备的合成路线,由与溴发生加成反应得到,在氢氧化钠的醇溶液中加热发生消去反应生成,与COOCH3反应生成,与氢气发生还原反应生成。
3. (1)sp2、sp3
(2)碳溴键、羧基 (3)加成反应
(4)
(5)
解析:(A)在1)NaOH、2)HCl作用下转化为(B),先与甲醛加成,再与HBr取代转化为(C),与甲醇在浓硫酸、加热条件下发生酯化反应生成(D),与反应生成(E),在HBr、HOAC条件下转化为(F),在一定条件下将羧基转化为羧酸钠生成(G)。
(1)B的结构简式为,分子中苯环上的碳原子和羧基上的碳原子的杂化方式均为sp2,环外饱和碳原子采取sp3杂化;
(2)C的结构简式为,其所含官能团名称为碳溴键、羧基;
(3)B→C的反应需经历B→X→C的过程,B的分子式为C9H10O2、X的分子式为C10H12O3,甲醛的分子式为CH2O,对比三者分子式,9+1=10、10+2=12、2+1=3,所以B→X的反应类型为加成反应;
(4)D的结构简式为,同时满足条件的同分异构体中含有酯基、且分子对称性高,其结构简式为或
(5)以CH3CH2OH、为原料制备
4. (1)3 (2)不能
(3)
(4)
(5)
解析:由流程图可知,A→B溴原子被氰基取代;B→C中,B与发生取代反应,生成C;C→D发生还原反应,氰基被还原为氨基;D→E中,D与发生取代反应,生成E;E→F中,“Boc—”被“H”取代,生成F;F→G中,F与发生取代反应,生成G。
(1)形成四个单键的碳原子为sp3杂化的碳原子,根据C的结构简式可知,C分子中采取sp3杂化的碳原子有3个。
(2)D分子中存在酰胺基,在KOH溶液中会发生水解,所以D→E的过程中不能用KOH替换K2CO3。
(3)由E→F可知,“Boc—”被“H”取代,Boc—结构简式为(CH3)3C—O—C—O,根据反应条件中可知,反应物中有HCl—CH3OH,又知该酯类产物的分子式为C3H6O3,所以该产物的结构简式为CH3O—C—OCH3O。
(4)C的一种同分异构体同时满足下列条件:分子中含有两个苯环和一个硝基,且分子中不同化学环境的氢原子个数比是1∶2∶2∶1,C中含有12个氢原子,则不同化学环境的氢原子个数为2、4、4、2,则两个苯环应对称,根据以上条件,可得该同分异构体的结构简式为CNO2NH2或NCH2—NO2。
(5)根据流程图可知,D→E→F可形成类似的结构,D中含有氨基,可用苯先与浓硫酸和浓硝酸反应,生成硝基苯,再用Fe和HCl还原,将硝基苯转化为苯胺,按照D→E的反应条件,让苯胺与反应,生成,再按照E→F的反应条件,使转化为,反应流程图为:NO2NH2。
5. (1)D (2)3∶1
(3)高 (4)
(5)
(6)
解析:A()与SOCl2发生反应生成B(),B()与CH3NH2在甲醇、THF条件下发生取代反应生成C();C()与D(O2NOH)在碳酸钾,DMF条件下发生取代反应生成E();E()与H2反应生成F(),F与G、CH2Cl2发生加成反应生成H(),根据原子守恒推知G为,据此分析解答。
(1)原子发射光谱是利用物质在热激发或电激发下,每种元素的原子或离子发射特征光谱来判断物质的组成,可测定元素的含量该方法,不能确定官能团的类别,A不符合题意;利用核磁共振仪记录下原子在共振下的有关信号绘制的图谱。吸收峰个数=等效氢原子种数,吸收峰面积之比=各种等效氢原子个数的最简整数比,可确定物质中氢原子的种类和数目,该方法不能确定官能团的类别,B不符合题意;质谱法中质荷比值最大的为物质的相对分子质量,不能确定官能团的类别,C不符合题意;红外光谱具有高度的特征性,利用红外光谱可确定化学基团和鉴定未知物质结构,D符合题意。故选D。
(2)B()与CH3NH2在甲醇、THF条件下发生取代反应生成C(),C在酸性条件下不稳定,B→C的反应中HCl、—COCl均与CH3NH2反应,应控制的投料比不低于3∶1;
(3)分子内氢键降低物质的熔沸点。邻硝基苯酚存在分子内氢键,使得熔点低于D(O2NOH);
(4)F()的一种同分异构体同时满足分子中所有碳原子轨道杂化类型相同;即C原子采取sp2杂化,含两个苯环;1 mol该物质完全水解最多消耗3 mol NaOH,水解产物之一的分子中不同化学环境的氢原子个数比为2∶1,含有两个—NH2处于对称位置,含有1个—OOCNH—直接连在两个苯环上,满足条件的物质结构为:;
(5)F()与G、CH2Cl2发生加成反应生成H(),根据G的分子式为C8H3ClF3NO推知G为。
(6)以和CH3CH2NH2为原料制备,对比原料和目标产物的结构要引入两个—CONH—官能团,由题目中B→C转化迁移可知应将与溴单质加成引入两个溴原子,在碱的醇溶液条件下水解生成1,3 环己二烯,该物质被酸性高锰酸钾氧化为己二酸,己二酸与SOCl2反应后的产物再与CH3NH2在甲醇、THF条件下发生取代反应生成。
6. (1)醚键、酰胺基 (2)加成反应
(3)
(4)
(5)
解析:由A和B的结构简式可知A和发生取代反应生成B,B和HCN发生加成反应生成C,C先在碱性条件下发生水解后酸化得到D,D发生还原反应生成E,E和SOCl2发生取代反应得到,由G的结构简式可知,在AlCl3的催化下发生了成环反应,结合化合物F的分子式C19H18O5,可以推知F的结构简式为,以此解答。
(1)由结构简式可知,G分子中含氧官能团的名称为醚键、酰胺基。
(2)由分析可知,B和HCN发生加成反应生成C。
(3)A的一种同分异构体同时满足条件:①分子能发生银镜反应、水解反应,且能与FeCl3溶液发生显色反应,说明其中含有苯环且苯环上连接羟基,另外其中还含有甲酸酯(—OOCH)的结构;②分子中含有四种不同化学环境的氢原子,说明该分子是对称的结构;结合A的分子式可以推知,苯环上的取代基为1个—OH、2个—CH3、1个—OOCH,且4个取代基要对称,该同分异构体的结构简式为OHH3CCOOHCH3或OHH3CCOOHCH3。
(4)由分析可知,F的结构简式为。
(5)由逆向合成法分析,可以由发生消去反应得到,由已知②的反应原理可知可由和N2H4发生还原反应得到,可由和H2O发生加成反应得到,可由O和CHOCH3发生加成再水解得到,O可由OH发生催化氧化得到,具体合成路线流程图见参考答案。
7. (1)还原反应
(2)保护酮羰基,防止F→G转化时被还原(加成)
(3)、
(4)
(5)
解析:由有机物的转化关系可知,CH3在氯化铝作用下与发生环加成反应,与锌(汞)、盐酸发生还原反应生成,与SOCl2发生取代反应生成,在氯化铝作用下发生取代反应生成H3CO,在酸性条件下,H3CO与乙二醇先发生加成反应,再发生取代反应生成,催化剂作用下,与氢气发生加成反应生成,酸性条件下转化为,先在无水乙醚作用下与CH3CH2MgBr发生取代反应,再在酸性条件下共热发生消去反应生成。
(1)由分析可知,B→C的反应为与锌(汞)、盐酸发生还原反应生成;
(2)由E、H的分子中都含有酮羰基可知,流程中设计E→F的目的是保护酮羰基,防止F→G转化时与氢气反应被还原(加成);
(3)由结构简式可知,A→B的反应中CH3在氯化铝作用下与发生环加成反应生成,则A→B得到的产物若不经提纯,依据B到E的合成路线会生成一种与E互为同分异构体的副产物CH3O;
(4)B的同分异构体有手性碳原子,与氯化铁溶液发生显色反应且能使溴的四氯化碳溶液褪色说明同分异构体分子中含有连有4个不同原子或原子团的饱和碳原子、酚羟基和碳碳双键,碱性条件下水解后酸化生成两种有机产物,产物之一分子中只有两种不同化学环境的氢原子说明同分异构体分子中含有酚酯基,则符合条件的结构简式为OOCCHCHCH3CH2OH;
(5)由题给有机物的转化关系可知,以苯、甲苯、CH3CHMgBrCH3为原料制备的合成步骤为CH3与酸性高锰酸钾溶液发生氧化反应生成COOH,COOH与SOCl2发生取代反应生成COCl,在氯化铝作用下COCl与苯发生取代反应生成,先在无水乙醚作用下与CH3CHMgBrCH3发生取代反应,再在酸性条件下共热发生消去反应生成,催化剂作用下与氢气共热发生加成反应生成。
8. (1)8 (2)取代反应
(3)
(4)
(5)
解析:由流程可知,A→B的反应为取代反应,B→C是进行取代位置的保护,如果直接硝化反应,会在硝基的间位上引入硝基,则达不到实验目的,C→D为硝化反应,在苯环的对位上引入硝基,D→E为酰胺键的水解反应,即取代反应,最后再进行硝基的还原得到最后产物。
(1)A中苯环上的碳原子和酯基上的碳原子都采用的是sp2杂化,故有8个碳原子采用sp2杂化;
(2)对比D和E的结构可知,D在酸性条件下发生水解反应得到E,反应类型为取代反应;
(3)B到C时为了在苯环的对位上引入基团,若B直接硝化,则会在B的苯环上的间位上引入硝基,则最后得到的产物会是;
(4)B的结构简式为,其同分异构体能与FeCl3溶液发生显色反应,说明有酚羟基,分子中含有2个苯环,则刚好把碳原子和不饱和度用完,说明其侧链为两个氨基和两个酚羟基,共有3种不同化学环境的氢原子,则结构为对称结构,故满足条件的同分异构体有H2NOHOHOHNH2OH或H2NOHOHOHNH2OH;
(5)CH3CH2OH、CH3CH2CH2NH2和为原料制备;上的碳原子要减少2个,则先与溴单质发生加成反应得到,再发生消去反应得到,再利用信息反应得到,再与CH3CH2OH酯化得到,最后利用流程图中A到B的反应得到目标产物。
9. (1)强 (2)CH3COCl (3)HCl (4)
(5)取代反应
(6)
解析:OH与C2H3OCl发生取代反应生成,可推知化学方程式为OH+CH3COCl―→+HCl,可知B为CH3COCl;发生水解反应得到F:,与G(C8H8Br2)发生取代反应得到,可知化学方程式为+―→+HBr,由此推知G为。
(1)化合物A:OH中含有酚羟基,酚羟基酸性强于醇羟基,故化合物A的酸性比环己醇的强。
(2)由分析可知B的结构简式为CH3COCl。
(3)A→C的化学方程式为OH+CH3COCl―→+HCl,(C2H5)3N显碱性可以与HCl发生中和反应促进OH+CH3COCl―→+HCl平衡正移,提供的产率,故A→C中加入(C2H5)3N是为了消耗反应中产生的HCl。
(4)的同分异构体碱性条件水解后酸化生成两种产物,产物之一的分子中碳原子轨道杂化类型相同且室温下不能使2%酸性KMnO4溶液褪色,说明其同分异构体为5,且该水解产物为苯甲酸;另一水解产物为丙醇,且加热条件下,铜催化该产物与氧气反应,所得有机产物的核磁共振氢谱中只有1个峰,由此确定该醇为2 丙醇,由此确定的同分异构体为。
(5)由分析可知F→H的反应为+―→+HBr,该反应为取代反应。
10. (1)CH3CH2OH (2)
(3)
(4)
(5)
解析:(1)将A、B分子中部分C原子编号为、,由此可知,该反应过程中A分子断开了3号C原子处的C—O,故所得的另一种有机产物为乙醇。
(2)由D、E的结构简式以及产物之一为HI可知,该反应为取代反应,故PinBH的结构简式为。
(3)根据DMS的结构简式以及H2SO4的结构简式(SOHOOO—H)可知,DMS水解生成H2SO4的同时可得到CH3OH。
(4)根据条件①可知,分子中含有醛基,根据条件②可知,分子中含有OCO,结合A的结构以及条件③可知,符合要求的同分异构体的结构简式为OCOCCH3CH3CHO。
(5)CH2CH2ClOH中氯原子水解可得到醇羟基,但酚羟基也可和NaOH反应,所以需要保护酚羟基,参考B→C的反应可知酚羟基和BnBr反应可得到CH2CH2ClOBn,然后与NaOH反应得到醇羟基,将醇羟基氧化成醛基,再将醛基氧化成羧基,最后根据路线可知,与H2,Pd/C反应即可得到CH2COOHOH。
素养评估
1. (1)sp2和sp3
(2)取代反应
(3)
(4)
(5)
解析:(1)A分子中,苯环上的碳原子和双键上的碳原子为sp2杂化,亚甲基上的碳原子为sp3杂化,即A分子中碳原子的杂化轨道类型为sp2和sp3。
(2)B→C的反应中,B中的羟基被氯原子代替,该反应为取代反应。
(3)D的分子式为C12H14O3,其一种同分异构体在碱性条件水解,酸化后得2种产物,其中一种含苯环且有2种含氧官能团,2种产物均能被银氨溶液氧化,说明该同分异构体为酯,且水解产物都含有醛基,则水解产物中,有一种是甲酸,另外一种含有羟基和醛基,该同分异构体属于甲酸酯;同时,该同分异构体分子中含有4种不同化学环境的氢原子,则该同分异构体的结构简式为。
(4)E经过还原反应转化为F,F再转化为G,其中G和F的分子式都是C12H17NO2,则F的结构简式为,F和G互为手性异构体。
(5)根据已知的第一个反应可知,与CH3MgBr反应生成,再被氧化为,根据已知的第二个反应可知,可以转化为,根据流程图中D→E的反应可知,和NH2OH反应生成。
2. (1)羰基、碳碳三键
(2)
(3)(或)
(4)4 甲基苯甲酸中的羰基O(δ-)原子进攻SOCl2中的S(δ+)原子,一根S—Cl键断裂,Cl得到共用电子对离去,随后Cl-进攻C原子,发生加成反应
(5)
解析:A和溴发生取代反应在苯环上引入溴原子得到B,B和镁反应生成C,C和二氧化碳反应后水解引入羧基得到D,D发生取代反应引入氯原子得到E,E和F生成G,F的分子式为C10H10,结合G结构可知,F为;G再转化为H。
(3)D中含有羧基,和乙二醇(HOCH2CH2OH)以物质的量之比为2∶1完全酯化的产物为COOCH2CH2OOC;其同分异构体同时满足下列条件:①分子中含有3种不同化学环境的氢原子,则结构对称;②能发生银镜反应,含有醛基或甲酸酯基;③能发生水解反应,且1 mol该分子水解时消耗4 mol NaOH,则含有2个甲酸酯基,且水解后生成酚羟基,故可以为或。
(5)苯乙烯和溴加成引入溴原子,再发生消去反应得到苯乙炔;苯甲酸和SOCl2发生D生成E的反应引入氯原子,再和苯乙炔发生E生成G的反应得到,再和发生G生成H的反应生成目标产物。
3. (1)取代反应
(2)保护羟基,防止其被氧化
(3)7
或
解析:(1)浓硝酸和浓硫酸的混合物在加热条件下发生取代反应。
(2)由已知Ⅰ的反应,可知A→B是酚羟基上的氢被取代,而D→E又变回酚羟基,则该反应的目的为保护羟基,防止其被氧化。
(3)苯环中的碳原子以及羧基中的碳原子,共有7个sp2杂化的碳原子。
(4)能发生银镜反应需要醛基,能使FeCl3溶液显色需要酚羟基,且含两个苯环的产物中存在三种化学环境的氢,该同分异构体为或HCOOOHOHOOCH。
4. (1)氨基、酯基
(2)消去反应 银氨溶液[或新制Cu(OH)2]
(3)
(4)
解析:(1)A中与苯环相连的官能团名称为氨基、酯基;
(2)D→E的过程中先发生加成反应生成,再发生消去反应生成,涉及的反应类型有:加成反应、消去反应;C不含醛基、D含有醛基,醛基能发生银镜反应,实验室中常用于鉴别C、D的试剂为银氨溶液。
(3)①分子中有一个含氮五元环;②核磁共振氢谱显示分子中有5种不同化学环境的氢原子,说明结构对称;③红外光谱显示分子中无甲基。符合条件的HONH2的同分异构体的结构简式为;
(4)由于NH2易被氧化,所以先用高锰酸钾把NO2CH3氧化为NO2COOH,NO2COOH再还原为NH2COOH,正丁醛和NH2COOH反应生成,和氢气发生加成反应生成。
复习要求 1. 认识有机合成的关键是碳骨架的构建和官能团的转化。2. 能综合应用有关知识完成有机化合物推断、官能团检验、有机合成路线设计等任务。3. 能参与环境保护等与有机化合物性质应用相关的社会性议题的讨论,并做出有科学依据的判断、评价和决策。
知识体系
考点一 有机推断
一、 常见官能团性质总结
官能团(或其他基团) 常见的特征反应及其性质
烷烃基 取代反应:在光照条件下与卤素单质反应
碳碳双键、碳碳三键 (1)加成反应:使________________________________褪色 (2)氧化反应:能使______________褪色
苯环 (1)取代反应:①在FeBr3催化下与液溴反应;②在浓硫酸催化下与浓硝酸反应(2)加成反应:在一定条件下与H2反应注意:苯与溴水、酸性高锰酸钾溶液都不反应
碳卤键(卤代烃) (1)水解反应:卤代烃在NaOH水溶液中加热生成醇(2)消去反应:(部分)卤代烃与NaOH醇溶液共热生成不饱和烃
醇羟基 (1)与活泼金属(Na)反应放出H2(2)催化氧化:在铜或银催化下被氧化成醛基或酮羰基(3)与羧酸发生酯化反应生成酯
酚羟基 (1)弱酸性:能与NaOH溶液反应(2)显色反应:遇FeCl3溶液显紫色(3)取代反应:与浓溴水反应生成白色沉淀
醛基 (1)氧化反应:①与银氨溶液反应产生光亮的银镜;②与新制的Cu(OH)2共热产生砖红色沉淀(2)还原反应:与H2加成生成醇
羧基 (1)使紫色石蕊溶液变红(2)与NaHCO3溶液反应产生CO2(3)与醇羟基发生酯化反应
酯基 水解反应:①酸性条件下水解生成羧酸和醇;②碱性条件下水解生成羧酸盐和醇
酰胺基 在强酸、强碱条件下均能发生水解反应
硝基
【思维拓展】
二、 有机推断的突破口
1. 根据分子式,利用不饱和度(Ω)推断可能含有的官能团
2. 根据特征现象推断官能团
反应现象 思考方向
溴水褪色 可能含有碳碳双键、碳碳三键或酚羟基、醛基等
酸性高锰酸钾溶液褪色 可能含有碳碳双键、碳碳三键、醛基、酚羟基或有机物为苯的同系物等
遇氯化铁溶液显紫色 含有酚羟基
生成银镜或砖红色沉淀 含有醛基或甲酸酯基
与钠反应产生H2 可能含有羟基或羧基
加入碳酸氢钠溶液产生CO2 含有羧基
加入浓溴水产生白色沉淀 含有酚羟基
3. 根据反应条件推断有机反应类型和官能团
反应条件 可能的反应
浓硫酸,△ ①醇的消去;②酯化反应;③苯环的硝化;④醇分子间脱水
NaOH/水,△ ①卤代烃的水解;②酯的水解
NaOH/醇,△ 卤代烃的消去
X2(如Cl2、Br2)/FeX3 苯环的卤代
X2(如Cl2、Br2)/光照 烷基的卤代
O3或KMnO4/H+ 氧化反应
Fe/HCl 硝基被还原为氨基
H2,催化剂、△ ①醛被还原为醇;②酮被还原为醇
LiAlH4 酯被还原为醇
4. 根据相对分子质量变化确定官能团的衍变和官能团个数
(1)RCOOHRCOOC2H5,羧酸与乙醇发生酯化反应,若含一个羧基,则产物的相对分子质量与RCOOH相比增加28,若含两个羧基,则产物的相对分子质量与RCOOH相比增加56。
(2)ROHCH3COOR,醇与乙酸发生酯化反应,若含一个羟基,则产物的相对分子质量与ROH相比增加42,若含两个羟基,则产物的相对分子质量与ROH相比增加84。
5. 根据题目给予的新信息推断陌生反应
观察新信息化学方程式的反应条件,找出题干合成线路图中相同条件,推出此转化过程发生的反应类型,同时也能确定反应物中参与反应的官能团及对应产物。
三、 典型有机物的性质及转化关系
1. 重要烃的性质及转化
2. 重要烃的衍生物之间的转化关系
【易错辨析】
1. 乙烯的聚合反应,可以使碳链减短。( )
2. 烯烃与酸性KMnO4溶液的反应,可以使碳链减短。( )
3. 卤代烃与NaCN的取代反应,可以使碳链减短。( )
4. 已知:。由苯乙烯制备有机材料中间体G的一种合成路线如图所示。X的结构简式为。( )
5. A→B过程中有一种分子式为C8H10O2的副产物生成,该副产物的结构简式为。( )
类型1 依据结构差异,推断断键位置
1. 吡贝地尔可用于治疗帕金森病,对于控制帕金森病的震颤、运动迟缓、肌张力增高有一定的作用。另外对于不宁腿综合征也有治疗效果。其部分合成路线如图:
A,
物质A的结构简式为________________。
类型2 依据特征条件,推断反应规律
2. (2024·江阴一模)化合物H是一种用于合成药物的中间体,其部分合成路线流程图如下:
已知:。H的分子式为C18H18O3,结构中含有三个六元环,其结构简式为________________。
3. (2024·南通如皋高三一模)一种药物中间体G的部分合成路线如下:
已知:RCH===CHR′RCOOH+R′COOH
转化①除物质B外,还有另一含苯环的有机产物生成。则A的结构简式为________________。
类型3 根据反应类型推断结构简式
4. (2024·宝应高三上期末)化合物G是一种重要的药物中间体,其部分人工合成路线如下:
B→C中经历BXYC的过程,写出中间体Y的结构简式:________________。
类型4 依据性质、分子式及前后结构简式推断
5. (2024·南京、盐城二模)化合物E是合成降糖药瑞格列净的重要中间体,其部分合成路线如图:
B→C的反应中有副产物X(C7H7OBr)生成,X的结构简式为______________。
6. (2024·苏锡常镇二模)有机物F是合成抗真菌药物泊沙康唑的重要中间体,其部分合成路线如图:
E→F中有一种分子式为C13H14O3F2的副产物生成,其结构简式为________________。
类型5 依据定量数据,推断基团数目
7. 有机物X与C(CH2CH3)互为同系物,且相对分子质量比C大14,有机物X的结构有________种,其中核磁共振氢谱中有两个吸收峰,且面积之比为3∶1的结构简式为______________________。
类型6 同分异构体
8. (2024·如皋高三二模)化合物G是制备一种生物碱的中间体,其部分合成路线如下:
F→G时会生成一种与G互为同分异构体的副产物,该副产物的结构简式为__________________。
9. (2024·泰州高三一模)化合物H是治疗胃癌的小分子靶向抗肿瘤药物,其部分合成路线如下:
G→H的反应中有一种与H互为同分异构体的副产物生成,其结构简式为______________________________。
考点二 有机合成路线设计
一、 有机合成的基本思路
二、 官能团的转化
1. 用衍变关系引入官能团,如:
卤代烃伯醇(R—CH2OH)醛(R—CHO)羧酸(R—COOH)
2. 通过不同反应,增加官能团的个数,如:
3. 通过不同反应,改变官能团的位置,如:
三、 有机合成中常见官能团的引入
官能团 引入方法
碳卤键(—X) ①烃、酚的取代;②不饱和烃与HX、X2(X代表卤素原子,下同)的加成;③醇与氢卤酸(HX)的取代
羟基(—OH) ①烯烃与水的加成;②醛、酮与氢气的加成;③卤代烃在碱性条件下的水解;④酯的水解;⑤葡萄糖发酵产生乙醇
①某些醇或卤代烃的消去;②炔烃不完全加成;③烷烃的裂化
①醇的催化氧化;②连在同一个碳上的两个羟基脱水;③寡糖或多糖水解可引入醛基;④含碳碳三键的物质与水的加成
羧基(—COOH) ①醛基的氧化;②酯、酰胺、肽、蛋白质、羧酸盐的水解
—CHO 含有—CH2OH结构的醇催化氧化
COO— 酯化反应
苯环上引入不同的官能团 ①卤代:X2和FeX3;②硝化:浓硝酸和浓硫酸共热;③烃基氧化;④先卤代后水解
四、 有机合成中官能团的消除
官能团 消除官能团的常用方法
—OH ①________反应;②________反应;③________反应
—X(卤素原子) ①________反应;②________反应
碳碳双键(或碳碳三键) ________反应
—CHO ①________反应;②________反应
________反应
—COOH ①与盐或碱反应;②________反应
________反应
五、 有机合成中官能团的保护和恢复
官能团 被保护的官能团性质 保护和恢复方法(举例)
碳碳双键 易与卤素单质加成,易被O2、臭氧、酸性KMnO4溶液等氧化
醇羟基 易被酸性KMnO4溶液氧化 成酯保护,再水解、酸化,重新转化为醇羟基
酚羟基 易被O2、酸性KMnO4溶液、浓硝酸等氧化
续表
醛基(或羰基) ①醛基易被氧化;②醛基(或羰基)易被还原
羧基 除了能与羟基酯化,还能与其他官能团反应 成酯保护,再水解、酸化,重新转化为羧基
氨基 易被氧化
【易错辨析】
1.可发生催化氧化反应引入羧基。( )
2. 可发生消去反应引入碳碳双键。( )
3. CH3CH2Br可发生取代反应引入羟基。( )
4. 如果以乙烯为原料,经过加成反应、取代反应可制得乙二醇。( )
5. 与CH2===CH2可发生加成反应引入环。(
)
1. 写出用乙醇为原料制备2 丁烯醛的合成路线(其他试剂任选)。
2. (2024·湖南卷)化合物H是一种具有生物活性的苯并呋喃衍生物,合成路线如下(部分条件忽略,溶剂未写出):
A B C D E F G H
依据以上流程信息,结合所学知识,设计以和Cl2CHOCH3为原料合成CHHO?COO?H的路线(HCN等无机试剂任选)。
3. (2025·天一中学模拟)酮基布洛芬片是用于治疗各种关节炎、强直性脊柱炎引起的关节肿痛以及痛经、牙痛、术后痛和癌性痛等的非处方药。其合成路线如图所示:
以乙烷和碳酸二甲酯()为原料(无机试剂任选),设计制备异丁酸的一种合成路线。
4. (2022·浙江1月选考)化合物H是一种具有多种生物活性的天然化合物。某课题组设计的合成路线如图(部分反应条件已省略):
已知:R1BrR1MgBr
+
以化合物苯乙炔()、溴苯和环氧乙烷()为原料,设计的合成路线(用流程图表示,无机试剂、有机溶剂任选)。
5. (2024·苏州高三上期末)二氢荆芥内酯(H)可用作驱虫剂,其人工合成路线如下:
写出以CH3CH===CH2和为原料制备的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程示例见本题题干)。
6. (2024·南京、盐城高三二模)F是一种治疗心脑血管疾病药物的中间体,其合成路线如下(—C6H5表示苯基):
已知:CH3COOHCH3COCl,写出以和为原料制备的合成路线(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
考点三 有机合成综合
一、 成环反应
举例 反应类型
成环烃 +2Na―→+2NaCl 取代反应
成环醚 ________反应
成环状酯 ________反应
双烯合成反应(Diels Alder反应) ; 由共轭双烯烃与烯烃或炔烃(或其衍生物)进行1,4 加成,生成环状化合物的反应称为双烯合成反应(该反应是合成六元环的常用方法)
二、 增长碳链的反应
举例 说明
醛、酮的加成反应 先加成后消去:具有α H的醛(或酮),在催化剂作用下,α H加成到羰基氧上,生成β 羟基醛(或酮),然后脱水生成α,β 不饱和醛(或酮)
续表
三、 缩短碳链的反应(烯烃或炔烃的氧化)
四、 胺的取代反应
五、 还原反应
六、 氧化反应
举例 说明
醇被氧化为醛 2RCH2OH+O2__________________ 伯醇可被催化氧化为醛
醇被氧化为酮 仲醇可被氧化为酮
氧化生成苯甲酸 苯环上含有CH结构的有机物均可被酸性KMnO4溶液氧化为苯甲酸
考点四 常考有机信息
Diels Alder反应
二、 双烯成环(或烯与炔)
三、 羟醛缩合反应
四、 烯烃的氧化反应
1. 烯烃被臭氧氧化
2. 烯烃被酸性高锰酸钾溶液氧化
五、 醛、酮与格氏试剂(RMgX)加成合成醇
六、 环氧烷的开环加成
七、 官能团的保护与恢复
有关α H的反应
举例 及时巩固
烯烃 CH3—CH===CH2+Cl2ClCH2—CH===CH2+HCl CH3CH2CH===CH2+Cl2____________________+HCl
续表
苯环侧链
羧酸 CH3COOHCH2BrCOOH
酮
酯
酮、酯
类型1 成环反应
1. (2024·苏锡常镇高三一模)以胍盐离子液体(GIL)为催化剂合成化合物G的路线如下:
(1)化合物G中sp、sp2杂化的碳原子数目之比为____________。
(2)B→D过程中还可能经历B→X→D,其中物质X与C互为同分异构体,X的结构简式为____________________________。
(3)E→F的反应过程中加入KOH溶液可以提高F的产率,其原因是___________________________________。
(4)写出同时满足下列条件的C的一种同分异构体的结构简式:________________________________________。
能发生水解反应,生成两种产物均含苯环,且两种产物中核磁共振氢谱分别为2个峰和4个峰。
(5)已知:①RCNRCOOH;②RCNRCH2NH2。
写出以CH3CHO、和CH3CN为原料制备的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
2. 天然产物F具有抗肿瘤、镇痉等生物活性,可通过以下路线合成:
(1)化合物C中含有的含氧官能团名称为____________________。
(2)E→F的反应类型为____________________。
(3)D→E中有一种副产品(分子式C14H14O3)生成,该副产品的结构简式为____________________。
(4)C的一种同分异构体同时满足以下条件,写出该同分异构体的结构简式:____________________。
a. 能与FeCl3溶液发生显色反应;
b. 碱性条件下水解生成两种产物,酸化后分子中均只有2种不同化学环境的氢。
(5)写出以和COOCH3为原料制备的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
3. (2024·连云港高三三模)洛索洛芬钠(G)是一种抗炎镇痛药物,其一种合成路线如下:
(1)B分子中碳原子的杂化方式为____________。
(2)C中所含官能团名称为________________。
(3)B→C的反应需经历B→X→C的过程。X的分子式为C10H12O3,B→X的反应类型为____________。
(4)D的一种同分异构体同时满足下列条件,写出该同分异构体的结构式:____________________。
①含有苯环。
②能水解,且一定条件下彻底完全水解后的产物都只含有两种不同化学环境的氢原子。
(5)写出以CH3CH2OH、为原料制备的合成路线流程图(涉及题干中条件任用、无机试剂任用,合成路线流程图示例见本题题干)。
4. (2024·南京、盐城高三上一模)匹唑派(G)是一种新型精神类药品,其合成路线之一如下:
已知:Boc—结构简式为。
回答下列问题:
(1)C分子中采取sp3杂化的碳原子数目是______________。
(2)D→E过程中____________(填“能”或者“不能”)用KOH替换K2CO3。
(3)E→F过程中还生成一种分子式为C3H6O3的酯类产物,该产物的结构简式为______________。
(4)C的一种同分异构体同时满足下列条件,该同分异构体的结构简式为______________________________________________________。
①分子中含有两个苯环和一个硝基;②分子中不同化学环境的氢原子个数比是1∶2∶2∶1。
已知:
写出以苯为原料制备的合成路线流程图(无机试剂和流程中的有机试剂任用,合成路线流程图示例见本题题干)。
类型2 开环反应
5. (2024·南京、盐城高三一模)索拉非尼(H)可用于肝癌的治疗,其一种合成路线如下:
(1)欲确定CH3OH中存在C—O和O—H化学键,可采取的仪器分析方法为__________(填字母)。
A. 原子发射光谱 B. 核磁共振氢谱 C. 质谱 D. 红外光谱
(2)C在酸性条件下不稳定,B→C的反应中应控制的投料比不低于__________。
(3)D的熔点比邻硝基苯酚的__________(填“高”或“低”或“无法确定”)。
(4)F的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式______________________。分子中所有碳原子轨道杂化类型相同;1 mol该物质完全水解最多消耗3 mol NaOH,水解产物之一的分子中不同化学环境的氢原子个数比为2∶1。
(5)G的分子式为C8H3ClF3NO,其结构简式为__________________________。
(6)请设计以和为原料制备的合成路线(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
类型3 增长碳链
6. (2024·苏锡常镇四市二调)化合物G是合成抗肿瘤化合物氯化两面针碱的中间体,其合成路线如下:
(1)G分子中含氧官能团的名称为____________。
(2)B→C的反应类型为____________。
(3)A的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:______________________。
①分子能发生银镜反应、水解反应,且能与FeCl3溶液发生显色反应;②分子中含有四种不同化学环境的氢原子。
(4)化合物F的分子式为C19H18O5,F的结构简式为__________________________________。
(5)已知:①卤代烃与肼在碱性条件下易生成胺和腈(R—CN);
②。
写出以为原料制备的合成路线流程图(无机试剂、有机溶剂任用,合成路线流程图示例见本题题干)。
7. (2024·苏州高三调研)有机物Ⅰ是一种药物合成的中间体,其合成路线如下:
(1)B→C的反应类型为__________。
(2)流程中设计E→F的目的是__________________________________________________________。
(3)A→B得到的产物若不经提纯,依据B到E的合成路线会生成一种与E互为同分异构体的副产物X,X的结构简式为________________。
(4)B的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:______________________。
①有手性碳原子,与FeCl3溶液发生显色反应且能使Br2的CCl4溶液褪色;
②碱性条件下水解后酸化生成两种有机产物,产物之一分子中只有两种不同化学环境的氢原子。
(5)写出以苯、甲苯、CH3CHMgBrCH3为原料制备的合成路线流程图(无机试剂和有机溶剂任用,合成路线示例见本题题干)。
类型4 缩短碳链——双键的氧化
8. (2024·泰州中学高三上期初)有机物F是一种新型大环芳酰胺的合成原料,可通过以下方法合成:
(1)A中采用sp2杂化方式的碳原子有__________个。
(2)D→E的反应类型为____________。
(3)若B直接硝化,最后主要产物的结构简式为________________________________。
(4)写出一种符合下列条件的B的同分异构体的结构简式:_________________________________________。
①能与FeCl3溶液发生显色反应;
②分子中含有2个苯环,共有3种不同化学环境的氢原子。
(5)已知:RCOOH+,写出以CH3CH2OH、CH3CH2CH2NH2和为原料制备的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
类型5 α H的取代反应
9. (2023·江苏卷)化合物I是鞘氨醇激酶抑制剂,其合成路线如下:
(1)化合物A的酸性比环己醇的__________(填“强”或“弱”或“无差别”)。
(2)B的分子式为C2H3OCl,可由乙酸与SOCl2反应合成,B的结构简式为____________。
(3)A→C中加入(C2H5)3N是为了消耗反应中产生的__________(填化学式)。
(4)写出同时满足下列条件的C的一种同分异构体的结构简式:________________________________。
碱性条件水解后酸化生成两种产物,产物之一的分子中碳原子轨道杂化类型相同且室温下不能使2%酸性KMnO4溶液褪色;加热条件下,铜催化另一产物与氧气反应,所得有机产物的核磁共振氢谱中只有1个峰。
(5)G的分子式为C8H8Br2,F→H的反应类型为______________。
(6)写出以、和CH2===CH2为原料制备的合成路线流图(须用NBS和AIBN,无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
类型6 官能团的保护和恢复
10. 汉黄芩素具有抗氧化、抗病毒等多种药理活性,其一种合成路线如下:
已知:BnBr的结构简式为。
(1)A―→B中除生成B外,该反应中所得另一有机产物的结构简式为__________________________。
(2)D―→E的反应有HI生成。PinBH的结构简式为____________________________。
(3)F―→G的反应中所用DMS易水解生成H2SO4,故合成反应须在无水环境中进行。DMS的结构简式:,其水解的化学方程式为____________________________________________。
(4)A的一种同分异构体同时满足下列条件,该同分异构体的结构简式为________________________。
①苯环上只有一个取代基,能发生银镜反应;
②能发生水解反应,且水解产物之一能与FeCl3溶液发生显色反应;
③分子中有5种不同化学环境的氢原子。
(5)写出以和BnBr为原料制备的合成路线流程图(无机试剂任用,合成路线流程图示例见本题题干)。
素 养 评 估
1. (2022·江苏卷)化合物G可用于药用多肽的结构修饰,其人工合成路线如下:
(1)A分子中碳原子的杂化轨道类型为__________。
(2)B→C的反应类型为__________。
(3)D的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:__________________________。
①分子中含有4种不同化学环境的氢原子;②碱性条件水解,酸化后得2种产物,其中一种含苯环且有2种含氧官能团,2种产物均能被银氨溶液氧化。
(4)F的分子式为C12H17NO2,其结构简式为____________。
(5)已知:(R和R′表示烃基或氢,R″表示烃基);
写出以和CH3MgBr为原料制备的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
2. (2025·扬州中学校考模拟预测)六羰基钼催化剂对于间位取代苯衍生物的合成至关重要,一种化合物H的合成路线如下:
(1)有机物G中的官能团名称为______________。
(2)有机物F的分子式为C10H10,则其结构简式为______________。
(3)D和乙二醇(HOCH2CH2OH)以物质的量之比为2∶1完全酯化的产物有多种同分异构体,其中一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:______________________________________。
①分子中含有3种不同化学环境的氢原子;
②能发生银镜反应;
③能发生水解反应,且1 mol该分子水解时消耗4 mol NaOH。
(4)D→E的过程为先发生加成反应,再发生消去反应,其反应机理如下:
试描述“加成反应”的历程:________________________________________________________________。
________________________________________________________________________
(5)写出以苯乙烯、苯甲酸、为原料制备的合成路线流程图(无机试剂和有机溶剂任用,合成路线示例见本题题干)。
3. (2025·靖江市统考模拟)呫吨酮衍生物是治疗糖尿病的有效药,某呫吨酮衍生物的合成路线如下。
A(C9H10O4)B C D E F eq \o(――→,\s\up7())G
已知:Ⅰ. PhOH+PhCH2ClPhOCH2PhPhOH
Ⅱ. Ph—为苯基:
(1)B→C的反应类型为__________。
(2)A→B过程的目的是______________。
(3)F中sp2杂化的碳原子数为________。
(4)G的一种同系物(比其相对分子质量大14)的同分异构体同时满足下列条件,写出该同分异构体的结构简式:__________________________。
①能发生银镜反应,能使FeCl3溶液显色;
②酸性条件下,水解产物只有两种,且含两个苯环的产物中存在三种不同化学环境的氢。
(5)写出以、为原料制备的合成路线流程图(无机试剂和有机溶剂任用,合成路线流程图示例见本题题干)。
4. (2025·江苏各地模拟优选)化合物F是合成某种祛痰止咳药的重要中间体,其合成路线如下:
(1)A中与苯环相连的官能团名称为____________。
(2)D→E的过程中,涉及的反应类型:加成反应、__________,实验室中常用于鉴别C、D的试剂为____________________。
(3)的一种同分异构体同时满足下列条件,写出该同分异构体的结构简式:________________________。
①分子中有一个含氮五元环;②核磁共振氢谱显示分子中有5种不同化学环境的氢原子;③红外光谱显示分子中无甲基。
(4)已知:易被氧化(R为H或烃基)。设计以和为原料制备的合成路线流程图(无机试剂和有机溶剂任用,合成路线示例见本题题干)。
第30讲 有机物推断与合成
考点一 有机推断
一、 溴水或溴的四氯化碳溶液 酸性KMnO4溶液
【易错辨析】
1. × 2. √ 3. × 4. √ 5. √
命题突破
1. OHCl
解析:由B的结构简式,可推出A的结构简式为:OHCl。
2.
解析:H的分子式为C18H18O3,结构中含有三个六元环,其结构简式为。
3.
解析:根据B的结构可知B中有8个C原子,则反应①的另一种含有苯环的有机产物含7个C原子,且有羧基,应为苯甲酸,结合已知,可以推出A的结构简式为:。
4.
解析:由B→C反应经历可知,B还原生成,和—CHO加成生成X为,X发生消去反应生成Y为,Y发生加成得到C,故答案为。
5.
解析:根据B的结构,B与HBr反应有副产物C7H7OBr产生,可推知X的结构是。
6.
解析:E发生还原反应生成F,酯基均变为羟基,F的分子式为C12H14O2F2,副产物的分子式为C13H14O3F2,对比可知副产物中还有一个酯基并未被还原为羟基,结构简式为:。
7. 8
解析:C为CH2CH3,有机物X与C互为同系物,且相对分子质量比C大14,①当X存在和—CH2CH2CH3或—CH(CH3)2基团时有2种结构;②当X存在苯环和—CH3、—CH2CH3基团时,存在邻间对3种结构;③当X存在苯环和—CH3、—CH3、—CH3基团时,有3种结构;有机物X的结构有2+3+3=8种,其中核磁共振氢谱中有两个吸收峰,且面积之比为3∶1的结构简式为H3CCH3CH3。
8.
解析:F→G本质为Diels Alder反应或双烯合成,含共轭二烯结构的含硅反应物与F五元环中的碳碳双键进行1,4 加成,生成六元环状化合物,即G,由于该含硅反应物中碳碳双键不对称,则F→G时会生成一种与G互为同分异构体的副产物,该副产物的结构简式为。
9.
解析:G→H的反应中有一种与H互为同分异构体的副产物生成,根据断键方式分析可以选择在不同的酮羰基上发生反应,其一得到H,另一得到其结构简式为。
考点二 有机合成路线设计
知识归纳
四、 消去 氧化 酯化 消去 水解 加成 还原 氧化 加成 酯化 水解
【易错辨析】
1. × 2. √ 3. √ 4. √ 5. √
命题突破
1.
解析:先把乙醇氧化为乙醛,然后2分子乙醛在氢氧化钠稀溶液中生成CH3CH—CH2CHOOH,最后CH3CH—CH2CHOOH脱水生成2 丁烯醛。
2.
3.
4.
5.
解析:以CH3CH===CH2和为原料制备,制备流程图可以为。
6.
考点三 有机合成综合
知识归纳
一、 取代 取代
三、 (酮)羰基 醛基 (酮)羰基 羧基
四、 RNHR′+HBr
六、 2RCHO+2H2O
考点四 常考有机信息
知识归纳
一、
二、
三、
四、 1.
2.
五、 CHCH3OMgCl CHCH3OH CCH3OMgClCH3CH2CH2CH3 CCH3OHCH3CH2CH2CH3 CH3CH2CHO
六、
八、
命题突破
1. (1)1∶9 (2)
(3)中和消去反应生成的HCN,降低HCN浓度促进反应正向进行
(4
(5)
解析:A与苯甲醛先在GIL下反应,产物在加热的条件下生成生成B,对比B、C、D的结构可知,B碳碳双键与NCCN加成生成C,C中碳氧双键与NCCN加成生成D,D在GIL下成环生成E,E发生消去反应生成F,同时有HCN生成,KOH中和生成的HCN,使平衡正向进行,提高F产率,F加热生成G。
(1)化合物G中sp杂化的C原子是—CN中的C,数目为2,苯环上的C均为sp2杂化,共18个,化合物G中sp、sp2杂化的碳原子数目之比为1∶9;
(2)对比B、C、D的结构可知,B碳碳双键与NCCN加成生成C,C中碳氧双键与NCCN加成生成D,B→D过程中还可能经历B→X→D,B中碳氧双键先与NCCN加成生成X,X中的碳碳双键再与NCCN加成生成D,X的结构为:;
(3)E发生消去反应生成F,同时有HCN生成,加入KOH溶液,中和生成的HCN,降低HCN浓度促进反应正向进行;
(4)C的同分异构体能发生水解反应,说明水解基团为肽键,生成两种产物均含苯环,说明结构为R1—CONH—R2,且R1和R2均含有苯环,两种产物中核磁共振氢谱分别为2个峰和4个峰,即等效氢的数目分别为2、4,符合条件的结构为:H2NNHCOCCHCH3CCH或H2NNHCOCHCCH3CHC;
(5)与CH3CHO先在GIL下反应,产物在加热的条件下生成
2. (1)(酮)羰基、酯基 (2)还原反应 (3)
(4)、
(5)
解析:A和X发生取代反应生成B,B加热后生成C,C发生氧化反应生成D,D与CH3I在NaH作用下发生反应生成E,E还原生成F。
(1)C的结构简式为,含有的含氧官能团名称为(酮)羰基、酯基;
(2)根据E和F的结构简式分析,羰基转化为羟基,反应过程中得到了H,则E→F的反应类型为还原反应;
(3)由E的结构简式知,E分子式为C15H16O3,副产物(分子式为C14H14O3)比E少1个CH2,则与E相比,生成E时有2个甲基取代了2个H,而生成副产物时只有1个甲基取代了H,故副产物的结构简式:;
(4)C的结构简式为,C的一种同分异构体同时满足:a.能与FeCl3溶液发生显色反应,则含有酚羟基;b.碱性条件下水解生成两种产物,酸化后分子中均只有2种不同化学环境的氢则高度对称,符合条件的同分异构体有OHOCCOC—C(CH3)3、;
(5)以和COOCH3为原料制备的合成路线,由与溴发生加成反应得到,在氢氧化钠的醇溶液中加热发生消去反应生成,与COOCH3反应生成,与氢气发生还原反应生成。
3. (1)sp2、sp3
(2)碳溴键、羧基 (3)加成反应
(4)
(5)
解析:(A)在1)NaOH、2)HCl作用下转化为(B),先与甲醛加成,再与HBr取代转化为(C),与甲醇在浓硫酸、加热条件下发生酯化反应生成(D),与反应生成(E),在HBr、HOAC条件下转化为(F),在一定条件下将羧基转化为羧酸钠生成(G)。
(1)B的结构简式为,分子中苯环上的碳原子和羧基上的碳原子的杂化方式均为sp2,环外饱和碳原子采取sp3杂化;
(2)C的结构简式为,其所含官能团名称为碳溴键、羧基;
(3)B→C的反应需经历B→X→C的过程,B的分子式为C9H10O2、X的分子式为C10H12O3,甲醛的分子式为CH2O,对比三者分子式,9+1=10、10+2=12、2+1=3,所以B→X的反应类型为加成反应;
(4)D的结构简式为,同时满足条件的同分异构体中含有酯基、且分子对称性高,其结构简式为或
(5)以CH3CH2OH、为原料制备
4. (1)3 (2)不能
(3)
(4)
(5)
解析:由流程图可知,A→B溴原子被氰基取代;B→C中,B与发生取代反应,生成C;C→D发生还原反应,氰基被还原为氨基;D→E中,D与发生取代反应,生成E;E→F中,“Boc—”被“H”取代,生成F;F→G中,F与发生取代反应,生成G。
(1)形成四个单键的碳原子为sp3杂化的碳原子,根据C的结构简式可知,C分子中采取sp3杂化的碳原子有3个。
(2)D分子中存在酰胺基,在KOH溶液中会发生水解,所以D→E的过程中不能用KOH替换K2CO3。
(3)由E→F可知,“Boc—”被“H”取代,Boc—结构简式为(CH3)3C—O—C—O,根据反应条件中可知,反应物中有HCl—CH3OH,又知该酯类产物的分子式为C3H6O3,所以该产物的结构简式为CH3O—C—OCH3O。
(4)C的一种同分异构体同时满足下列条件:分子中含有两个苯环和一个硝基,且分子中不同化学环境的氢原子个数比是1∶2∶2∶1,C中含有12个氢原子,则不同化学环境的氢原子个数为2、4、4、2,则两个苯环应对称,根据以上条件,可得该同分异构体的结构简式为CNO2NH2或NCH2—NO2。
(5)根据流程图可知,D→E→F可形成类似的结构,D中含有氨基,可用苯先与浓硫酸和浓硝酸反应,生成硝基苯,再用Fe和HCl还原,将硝基苯转化为苯胺,按照D→E的反应条件,让苯胺与反应,生成,再按照E→F的反应条件,使转化为,反应流程图为:NO2NH2。
5. (1)D (2)3∶1
(3)高 (4)
(5)
(6)
解析:A()与SOCl2发生反应生成B(),B()与CH3NH2在甲醇、THF条件下发生取代反应生成C();C()与D(O2NOH)在碳酸钾,DMF条件下发生取代反应生成E();E()与H2反应生成F(),F与G、CH2Cl2发生加成反应生成H(),根据原子守恒推知G为,据此分析解答。
(1)原子发射光谱是利用物质在热激发或电激发下,每种元素的原子或离子发射特征光谱来判断物质的组成,可测定元素的含量该方法,不能确定官能团的类别,A不符合题意;利用核磁共振仪记录下原子在共振下的有关信号绘制的图谱。吸收峰个数=等效氢原子种数,吸收峰面积之比=各种等效氢原子个数的最简整数比,可确定物质中氢原子的种类和数目,该方法不能确定官能团的类别,B不符合题意;质谱法中质荷比值最大的为物质的相对分子质量,不能确定官能团的类别,C不符合题意;红外光谱具有高度的特征性,利用红外光谱可确定化学基团和鉴定未知物质结构,D符合题意。故选D。
(2)B()与CH3NH2在甲醇、THF条件下发生取代反应生成C(),C在酸性条件下不稳定,B→C的反应中HCl、—COCl均与CH3NH2反应,应控制的投料比不低于3∶1;
(3)分子内氢键降低物质的熔沸点。邻硝基苯酚存在分子内氢键,使得熔点低于D(O2NOH);
(4)F()的一种同分异构体同时满足分子中所有碳原子轨道杂化类型相同;即C原子采取sp2杂化,含两个苯环;1 mol该物质完全水解最多消耗3 mol NaOH,水解产物之一的分子中不同化学环境的氢原子个数比为2∶1,含有两个—NH2处于对称位置,含有1个—OOCNH—直接连在两个苯环上,满足条件的物质结构为:;
(5)F()与G、CH2Cl2发生加成反应生成H(),根据G的分子式为C8H3ClF3NO推知G为。
(6)以和CH3CH2NH2为原料制备,对比原料和目标产物的结构要引入两个—CONH—官能团,由题目中B→C转化迁移可知应将与溴单质加成引入两个溴原子,在碱的醇溶液条件下水解生成1,3 环己二烯,该物质被酸性高锰酸钾氧化为己二酸,己二酸与SOCl2反应后的产物再与CH3NH2在甲醇、THF条件下发生取代反应生成。
6. (1)醚键、酰胺基 (2)加成反应
(3)
(4)
(5)
解析:由A和B的结构简式可知A和发生取代反应生成B,B和HCN发生加成反应生成C,C先在碱性条件下发生水解后酸化得到D,D发生还原反应生成E,E和SOCl2发生取代反应得到,由G的结构简式可知,在AlCl3的催化下发生了成环反应,结合化合物F的分子式C19H18O5,可以推知F的结构简式为,以此解答。
(1)由结构简式可知,G分子中含氧官能团的名称为醚键、酰胺基。
(2)由分析可知,B和HCN发生加成反应生成C。
(3)A的一种同分异构体同时满足条件:①分子能发生银镜反应、水解反应,且能与FeCl3溶液发生显色反应,说明其中含有苯环且苯环上连接羟基,另外其中还含有甲酸酯(—OOCH)的结构;②分子中含有四种不同化学环境的氢原子,说明该分子是对称的结构;结合A的分子式可以推知,苯环上的取代基为1个—OH、2个—CH3、1个—OOCH,且4个取代基要对称,该同分异构体的结构简式为OHH3CCOOHCH3或OHH3CCOOHCH3。
(4)由分析可知,F的结构简式为。
(5)由逆向合成法分析,可以由发生消去反应得到,由已知②的反应原理可知可由和N2H4发生还原反应得到,可由和H2O发生加成反应得到,可由O和CHOCH3发生加成再水解得到,O可由OH发生催化氧化得到,具体合成路线流程图见参考答案。
7. (1)还原反应
(2)保护酮羰基,防止F→G转化时被还原(加成)
(3)、
(4)
(5)
解析:由有机物的转化关系可知,CH3在氯化铝作用下与发生环加成反应,与锌(汞)、盐酸发生还原反应生成,与SOCl2发生取代反应生成,在氯化铝作用下发生取代反应生成H3CO,在酸性条件下,H3CO与乙二醇先发生加成反应,再发生取代反应生成,催化剂作用下,与氢气发生加成反应生成,酸性条件下转化为,先在无水乙醚作用下与CH3CH2MgBr发生取代反应,再在酸性条件下共热发生消去反应生成。
(1)由分析可知,B→C的反应为与锌(汞)、盐酸发生还原反应生成;
(2)由E、H的分子中都含有酮羰基可知,流程中设计E→F的目的是保护酮羰基,防止F→G转化时与氢气反应被还原(加成);
(3)由结构简式可知,A→B的反应中CH3在氯化铝作用下与发生环加成反应生成,则A→B得到的产物若不经提纯,依据B到E的合成路线会生成一种与E互为同分异构体的副产物CH3O;
(4)B的同分异构体有手性碳原子,与氯化铁溶液发生显色反应且能使溴的四氯化碳溶液褪色说明同分异构体分子中含有连有4个不同原子或原子团的饱和碳原子、酚羟基和碳碳双键,碱性条件下水解后酸化生成两种有机产物,产物之一分子中只有两种不同化学环境的氢原子说明同分异构体分子中含有酚酯基,则符合条件的结构简式为OOCCHCHCH3CH2OH;
(5)由题给有机物的转化关系可知,以苯、甲苯、CH3CHMgBrCH3为原料制备的合成步骤为CH3与酸性高锰酸钾溶液发生氧化反应生成COOH,COOH与SOCl2发生取代反应生成COCl,在氯化铝作用下COCl与苯发生取代反应生成,先在无水乙醚作用下与CH3CHMgBrCH3发生取代反应,再在酸性条件下共热发生消去反应生成,催化剂作用下与氢气共热发生加成反应生成。
8. (1)8 (2)取代反应
(3)
(4)
(5)
解析:由流程可知,A→B的反应为取代反应,B→C是进行取代位置的保护,如果直接硝化反应,会在硝基的间位上引入硝基,则达不到实验目的,C→D为硝化反应,在苯环的对位上引入硝基,D→E为酰胺键的水解反应,即取代反应,最后再进行硝基的还原得到最后产物。
(1)A中苯环上的碳原子和酯基上的碳原子都采用的是sp2杂化,故有8个碳原子采用sp2杂化;
(2)对比D和E的结构可知,D在酸性条件下发生水解反应得到E,反应类型为取代反应;
(3)B到C时为了在苯环的对位上引入基团,若B直接硝化,则会在B的苯环上的间位上引入硝基,则最后得到的产物会是;
(4)B的结构简式为,其同分异构体能与FeCl3溶液发生显色反应,说明有酚羟基,分子中含有2个苯环,则刚好把碳原子和不饱和度用完,说明其侧链为两个氨基和两个酚羟基,共有3种不同化学环境的氢原子,则结构为对称结构,故满足条件的同分异构体有H2NOHOHOHNH2OH或H2NOHOHOHNH2OH;
(5)CH3CH2OH、CH3CH2CH2NH2和为原料制备;上的碳原子要减少2个,则先与溴单质发生加成反应得到,再发生消去反应得到,再利用信息反应得到,再与CH3CH2OH酯化得到,最后利用流程图中A到B的反应得到目标产物。
9. (1)强 (2)CH3COCl (3)HCl (4)
(5)取代反应
(6)
解析:OH与C2H3OCl发生取代反应生成,可推知化学方程式为OH+CH3COCl―→+HCl,可知B为CH3COCl;发生水解反应得到F:,与G(C8H8Br2)发生取代反应得到,可知化学方程式为+―→+HBr,由此推知G为。
(1)化合物A:OH中含有酚羟基,酚羟基酸性强于醇羟基,故化合物A的酸性比环己醇的强。
(2)由分析可知B的结构简式为CH3COCl。
(3)A→C的化学方程式为OH+CH3COCl―→+HCl,(C2H5)3N显碱性可以与HCl发生中和反应促进OH+CH3COCl―→+HCl平衡正移,提供的产率,故A→C中加入(C2H5)3N是为了消耗反应中产生的HCl。
(4)的同分异构体碱性条件水解后酸化生成两种产物,产物之一的分子中碳原子轨道杂化类型相同且室温下不能使2%酸性KMnO4溶液褪色,说明其同分异构体为5,且该水解产物为苯甲酸;另一水解产物为丙醇,且加热条件下,铜催化该产物与氧气反应,所得有机产物的核磁共振氢谱中只有1个峰,由此确定该醇为2 丙醇,由此确定的同分异构体为。
(5)由分析可知F→H的反应为+―→+HBr,该反应为取代反应。
10. (1)CH3CH2OH (2)
(3)
(4)
(5)
解析:(1)将A、B分子中部分C原子编号为、,由此可知,该反应过程中A分子断开了3号C原子处的C—O,故所得的另一种有机产物为乙醇。
(2)由D、E的结构简式以及产物之一为HI可知,该反应为取代反应,故PinBH的结构简式为。
(3)根据DMS的结构简式以及H2SO4的结构简式(SOHOOO—H)可知,DMS水解生成H2SO4的同时可得到CH3OH。
(4)根据条件①可知,分子中含有醛基,根据条件②可知,分子中含有OCO,结合A的结构以及条件③可知,符合要求的同分异构体的结构简式为OCOCCH3CH3CHO。
(5)CH2CH2ClOH中氯原子水解可得到醇羟基,但酚羟基也可和NaOH反应,所以需要保护酚羟基,参考B→C的反应可知酚羟基和BnBr反应可得到CH2CH2ClOBn,然后与NaOH反应得到醇羟基,将醇羟基氧化成醛基,再将醛基氧化成羧基,最后根据路线可知,与H2,Pd/C反应即可得到CH2COOHOH。
素养评估
1. (1)sp2和sp3
(2)取代反应
(3)
(4)
(5)
解析:(1)A分子中,苯环上的碳原子和双键上的碳原子为sp2杂化,亚甲基上的碳原子为sp3杂化,即A分子中碳原子的杂化轨道类型为sp2和sp3。
(2)B→C的反应中,B中的羟基被氯原子代替,该反应为取代反应。
(3)D的分子式为C12H14O3,其一种同分异构体在碱性条件水解,酸化后得2种产物,其中一种含苯环且有2种含氧官能团,2种产物均能被银氨溶液氧化,说明该同分异构体为酯,且水解产物都含有醛基,则水解产物中,有一种是甲酸,另外一种含有羟基和醛基,该同分异构体属于甲酸酯;同时,该同分异构体分子中含有4种不同化学环境的氢原子,则该同分异构体的结构简式为。
(4)E经过还原反应转化为F,F再转化为G,其中G和F的分子式都是C12H17NO2,则F的结构简式为,F和G互为手性异构体。
(5)根据已知的第一个反应可知,与CH3MgBr反应生成,再被氧化为,根据已知的第二个反应可知,可以转化为,根据流程图中D→E的反应可知,和NH2OH反应生成。
2. (1)羰基、碳碳三键
(2)
(3)(或)
(4)4 甲基苯甲酸中的羰基O(δ-)原子进攻SOCl2中的S(δ+)原子,一根S—Cl键断裂,Cl得到共用电子对离去,随后Cl-进攻C原子,发生加成反应
(5)
解析:A和溴发生取代反应在苯环上引入溴原子得到B,B和镁反应生成C,C和二氧化碳反应后水解引入羧基得到D,D发生取代反应引入氯原子得到E,E和F生成G,F的分子式为C10H10,结合G结构可知,F为;G再转化为H。
(3)D中含有羧基,和乙二醇(HOCH2CH2OH)以物质的量之比为2∶1完全酯化的产物为COOCH2CH2OOC;其同分异构体同时满足下列条件:①分子中含有3种不同化学环境的氢原子,则结构对称;②能发生银镜反应,含有醛基或甲酸酯基;③能发生水解反应,且1 mol该分子水解时消耗4 mol NaOH,则含有2个甲酸酯基,且水解后生成酚羟基,故可以为或。
(5)苯乙烯和溴加成引入溴原子,再发生消去反应得到苯乙炔;苯甲酸和SOCl2发生D生成E的反应引入氯原子,再和苯乙炔发生E生成G的反应得到,再和发生G生成H的反应生成目标产物。
3. (1)取代反应
(2)保护羟基,防止其被氧化
(3)7
或
解析:(1)浓硝酸和浓硫酸的混合物在加热条件下发生取代反应。
(2)由已知Ⅰ的反应,可知A→B是酚羟基上的氢被取代,而D→E又变回酚羟基,则该反应的目的为保护羟基,防止其被氧化。
(3)苯环中的碳原子以及羧基中的碳原子,共有7个sp2杂化的碳原子。
(4)能发生银镜反应需要醛基,能使FeCl3溶液显色需要酚羟基,且含两个苯环的产物中存在三种化学环境的氢,该同分异构体为或HCOOOHOHOOCH。
4. (1)氨基、酯基
(2)消去反应 银氨溶液[或新制Cu(OH)2]
(3)
(4)
解析:(1)A中与苯环相连的官能团名称为氨基、酯基;
(2)D→E的过程中先发生加成反应生成,再发生消去反应生成,涉及的反应类型有:加成反应、消去反应;C不含醛基、D含有醛基,醛基能发生银镜反应,实验室中常用于鉴别C、D的试剂为银氨溶液。
(3)①分子中有一个含氮五元环;②核磁共振氢谱显示分子中有5种不同化学环境的氢原子,说明结构对称;③红外光谱显示分子中无甲基。符合条件的HONH2的同分异构体的结构简式为;
(4)由于NH2易被氧化,所以先用高锰酸钾把NO2CH3氧化为NO2COOH,NO2COOH再还原为NH2COOH,正丁醛和NH2COOH反应生成,和氢气发生加成反应生成。
同课章节目录
