山西省阳泉市第一中学校2024-2025学年高一下学期4月期中考试 化学试题(含答案)
文档属性
| 名称 | 山西省阳泉市第一中学校2024-2025学年高一下学期4月期中考试 化学试题(含答案) | 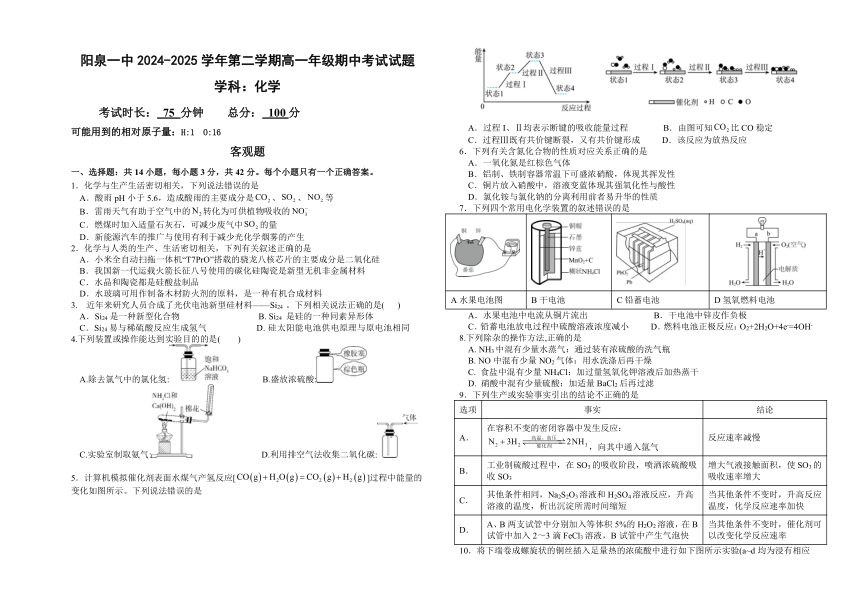 | |
| 格式 | docx | ||
| 文件大小 | 854.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-28 10:58:35 | ||
图片预览


文档简介
阳泉一中2024-2025学年第二学期高一年级期中考试试题
学科:化学
考试时长: 75 分钟 总分: 100分
可能用到的相对原子量:H:1 O:16
客观题
一、选择题:共14小题,每小题3分,共42分。每个小题只有一个正确答案。
1.化学与生产生活密切相关,下列说法错误的是
A.酸雨pH小于5.6,造成酸雨的主要成分是、、等
B.雷雨天气有助于空气中的转化为可供植物吸收的
C.燃煤时加入适量石灰石,可减少废气中的量
D.新能源汽车的推广与使用有利于减少光化学烟雾的产生
2.化学与人类的生产、生活密切相关,下列有关叙述正确的是
A.小米全自动扫拖一体机“T7PrO”搭载的骁龙八核芯片的主要成分是二氧化硅
B.我国新一代运载火箭长征八号使用的碳化硅陶瓷是新型无机非金属材料
C.水晶和陶瓷都是硅酸盐制品
D.水玻璃可用作制备木材防火剂的原料,是一种有机合成材料
3. 近年来研究人员合成了光伏电池新型硅材料——Si24 。下列相关说法正确的是( )
A.Si24 是一种新型化合物 B. Si24 是硅的一种同素异形体
C.Si24 易与稀硫酸反应生成氢气 D. 硅太阳能电池供电原理与原电池相同
4.下列装置或操作能达到实验目的的是( )
A.除去氯气中的氯化氢: B.盛放浓硫酸:
C.实验室制取氨气: D.利用排空气法收集二氧化碳:
5.计算机模拟催化剂表面水煤气产氢反应[]过程中能量的变化如图所示。下列说法错误的是
A.过程I、Ⅱ均表示断键的吸收能量过程 B.由图可知比CO稳定
C.过程Ⅲ既有共价键断裂,又有共价键形成 D.该反应为放热反应
6.下列有关含氮化合物的性质对应关系正确的是
A.一氧化氮是红棕色气体
B.铝制、铁制容器常温下可盛浓硝酸,体现其挥发性
C.铜片放入硝酸中,溶液变蓝体现其强氧化性与酸性
D.氯化铵与氯化钠的分离利用前者易升华的性质
7.下列四个常用电化学装置的叙述错误的是
A水果电池图 B干电池 C铅蓄电池 D氢氧燃料电池
A.水果电池中电流从铜片流出 B.干电池中锌皮作负极
C.铅蓄电池放电过程中硫酸溶液浓度减小 D.燃料电池正极反应:O2+2H2O+4e-=4OH-
8.下列除杂的操作方法,正确的是
A. NH3中混有少量水蒸气:通过装有浓硫酸的洗气瓶
B. NO中混有少量NO2气体:用水洗涤后再干燥
C. 食盐中混有少量NH4Cl:加过量氢氧化钾溶液后加热蒸干
D. 硝酸中混有少量硫酸:加适量BaCl2后再过滤
9.下列生产或实验事实引出的结论不正确的是
选项 事实 结论
A. 在容积不变的密闭容器中发生反应: ,向其中通入氩气 反应速率减慢
B. 工业制硫酸过程中,在SO3的吸收阶段,喷洒浓硫酸吸收SO3 增大气液接触面积,使SO3的吸收速率增大
C. 其他条件相同,Na2S2O3溶液和H2SO4溶液反应,升高溶液的温度,析出沉淀所需时间缩短 当其他条件不变时,升高反应温度,化学反应速率加快
D. A、B两支试管中分别加入等体积5%的H2O2溶液,在B试管中加入2~3滴FeCl3溶液,B试管中产生气泡快 当其他条件不变时,催化剂可以改变化学反应速率
10.将下端卷成螺旋状的铜丝插入足量热的浓硫酸中进行如下图所示实验(a~d均为浸有相应试液的棉花)。下列分析正确的是
A.a处现象:先变红后褪色
B.b和c处褪色原理相同
C.铜与浓硫酸反应,硫酸只体现酸性
D.试管底部出现白色固体,体现浓硫酸的吸水性
11.如图所示,利用培养皿探究的性质。实验时向NaOH固体上滴几滴浓氨水,立即用另一培养皿扣在上面。下表中对实验现象所做的解释正确的是
选项 实验现象 解释
A 浓盐酸附近产生白烟 与HCl反应生成固体
B 浓硫酸附近无现象 与浓硫酸不反应
C 氯化物溶液变浑浊 该溶液一定是溶液
D 干燥红色石蕊试纸不变色,湿润红色石蕊试纸变蓝 是可溶性碱
12.A与B在容积为1L的密闭容器中发生反应:aA(g)+bB(g)cC(g)+dD(g),t1、t2时刻分别测得部分数据如下表;
n(B)/mol n(C)/mol n(D)/mol 反应时间/min
0.12 0.06 0.10 t1
0.06 0.12 0.20 t2
下列说法正确的是
A.0~t1内,平均反应速率
B.若起始时,n(D)=0,则t2时
C.升高温度时,、、均增大
D.b:d=5:3
13. 下列离子方程式能用来解释相应实验现象的是
A.用 Na SO 溶液吸收少量 Cl :SO - + Cl + H O == SO - + 2Cl- + 2H+
B. 用足量的氨水处理硫酸工业的尾气:SO + NH ·H O == NH + + HSO -
C. 氢氧化钠腐蚀磨口玻璃塞:SiO + 2OH- == SiO32- + H O
D. 向氢氧化亚铁中加入足量的稀硝酸:Fe(OH) + 2H+ == Fe + + 2H O
14.下图装置可用于检验木炭与浓硫酸反应的产物,下列说法正确的是
A.①③④②可以检出,检不出、
B.①④③②可以检出、、
C.①④②③可以检出、,检不出
D.①②③④可以检出,检不出、
主观题
二、非选择题:本题共4小题,共58分。
15.(10分)(1)20世纪30年代,Eyring和Pzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态。如图是NO2和CO反应生成CO2和NO过程中的能量变化示意图,说明这个反应是________(填“吸热”或“放热”)反应,NO2和CO的总能量________(填“大于”“小于”或“等于”)CO2和NO的总能量。
(2)化学反应速率与限度跟生产、生活密切相关。
Ⅰ.某学生为了探究锌与盐酸反应过程中的速率变化,他在400mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如表(累计值,设溶液体积不变):
时间/min 1 2 3 4 5
氢气体积/mL(标准状况) 100 240 464 576 620
①哪一时间段(指0-1min、1-2min、2-3min、3-4min或4-5min)反应速率最快?_______。
②求2-4min时间段以盐酸的浓度变化来表示的该反应速率:_______。
Ⅱ.另一学生也做同样的实验,为更准确测量氢气的体积,需减缓化学反应速率且不影响产生氢气的量,他欲在盐酸中加入下列试剂,你认为可行的是_______。
A.溶液 B.KCl溶液 C.固体
16.(16分)如图所示,是原电池的装置图。请回答:
(1)若溶液C为稀H2SO4溶液,电流表指针发生偏转,B电极材料为Fe且作负极,则A电极上发生的电极反应式为 ; 反应进行一段时间后溶液C的酸性 (填“升高”“降低”或“基本不变”)。
(2)若需将反应Cu+2Fe3+Cu2++2Fe2+设计成如图所示的原电池装置,则A极(负极)材料为 ,B极电极反应式为 。
(3)用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图如下:
①电极c是 (填“正极”或“负极”),写出正极电极反应式: 。若线路中转移2 mol电子,则上述CH3OH燃料电池,消耗的O2在标准状况下的体积为 L。
②如果上述电池的电解质溶液换成NaOH,写出负极电极反应式: 。
17.(17分)Ⅰ.某兴趣小组为探究铜与浓硫酸的反应,设计如图所示装置进行实验。
请回答有关问题:
(1)装置A中发生反应的化学方程式为 。
(2)实验过程中,装置D内产生的现象分别说明了具有的性质是 。若加热装置D,可观察到的现象是 。
(3)装置B的作用是储存多余的气体。当装置D处有明显现象后,关闭K,移去酒精灯,但由于余热的作用,装置A处仍有气体产生,此时装置B中的现象是 。装置B中应放置的液体是 (填字母)。
a.水 b.酸性溶液 c.浓溴水 d.饱和溶液
(4)某小组利用下列装置测定空气中的含量。
装置中与碘(I2)溶液发生反应的离子方程式为: 。
Ⅱ.2021年,贵阳市空气质量优良率达98.9%,这得益于贵阳市对含硫化合物等排放的有效控制。回答下列问题:
(5)燃煤的烟气中含有,为了治理雾霾,工厂采用如图所示多种方法实现烟气脱硫。
①写出与反应的化学方程式___________。
②用含的烟气处理含的酸性废水时,所发生的离子反应为:
______+______+_____ == ____+______+______
18.(15分)Ⅰ.某课外活动小组在实验室制备氨气、验证氨气的某些性质。
氨气的制备:
(1)图中三套装置中能制备干燥的是 (“甲”、“乙”、“丙”)。
(2)上述方案中制备的化学方程式: 。
如图所示的实验收置模拟工业生产制备少量硝酸:
(3)实验时先用酒精喷灯预热催化剂,然后通入反应气体,当催化剂红热后撤离酒精喷灯,催化剂始终保持红热,温度可达到以上,由此可知该反应是 (填“吸热”或“放热”)反应,反应的化学方程式为: 。
Ⅱ.硝酸是重要的化工原料。下图是以合成氨为基础的传统硝酸生产工艺流程(其中空气等基础原料已略去)。
(4)合成氨反应的反应方程式为,这是一个正反应放热的可逆反应,下列说法不正确的是 (填字母)。
a.使用催化剂是为了增大反应速率,提高生产效率
b.在上述条件下,不可能100%转化为
c.提高反应时的温度,可以实现的完全转化
d.该反应采用高温、高压等苛刻条件,与化学性质很稳定有关
(5)合成氨、聚合装置中,含氮物质转化的主要反应包括
① ② ③
其中属于氧化还原反应的是 (填序号)。
(6)催化还原氮氧化物(SCR)技术是目前应用最广泛的氮氧化物脱除技术,可用于上述硝酸生产工艺的废气处理,反应原理如下图所示:
写出和NO在催化剂表面发生反应的化学方程式为 。
2024-2025学年第二学期 高一 年级期中考试试题
化学答案
1 2 3 4 5 6 7 8 9 10 11 12 13 14
A B B C B C D B A D A C C B
15.(10分,每空2分)
(1) 放热 大于
(2) Ⅰ. ① 2-3min ② 0.0375mol·L-1·min-1
Ⅱ. B
16.(16分,每空2分)
(1) 2H++2e-H2↑ 降低
(2) Cu Fe3++e-Fe2+
(3) ①负极 O2+ 4H++4e- = 2H2O 11.2
②CH3OH - 6e- + 8OH- = CO32- + 6H2O
17.(17分,除标记外每空2分)
Ⅰ.(1)
(2) 漂白性 品红溶液恢复原色
(3) 集气瓶中液面下降,长颈漏斗中液面上升 d
(4)
Ⅱ.(5)
(3分)
18.(15分,除标记外每空2分)
(1) 丙
(2) 2NH4Cl+Ca(OH)22NH3↑+CaCl2+2H2O
(3) 放热 4NH3+5O24NO+6H2O
(4) c
(5) ①②
(6) (3分)
学科:化学
考试时长: 75 分钟 总分: 100分
可能用到的相对原子量:H:1 O:16
客观题
一、选择题:共14小题,每小题3分,共42分。每个小题只有一个正确答案。
1.化学与生产生活密切相关,下列说法错误的是
A.酸雨pH小于5.6,造成酸雨的主要成分是、、等
B.雷雨天气有助于空气中的转化为可供植物吸收的
C.燃煤时加入适量石灰石,可减少废气中的量
D.新能源汽车的推广与使用有利于减少光化学烟雾的产生
2.化学与人类的生产、生活密切相关,下列有关叙述正确的是
A.小米全自动扫拖一体机“T7PrO”搭载的骁龙八核芯片的主要成分是二氧化硅
B.我国新一代运载火箭长征八号使用的碳化硅陶瓷是新型无机非金属材料
C.水晶和陶瓷都是硅酸盐制品
D.水玻璃可用作制备木材防火剂的原料,是一种有机合成材料
3. 近年来研究人员合成了光伏电池新型硅材料——Si24 。下列相关说法正确的是( )
A.Si24 是一种新型化合物 B. Si24 是硅的一种同素异形体
C.Si24 易与稀硫酸反应生成氢气 D. 硅太阳能电池供电原理与原电池相同
4.下列装置或操作能达到实验目的的是( )
A.除去氯气中的氯化氢: B.盛放浓硫酸:
C.实验室制取氨气: D.利用排空气法收集二氧化碳:
5.计算机模拟催化剂表面水煤气产氢反应[]过程中能量的变化如图所示。下列说法错误的是
A.过程I、Ⅱ均表示断键的吸收能量过程 B.由图可知比CO稳定
C.过程Ⅲ既有共价键断裂,又有共价键形成 D.该反应为放热反应
6.下列有关含氮化合物的性质对应关系正确的是
A.一氧化氮是红棕色气体
B.铝制、铁制容器常温下可盛浓硝酸,体现其挥发性
C.铜片放入硝酸中,溶液变蓝体现其强氧化性与酸性
D.氯化铵与氯化钠的分离利用前者易升华的性质
7.下列四个常用电化学装置的叙述错误的是
A水果电池图 B干电池 C铅蓄电池 D氢氧燃料电池
A.水果电池中电流从铜片流出 B.干电池中锌皮作负极
C.铅蓄电池放电过程中硫酸溶液浓度减小 D.燃料电池正极反应:O2+2H2O+4e-=4OH-
8.下列除杂的操作方法,正确的是
A. NH3中混有少量水蒸气:通过装有浓硫酸的洗气瓶
B. NO中混有少量NO2气体:用水洗涤后再干燥
C. 食盐中混有少量NH4Cl:加过量氢氧化钾溶液后加热蒸干
D. 硝酸中混有少量硫酸:加适量BaCl2后再过滤
9.下列生产或实验事实引出的结论不正确的是
选项 事实 结论
A. 在容积不变的密闭容器中发生反应: ,向其中通入氩气 反应速率减慢
B. 工业制硫酸过程中,在SO3的吸收阶段,喷洒浓硫酸吸收SO3 增大气液接触面积,使SO3的吸收速率增大
C. 其他条件相同,Na2S2O3溶液和H2SO4溶液反应,升高溶液的温度,析出沉淀所需时间缩短 当其他条件不变时,升高反应温度,化学反应速率加快
D. A、B两支试管中分别加入等体积5%的H2O2溶液,在B试管中加入2~3滴FeCl3溶液,B试管中产生气泡快 当其他条件不变时,催化剂可以改变化学反应速率
10.将下端卷成螺旋状的铜丝插入足量热的浓硫酸中进行如下图所示实验(a~d均为浸有相应试液的棉花)。下列分析正确的是
A.a处现象:先变红后褪色
B.b和c处褪色原理相同
C.铜与浓硫酸反应,硫酸只体现酸性
D.试管底部出现白色固体,体现浓硫酸的吸水性
11.如图所示,利用培养皿探究的性质。实验时向NaOH固体上滴几滴浓氨水,立即用另一培养皿扣在上面。下表中对实验现象所做的解释正确的是
选项 实验现象 解释
A 浓盐酸附近产生白烟 与HCl反应生成固体
B 浓硫酸附近无现象 与浓硫酸不反应
C 氯化物溶液变浑浊 该溶液一定是溶液
D 干燥红色石蕊试纸不变色,湿润红色石蕊试纸变蓝 是可溶性碱
12.A与B在容积为1L的密闭容器中发生反应:aA(g)+bB(g)cC(g)+dD(g),t1、t2时刻分别测得部分数据如下表;
n(B)/mol n(C)/mol n(D)/mol 反应时间/min
0.12 0.06 0.10 t1
0.06 0.12 0.20 t2
下列说法正确的是
A.0~t1内,平均反应速率
B.若起始时,n(D)=0,则t2时
C.升高温度时,、、均增大
D.b:d=5:3
13. 下列离子方程式能用来解释相应实验现象的是
A.用 Na SO 溶液吸收少量 Cl :SO - + Cl + H O == SO - + 2Cl- + 2H+
B. 用足量的氨水处理硫酸工业的尾气:SO + NH ·H O == NH + + HSO -
C. 氢氧化钠腐蚀磨口玻璃塞:SiO + 2OH- == SiO32- + H O
D. 向氢氧化亚铁中加入足量的稀硝酸:Fe(OH) + 2H+ == Fe + + 2H O
14.下图装置可用于检验木炭与浓硫酸反应的产物,下列说法正确的是
A.①③④②可以检出,检不出、
B.①④③②可以检出、、
C.①④②③可以检出、,检不出
D.①②③④可以检出,检不出、
主观题
二、非选择题:本题共4小题,共58分。
15.(10分)(1)20世纪30年代,Eyring和Pzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量的过渡态。如图是NO2和CO反应生成CO2和NO过程中的能量变化示意图,说明这个反应是________(填“吸热”或“放热”)反应,NO2和CO的总能量________(填“大于”“小于”或“等于”)CO2和NO的总能量。
(2)化学反应速率与限度跟生产、生活密切相关。
Ⅰ.某学生为了探究锌与盐酸反应过程中的速率变化,他在400mL稀盐酸中加入足量的锌粉,用排水集气法收集反应放出的氢气,实验记录如表(累计值,设溶液体积不变):
时间/min 1 2 3 4 5
氢气体积/mL(标准状况) 100 240 464 576 620
①哪一时间段(指0-1min、1-2min、2-3min、3-4min或4-5min)反应速率最快?_______。
②求2-4min时间段以盐酸的浓度变化来表示的该反应速率:_______。
Ⅱ.另一学生也做同样的实验,为更准确测量氢气的体积,需减缓化学反应速率且不影响产生氢气的量,他欲在盐酸中加入下列试剂,你认为可行的是_______。
A.溶液 B.KCl溶液 C.固体
16.(16分)如图所示,是原电池的装置图。请回答:
(1)若溶液C为稀H2SO4溶液,电流表指针发生偏转,B电极材料为Fe且作负极,则A电极上发生的电极反应式为 ; 反应进行一段时间后溶液C的酸性 (填“升高”“降低”或“基本不变”)。
(2)若需将反应Cu+2Fe3+Cu2++2Fe2+设计成如图所示的原电池装置,则A极(负极)材料为 ,B极电极反应式为 。
(3)用CH3OH和O2组合形成的质子交换膜燃料电池的结构示意图如下:
①电极c是 (填“正极”或“负极”),写出正极电极反应式: 。若线路中转移2 mol电子,则上述CH3OH燃料电池,消耗的O2在标准状况下的体积为 L。
②如果上述电池的电解质溶液换成NaOH,写出负极电极反应式: 。
17.(17分)Ⅰ.某兴趣小组为探究铜与浓硫酸的反应,设计如图所示装置进行实验。
请回答有关问题:
(1)装置A中发生反应的化学方程式为 。
(2)实验过程中,装置D内产生的现象分别说明了具有的性质是 。若加热装置D,可观察到的现象是 。
(3)装置B的作用是储存多余的气体。当装置D处有明显现象后,关闭K,移去酒精灯,但由于余热的作用,装置A处仍有气体产生,此时装置B中的现象是 。装置B中应放置的液体是 (填字母)。
a.水 b.酸性溶液 c.浓溴水 d.饱和溶液
(4)某小组利用下列装置测定空气中的含量。
装置中与碘(I2)溶液发生反应的离子方程式为: 。
Ⅱ.2021年,贵阳市空气质量优良率达98.9%,这得益于贵阳市对含硫化合物等排放的有效控制。回答下列问题:
(5)燃煤的烟气中含有,为了治理雾霾,工厂采用如图所示多种方法实现烟气脱硫。
①写出与反应的化学方程式___________。
②用含的烟气处理含的酸性废水时,所发生的离子反应为:
______+______+_____ == ____+______+______
18.(15分)Ⅰ.某课外活动小组在实验室制备氨气、验证氨气的某些性质。
氨气的制备:
(1)图中三套装置中能制备干燥的是 (“甲”、“乙”、“丙”)。
(2)上述方案中制备的化学方程式: 。
如图所示的实验收置模拟工业生产制备少量硝酸:
(3)实验时先用酒精喷灯预热催化剂,然后通入反应气体,当催化剂红热后撤离酒精喷灯,催化剂始终保持红热,温度可达到以上,由此可知该反应是 (填“吸热”或“放热”)反应,反应的化学方程式为: 。
Ⅱ.硝酸是重要的化工原料。下图是以合成氨为基础的传统硝酸生产工艺流程(其中空气等基础原料已略去)。
(4)合成氨反应的反应方程式为,这是一个正反应放热的可逆反应,下列说法不正确的是 (填字母)。
a.使用催化剂是为了增大反应速率,提高生产效率
b.在上述条件下,不可能100%转化为
c.提高反应时的温度,可以实现的完全转化
d.该反应采用高温、高压等苛刻条件,与化学性质很稳定有关
(5)合成氨、聚合装置中,含氮物质转化的主要反应包括
① ② ③
其中属于氧化还原反应的是 (填序号)。
(6)催化还原氮氧化物(SCR)技术是目前应用最广泛的氮氧化物脱除技术,可用于上述硝酸生产工艺的废气处理,反应原理如下图所示:
写出和NO在催化剂表面发生反应的化学方程式为 。
2024-2025学年第二学期 高一 年级期中考试试题
化学答案
1 2 3 4 5 6 7 8 9 10 11 12 13 14
A B B C B C D B A D A C C B
15.(10分,每空2分)
(1) 放热 大于
(2) Ⅰ. ① 2-3min ② 0.0375mol·L-1·min-1
Ⅱ. B
16.(16分,每空2分)
(1) 2H++2e-H2↑ 降低
(2) Cu Fe3++e-Fe2+
(3) ①负极 O2+ 4H++4e- = 2H2O 11.2
②CH3OH - 6e- + 8OH- = CO32- + 6H2O
17.(17分,除标记外每空2分)
Ⅰ.(1)
(2) 漂白性 品红溶液恢复原色
(3) 集气瓶中液面下降,长颈漏斗中液面上升 d
(4)
Ⅱ.(5)
(3分)
18.(15分,除标记外每空2分)
(1) 丙
(2) 2NH4Cl+Ca(OH)22NH3↑+CaCl2+2H2O
(3) 放热 4NH3+5O24NO+6H2O
(4) c
(5) ①②
(6) (3分)
同课章节目录
