人教版初中化学课件九下8.2_金属的化学性质(共27张PPT)
文档属性
| 名称 | 人教版初中化学课件九下8.2_金属的化学性质(共27张PPT) |  | |
| 格式 | zip | ||
| 文件大小 | 677.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(新课程标准) | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-06-02 16:09:13 | ||
图片预览







文档简介
课件27张PPT。金属的化学性质 黄铜(铜锌合金)与黄金的外观很相似,一些不法商贩就会利用这一点,以次充好,贩卖假黄金(实际就是黄铜)。你用什么方法来识别真假金饰品呢?
你能否得出金属和化合物溶液反应的一般规律吗?现象:_________________________________________________
________________________________________________________将铁钉投入到硫酸铜溶液中有何现象? 铁钉表面会有红色物质析出,若时间足够
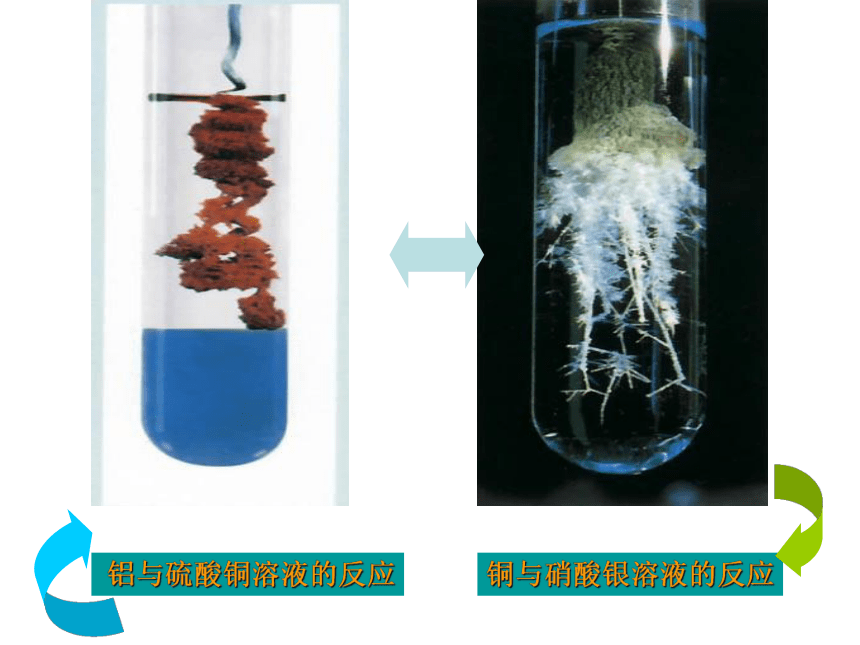
长,则溶液会从蓝色变为浅绿色。Fe + CuSO4 = Cu + FeSO4 该反应的化学方程式:回忆:活动性: Fe﹥CuAl、Cu、Ag的活动性,谁强谁弱如何判断? 铝与硫酸铜溶液的反应铜与硝酸银溶液的反应以上三种金属活动性顺序为:
Al Cu Ag 金属活动性由强到弱结论:2、可根据金属能不能把另一种金属从金属化合物的溶液中置换出来,判断金属活动性的强弱。结 论:1、部分金属能与金属化合物的溶液反应。3、在金属活动顺序里,位于前面的金属能把位于后面的金属从它们化合物的溶液中置换出来。 金属活动性顺序的应用:1、在金属活动顺序里,金属的位置越靠前,它的活动性就越强。2、在金属活动性顺序里,位于氢之前的金属能置换出盐酸(稀硫酸)中的氢。4、铁与溶液发生置换反应,生成亚铁化合物。思考题:
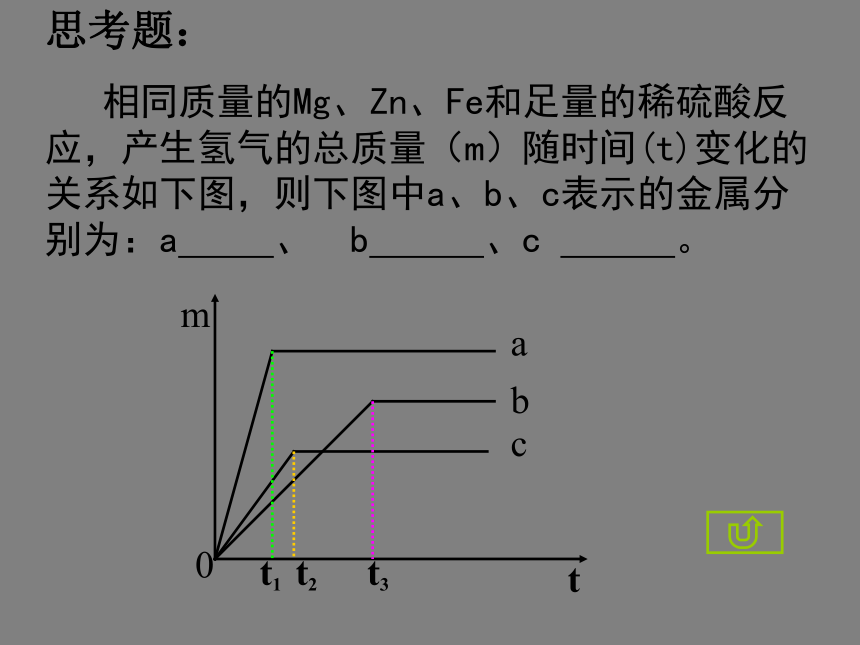
相同质量的Mg、Zn、Fe和足量的稀硫酸反应,产生氢气的总质量(m)随时间(t)变化的关系如下图,则下图中a、b、c表示的金属分别为:a 、 b 、c 。
mtabc0t2t1t31、判断下列物质能否发生反应?若能,
写出相关化学方程式。
⑴银与稀盐酸 ⑵锌与硫酸铜溶液
⑶铜与硫酸锌溶液 ⑷铝与硝酸银溶液
⑸银与氯化铜溶液 ⑹镁与硫酸亚铁溶液
练习:2、下列物质不能由金属和酸反应直接生
成的是 ( )
A、 ZnCl2 B、 CuSO4
C 、FeCl2 D 、Al2(SO4)33、实验室制氢气常选择锌与稀硫酸反应,
(1)选用的依据是什么?
(2)不选铜的理由?
(3)猜想:为什么也不选钾、钙、钠?
4、有X Y Z三种金属,如果把X和Y分别放入
稀硫酸中, X 溶解并产生氢气,Y不反应;如果
把Y和Z分别放入硝酸银溶液中,过一会儿,在Y
的表面有银析出,而Z无变化.根据以上事实,判
断X Y Z的金属活动顺序.课堂练习5、有X、Y、Z三种金属。X、Y、Z分别放入稀盐酸中,X溶解并放出氢气,Y、Z无变化;将Y放入Z的化合物溶液中无变化;Z放入Y的化合物溶液中有Y析出:则X、Y、Z的活动性顺序如何?6、X、Y、Z是三种金属,根据下列有关化学方程式可知,三种金属的活动性顺序是( )
①Z+YSO4==ZSO4+Y ②X+ YSO4==XSO4+Y
③X+ H2SO4== XSO4+ H2↑ ④Z+ H2SO4不反应
A、Z>X>Y B、Z>Y>X
C、X>Y>Z D、X>Z>Y
7、现有X、Y、Z三种金属,若将Z放入X的盐溶液中,Z表面覆盖有X,将Y和Z分别投入稀盐酸中,Y 溶解而Z不溶,则三种金属的活动顺序正确的是( )
A、Y>X>Z B、Y>Z>X
C、X>Y>Z D、X>Z>Y8、为了测定Ag,Zn,Cu,H的化学活动性强弱,某同学利用Zn粉,Cu片,AgNO3溶液和盐酸4种物质,设计了如下实验方案,其中可行的是( )
A、? Zn+HCl Cu+HCl Zn+AgNO3
B、Zn+HCl Cu+ AgNO3 Zn+AgNO3
C、Cu+HCl Zn+AgNO3 Cu+ AgNO3
D、Zn+HCl Cu+HCl Cu+ AgNO3
9、分别用以下三组物质比较锌和铜的金属活动性(1)Zn、Cu、稀硫酸;(2)Zn、Cu、MgSO4溶液;(3)Zn、Cu、AgNO3溶液。仅用组内物质就能够直接达到目的的是( )A、仅有(1) B、(2)(3)
C、(1)(3) D、(1)(2)(3)
10、将甲、乙两种金属片分别放入硫酸铜溶液中,甲的表面析出金属铜,乙没有明显现象。据此判断,三种金属的金属活动性顺序是( )
A、甲>铜>乙 B、 乙>铜>甲 C、 铜>甲>乙 D、甲>乙>铜金属与盐溶液反应的应用一、一种金属,多种溶液将一种金属单质放入几种金属的盐溶液的混合液中时,其中排在金属活动性顺序表中最靠后的金属最先被置换出来,然后再依次置换出稍靠后的金属。简记为“弱者先”。将金属Zn放入FeSO4和CuSO4的混合溶液中,Zn先与CuSO4发生置换反应,与CuSO4反应完后再与FeSO4 发生置换反应。根据金属锌的最不同可分为以下几种情况: 1、向硝酸银和硝酸铜的溶液中加入一定量的铁粉,充分反应后溶液中仍有金属固体,过滤后往滤液中加入盐酸,有无色气体放出,则滤液中一定存在的溶质是( )
A硝酸亚铁、硝酸铜
B硝酸亚铁、硝酸
C硝酸亚铁、硝酸铜、硝酸银
D硝酸亚铁2、在ZnSO4和CuSO4的混合溶液中,加入过量的铁粉,充分反应后过滤,在滤纸上的固体是( )
A、铁和铜 B、铁、铜、锌 C、铜和锌 D、只有铜3、在Cu(NO3)2、AgNO3 的混合溶液中,加入一定量的锌粉,充分反应后,可能有下列情况:
(1)若反应后锌有剩余,则此时溶液中所含的溶质是 ;
(2)若将反应后的混合物过滤,向所得固体中滴加稀盐酸,①若没有气泡产生,则固体物质中一定有 ,可能有 ;滤液中的溶质一定有 可能有 ②若有气泡产生,则固体物质中一定有 。滤液中的溶质一定有 。4、在CuCl2和NaCl的混合溶液中加入过量的Zn粉,充分反应后过滤,留在滤纸上的固体( ) A、只有Zn B、只有Cu C、有Cu和Na D、有Cu和Zn
5、把足量锌粉分别加入到含下列各组物质的混合溶液中,充分反应后过滤,滤液中只有一种溶质的是( )(双选)
A、MgSO4 CuSO4 B、CuSO4 H2SO4
C、Cu(NO3)2 AgNO3 D、HCl CuSO4
二、一种溶液,多种金属将几种不同的金属放入同一种盐溶液中,在金属活动性顺序表中,距离越远的先反应,然后是距离较远的反应。强者先 8.[7分]小华想测定Cu-Zn合金和Cu-Ag合金中铜的质量分数,实验室只提供了一瓶稀盐酸和相关的仪器。
(1)根据现有的条件,你认为只能测出_____________合金中铜的质量分数。
(2)为了测定该合金的组成,小华称取10 g该合金粉末,在粉末中连续三次加入稀盐酸反应。每加一次盐酸,小华记录所得气体的质量,实验数据如下:
第一次 第二次 第三次
连续加入盐酸的体积(ml) 10 10 1
生成氢气的质量(g) 0.08 0.08 0.04
(3)从上表数据分析,小华用10 g合金粉末总共收集到氢气_______g。
(4)求出该合金中铜的质量分数。
谢谢大家
你能否得出金属和化合物溶液反应的一般规律吗?现象:_________________________________________________
________________________________________________________将铁钉投入到硫酸铜溶液中有何现象? 铁钉表面会有红色物质析出,若时间足够
长,则溶液会从蓝色变为浅绿色。Fe + CuSO4 = Cu + FeSO4 该反应的化学方程式:回忆:活动性: Fe﹥CuAl、Cu、Ag的活动性,谁强谁弱如何判断? 铝与硫酸铜溶液的反应铜与硝酸银溶液的反应以上三种金属活动性顺序为:
Al Cu Ag 金属活动性由强到弱结论:2、可根据金属能不能把另一种金属从金属化合物的溶液中置换出来,判断金属活动性的强弱。结 论:1、部分金属能与金属化合物的溶液反应。3、在金属活动顺序里,位于前面的金属能把位于后面的金属从它们化合物的溶液中置换出来。 金属活动性顺序的应用:1、在金属活动顺序里,金属的位置越靠前,它的活动性就越强。2、在金属活动性顺序里,位于氢之前的金属能置换出盐酸(稀硫酸)中的氢。4、铁与溶液发生置换反应,生成亚铁化合物。思考题:
相同质量的Mg、Zn、Fe和足量的稀硫酸反应,产生氢气的总质量(m)随时间(t)变化的关系如下图,则下图中a、b、c表示的金属分别为:a 、 b 、c 。
mtabc0t2t1t31、判断下列物质能否发生反应?若能,
写出相关化学方程式。
⑴银与稀盐酸 ⑵锌与硫酸铜溶液
⑶铜与硫酸锌溶液 ⑷铝与硝酸银溶液
⑸银与氯化铜溶液 ⑹镁与硫酸亚铁溶液
练习:2、下列物质不能由金属和酸反应直接生
成的是 ( )
A、 ZnCl2 B、 CuSO4
C 、FeCl2 D 、Al2(SO4)33、实验室制氢气常选择锌与稀硫酸反应,
(1)选用的依据是什么?
(2)不选铜的理由?
(3)猜想:为什么也不选钾、钙、钠?
4、有X Y Z三种金属,如果把X和Y分别放入
稀硫酸中, X 溶解并产生氢气,Y不反应;如果
把Y和Z分别放入硝酸银溶液中,过一会儿,在Y
的表面有银析出,而Z无变化.根据以上事实,判
断X Y Z的金属活动顺序.课堂练习5、有X、Y、Z三种金属。X、Y、Z分别放入稀盐酸中,X溶解并放出氢气,Y、Z无变化;将Y放入Z的化合物溶液中无变化;Z放入Y的化合物溶液中有Y析出:则X、Y、Z的活动性顺序如何?6、X、Y、Z是三种金属,根据下列有关化学方程式可知,三种金属的活动性顺序是( )
①Z+YSO4==ZSO4+Y ②X+ YSO4==XSO4+Y
③X+ H2SO4== XSO4+ H2↑ ④Z+ H2SO4不反应
A、Z>X>Y B、Z>Y>X
C、X>Y>Z D、X>Z>Y
7、现有X、Y、Z三种金属,若将Z放入X的盐溶液中,Z表面覆盖有X,将Y和Z分别投入稀盐酸中,Y 溶解而Z不溶,则三种金属的活动顺序正确的是( )
A、Y>X>Z B、Y>Z>X
C、X>Y>Z D、X>Z>Y8、为了测定Ag,Zn,Cu,H的化学活动性强弱,某同学利用Zn粉,Cu片,AgNO3溶液和盐酸4种物质,设计了如下实验方案,其中可行的是( )
A、? Zn+HCl Cu+HCl Zn+AgNO3
B、Zn+HCl Cu+ AgNO3 Zn+AgNO3
C、Cu+HCl Zn+AgNO3 Cu+ AgNO3
D、Zn+HCl Cu+HCl Cu+ AgNO3
9、分别用以下三组物质比较锌和铜的金属活动性(1)Zn、Cu、稀硫酸;(2)Zn、Cu、MgSO4溶液;(3)Zn、Cu、AgNO3溶液。仅用组内物质就能够直接达到目的的是( )A、仅有(1) B、(2)(3)
C、(1)(3) D、(1)(2)(3)
10、将甲、乙两种金属片分别放入硫酸铜溶液中,甲的表面析出金属铜,乙没有明显现象。据此判断,三种金属的金属活动性顺序是( )
A、甲>铜>乙 B、 乙>铜>甲 C、 铜>甲>乙 D、甲>乙>铜金属与盐溶液反应的应用一、一种金属,多种溶液将一种金属单质放入几种金属的盐溶液的混合液中时,其中排在金属活动性顺序表中最靠后的金属最先被置换出来,然后再依次置换出稍靠后的金属。简记为“弱者先”。将金属Zn放入FeSO4和CuSO4的混合溶液中,Zn先与CuSO4发生置换反应,与CuSO4反应完后再与FeSO4 发生置换反应。根据金属锌的最不同可分为以下几种情况: 1、向硝酸银和硝酸铜的溶液中加入一定量的铁粉,充分反应后溶液中仍有金属固体,过滤后往滤液中加入盐酸,有无色气体放出,则滤液中一定存在的溶质是( )
A硝酸亚铁、硝酸铜
B硝酸亚铁、硝酸
C硝酸亚铁、硝酸铜、硝酸银
D硝酸亚铁2、在ZnSO4和CuSO4的混合溶液中,加入过量的铁粉,充分反应后过滤,在滤纸上的固体是( )
A、铁和铜 B、铁、铜、锌 C、铜和锌 D、只有铜3、在Cu(NO3)2、AgNO3 的混合溶液中,加入一定量的锌粉,充分反应后,可能有下列情况:
(1)若反应后锌有剩余,则此时溶液中所含的溶质是 ;
(2)若将反应后的混合物过滤,向所得固体中滴加稀盐酸,①若没有气泡产生,则固体物质中一定有 ,可能有 ;滤液中的溶质一定有 可能有 ②若有气泡产生,则固体物质中一定有 。滤液中的溶质一定有 。4、在CuCl2和NaCl的混合溶液中加入过量的Zn粉,充分反应后过滤,留在滤纸上的固体( ) A、只有Zn B、只有Cu C、有Cu和Na D、有Cu和Zn
5、把足量锌粉分别加入到含下列各组物质的混合溶液中,充分反应后过滤,滤液中只有一种溶质的是( )(双选)
A、MgSO4 CuSO4 B、CuSO4 H2SO4
C、Cu(NO3)2 AgNO3 D、HCl CuSO4
二、一种溶液,多种金属将几种不同的金属放入同一种盐溶液中,在金属活动性顺序表中,距离越远的先反应,然后是距离较远的反应。强者先 8.[7分]小华想测定Cu-Zn合金和Cu-Ag合金中铜的质量分数,实验室只提供了一瓶稀盐酸和相关的仪器。
(1)根据现有的条件,你认为只能测出_____________合金中铜的质量分数。
(2)为了测定该合金的组成,小华称取10 g该合金粉末,在粉末中连续三次加入稀盐酸反应。每加一次盐酸,小华记录所得气体的质量,实验数据如下:
第一次 第二次 第三次
连续加入盐酸的体积(ml) 10 10 1
生成氢气的质量(g) 0.08 0.08 0.04
(3)从上表数据分析,小华用10 g合金粉末总共收集到氢气_______g。
(4)求出该合金中铜的质量分数。
谢谢大家
同课章节目录
