基础小练3 有机化合物组成和结构的研究 (含答案)2024-2025学年高中化学选择性必修3(苏教版2019)
文档属性
| 名称 | 基础小练3 有机化合物组成和结构的研究 (含答案)2024-2025学年高中化学选择性必修3(苏教版2019) |
|
|
| 格式 | doc | ||
| 文件大小 | 614.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-29 00:00:00 | ||
图片预览




文档简介
基础小练3 有机化合物组成和结构的研究
1. (淮安期中)下列测定手段中,主要用来测定有机物官能团的是( )
A. 质谱法 B. 李比希燃烧实验
C. 红外光谱 D. 核磁共振氢谱
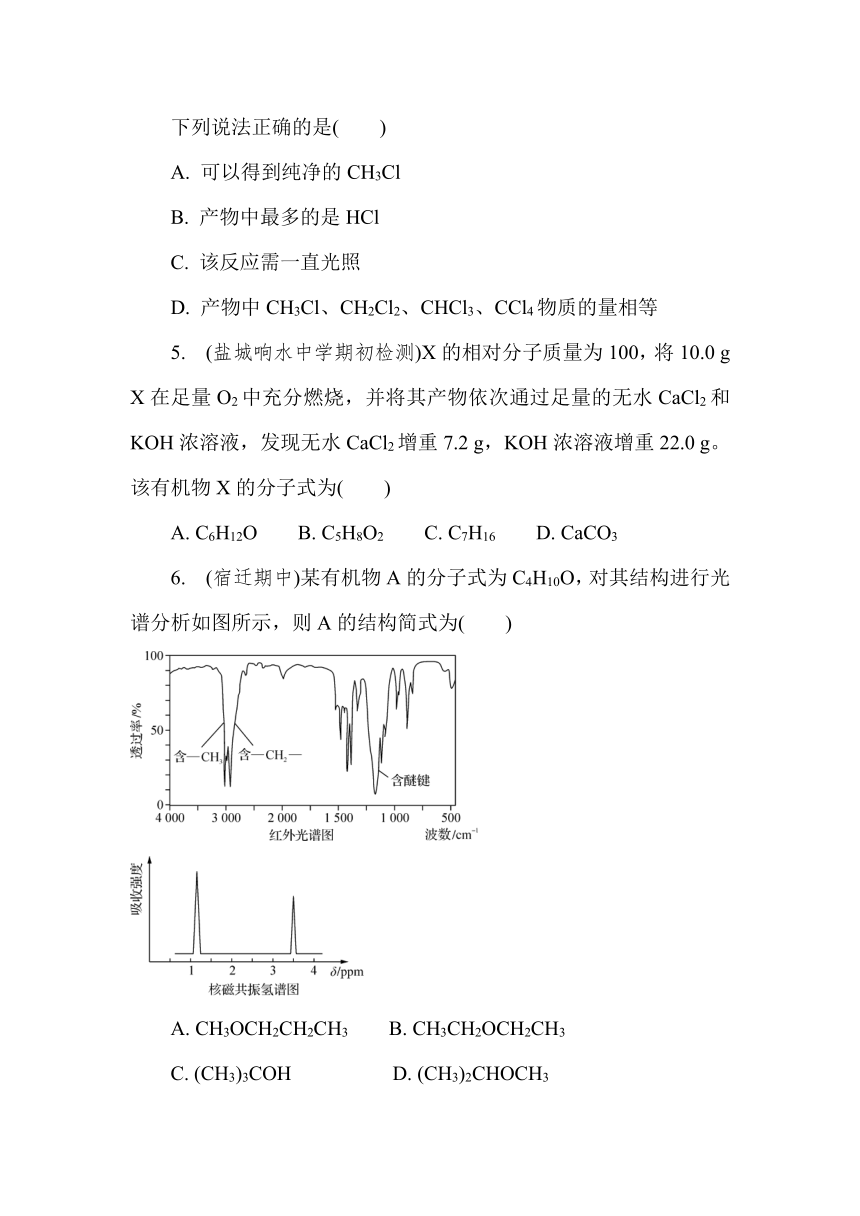
2. (南通海安高级中学月考)下列有机物的核磁共振氢谱有6组峰的是( )
3. (江门第一中学高段考)如图是一种分子式为C4H8O2的有机化合物的红外光谱图,则该有机化合物的结构简式是( )
A. CH3CH2CH2COOH B. CH3COOCH2CH3
C. CH3CH(CH3)COOH D. HCOOCH(CH3)2
4. CH4与Cl2反应的机理是①Cl2·Cl+·Cl;②·Cl+CH4―→·CH3+HCl;③·CH3+Cl2―→·Cl+CH3Cl。
下列说法正确的是( )
A. 可以得到纯净的CH3Cl
B. 产物中最多的是HCl
C. 该反应需一直光照
D. 产物中CH3Cl、CH2Cl2、CHCl3、CCl4物质的量相等
5. (盐城响水中学期初检测)X的相对分子质量为100,将10.0 g X在足量O2中充分燃烧,并将其产物依次通过足量的无水CaCl2和KOH浓溶液,发现无水CaCl2增重7.2 g,KOH浓溶液增重22.0 g。该有机物X的分子式为( )
A. C6H12O B. C5H8O2 C. C7H16 D. CaCO3
6. (宿迁期中)某有机物A的分子式为C4H10O,对其结构进行光谱分析如图所示,则A的结构简式为( )
A. CH3OCH2CH2CH3 B. CH3CH2OCH2CH3
C. (CH3)3COH D. (CH3)2CHOCH3
7. (南通海安高级中学月考)完成下列问题。
(1) 研究有机物的方法有很多,常用的有①核磁共振氢谱、②蒸馏、③重结晶、④萃取、⑤红外光谱、⑥过滤,其中用于分子结构确定的有________(填序号)。
(2) 下列物质中,其核磁共振氢谱中只有一个吸收峰的是________(填字母)。
A. CH3CH3 B. CH3COOH
C. CH3COOCH3 D. CH3OCH3
(3) 某含碳、氢、氧三种元素的有机物甲,经燃烧分析实验测定其碳的质量分数是64.86%,氢的质量分数是13.51%,则甲的实验式(最简式)是________。
①下图是该有机物甲的质谱图,则其相对分子质量为________,分子式为________。
②确定甲的官能团:通过实验可知甲中一定含有羟基,写出羟基的电子式____________;甲可能的结构有________种。
③经测定有机物甲的核磁共振氢谱如图所示,则甲的结构简式为___________。
8. 某有机物常用于生产聚酯纤维和树脂,是一种重要的化工合成原料,使用现代仪器对该有机物的结构进行测定,相关谱图如下。下列有关说法错误的是( )
A. 由质谱图可知该有机物相对分子质量为91
B. 由核磁共振氢谱可知该有机物中有2种不同化学环境的氢原子
C. 由红外光谱可获得该有机物的化学键或官能团信息
D. 综合以上信息可知该有机物为对二甲苯
9. (黄冈期末)某同学尝试利用李比希法测定液态烃X的实验式,设计了如下实验:准确称取1.06 g样品并置于试样盒中,加热样品,使蒸气通过氧化铜(催化剂),准确称量生成的二氧化碳和水的质量,分别是3.52 g和0.9 g。下列说法正确的是( )
A. 甲处放置碱石灰
B. 该烃的实验式是C8H10
C. 停止加热后,立即停止通入O2,防止浪费
D. 乙装置后加装一个盛碱石灰的干燥管,实验结果会更准确
10. (大同浑源中学期末)将6.8 g的X完全燃烧生成3.6 g的H2O和8.96 L(标准状况)的CO2。X的核磁共振氢谱有4个峰且面积之比为3∶2∶2∶1。X分子中只含一个苯环且苯环上只有一个取代基,其质谱图、核磁共振氢谱、红外光谱如下图所示。下列关于X的叙述正确的是( )
A. 化合物X的摩尔质量为106 g· mol-1
B. 化合物X为
C. 化合物X可能的结构有2种
D. 化合物X可能是苯乙酸
11. (徐州沛县学情调研)通常用燃烧的方法测定有机物的分子式,可在燃烧室内将有机物样品与纯氧在电炉加热下充分燃烧,根据产品的质量确定有机物的组成。如图所示的是用燃烧法确定有机物分子式的常用装置。
现准确称取1.8 g样品(只含C、H、O三种元素中的两种或三种),经燃烧后A管增重1.76 g,B管增重0.36 g。请回答:
(1) 用该方法可测定含有哪些元素的有机物:____________________。
(2) 分离和提纯固体有机物的一个操作方法是重结晶,在静置条件下结晶的原因是________________________________。
(3) A、B管内均盛有固态试剂,B管的作用是____________________________。
(4) 根据气流方向将装置进行连接,连接的顺序是_______________________
(填接口字母,用“→”连接)。
(5) E中应盛装的试剂能使硫酸酸化的高锰酸钾溶液褪色,写出该反应的离子方程式______________________________________________________。
(6) 如果把CuO网去掉,A管增重将________(填“增大”“减小”或“不变”)。
(7) 某同学认为A和空气相通,会影响测定结果准确性,应在A后再增加一个A装置,其主要目的是______________________________。
(8) 该有机物的最简式为__________(写出计算过程)。
基础小练3 有机化合物组成和结构的研究
1. C 质谱法测定有机物的相对分子质量,A错误;李比希燃烧实验确定有机物的实验式,B错误;红外光谱测定有机物的化学键和官能团,C正确;核磁共振氢谱测定有机物中氢原子的化学环境,D错误。
2. A 分子结构不对称,含6种不同化学环境的H,核磁共振氢谱有6组峰,A正确;分子中含4种不同化学环境的H,核磁共振氢谱有4组峰,B错误;分子中含4种不同化学环境的H,核磁共振氢谱有4组峰,C错误;苯中的六个氢原子是完全相同的,核磁共振氢谱有1组峰,D错误。
等效氢法判断同分异构体的数目
①同一碳原子上的氢原子等效;
②同一碳原子上的甲基上的氢原子等效;
③位于对称位置上的碳原子上的氢原子等效。
3. B 由红外光谱图可看出该分子中有不对称—CH3,因此该分子中有2个—CH3,由图也可以看出含有碳氧双键和C—O—C键。所以可能的结构简式为CH3COOCH2CH3或CH3CH2COOCH3,故选B。
①质谱——可快速、准确测定有机物的相对分子质量。
②红外光谱——可以获得分子中含有何种化学键或官能团的信息。
③核磁共振氢谱——可推知有机物分子中有几种不同类型的氢原子及它们的数目之比。
4. B 由反应机理②知,·Cl与烃中的氢原子结合生成HCl,故产物中有机物除CH3Cl外还有CH2Cl2、CHCl3、CCl4,物质的量无法确定,最多的产物为HCl,A、D错误,B正确;由反应机理②③知,CH4+Cl2CH3Cl+HCl,·Cl起催化作用,故一旦光照下产生·Cl,反应即可进行完全,C错误。
5. B 无水CaCl2增重的7.2 g是水的质量,10.0 g X中氢元素的物质的量为×2=0.8 mol,KOH浓溶液增重的22.0 g是二氧化碳的质量,10.0 g X中碳元素的物质的量为=0.5 mol,根据质量守恒,氧元素的质量为10.0 g-0.8 mol×1 g·mol-1-0.5 mol×12 g·mol-1=3.2 g。则氧元素的物质的量为=0.2 mol,则该分子中碳、氢、氧原子的个数之比为0.5 mol∶0.8 mol∶0.2 mol=5∶8∶2,结合X的相对分子质量可知,有机物X的分子式为C5H8O2,故选B。
根据CO2的质量确定有机化合物中C的质量,根据H2O的质量确定有机化合物中H的质量,再结合总质量判断有机化合物中O的质量。
6. B 该有机物分子式为C4H10O,红外光谱显示存在甲基(—CH3),亚甲基(—CH2—)和醚键,由核磁共振氢谱可知存在两种不同化学环境的氢原子。A项有4种不同化学环境的氢原子,错误;B项有2种不同化学环境的氢原子,且存在醚键、甲基和亚甲基,正确;C项有2种不同化学环境的氢原子,但不存在醚键,错误;D项有3种不同化学环境的氢原子,错误。
7. (1) ①⑤ (2) AD (3) C4H10O ①74 C4H10O ②H 4 ③(CH3)3COH
解析:(1) 在上述各种研究方法中,蒸馏、重结晶、萃取、过滤是有机物分离或提纯的方法,核磁共振氢谱、红外光谱常用于分子结构确定。(2) 其核磁共振氢谱中只有一个吸收峰,说明有机物分子中只有一类氢原子。CH3CH3分子中只有一类氢原子,A正确;CH3COOH分子中含有两类氢原子,B错误;CH3COOCH3分子中含有两类氢原子,C错误;CH3OCH3分子中只有一类氢原子,D正确。(3) 碳的质量分数是64.86%,氢的质量分数是13.51%,因此氧元素质量分数是21.63%,则该物质中碳、氢、氧原子个数之比为∶∶=4∶10∶1,所以其实验式为C4H10O。①根据质谱图知,其相对分子质量是74,结合其实验式知其分子式为C4H10O。②甲为一元饱和醇,则可能的结构有4种,结构简式为HOCH2CH2CH2CH3、CH3CH(OH)CH2CH3、(CH3)2CHCH2OH、(CH3)3COH。③甲的核磁共振氢谱图中出现2组峰,说明该结构中有2种氢原子,则结构简式为(CH3)3COH。
8. A 由质谱图可知该有机物相对分子质量为106,A错误;核磁共振氢谱图中出现2组峰,则该有机物中有2种不同化学环境的氢原子,B正确;由红外光谱可获得该有机物的化学键或官能团信息,该有机物中含有碳氢键、苯环、苯环连碳,C正确;根据红外光谱、核磁共振氢谱图,质谱图分析得到该有机物为对二甲苯,D正确。
9. D 甲装置吸收水蒸气,应该盛放无水氯化钙,碱石灰既能吸收水蒸气也能吸收二氧化碳,A错误;生成的二氧化碳和水的质量分别是3.52 g和0.9 g,物质的量分别是=0.08 mol、=0.05 mol,因此C和H的原子个数之比是0.08∶0.1=4∶5,该烃的实验式是C4H5,B错误;停止加热后,应继续通入O2,把生成的气体全部排入后续的装置中,以便充分吸收,C错误;为防止空气中的水蒸气和二氧化碳被吸收,乙装置后加装一个盛碱石灰的干燥管,实验结果会更准确,D正确。
10. B 从质谱图可以得出质荷比最大是136,相对分子质量是136,摩尔质量为136 g·mol-1,A错误;6.8 g X的物质的量为0.05 mol,燃烧后得到3.6 g水即0.4 mol H原子,标况下8.96 L CO2即0.4 mol C原子,O原子的物质的量为=0.1 mol,得出分子式为C8H8O2,核磁共振氢谱有四个峰,面积比为3∶2∶2∶1,说明结构中有四种氢原子,H原子个数比为3∶2∶2∶1,由红外光谱图得出分子结构中有苯环、碳氧双键,碳氧单键等结构,X分子只有一个苯环且苯环上只有一个取代基,符合条件的结构只有,B正确,C错误;X不可能是苯乙酸,苯乙酸不符合四种等效氢原子个数比是3∶2∶2∶1,且苯乙酸中也没有C—O—C结构,D错误。
11. (1) 含C、H或C、H、O元素
(2) 得到较大的晶体,减少吸附的杂质
(3) 吸收燃烧后产生的H2O(g)
(4) g→f→e→h→i→c(d)→d(c)→a(b)
(5) 5H2O2+2MnO+6H+===5O2↑+2Mn2++8H2O
(6) 减小
(7) 吸收空气中的二氧化碳和水蒸气
(8) B管增重0.36 g,则n(H2O)==0.02 mol,A管增重1.76 g,则n(CO2)==0.04 mol,n(O)==0.08 mol,n(C)∶n(H)∶n(O)=0.04 mol∶0.04 mol∶0.08 mol=1∶1∶2,该有机物的最简式为CHO2。
解析:(1) 用F装置加热固体样品,用碱石灰测定二氧化碳的质量,用无水氯化钙测定水的质量,根据有机物的质量,可以确定有机物中是否含有氧元素,故该方法可以测定含C、H、O或C、H元素的固态有机物。(2) 为了得到较大的晶体,减少吸附的杂质,所以要在静置条件下结晶。(3) B管的作用是吸收有机物燃烧产生的水蒸气。(4) D装置中生成氧气,先通过装有浓硫酸的C装置除去水蒸气,然后进入F装置与样品反应,生成物先通过B装置吸收反应产生的水蒸气,再通过A装置吸收产生的二氧化碳,故连接顺序为g→f→e→h→i→c(或d)→d(或c)→a(或b)。(5) E中装有过氧化氢,过氧化氢与酸性高锰酸钾溶液发生氧化还原反应。(6) CuO网可与有机物不完全燃烧产生的CO反应生成CO2,如果去掉CuO网,可能存在部分CO不能被A装置吸收,导致A管增重减小。(7) 空气中的二氧化碳和水蒸气会进入A中,影响二氧化碳质量的测定,故A后再增加一个A装置,其主要目的是吸收空气中的二氧化碳和水蒸气。
1. (淮安期中)下列测定手段中,主要用来测定有机物官能团的是( )
A. 质谱法 B. 李比希燃烧实验
C. 红外光谱 D. 核磁共振氢谱
2. (南通海安高级中学月考)下列有机物的核磁共振氢谱有6组峰的是( )
3. (江门第一中学高段考)如图是一种分子式为C4H8O2的有机化合物的红外光谱图,则该有机化合物的结构简式是( )
A. CH3CH2CH2COOH B. CH3COOCH2CH3
C. CH3CH(CH3)COOH D. HCOOCH(CH3)2
4. CH4与Cl2反应的机理是①Cl2·Cl+·Cl;②·Cl+CH4―→·CH3+HCl;③·CH3+Cl2―→·Cl+CH3Cl。
下列说法正确的是( )
A. 可以得到纯净的CH3Cl
B. 产物中最多的是HCl
C. 该反应需一直光照
D. 产物中CH3Cl、CH2Cl2、CHCl3、CCl4物质的量相等
5. (盐城响水中学期初检测)X的相对分子质量为100,将10.0 g X在足量O2中充分燃烧,并将其产物依次通过足量的无水CaCl2和KOH浓溶液,发现无水CaCl2增重7.2 g,KOH浓溶液增重22.0 g。该有机物X的分子式为( )
A. C6H12O B. C5H8O2 C. C7H16 D. CaCO3
6. (宿迁期中)某有机物A的分子式为C4H10O,对其结构进行光谱分析如图所示,则A的结构简式为( )
A. CH3OCH2CH2CH3 B. CH3CH2OCH2CH3
C. (CH3)3COH D. (CH3)2CHOCH3
7. (南通海安高级中学月考)完成下列问题。
(1) 研究有机物的方法有很多,常用的有①核磁共振氢谱、②蒸馏、③重结晶、④萃取、⑤红外光谱、⑥过滤,其中用于分子结构确定的有________(填序号)。
(2) 下列物质中,其核磁共振氢谱中只有一个吸收峰的是________(填字母)。
A. CH3CH3 B. CH3COOH
C. CH3COOCH3 D. CH3OCH3
(3) 某含碳、氢、氧三种元素的有机物甲,经燃烧分析实验测定其碳的质量分数是64.86%,氢的质量分数是13.51%,则甲的实验式(最简式)是________。
①下图是该有机物甲的质谱图,则其相对分子质量为________,分子式为________。
②确定甲的官能团:通过实验可知甲中一定含有羟基,写出羟基的电子式____________;甲可能的结构有________种。
③经测定有机物甲的核磁共振氢谱如图所示,则甲的结构简式为___________。
8. 某有机物常用于生产聚酯纤维和树脂,是一种重要的化工合成原料,使用现代仪器对该有机物的结构进行测定,相关谱图如下。下列有关说法错误的是( )
A. 由质谱图可知该有机物相对分子质量为91
B. 由核磁共振氢谱可知该有机物中有2种不同化学环境的氢原子
C. 由红外光谱可获得该有机物的化学键或官能团信息
D. 综合以上信息可知该有机物为对二甲苯
9. (黄冈期末)某同学尝试利用李比希法测定液态烃X的实验式,设计了如下实验:准确称取1.06 g样品并置于试样盒中,加热样品,使蒸气通过氧化铜(催化剂),准确称量生成的二氧化碳和水的质量,分别是3.52 g和0.9 g。下列说法正确的是( )
A. 甲处放置碱石灰
B. 该烃的实验式是C8H10
C. 停止加热后,立即停止通入O2,防止浪费
D. 乙装置后加装一个盛碱石灰的干燥管,实验结果会更准确
10. (大同浑源中学期末)将6.8 g的X完全燃烧生成3.6 g的H2O和8.96 L(标准状况)的CO2。X的核磁共振氢谱有4个峰且面积之比为3∶2∶2∶1。X分子中只含一个苯环且苯环上只有一个取代基,其质谱图、核磁共振氢谱、红外光谱如下图所示。下列关于X的叙述正确的是( )
A. 化合物X的摩尔质量为106 g· mol-1
B. 化合物X为
C. 化合物X可能的结构有2种
D. 化合物X可能是苯乙酸
11. (徐州沛县学情调研)通常用燃烧的方法测定有机物的分子式,可在燃烧室内将有机物样品与纯氧在电炉加热下充分燃烧,根据产品的质量确定有机物的组成。如图所示的是用燃烧法确定有机物分子式的常用装置。
现准确称取1.8 g样品(只含C、H、O三种元素中的两种或三种),经燃烧后A管增重1.76 g,B管增重0.36 g。请回答:
(1) 用该方法可测定含有哪些元素的有机物:____________________。
(2) 分离和提纯固体有机物的一个操作方法是重结晶,在静置条件下结晶的原因是________________________________。
(3) A、B管内均盛有固态试剂,B管的作用是____________________________。
(4) 根据气流方向将装置进行连接,连接的顺序是_______________________
(填接口字母,用“→”连接)。
(5) E中应盛装的试剂能使硫酸酸化的高锰酸钾溶液褪色,写出该反应的离子方程式______________________________________________________。
(6) 如果把CuO网去掉,A管增重将________(填“增大”“减小”或“不变”)。
(7) 某同学认为A和空气相通,会影响测定结果准确性,应在A后再增加一个A装置,其主要目的是______________________________。
(8) 该有机物的最简式为__________(写出计算过程)。
基础小练3 有机化合物组成和结构的研究
1. C 质谱法测定有机物的相对分子质量,A错误;李比希燃烧实验确定有机物的实验式,B错误;红外光谱测定有机物的化学键和官能团,C正确;核磁共振氢谱测定有机物中氢原子的化学环境,D错误。
2. A 分子结构不对称,含6种不同化学环境的H,核磁共振氢谱有6组峰,A正确;分子中含4种不同化学环境的H,核磁共振氢谱有4组峰,B错误;分子中含4种不同化学环境的H,核磁共振氢谱有4组峰,C错误;苯中的六个氢原子是完全相同的,核磁共振氢谱有1组峰,D错误。
等效氢法判断同分异构体的数目
①同一碳原子上的氢原子等效;
②同一碳原子上的甲基上的氢原子等效;
③位于对称位置上的碳原子上的氢原子等效。
3. B 由红外光谱图可看出该分子中有不对称—CH3,因此该分子中有2个—CH3,由图也可以看出含有碳氧双键和C—O—C键。所以可能的结构简式为CH3COOCH2CH3或CH3CH2COOCH3,故选B。
①质谱——可快速、准确测定有机物的相对分子质量。
②红外光谱——可以获得分子中含有何种化学键或官能团的信息。
③核磁共振氢谱——可推知有机物分子中有几种不同类型的氢原子及它们的数目之比。
4. B 由反应机理②知,·Cl与烃中的氢原子结合生成HCl,故产物中有机物除CH3Cl外还有CH2Cl2、CHCl3、CCl4,物质的量无法确定,最多的产物为HCl,A、D错误,B正确;由反应机理②③知,CH4+Cl2CH3Cl+HCl,·Cl起催化作用,故一旦光照下产生·Cl,反应即可进行完全,C错误。
5. B 无水CaCl2增重的7.2 g是水的质量,10.0 g X中氢元素的物质的量为×2=0.8 mol,KOH浓溶液增重的22.0 g是二氧化碳的质量,10.0 g X中碳元素的物质的量为=0.5 mol,根据质量守恒,氧元素的质量为10.0 g-0.8 mol×1 g·mol-1-0.5 mol×12 g·mol-1=3.2 g。则氧元素的物质的量为=0.2 mol,则该分子中碳、氢、氧原子的个数之比为0.5 mol∶0.8 mol∶0.2 mol=5∶8∶2,结合X的相对分子质量可知,有机物X的分子式为C5H8O2,故选B。
根据CO2的质量确定有机化合物中C的质量,根据H2O的质量确定有机化合物中H的质量,再结合总质量判断有机化合物中O的质量。
6. B 该有机物分子式为C4H10O,红外光谱显示存在甲基(—CH3),亚甲基(—CH2—)和醚键,由核磁共振氢谱可知存在两种不同化学环境的氢原子。A项有4种不同化学环境的氢原子,错误;B项有2种不同化学环境的氢原子,且存在醚键、甲基和亚甲基,正确;C项有2种不同化学环境的氢原子,但不存在醚键,错误;D项有3种不同化学环境的氢原子,错误。
7. (1) ①⑤ (2) AD (3) C4H10O ①74 C4H10O ②H 4 ③(CH3)3COH
解析:(1) 在上述各种研究方法中,蒸馏、重结晶、萃取、过滤是有机物分离或提纯的方法,核磁共振氢谱、红外光谱常用于分子结构确定。(2) 其核磁共振氢谱中只有一个吸收峰,说明有机物分子中只有一类氢原子。CH3CH3分子中只有一类氢原子,A正确;CH3COOH分子中含有两类氢原子,B错误;CH3COOCH3分子中含有两类氢原子,C错误;CH3OCH3分子中只有一类氢原子,D正确。(3) 碳的质量分数是64.86%,氢的质量分数是13.51%,因此氧元素质量分数是21.63%,则该物质中碳、氢、氧原子个数之比为∶∶=4∶10∶1,所以其实验式为C4H10O。①根据质谱图知,其相对分子质量是74,结合其实验式知其分子式为C4H10O。②甲为一元饱和醇,则可能的结构有4种,结构简式为HOCH2CH2CH2CH3、CH3CH(OH)CH2CH3、(CH3)2CHCH2OH、(CH3)3COH。③甲的核磁共振氢谱图中出现2组峰,说明该结构中有2种氢原子,则结构简式为(CH3)3COH。
8. A 由质谱图可知该有机物相对分子质量为106,A错误;核磁共振氢谱图中出现2组峰,则该有机物中有2种不同化学环境的氢原子,B正确;由红外光谱可获得该有机物的化学键或官能团信息,该有机物中含有碳氢键、苯环、苯环连碳,C正确;根据红外光谱、核磁共振氢谱图,质谱图分析得到该有机物为对二甲苯,D正确。
9. D 甲装置吸收水蒸气,应该盛放无水氯化钙,碱石灰既能吸收水蒸气也能吸收二氧化碳,A错误;生成的二氧化碳和水的质量分别是3.52 g和0.9 g,物质的量分别是=0.08 mol、=0.05 mol,因此C和H的原子个数之比是0.08∶0.1=4∶5,该烃的实验式是C4H5,B错误;停止加热后,应继续通入O2,把生成的气体全部排入后续的装置中,以便充分吸收,C错误;为防止空气中的水蒸气和二氧化碳被吸收,乙装置后加装一个盛碱石灰的干燥管,实验结果会更准确,D正确。
10. B 从质谱图可以得出质荷比最大是136,相对分子质量是136,摩尔质量为136 g·mol-1,A错误;6.8 g X的物质的量为0.05 mol,燃烧后得到3.6 g水即0.4 mol H原子,标况下8.96 L CO2即0.4 mol C原子,O原子的物质的量为=0.1 mol,得出分子式为C8H8O2,核磁共振氢谱有四个峰,面积比为3∶2∶2∶1,说明结构中有四种氢原子,H原子个数比为3∶2∶2∶1,由红外光谱图得出分子结构中有苯环、碳氧双键,碳氧单键等结构,X分子只有一个苯环且苯环上只有一个取代基,符合条件的结构只有,B正确,C错误;X不可能是苯乙酸,苯乙酸不符合四种等效氢原子个数比是3∶2∶2∶1,且苯乙酸中也没有C—O—C结构,D错误。
11. (1) 含C、H或C、H、O元素
(2) 得到较大的晶体,减少吸附的杂质
(3) 吸收燃烧后产生的H2O(g)
(4) g→f→e→h→i→c(d)→d(c)→a(b)
(5) 5H2O2+2MnO+6H+===5O2↑+2Mn2++8H2O
(6) 减小
(7) 吸收空气中的二氧化碳和水蒸气
(8) B管增重0.36 g,则n(H2O)==0.02 mol,A管增重1.76 g,则n(CO2)==0.04 mol,n(O)==0.08 mol,n(C)∶n(H)∶n(O)=0.04 mol∶0.04 mol∶0.08 mol=1∶1∶2,该有机物的最简式为CHO2。
解析:(1) 用F装置加热固体样品,用碱石灰测定二氧化碳的质量,用无水氯化钙测定水的质量,根据有机物的质量,可以确定有机物中是否含有氧元素,故该方法可以测定含C、H、O或C、H元素的固态有机物。(2) 为了得到较大的晶体,减少吸附的杂质,所以要在静置条件下结晶。(3) B管的作用是吸收有机物燃烧产生的水蒸气。(4) D装置中生成氧气,先通过装有浓硫酸的C装置除去水蒸气,然后进入F装置与样品反应,生成物先通过B装置吸收反应产生的水蒸气,再通过A装置吸收产生的二氧化碳,故连接顺序为g→f→e→h→i→c(或d)→d(或c)→a(或b)。(5) E中装有过氧化氢,过氧化氢与酸性高锰酸钾溶液发生氧化还原反应。(6) CuO网可与有机物不完全燃烧产生的CO反应生成CO2,如果去掉CuO网,可能存在部分CO不能被A装置吸收,导致A管增重减小。(7) 空气中的二氧化碳和水蒸气会进入A中,影响二氧化碳质量的测定,故A后再增加一个A装置,其主要目的是吸收空气中的二氧化碳和水蒸气。
