2.4.1 羧酸 同步课时作业(含解析)高二化学鲁科版(2019)选择性必修三
文档属性
| 名称 | 2.4.1 羧酸 同步课时作业(含解析)高二化学鲁科版(2019)选择性必修三 |  | |
| 格式 | docx | ||
| 文件大小 | 443.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-04-30 15:36:10 | ||
图片预览




文档简介
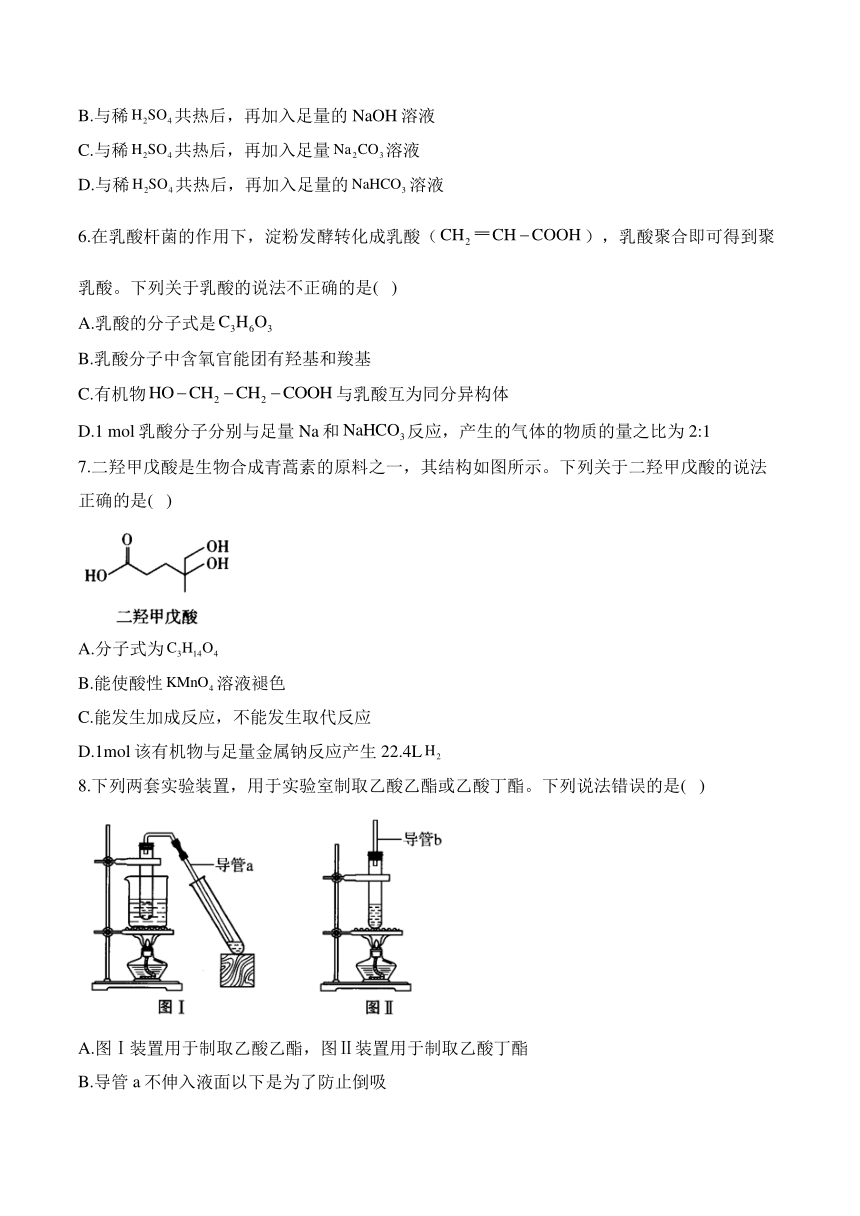
2.4.1 羧酸——高二化学鲁科版(2019)选择性必修三同步课时作业
1.分子式为的羧酸类物质的同分异构体数目为( )
A.6种 B.7种 C.8种 D.9种
2.丙烯酸()可能发生的反应有( )
①加成反应;②酯化反应;③中和反应;④氧化反应。
A.①③ B.①③④ C.①②③④ D.①④
3.有机物,的名称是( )
A.2-甲基-3-乙基丁酸
B.2,3-二甲基戊酸
C.3,4-二甲基戊酸
D.3,4-二甲基丁酸
4.连花清瘟因含连翘、金银花而得名,其有效成分绿原酸的结构简式如图所示。下列有关绿原酸的说法正确的是( )
A.绿原酸的分子式为
B.1个绿原酸分子中含有4个手性碳原子
C.1 mol绿原酸分子可消耗3 mol NaOH
D.绿原酸分子中含氧官能团有羟基、酯基、羧基、醚键
5.已知酸性:,现要将转变为,可行的方法是( )
A.与足量的NaOH溶液共热,再通入足量的气体
B.与稀共热后,再加入足量的NaOH溶液
C.与稀共热后,再加入足量溶液
D.与稀共热后,再加入足量的溶液
6.在乳酸杆菌的作用下,淀粉发酵转化成乳酸(),乳酸聚合即可得到聚乳酸。下列关于乳酸的说法不正确的是( )
A.乳酸的分子式是
B.乳酸分子中含氧官能团有羟基和羧基
C.有机物与乳酸互为同分异构体
D.1 mol乳酸分子分别与足量Na和反应,产生的气体的物质的量之比为2:1
7.二羟甲戊酸是生物合成青蒿素的原料之一,其结构如图所示。下列关于二羟甲戊酸的说法正确的是( )
A.分子式为
B.能使酸性溶液褪色
C.能发生加成反应,不能发生取代反应
D.1mol该有机物与足量金属钠反应产生22.4L
8.下列两套实验装置,用于实验室制取乙酸乙酯或乙酸丁酯。下列说法错误的是( )
A.图Ⅰ装置用于制取乙酸乙酯,图Ⅱ装置用于制取乙酸丁酯
B.导管a不伸入液面以下是为了防止倒吸
C.都可用饱和溶液洗去酯中的酸和醇
D.乙酸丁酯可能的结构共有6种
9.一定质量的某有机物与足量金属钠反应,可得气体。相同质量的该有机物与适量的浓溶液反应,可得气体。已知在同温、同压下和不相同,则该有机物可能是( )
①
②
③
④
A.①②
B.②③
C.③④
D.①④
10.用标记的与乙酸反应制取乙酸乙酯,当反应达到平衡时,下列说法正确的是( )
A.只存在于乙酸乙酯中
B.存在于水、乙酸、乙醇以及乙酸乙酯中
C.存在于乙酸乙酯、乙醇中
D.有的乙醇分子可能不含
11.已知伞形酮可用雷琐苯乙酮和苹果酸()在一定条件下反应制得,下列说法正确的是( )
A.1mol雷琐苯乙酮最多能与3mol氢气发生加成反应
B.两分子苹果酸的一种缩合产物是
C.1mol产物伞形酮与溴水反应,最多可消耗3 mol ,且均发生取代反应
D.反应中涉及的三种有机物都能跟溶液发生显色反应
12.荧光黄的结构如图所示,下列说法正确的是( )
A.其分子式为,分子中存在3种官能团
B.1 mol荧光黄分子最多可消耗1 mol
C.分子中所有碳原子可共平面,且能与发生显色反应
D.1 mol荧光黄分子与足量溴水反应,最多可消耗2 mol
13.乙酸分子的结构式为,下列反应及断键部位不正确的是( )
A.乙酸与NaOH溶液的反应,断裂②键
B.乙酸与乙醇发生酯化反应,断裂②键
C.在红磷存在时,与的反应:,断裂③键
D.乙酸变成乙酸酐的反应:,断裂①②键
14.红葡萄酒密封储存时间越长,质量越好,原因之一是储存过程中生成了酯。在实验室可用如图所示的装置制取乙酸乙酯。请回答下列问题。
(1)制取乙酸乙酯时,混合溶液的加入顺序为_______________________________。
(2)试管a中加入几块碎瓷片的作用是___________,发生反应的化学方程式_______________________,为反应类型为__________。
(3)反应时生成的乙酸乙酯的密度比水________,可以闻到________味。
(4)装置b中通蒸气的导管不插入溶液中,目的是_______________________________。
(5)饱和溶液的作用是____________(填字母)。
A.中和浓硫酸
B.中和乙酸并吸收乙醇
C.乙酸乙酯在饱和溶液中的溶解度比在水中更小,有利于分层析出
D.加速酯的生成,提高其产率
15.化合物A最早发现于酸牛奶中,它是人体内糖代谢的中间体,可由马铃薯、玉米淀粉等发酵制得,A的钙盐是人们喜爱的补钙剂之一。A在某种催化剂的存在下进行氧化,其产物不能发生银镜反应。在浓硫酸存在下,A可发生如下所示的反应。
试写出:
(1)化合物A、B、D的结构简式:A________,B________,D________。
(2)化学方程式:
A→E________,
A→F________。
(3)反应类型:A→E________,A→F________。
答案以及解析
1.答案:C
解析:判断羧酸类的物质的同分异构体时,可将改写为,戊基有8种结构,故的羧酸类物质的同分异构体数目为8种,C项正确。
2.答案:C
解析:丙烯酸()中含有碳碳双键和羧基两种官能团,碳碳双键能发生加成反应与氧化反应,羧基能发生中和反应与酯化反应,①②③④均符合,故选C。
3.答案:B
解析:选含有—COOH的最长碳链为主链,从—COOH上碳原子开始编号即得,2、3号碳原子上各有一个甲基,因此该物质的名称为2,3-二甲基戊酸,B项正确。
4.答案:B
解析:绿原酸的分子式为,A错误;连接4个不同原子或原子团的碳原子为手性碳原子,右侧六元环上与O原子相连的4个C原子均为手性碳原子,共有4个,B正确;绿原酸分子中的酚羟基、羧基、酯基均可与NaOH反应,因此1 mol绿原酸分子可消耗4mol NaOH,C错误;绿原酸中含氧官能团有羟基、酯基、羧基,但无醚键,D错误。
5.答案:AD
解析:A项,;B项,;C项,;D项,。
6.答案:D
解析:乳酸的分子式是,A正确;乳酸分子中含氧官能团有羟基和羧基,B正确;该有机物与乳酸的分子式相同,但结构不同,二者互为同分异构体,C正确:乳酸中的羟基、羧基均能与Na反应,1 mol乳酸与足量Na反应产生1 mol ,只有羧基能与反应生成,1 mol乳酸和反应产生1 mol ,则产生的气体的物质的量之比为1:1,D错误。
7.答案:B
解析:由结构可知分子式为,故A错误;该分子中含有羟基,且与羟基直接相连的碳原子上有氢,具有乙醇的结构特点,可被酸性高锰酸钾氧化,故B正确;该分子中含有羧基,羧基不能发生加成反应,可发生取代反应,故C错误;1mol该有机物与足量金属钠反应可生成1.5mol氢气,但状况未知,不能计算体积,故D错误。
8.答案:D
解析:乙酸乙酯的沸点低,易挥发,可在右侧试管中收集,故采取边反应边蒸馏的方法制备,用图Ⅰ装置,但乙酸丁酯的相对分子质量较大,沸点较高,故采取直接回流的方法制备,用图Ⅱ装置,A正确;由于乙醇、乙酸和水互溶,则导管a不伸入液面以下是为了防止倒吸,B正确;饱和溶液能溶解醇、中和酸,并且还能降低酯的溶解度,所以可用饱和溶液洗去酯中的酸和醇,C正确;乙酸只有1种结构,丁醇相当于丁烷中的1个H原子被羟基取代,丁烷有正丁烷和异丁烷,两分子中均含有2种不同化学环境的氢原子,则丁醇有4种结构,因此乙酸丁酯可能的结构共有4种,D错误。
9.答案:D
解析:①1mol该物质与钠反应可生成1mol氢气,与碳酸钠反应可生成0.5mol二氧化碳,两者不相同,正确;②1mol该物质与钠反应可生成1mol氢气,与碳酸钠反应可生成1mol二氧化碳,两者相同,错误;③1mol该物质与钠反应可生成0.5mol氢气,与碳酸钠反应可生成0.5mol二氧化碳,两者相同,错误;④1mol该物质与钠反应可生成1.5mol氢气,与碳酸钠反应可生成1mol二氧化碳,两者不相同,正确。综上分析可知,D项正确。
10.答案:C
解析:发生酯化反应时,酸脱羟基醇脱氢,由于酯化反应为可逆反应,所以存在于生成物乙酸乙酯和反应物乙醇中,水、乙酸中不存在,故选C。
11.答案:B
解析:1mol苯环与3mol氢气加成,1mol羰基与1mol氢气加成,故1mol雷琐苯乙酮最多能与4mol氢气发生加成反应,A错误;苹果酸()同时含有羟基和羧基,两分子苹果酸可发生酯化反应生成,B正确;含酚羟基,酚羟基邻位的2个H可被2个Br取代,同时也含一个碳碳双键,可和一分子溴发生加成反应,故1mol产物伞形酮与溴水反应,最多可消耗3mol ,发生了取代反应、加成反应,C错误;能跟溶液发生显色反应的物质需要含酚羟基,苹果酸不含酚羟基,不能和溶液发生显色反应,D错误。
12.答案:C
解析:荧光黄的分子式为,含有的官能团为酚羟基、醚键、碳碳双键、羰基、羧基,存在5种官能团,A错误;酚羟基和以1:1反应,羧基和最多以1:1反应,所以1 mol荧光黄分子最多消耗2 mol ,B错误;苯环和碳碳双键中所有原子共平面,单键可以旋转,所以该分子中所有碳原子可能共平面,含有酚羟基,能与发生显色反应,C正确;碳碳双键能和发生加成反应,苯环上酚羟基邻位上的氢原子能和发生取代反应,所以1 mol荧光黄分子最多消耗5 mol ,D错误。
13.答案:A
解析:A项,羧基中氢氧键的极性较强,在溶液中易电离出氢离子,因此与氢氧化钠反应时断裂的是①键,错误;B项,酯化反应的机理是“酸脱羟基醇脱氢”,因此酯化反应时断裂的是②键,正确;C项,受羧基的影响,活性增强因此发生取代反应时断裂的是③键,正确;D项,由题给反应可知,一个乙酸分子断裂的是①键,另一个乙酸分子断裂的是②键,正确。
14.答案:(1)先加乙醇,再加浓硫酸,最后加乙酸
(2)防止液浓硫酸体暴沸;;取代反应(或酯化反应)
(3)小;香(或芳香气)
(4)防止倒吸
(5)BC
解析:乙醇与乙酸发生酯化反应生成乙酸乙酯,生成的乙酸乙酯的密度小于水,不溶于水,低级酯具有芳香气味,试管b中盛放饱和溶液,可除杂并降低乙酸乙酯的溶解度。
(1)浓硫酸溶于水放热,且密度大于水,应将密度大的液体加入密度小的液体中,则混合溶液的加入顺序是先加入乙醇,再加入浓硫酸,最后加入乙酸。
(2)试管a中加入几块碎瓷片,可防止液体加热时剧烈沸腾。乙酸和乙醇发生酯化反应生成乙酸乙酯,属于取代反应。
(3)乙酸乙酯的密度比水的小,乙酸乙酯具有芳香气味,可以闻到香味。
(4)装置b中通蒸气的导管不插入溶液中,目的是防止倒吸。
(5)饱和溶液可以中和挥发出来的乙酸,使之转化为易溶于水的乙酸钠,可以溶解挥发出的乙醇,降低乙酸乙酯在水中的溶解度,便于分层得到酯,故选BC。
15.答案:(1)
(2)
(3)消去反应;取代反应(或酯化反应)
解析:(1)A在浓硫酸存在下既能和乙醇反应,又能和乙酸反应,说明A中既有羧基又有羟基,A催化氧化的产物不能发生银镜反应,说明羟基不在碳链的端点,根据A的化学式,可推知A的结构简式为。根据反应条件可知B为、D为、E为、F为。
(3)A→E和A→F的反应类型分别为消去反应和取代反应(或酯化反应)。
1.分子式为的羧酸类物质的同分异构体数目为( )
A.6种 B.7种 C.8种 D.9种
2.丙烯酸()可能发生的反应有( )
①加成反应;②酯化反应;③中和反应;④氧化反应。
A.①③ B.①③④ C.①②③④ D.①④
3.有机物,的名称是( )
A.2-甲基-3-乙基丁酸
B.2,3-二甲基戊酸
C.3,4-二甲基戊酸
D.3,4-二甲基丁酸
4.连花清瘟因含连翘、金银花而得名,其有效成分绿原酸的结构简式如图所示。下列有关绿原酸的说法正确的是( )
A.绿原酸的分子式为
B.1个绿原酸分子中含有4个手性碳原子
C.1 mol绿原酸分子可消耗3 mol NaOH
D.绿原酸分子中含氧官能团有羟基、酯基、羧基、醚键
5.已知酸性:,现要将转变为,可行的方法是( )
A.与足量的NaOH溶液共热,再通入足量的气体
B.与稀共热后,再加入足量的NaOH溶液
C.与稀共热后,再加入足量溶液
D.与稀共热后,再加入足量的溶液
6.在乳酸杆菌的作用下,淀粉发酵转化成乳酸(),乳酸聚合即可得到聚乳酸。下列关于乳酸的说法不正确的是( )
A.乳酸的分子式是
B.乳酸分子中含氧官能团有羟基和羧基
C.有机物与乳酸互为同分异构体
D.1 mol乳酸分子分别与足量Na和反应,产生的气体的物质的量之比为2:1
7.二羟甲戊酸是生物合成青蒿素的原料之一,其结构如图所示。下列关于二羟甲戊酸的说法正确的是( )
A.分子式为
B.能使酸性溶液褪色
C.能发生加成反应,不能发生取代反应
D.1mol该有机物与足量金属钠反应产生22.4L
8.下列两套实验装置,用于实验室制取乙酸乙酯或乙酸丁酯。下列说法错误的是( )
A.图Ⅰ装置用于制取乙酸乙酯,图Ⅱ装置用于制取乙酸丁酯
B.导管a不伸入液面以下是为了防止倒吸
C.都可用饱和溶液洗去酯中的酸和醇
D.乙酸丁酯可能的结构共有6种
9.一定质量的某有机物与足量金属钠反应,可得气体。相同质量的该有机物与适量的浓溶液反应,可得气体。已知在同温、同压下和不相同,则该有机物可能是( )
①
②
③
④
A.①②
B.②③
C.③④
D.①④
10.用标记的与乙酸反应制取乙酸乙酯,当反应达到平衡时,下列说法正确的是( )
A.只存在于乙酸乙酯中
B.存在于水、乙酸、乙醇以及乙酸乙酯中
C.存在于乙酸乙酯、乙醇中
D.有的乙醇分子可能不含
11.已知伞形酮可用雷琐苯乙酮和苹果酸()在一定条件下反应制得,下列说法正确的是( )
A.1mol雷琐苯乙酮最多能与3mol氢气发生加成反应
B.两分子苹果酸的一种缩合产物是
C.1mol产物伞形酮与溴水反应,最多可消耗3 mol ,且均发生取代反应
D.反应中涉及的三种有机物都能跟溶液发生显色反应
12.荧光黄的结构如图所示,下列说法正确的是( )
A.其分子式为,分子中存在3种官能团
B.1 mol荧光黄分子最多可消耗1 mol
C.分子中所有碳原子可共平面,且能与发生显色反应
D.1 mol荧光黄分子与足量溴水反应,最多可消耗2 mol
13.乙酸分子的结构式为,下列反应及断键部位不正确的是( )
A.乙酸与NaOH溶液的反应,断裂②键
B.乙酸与乙醇发生酯化反应,断裂②键
C.在红磷存在时,与的反应:,断裂③键
D.乙酸变成乙酸酐的反应:,断裂①②键
14.红葡萄酒密封储存时间越长,质量越好,原因之一是储存过程中生成了酯。在实验室可用如图所示的装置制取乙酸乙酯。请回答下列问题。
(1)制取乙酸乙酯时,混合溶液的加入顺序为_______________________________。
(2)试管a中加入几块碎瓷片的作用是___________,发生反应的化学方程式_______________________,为反应类型为__________。
(3)反应时生成的乙酸乙酯的密度比水________,可以闻到________味。
(4)装置b中通蒸气的导管不插入溶液中,目的是_______________________________。
(5)饱和溶液的作用是____________(填字母)。
A.中和浓硫酸
B.中和乙酸并吸收乙醇
C.乙酸乙酯在饱和溶液中的溶解度比在水中更小,有利于分层析出
D.加速酯的生成,提高其产率
15.化合物A最早发现于酸牛奶中,它是人体内糖代谢的中间体,可由马铃薯、玉米淀粉等发酵制得,A的钙盐是人们喜爱的补钙剂之一。A在某种催化剂的存在下进行氧化,其产物不能发生银镜反应。在浓硫酸存在下,A可发生如下所示的反应。
试写出:
(1)化合物A、B、D的结构简式:A________,B________,D________。
(2)化学方程式:
A→E________,
A→F________。
(3)反应类型:A→E________,A→F________。
答案以及解析
1.答案:C
解析:判断羧酸类的物质的同分异构体时,可将改写为,戊基有8种结构,故的羧酸类物质的同分异构体数目为8种,C项正确。
2.答案:C
解析:丙烯酸()中含有碳碳双键和羧基两种官能团,碳碳双键能发生加成反应与氧化反应,羧基能发生中和反应与酯化反应,①②③④均符合,故选C。
3.答案:B
解析:选含有—COOH的最长碳链为主链,从—COOH上碳原子开始编号即得,2、3号碳原子上各有一个甲基,因此该物质的名称为2,3-二甲基戊酸,B项正确。
4.答案:B
解析:绿原酸的分子式为,A错误;连接4个不同原子或原子团的碳原子为手性碳原子,右侧六元环上与O原子相连的4个C原子均为手性碳原子,共有4个,B正确;绿原酸分子中的酚羟基、羧基、酯基均可与NaOH反应,因此1 mol绿原酸分子可消耗4mol NaOH,C错误;绿原酸中含氧官能团有羟基、酯基、羧基,但无醚键,D错误。
5.答案:AD
解析:A项,;B项,;C项,;D项,。
6.答案:D
解析:乳酸的分子式是,A正确;乳酸分子中含氧官能团有羟基和羧基,B正确;该有机物与乳酸的分子式相同,但结构不同,二者互为同分异构体,C正确:乳酸中的羟基、羧基均能与Na反应,1 mol乳酸与足量Na反应产生1 mol ,只有羧基能与反应生成,1 mol乳酸和反应产生1 mol ,则产生的气体的物质的量之比为1:1,D错误。
7.答案:B
解析:由结构可知分子式为,故A错误;该分子中含有羟基,且与羟基直接相连的碳原子上有氢,具有乙醇的结构特点,可被酸性高锰酸钾氧化,故B正确;该分子中含有羧基,羧基不能发生加成反应,可发生取代反应,故C错误;1mol该有机物与足量金属钠反应可生成1.5mol氢气,但状况未知,不能计算体积,故D错误。
8.答案:D
解析:乙酸乙酯的沸点低,易挥发,可在右侧试管中收集,故采取边反应边蒸馏的方法制备,用图Ⅰ装置,但乙酸丁酯的相对分子质量较大,沸点较高,故采取直接回流的方法制备,用图Ⅱ装置,A正确;由于乙醇、乙酸和水互溶,则导管a不伸入液面以下是为了防止倒吸,B正确;饱和溶液能溶解醇、中和酸,并且还能降低酯的溶解度,所以可用饱和溶液洗去酯中的酸和醇,C正确;乙酸只有1种结构,丁醇相当于丁烷中的1个H原子被羟基取代,丁烷有正丁烷和异丁烷,两分子中均含有2种不同化学环境的氢原子,则丁醇有4种结构,因此乙酸丁酯可能的结构共有4种,D错误。
9.答案:D
解析:①1mol该物质与钠反应可生成1mol氢气,与碳酸钠反应可生成0.5mol二氧化碳,两者不相同,正确;②1mol该物质与钠反应可生成1mol氢气,与碳酸钠反应可生成1mol二氧化碳,两者相同,错误;③1mol该物质与钠反应可生成0.5mol氢气,与碳酸钠反应可生成0.5mol二氧化碳,两者相同,错误;④1mol该物质与钠反应可生成1.5mol氢气,与碳酸钠反应可生成1mol二氧化碳,两者不相同,正确。综上分析可知,D项正确。
10.答案:C
解析:发生酯化反应时,酸脱羟基醇脱氢,由于酯化反应为可逆反应,所以存在于生成物乙酸乙酯和反应物乙醇中,水、乙酸中不存在,故选C。
11.答案:B
解析:1mol苯环与3mol氢气加成,1mol羰基与1mol氢气加成,故1mol雷琐苯乙酮最多能与4mol氢气发生加成反应,A错误;苹果酸()同时含有羟基和羧基,两分子苹果酸可发生酯化反应生成,B正确;含酚羟基,酚羟基邻位的2个H可被2个Br取代,同时也含一个碳碳双键,可和一分子溴发生加成反应,故1mol产物伞形酮与溴水反应,最多可消耗3mol ,发生了取代反应、加成反应,C错误;能跟溶液发生显色反应的物质需要含酚羟基,苹果酸不含酚羟基,不能和溶液发生显色反应,D错误。
12.答案:C
解析:荧光黄的分子式为,含有的官能团为酚羟基、醚键、碳碳双键、羰基、羧基,存在5种官能团,A错误;酚羟基和以1:1反应,羧基和最多以1:1反应,所以1 mol荧光黄分子最多消耗2 mol ,B错误;苯环和碳碳双键中所有原子共平面,单键可以旋转,所以该分子中所有碳原子可能共平面,含有酚羟基,能与发生显色反应,C正确;碳碳双键能和发生加成反应,苯环上酚羟基邻位上的氢原子能和发生取代反应,所以1 mol荧光黄分子最多消耗5 mol ,D错误。
13.答案:A
解析:A项,羧基中氢氧键的极性较强,在溶液中易电离出氢离子,因此与氢氧化钠反应时断裂的是①键,错误;B项,酯化反应的机理是“酸脱羟基醇脱氢”,因此酯化反应时断裂的是②键,正确;C项,受羧基的影响,活性增强因此发生取代反应时断裂的是③键,正确;D项,由题给反应可知,一个乙酸分子断裂的是①键,另一个乙酸分子断裂的是②键,正确。
14.答案:(1)先加乙醇,再加浓硫酸,最后加乙酸
(2)防止液浓硫酸体暴沸;;取代反应(或酯化反应)
(3)小;香(或芳香气)
(4)防止倒吸
(5)BC
解析:乙醇与乙酸发生酯化反应生成乙酸乙酯,生成的乙酸乙酯的密度小于水,不溶于水,低级酯具有芳香气味,试管b中盛放饱和溶液,可除杂并降低乙酸乙酯的溶解度。
(1)浓硫酸溶于水放热,且密度大于水,应将密度大的液体加入密度小的液体中,则混合溶液的加入顺序是先加入乙醇,再加入浓硫酸,最后加入乙酸。
(2)试管a中加入几块碎瓷片,可防止液体加热时剧烈沸腾。乙酸和乙醇发生酯化反应生成乙酸乙酯,属于取代反应。
(3)乙酸乙酯的密度比水的小,乙酸乙酯具有芳香气味,可以闻到香味。
(4)装置b中通蒸气的导管不插入溶液中,目的是防止倒吸。
(5)饱和溶液可以中和挥发出来的乙酸,使之转化为易溶于水的乙酸钠,可以溶解挥发出的乙醇,降低乙酸乙酯在水中的溶解度,便于分层得到酯,故选BC。
15.答案:(1)
(2)
(3)消去反应;取代反应(或酯化反应)
解析:(1)A在浓硫酸存在下既能和乙醇反应,又能和乙酸反应,说明A中既有羧基又有羟基,A催化氧化的产物不能发生银镜反应,说明羟基不在碳链的端点,根据A的化学式,可推知A的结构简式为。根据反应条件可知B为、D为、E为、F为。
(3)A→E和A→F的反应类型分别为消去反应和取代反应(或酯化反应)。
