(17)3.2.1几种简单的晶体结构模型__高二化学鲁科版(2019)选择性必修二同步课时作业(含解析)
文档属性
| 名称 | (17)3.2.1几种简单的晶体结构模型__高二化学鲁科版(2019)选择性必修二同步课时作业(含解析) | 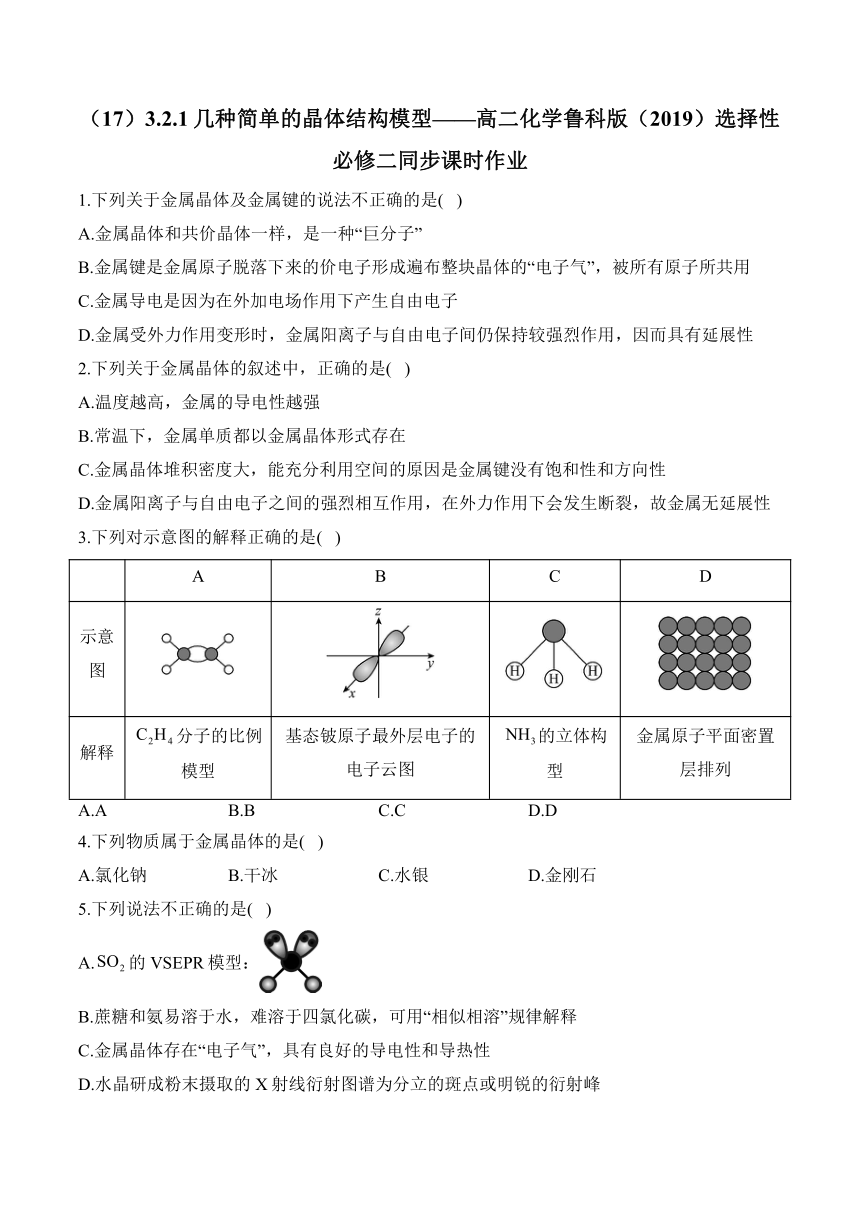 | |
| 格式 | docx | ||
| 文件大小 | 362.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁科版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-05-04 15:55:57 | ||
图片预览



文档简介
(17)3.2.1几种简单的晶体结构模型——高二化学鲁科版(2019)选择性必修二同步课时作业
1.下列关于金属晶体及金属键的说法不正确的是( )
A.金属晶体和共价晶体一样,是一种“巨分子”
B.金属键是金属原子脱落下来的价电子形成遍布整块晶体的“电子气”,被所有原子所共用
C.金属导电是因为在外加电场作用下产生自由电子
D.金属受外力作用变形时,金属阳离子与自由电子间仍保持较强烈作用,因而具有延展性
2.下列关于金属晶体的叙述中,正确的是( )
A.温度越高,金属的导电性越强
B.常温下,金属单质都以金属晶体形式存在
C.金属晶体堆积密度大,能充分利用空间的原因是金属键没有饱和性和方向性
D.金属阳离子与自由电子之间的强烈相互作用,在外力作用下会发生断裂,故金属无延展性
3.下列对示意图的解释正确的是( )
A B C D
示意图
解释 分子的比例模型 基态铍原子最外层电子的电子云图 的立体构型 金属原子平面密置层排列
A.A B.B C.C D.D
4.下列物质属于金属晶体的是( )
A.氯化钠 B.干冰 C.水银 D.金刚石
5.下列说法不正确的是( )
A.的VSEPR模型:
B.蔗糖和氨易溶于水,难溶于四氯化碳,可用“相似相溶”规律解释
C.金属晶体存在“电子气”,具有良好的导电性和导热性
D.水晶研成粉末摄取的X射线衍射图谱为分立的斑点或明锐的衍射峰
6.金属铅的晶粒大小与熔点关系如图所示。下列叙述正确的是( )
A.铅与锗位于同主族且单质晶体类型相同
B.铅晶粒越大,其熔点越低
C.铅晶体中含阳离子,必含阴离子
D.铅晶体熔点高低与晶粒表面积大小有关
7.基本概念和理论是化学思维的基石。下列叙述不正确的是( )
A.VSEPR理论认为VSEPR模型与分子的空间结构不一定相同
B.电子云图中的小黑点越密,表示电子在核外空间出现的概率密度越大
C.五彩斑斓的霓虹灯光,与原子核外电子跃迁有关,属于吸收光谐
D.“电子气理论”可以解释金属晶体的延展性,导电性和导热性
8.、、均位于第四周期Ⅶ族,属于副族元素。某合金的立方晶胞结构如图所示,已知其晶胞参数为。下列说法错误的是( )
A.单质中含有金属键 B.基态原子核外电子排布式为
C.晶体中,与原子个数比为 D.与之间的最短距离为
9.下列关于金属晶体的叙述正确的是( )
A.用铂金做首饰不能用金属键理论解释
B.固态和熔融时易导电,熔点在1000℃左右的晶体可能是金属晶体
C.Li、Na、K的熔点逐渐升高
D.金属导电和熔融电解质(或电解质溶液)导电的原理一样。
10.下列关于金属晶体的叙述不正确的是( )
A.常温下,金属单质都以金属晶体形式存在
B.金属键在一定外力作用下,不会因形变而消失
C.Ca的熔、沸点高于K的熔、沸点
D.温度越高,金属的导电性越弱
11.钾型晶体的晶胞如图所示。下列关于该晶胞的叙述正确的是( )
A.晶胞是六棱柱 B.是密置层的一种堆积方式
C.每个晶胞内含有2个原子 D.每个晶胞内含有6个原子
12.有四种不同堆积方式的金属晶体的晶胞如图所示(原子半径为r cm),下列叙述错误的是( )
A.晶胞①的空间利用率
B.金属晶体是一种“巨分子”,可能存在分子间作用力
C.晶胞中含有的原子数:晶胞③—2,晶胞
D.晶胞中原子的配位数:晶胞①—6,晶胞
13.下列叙述正确的是( )
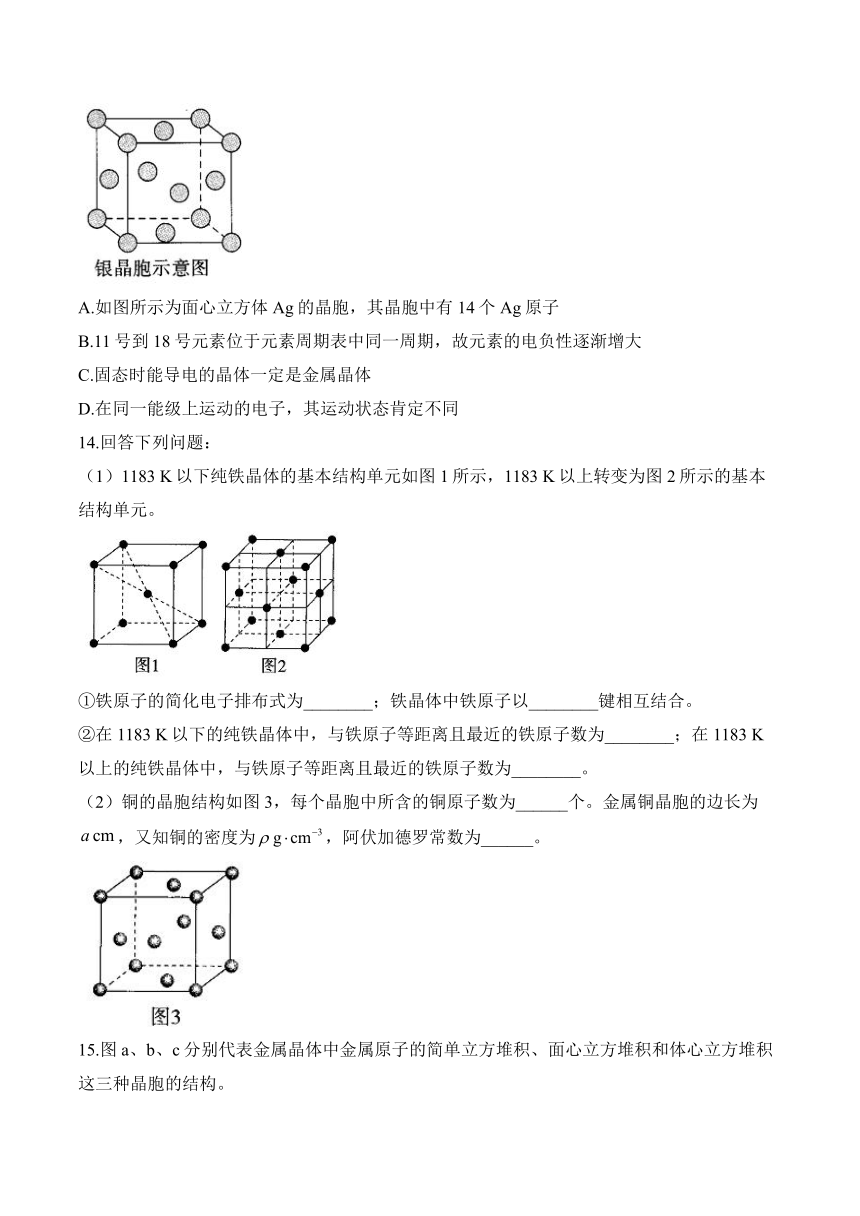
A.如图所示为面心立方体Ag的晶胞,其晶胞中有14个Ag原子
B.11号到18号元素位于元素周期表中同一周期,故元素的电负性逐渐增大
C.固态时能导电的晶体一定是金属晶体
D.在同一能级上运动的电子,其运动状态肯定不同
14.回答下列问题:
(1)1183 K以下纯铁晶体的基本结构单元如图1所示,1183 K以上转变为图2所示的基本结构单元。
①铁原子的简化电子排布式为________;铁晶体中铁原子以________键相互结合。
②在1183 K以下的纯铁晶体中,与铁原子等距离且最近的铁原子数为________;在1183 K以上的纯铁晶体中,与铁原子等距离且最近的铁原子数为________。
(2)铜的晶胞结构如图3,每个晶胞中所含的铜原子数为______个。金属铜晶胞的边长为,又知铜的密度为,阿伏加德罗常数为______。
15.图a、b、c分别代表金属晶体中金属原子的简单立方堆积、面心立方堆积和体心立方堆积这三种晶胞的结构。
(1)a、b、c三种晶胞内金属原子数目之比为___________。
(2)三种堆积方式的实质是金属阳离子的堆积方式,那么自由电子有无确切的堆积方式?________(填“有”或“无”)。
(3)一种铜、金合金晶体具有立方最密堆积的结构(见下图),在晶胞中Cū原子处于面心,Au原子处于顶点位置,则该合金中C原子与Au原子的数量之比为_______。
答案以及解析
1.答案:C
解析:A.把金属键描述为金属原子脱落的价电子形成的电子气遍布于整个晶体被所有原子共用,从而将所有原子维系在了一起,金属晶体是一种“巨大的分子”。而共价晶体以无数共价键将所有原子连接形成的巨大的网状结构,A项正确;
B.把金属键描述为金属原子脱落的价电子形成的电子气遍布于整个晶体被所有原子共用,B项正确;
C.金属中存在自由移动的电子,在外加电场的作用下可以定向移动,C项错误;
D.电子气遍布于整个晶体被所有原子共用,从而将所有原子维系在了一起,金属晶体具有延展性,D项正确;
故选C。
2.答案:C
解析:温度高,金属阳离子的热运动加快,对自由电子的移动造成阻碍,导电性减弱,故A错误;常温下,Hg为液态,不属于晶体形态,故B错误;正是因为金属键无方向性和饱和性,所以金属晶体中的金属原子可以采用最密堆积,尽量充分利用空间,故C正确;在外力作用下,金属阳离子与自由电子之间仍有强烈相互作用,不会断裂,所以金属有延展性,故D错误。
3.答案:C
解析:A.为乙烯分子的球棍模型,故A错误;
B.基态铍原子最外层电子排布式为,电子云图应为球形,故B错误;
C.分子中N原子的价层电子对数为,采取杂化,有一对孤电子对,分子的空间构型为三角锥形,故C正确;
D.该图示表示金属原子平面非密置层排列,配位数为4;金属原子的密置层排列的配位数为6,应为,故D错误;
古答案选C。
4.答案:C
解析:金属晶体只含金属元素,C项符合题意。
5.答案:A
解析:A.的成键电子对数是2,孤电子对数是1,价层电子对数为3,VSEPR模型为平面三角形,A错误;
B.蔗糖和氨是极性分子,易溶于水,四氯化碳是非极性分子,难溶于四氯化碳,B正确;
C.金属晶体存在的“电子气”,电子气在外电场作用下定向移动,金属有良好的导电性;金属受热,加速自由电子与金属离子之间的能量交换将热能从一端传递到另一端而使金属有良好的导热性,C正确;
D.水晶为晶态二氧化硅,X射线衍射图谱上有分立的斑点或明锐的衍射峰,D正确;
故选A。
6.答案:D
解析:铅晶体是金属晶体,而锗晶体是共价晶体,类似金刚石类型,呈正四面体形,A项错误;
图中纵坐标由大到小,即铅晶粒越大,其熔点越高,B项错误;
铅晶体是金属晶体,由金属离子和自由电子靠金属键构成,含阳离子,不含阴离子,C项错误;
铅晶粒表面积越大,颗粒越小,晶体熔点越低,D项正确。
7.答案:C
解析:A.VSEPR模型是价层电子对的空间结构模型,当中心原子无孤电子对时,与分子空间结构相同,当中心原子有孤电子对时,与分子空间结构不同,A正确;
B.电子云图中的小黑点越密,表示电子在核外空间的出现的概率密度越大,B正确;
C.电子从较高能量的激发态回到基态释放出能量,属于发射光谱,C错误;
D.电子气理论把金属键描述成从金属原子脱落下来的价电子形成遍布整块晶体的“电子气”,可用于解释金属晶体的延展性、导电性和导热性,D正确;
答案选C。
8.答案:B
解析:单质是金属晶体,含有金属键,A项正确;基态原子核外电子排布式为,B项错误;由晶胞图,根据均摊法可知,与原子个数比为,C项正确;与之间的最短距离为面对角线的一半即,D项正确。
9.答案:B
解析:用铂金做首饰是因为有金属光泽,金属具有光泽是因为自由电子能够吸收可见光,能用金属键理论知识解释,故A错误;
金属晶体中有电子,能导电,大多数在常温下为固体,熔点较高,所以固体或熔融状态易导电,熔点在1000℃左右可能属于金属.晶体,故B正确;
碱金属元素的单质,原子序数越大,原子半径越大,金属键越弱熔沸点越低,则单质熔点:Li>Na>K,故C错误;
金属导电是靠自由移动的电子,电解质导电是靠自由移动的离子,导电的原理不一样,故D错误;
10.答案:A
解析:常温下,Hg为液态,不是晶体,A错误。
11.答案:C
解析:钾型晶体的晶胞为立方体,A错误;是非密置层的一种堆积方式,B错误;每个晶胞中有8个顶点原子和1个体心原子,晶胞内含有的原子个数,C正确,D错误。
12.答案:B
解析:晶胞①的边长是2r cm,体积是,由均摊法可知,晶胞①中金属原子的个数,1个原子的体积是,故空间利用率,A正确;金属原子脱落下来的价电子形成遍布整块晶体的“电子气”,被所有原子所共有,从而把所有金属原子维系在一起,金属晶体是一种“巨分子”,只存在金属键,B错误;根据均炸法可知,晶胞③中含有的原子数,晶胞④中含有的原子数,C正确;根据晶胞结构可知,晶胞①和晶胞②中原子的配位数分别为6、8,D正确。
13.答案:D
解析:由均摊法可知,每个Ag晶胞中含有的Ag的个数,A错误;同周期主族元素从左到右,电负性逐渐增大,但不包括稀有气体元素,B错误;固态时能导电的晶体不一定是金属晶体,例如石墨能导电,但石墨不是金属晶体,C错误;在同一能级上运动的电子,可能位于不同轨道,也可能位于同一轨道,但二者的自旋状态不同,原子核外有多少个电子,就有多少种不同的运动状态,D正确。
14.答案:(1)①;金属
②8;12
(2)4;
解析:(1)②在1183 K以下的纯铁晶体中,与晶胞体心铁原子等距离且最近的铁原子是8个顶点的铁原子;在1183 K以上的纯铁晶体中,与晶胞面心铁原子等距离且最近的铁原子有12个。
(2)铜晶胞为面心立方晶胞,1个晶胞平均有4个铜原子;1个晶胞的体积为;一个晶胞的质量为;由,得到。
15.答案:(1)1:4:2
(2)无
(3)3:1
解析:(1)晶胞a中金属原子数目为,晶胞b中金属原子数目为,晶胞c中金属原子数目为,所以a、b、c三种晶胞内金属原子数目之比为1:4:2。
(2)由于金属晶体中的自由电子不属于每个固定的原子,而是在整个晶体中自由移动,故自由电子无确切的堆积方式。
(3)该晶胞中Cu原子数为原子数为,故该合金中Cu原子与Au原子的数量之比为3:1。
1.下列关于金属晶体及金属键的说法不正确的是( )
A.金属晶体和共价晶体一样,是一种“巨分子”
B.金属键是金属原子脱落下来的价电子形成遍布整块晶体的“电子气”,被所有原子所共用
C.金属导电是因为在外加电场作用下产生自由电子
D.金属受外力作用变形时,金属阳离子与自由电子间仍保持较强烈作用,因而具有延展性
2.下列关于金属晶体的叙述中,正确的是( )
A.温度越高,金属的导电性越强
B.常温下,金属单质都以金属晶体形式存在
C.金属晶体堆积密度大,能充分利用空间的原因是金属键没有饱和性和方向性
D.金属阳离子与自由电子之间的强烈相互作用,在外力作用下会发生断裂,故金属无延展性
3.下列对示意图的解释正确的是( )
A B C D
示意图
解释 分子的比例模型 基态铍原子最外层电子的电子云图 的立体构型 金属原子平面密置层排列
A.A B.B C.C D.D
4.下列物质属于金属晶体的是( )
A.氯化钠 B.干冰 C.水银 D.金刚石
5.下列说法不正确的是( )
A.的VSEPR模型:
B.蔗糖和氨易溶于水,难溶于四氯化碳,可用“相似相溶”规律解释
C.金属晶体存在“电子气”,具有良好的导电性和导热性
D.水晶研成粉末摄取的X射线衍射图谱为分立的斑点或明锐的衍射峰
6.金属铅的晶粒大小与熔点关系如图所示。下列叙述正确的是( )
A.铅与锗位于同主族且单质晶体类型相同
B.铅晶粒越大,其熔点越低
C.铅晶体中含阳离子,必含阴离子
D.铅晶体熔点高低与晶粒表面积大小有关
7.基本概念和理论是化学思维的基石。下列叙述不正确的是( )
A.VSEPR理论认为VSEPR模型与分子的空间结构不一定相同
B.电子云图中的小黑点越密,表示电子在核外空间出现的概率密度越大
C.五彩斑斓的霓虹灯光,与原子核外电子跃迁有关,属于吸收光谐
D.“电子气理论”可以解释金属晶体的延展性,导电性和导热性
8.、、均位于第四周期Ⅶ族,属于副族元素。某合金的立方晶胞结构如图所示,已知其晶胞参数为。下列说法错误的是( )
A.单质中含有金属键 B.基态原子核外电子排布式为
C.晶体中,与原子个数比为 D.与之间的最短距离为
9.下列关于金属晶体的叙述正确的是( )
A.用铂金做首饰不能用金属键理论解释
B.固态和熔融时易导电,熔点在1000℃左右的晶体可能是金属晶体
C.Li、Na、K的熔点逐渐升高
D.金属导电和熔融电解质(或电解质溶液)导电的原理一样。
10.下列关于金属晶体的叙述不正确的是( )
A.常温下,金属单质都以金属晶体形式存在
B.金属键在一定外力作用下,不会因形变而消失
C.Ca的熔、沸点高于K的熔、沸点
D.温度越高,金属的导电性越弱
11.钾型晶体的晶胞如图所示。下列关于该晶胞的叙述正确的是( )
A.晶胞是六棱柱 B.是密置层的一种堆积方式
C.每个晶胞内含有2个原子 D.每个晶胞内含有6个原子
12.有四种不同堆积方式的金属晶体的晶胞如图所示(原子半径为r cm),下列叙述错误的是( )
A.晶胞①的空间利用率
B.金属晶体是一种“巨分子”,可能存在分子间作用力
C.晶胞中含有的原子数:晶胞③—2,晶胞
D.晶胞中原子的配位数:晶胞①—6,晶胞
13.下列叙述正确的是( )
A.如图所示为面心立方体Ag的晶胞,其晶胞中有14个Ag原子
B.11号到18号元素位于元素周期表中同一周期,故元素的电负性逐渐增大
C.固态时能导电的晶体一定是金属晶体
D.在同一能级上运动的电子,其运动状态肯定不同
14.回答下列问题:
(1)1183 K以下纯铁晶体的基本结构单元如图1所示,1183 K以上转变为图2所示的基本结构单元。
①铁原子的简化电子排布式为________;铁晶体中铁原子以________键相互结合。
②在1183 K以下的纯铁晶体中,与铁原子等距离且最近的铁原子数为________;在1183 K以上的纯铁晶体中,与铁原子等距离且最近的铁原子数为________。
(2)铜的晶胞结构如图3,每个晶胞中所含的铜原子数为______个。金属铜晶胞的边长为,又知铜的密度为,阿伏加德罗常数为______。
15.图a、b、c分别代表金属晶体中金属原子的简单立方堆积、面心立方堆积和体心立方堆积这三种晶胞的结构。
(1)a、b、c三种晶胞内金属原子数目之比为___________。
(2)三种堆积方式的实质是金属阳离子的堆积方式,那么自由电子有无确切的堆积方式?________(填“有”或“无”)。
(3)一种铜、金合金晶体具有立方最密堆积的结构(见下图),在晶胞中Cū原子处于面心,Au原子处于顶点位置,则该合金中C原子与Au原子的数量之比为_______。
答案以及解析
1.答案:C
解析:A.把金属键描述为金属原子脱落的价电子形成的电子气遍布于整个晶体被所有原子共用,从而将所有原子维系在了一起,金属晶体是一种“巨大的分子”。而共价晶体以无数共价键将所有原子连接形成的巨大的网状结构,A项正确;
B.把金属键描述为金属原子脱落的价电子形成的电子气遍布于整个晶体被所有原子共用,B项正确;
C.金属中存在自由移动的电子,在外加电场的作用下可以定向移动,C项错误;
D.电子气遍布于整个晶体被所有原子共用,从而将所有原子维系在了一起,金属晶体具有延展性,D项正确;
故选C。
2.答案:C
解析:温度高,金属阳离子的热运动加快,对自由电子的移动造成阻碍,导电性减弱,故A错误;常温下,Hg为液态,不属于晶体形态,故B错误;正是因为金属键无方向性和饱和性,所以金属晶体中的金属原子可以采用最密堆积,尽量充分利用空间,故C正确;在外力作用下,金属阳离子与自由电子之间仍有强烈相互作用,不会断裂,所以金属有延展性,故D错误。
3.答案:C
解析:A.为乙烯分子的球棍模型,故A错误;
B.基态铍原子最外层电子排布式为,电子云图应为球形,故B错误;
C.分子中N原子的价层电子对数为,采取杂化,有一对孤电子对,分子的空间构型为三角锥形,故C正确;
D.该图示表示金属原子平面非密置层排列,配位数为4;金属原子的密置层排列的配位数为6,应为,故D错误;
古答案选C。
4.答案:C
解析:金属晶体只含金属元素,C项符合题意。
5.答案:A
解析:A.的成键电子对数是2,孤电子对数是1,价层电子对数为3,VSEPR模型为平面三角形,A错误;
B.蔗糖和氨是极性分子,易溶于水,四氯化碳是非极性分子,难溶于四氯化碳,B正确;
C.金属晶体存在的“电子气”,电子气在外电场作用下定向移动,金属有良好的导电性;金属受热,加速自由电子与金属离子之间的能量交换将热能从一端传递到另一端而使金属有良好的导热性,C正确;
D.水晶为晶态二氧化硅,X射线衍射图谱上有分立的斑点或明锐的衍射峰,D正确;
故选A。
6.答案:D
解析:铅晶体是金属晶体,而锗晶体是共价晶体,类似金刚石类型,呈正四面体形,A项错误;
图中纵坐标由大到小,即铅晶粒越大,其熔点越高,B项错误;
铅晶体是金属晶体,由金属离子和自由电子靠金属键构成,含阳离子,不含阴离子,C项错误;
铅晶粒表面积越大,颗粒越小,晶体熔点越低,D项正确。
7.答案:C
解析:A.VSEPR模型是价层电子对的空间结构模型,当中心原子无孤电子对时,与分子空间结构相同,当中心原子有孤电子对时,与分子空间结构不同,A正确;
B.电子云图中的小黑点越密,表示电子在核外空间的出现的概率密度越大,B正确;
C.电子从较高能量的激发态回到基态释放出能量,属于发射光谱,C错误;
D.电子气理论把金属键描述成从金属原子脱落下来的价电子形成遍布整块晶体的“电子气”,可用于解释金属晶体的延展性、导电性和导热性,D正确;
答案选C。
8.答案:B
解析:单质是金属晶体,含有金属键,A项正确;基态原子核外电子排布式为,B项错误;由晶胞图,根据均摊法可知,与原子个数比为,C项正确;与之间的最短距离为面对角线的一半即,D项正确。
9.答案:B
解析:用铂金做首饰是因为有金属光泽,金属具有光泽是因为自由电子能够吸收可见光,能用金属键理论知识解释,故A错误;
金属晶体中有电子,能导电,大多数在常温下为固体,熔点较高,所以固体或熔融状态易导电,熔点在1000℃左右可能属于金属.晶体,故B正确;
碱金属元素的单质,原子序数越大,原子半径越大,金属键越弱熔沸点越低,则单质熔点:Li>Na>K,故C错误;
金属导电是靠自由移动的电子,电解质导电是靠自由移动的离子,导电的原理不一样,故D错误;
10.答案:A
解析:常温下,Hg为液态,不是晶体,A错误。
11.答案:C
解析:钾型晶体的晶胞为立方体,A错误;是非密置层的一种堆积方式,B错误;每个晶胞中有8个顶点原子和1个体心原子,晶胞内含有的原子个数,C正确,D错误。
12.答案:B
解析:晶胞①的边长是2r cm,体积是,由均摊法可知,晶胞①中金属原子的个数,1个原子的体积是,故空间利用率,A正确;金属原子脱落下来的价电子形成遍布整块晶体的“电子气”,被所有原子所共有,从而把所有金属原子维系在一起,金属晶体是一种“巨分子”,只存在金属键,B错误;根据均炸法可知,晶胞③中含有的原子数,晶胞④中含有的原子数,C正确;根据晶胞结构可知,晶胞①和晶胞②中原子的配位数分别为6、8,D正确。
13.答案:D
解析:由均摊法可知,每个Ag晶胞中含有的Ag的个数,A错误;同周期主族元素从左到右,电负性逐渐增大,但不包括稀有气体元素,B错误;固态时能导电的晶体不一定是金属晶体,例如石墨能导电,但石墨不是金属晶体,C错误;在同一能级上运动的电子,可能位于不同轨道,也可能位于同一轨道,但二者的自旋状态不同,原子核外有多少个电子,就有多少种不同的运动状态,D正确。
14.答案:(1)①;金属
②8;12
(2)4;
解析:(1)②在1183 K以下的纯铁晶体中,与晶胞体心铁原子等距离且最近的铁原子是8个顶点的铁原子;在1183 K以上的纯铁晶体中,与晶胞面心铁原子等距离且最近的铁原子有12个。
(2)铜晶胞为面心立方晶胞,1个晶胞平均有4个铜原子;1个晶胞的体积为;一个晶胞的质量为;由,得到。
15.答案:(1)1:4:2
(2)无
(3)3:1
解析:(1)晶胞a中金属原子数目为,晶胞b中金属原子数目为,晶胞c中金属原子数目为,所以a、b、c三种晶胞内金属原子数目之比为1:4:2。
(2)由于金属晶体中的自由电子不属于每个固定的原子,而是在整个晶体中自由移动,故自由电子无确切的堆积方式。
(3)该晶胞中Cu原子数为原子数为,故该合金中Cu原子与Au原子的数量之比为3:1。
