4.3.1 化学方程式的意义及其书写 优质课件 (共28张PPT)初中科粤版(2024)九年级上册
文档属性
| 名称 | 4.3.1 化学方程式的意义及其书写 优质课件 (共28张PPT)初中科粤版(2024)九年级上册 |  | |
| 格式 | pptx | ||
| 文件大小 | 55.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 科粤版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-05-01 10:37:31 | ||
图片预览








文档简介
(共28张PPT)
4.3 化学方程式的意义及其书写
核心素养目标
一、化学观念
理解化学方程式的概念,认识到化学方程式是一种表示化学反应的通用语言,能从物质变化和质量守恒的角度理解化学反应;理解化学方程式所体现的反应物、生成物及反应条件之间的关系。
二、科学思维
掌握书写化学方程式的方法和步骤,通过配平化学方程式,锻炼归纳总结和推理能力。
三、科学态度与责任
认识到化学方程式在化学研究和工业生产等方面的重要性,严谨、规范书写化学方程式,培养科学严谨的态度。
学习重难点
重点:
1. 化学方程式的含义,包括定性(反应物、生成物、反应条件)和定量(质量关系、微粒个数关系)方面
2. 正确书写化学方程式的步骤和方法,尤其是根据质量守恒定律进行配平
难点:
1. 理解化学方程式所表示的微观粒子数量关系和宏观质量关系
2. 熟练运用合适的配平方法准确书写化学方程式
问题探讨
01 什么是化学方程式
请写出碳和氧气反应的文字表达式
优点:能表明反应物、生成物、反应条件。
缺点:不能表示反应过程的质量关系,不简明,不利于国际交流。
请写出碳和氧气反应的符号表达式
优点:能表明反应物、生成物、反应条件,利于国际交流。
缺点:不能表示反应过程的质量关系。
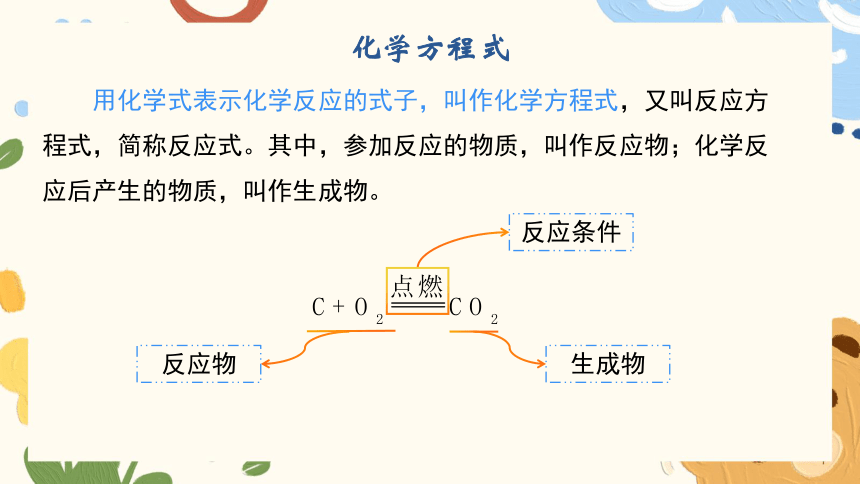
化学方程式
用化学式表示化学反应的式子,叫作化学方程式,又叫反应方
程式,简称反应式。其中,参加反应的物质,叫作反应物;化学反
应后产生的物质,叫作生成物。
反应物
生成物
反应条件
化学方程式的意义
化学方程式表明了反应物、生成物和反应条件。
例如,上面列出的反应,表示反应物是碳和氧气,生成物是二氧
化碳,反应条件为“点燃”。
定性角度
化学方程式的意义
微观上化学方程式表示了反应中构成各物质的微观粒子间的数量
关系,宏观上表示质量关系。
定量角度
构成各物质的微观粒子:
一个碳原子
两个氧原子构成一个氧分子
两个氧原子和一个碳原子构成一个二氧化碳分子
化学方程式的意义
相对分子(原子)质量:
12
2×16
12+2×16
质量关系:
12
32
:
44
:
每 12 份质量的碳与 32 份质量的氧气恰好完全反应,生成 44 份质量的二氧化碳,这符合质量守恒定律。
化学方程式的意义
化学方程式的意义
定性:
表示反应物、生成物和反应条件
定量
反应物、生成物之间的质量比
[即相对分子质量(或相对原子质量)与化学计量数的乘积之比
反应物、生成物之间的粒子个数比
(即化学式前面的化学计量数之比)
化学方程式的读法
(1)直接读出反应物,生成物的名称和反应条件
碳和氧气在点燃条件下反应,生成二氧化碳
(2)读出反应物和生成物之间各物质的质量比
每12份质量的碳与32份质量的氧气反应,点燃生成44份质量的二氧化碳。
(3)读出反应物和生成物的各粒子个数比
每1个碳原子与1个氧分子反应,生成1个二氧化碳分子
讨论与交流
①根据电解水的化学方程式:2H2O === 2H2↑+O2↑,说出该反应式可以表示哪些含义。
通电
定性:
该反应物中反应物为水,生成物为氢气和氧气。
定量
参与反应的分子个数比——
2:2:1
质量比——
2×(1×2+16) :2×1 :2×16 = 9 :1 :8
②你认为书写化学方程式的依据是什么?
02 怎样书写化学方程式
化学方程式的书写原则
②必须遵守质量守恒定律
写出反应物和生成物的化学式,以及反应条件
①必须以客观事实为基础
等号两边各种原子的种类和数目必须相同
化学方程式的书写步骤
写化学式。根据实验事实,在左、右两边分别写出反应物和生成物的化学式,中间用“ ”连接(若反应物或生成物不止一种,用“+”连接)
写
以磷与氧气反应生成五氧化二磷为例
P +O2 P2O5
化学方程式的书写步骤
配平。根据质量守恒定律,在有关化学式前配上适当的化学计量数,使反应前后各元素的原子个数相等,把“ ”改成“ ”
配
4P + 5O2 2P2O5
标明反应条件和生成物状态
标
4P + 5O2 2P2O5
点燃
检查化学式书写是否正确,化学方程式是否配平,反应条件标注是否正确,生成物状态符号是否正确
查
化学方程式的配平方法——最小公倍数法
①左边写反应物化学式,右边写生成物化学式
②配平
③标明反应条件
P2O5前配2,O2前配5
求最小公倍数: 2×5=10
求化学计量数
配平其它化学计量数
右边是5个O原子,左边是2个O原子,最小公倍数是10
因而P前配4
适用范围:适用于左右两边某种原子个数差异较大的化学方程式
化学方程式的配平方法——奇数配偶法
左右两端的原子总数为一奇一偶,在其含有奇数个原子的化学式前配上一个偶数2,变奇数为偶数,然后依次配平与其相关的其他元素原子。
FeS2+ O2 Fe2O3 + SO2
点燃
2
4
8
11
适用范围:适用于方程式两边某一元素多次出现,并且式子两边该元素原子的数目为一奇一偶。
化学方程式的配平方法——观察法
适用范围:适用于反应物或生成物中某物质的化学式比较复杂(含原子团)的化学方程式。
最基本、常用的配平方法,任何特殊的配平方法都离不开观察法的配合。对于一些比较简单的化学反应,配平时可直接观察看出结果。
H2O H2 ↑ + O2 ↑
通电
2
2
化学方程式的配平方法——设1法
适用范围:适用于碳氢化合物(或含碳、氢、氧的化合物)与氧气的反应。
从反应物或生成物中找出化学式比较复杂的一种物质,将其化学式的计量数定为1,以此为基准,求解其他化学计量数。
C3H8 + O2 CO2 + H2O
通电
3
5
4
符号“↑”“↓”的使用
“↑” “↓”都是表示生成物状态的符号,只能标注在生成物右边。
(1)如果反应物中没有气体,而生成物有气体,则后者用“↑”号标明;溶液中的反应,如果反应物中没有难溶物质,而在生成物中有沉淀,则后者用“↓”号标明。
“无中生有”才标
化学方程式所用符号
总结归纳
随堂练习
1. 下列关于化学方程式 的叙述中,
正确的是 ( )
A. 读作铝加氧气等于氧化铝
B. 表示氧化铝分解生成铝和氧气
C. 表示 4 个铝和 3 个氧气在点燃的条件下生成 2 个氧化铝
D. 表示每 108 份质量的铝恰好与 96 份质量的氧气完全反应,生成 204 份质量的氧化铝
D
2. 下列化学方程式书写正确的是( )
A.
B.
C.
D.
随堂练习
A
随堂练习
3. 配平或书写下列化学方程式
(1)
(2)
(3)汽车尾气中的一氧化氮与一氧化碳在催化剂的作用下,反应生成二氧化碳和一种无污染的单质气体。写出该反应的化学方程式 。
2
3
2
1
3
2
3
随堂练习
4. 根据化学方程式: ,无法获取的信息是( )
A. 反应所需条件 B. 生成物的状态
C. 生成物的物质的量之比 D. 氧气可助燃
D
感谢您的观看
“THANK YOU”
4.3 化学方程式的意义及其书写
核心素养目标
一、化学观念
理解化学方程式的概念,认识到化学方程式是一种表示化学反应的通用语言,能从物质变化和质量守恒的角度理解化学反应;理解化学方程式所体现的反应物、生成物及反应条件之间的关系。
二、科学思维
掌握书写化学方程式的方法和步骤,通过配平化学方程式,锻炼归纳总结和推理能力。
三、科学态度与责任
认识到化学方程式在化学研究和工业生产等方面的重要性,严谨、规范书写化学方程式,培养科学严谨的态度。
学习重难点
重点:
1. 化学方程式的含义,包括定性(反应物、生成物、反应条件)和定量(质量关系、微粒个数关系)方面
2. 正确书写化学方程式的步骤和方法,尤其是根据质量守恒定律进行配平
难点:
1. 理解化学方程式所表示的微观粒子数量关系和宏观质量关系
2. 熟练运用合适的配平方法准确书写化学方程式
问题探讨
01 什么是化学方程式
请写出碳和氧气反应的文字表达式
优点:能表明反应物、生成物、反应条件。
缺点:不能表示反应过程的质量关系,不简明,不利于国际交流。
请写出碳和氧气反应的符号表达式
优点:能表明反应物、生成物、反应条件,利于国际交流。
缺点:不能表示反应过程的质量关系。
化学方程式
用化学式表示化学反应的式子,叫作化学方程式,又叫反应方
程式,简称反应式。其中,参加反应的物质,叫作反应物;化学反
应后产生的物质,叫作生成物。
反应物
生成物
反应条件
化学方程式的意义
化学方程式表明了反应物、生成物和反应条件。
例如,上面列出的反应,表示反应物是碳和氧气,生成物是二氧
化碳,反应条件为“点燃”。
定性角度
化学方程式的意义
微观上化学方程式表示了反应中构成各物质的微观粒子间的数量
关系,宏观上表示质量关系。
定量角度
构成各物质的微观粒子:
一个碳原子
两个氧原子构成一个氧分子
两个氧原子和一个碳原子构成一个二氧化碳分子
化学方程式的意义
相对分子(原子)质量:
12
2×16
12+2×16
质量关系:
12
32
:
44
:
每 12 份质量的碳与 32 份质量的氧气恰好完全反应,生成 44 份质量的二氧化碳,这符合质量守恒定律。
化学方程式的意义
化学方程式的意义
定性:
表示反应物、生成物和反应条件
定量
反应物、生成物之间的质量比
[即相对分子质量(或相对原子质量)与化学计量数的乘积之比
反应物、生成物之间的粒子个数比
(即化学式前面的化学计量数之比)
化学方程式的读法
(1)直接读出反应物,生成物的名称和反应条件
碳和氧气在点燃条件下反应,生成二氧化碳
(2)读出反应物和生成物之间各物质的质量比
每12份质量的碳与32份质量的氧气反应,点燃生成44份质量的二氧化碳。
(3)读出反应物和生成物的各粒子个数比
每1个碳原子与1个氧分子反应,生成1个二氧化碳分子
讨论与交流
①根据电解水的化学方程式:2H2O === 2H2↑+O2↑,说出该反应式可以表示哪些含义。
通电
定性:
该反应物中反应物为水,生成物为氢气和氧气。
定量
参与反应的分子个数比——
2:2:1
质量比——
2×(1×2+16) :2×1 :2×16 = 9 :1 :8
②你认为书写化学方程式的依据是什么?
02 怎样书写化学方程式
化学方程式的书写原则
②必须遵守质量守恒定律
写出反应物和生成物的化学式,以及反应条件
①必须以客观事实为基础
等号两边各种原子的种类和数目必须相同
化学方程式的书写步骤
写化学式。根据实验事实,在左、右两边分别写出反应物和生成物的化学式,中间用“ ”连接(若反应物或生成物不止一种,用“+”连接)
写
以磷与氧气反应生成五氧化二磷为例
P +O2 P2O5
化学方程式的书写步骤
配平。根据质量守恒定律,在有关化学式前配上适当的化学计量数,使反应前后各元素的原子个数相等,把“ ”改成“ ”
配
4P + 5O2 2P2O5
标明反应条件和生成物状态
标
4P + 5O2 2P2O5
点燃
检查化学式书写是否正确,化学方程式是否配平,反应条件标注是否正确,生成物状态符号是否正确
查
化学方程式的配平方法——最小公倍数法
①左边写反应物化学式,右边写生成物化学式
②配平
③标明反应条件
P2O5前配2,O2前配5
求最小公倍数: 2×5=10
求化学计量数
配平其它化学计量数
右边是5个O原子,左边是2个O原子,最小公倍数是10
因而P前配4
适用范围:适用于左右两边某种原子个数差异较大的化学方程式
化学方程式的配平方法——奇数配偶法
左右两端的原子总数为一奇一偶,在其含有奇数个原子的化学式前配上一个偶数2,变奇数为偶数,然后依次配平与其相关的其他元素原子。
FeS2+ O2 Fe2O3 + SO2
点燃
2
4
8
11
适用范围:适用于方程式两边某一元素多次出现,并且式子两边该元素原子的数目为一奇一偶。
化学方程式的配平方法——观察法
适用范围:适用于反应物或生成物中某物质的化学式比较复杂(含原子团)的化学方程式。
最基本、常用的配平方法,任何特殊的配平方法都离不开观察法的配合。对于一些比较简单的化学反应,配平时可直接观察看出结果。
H2O H2 ↑ + O2 ↑
通电
2
2
化学方程式的配平方法——设1法
适用范围:适用于碳氢化合物(或含碳、氢、氧的化合物)与氧气的反应。
从反应物或生成物中找出化学式比较复杂的一种物质,将其化学式的计量数定为1,以此为基准,求解其他化学计量数。
C3H8 + O2 CO2 + H2O
通电
3
5
4
符号“↑”“↓”的使用
“↑” “↓”都是表示生成物状态的符号,只能标注在生成物右边。
(1)如果反应物中没有气体,而生成物有气体,则后者用“↑”号标明;溶液中的反应,如果反应物中没有难溶物质,而在生成物中有沉淀,则后者用“↓”号标明。
“无中生有”才标
化学方程式所用符号
总结归纳
随堂练习
1. 下列关于化学方程式 的叙述中,
正确的是 ( )
A. 读作铝加氧气等于氧化铝
B. 表示氧化铝分解生成铝和氧气
C. 表示 4 个铝和 3 个氧气在点燃的条件下生成 2 个氧化铝
D. 表示每 108 份质量的铝恰好与 96 份质量的氧气完全反应,生成 204 份质量的氧化铝
D
2. 下列化学方程式书写正确的是( )
A.
B.
C.
D.
随堂练习
A
随堂练习
3. 配平或书写下列化学方程式
(1)
(2)
(3)汽车尾气中的一氧化氮与一氧化碳在催化剂的作用下,反应生成二氧化碳和一种无污染的单质气体。写出该反应的化学方程式 。
2
3
2
1
3
2
3
随堂练习
4. 根据化学方程式: ,无法获取的信息是( )
A. 反应所需条件 B. 生成物的状态
C. 生成物的物质的量之比 D. 氧气可助燃
D
感谢您的观看
“THANK YOU”
同课章节目录
