苏教版高二化学选修五《有机化学基础》专题四第三单元《醛 羧酸 》教学课件(共48张PPT)
文档属性
| 名称 | 苏教版高二化学选修五《有机化学基础》专题四第三单元《醛 羧酸 》教学课件(共48张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2016-06-03 00:00:00 | ||
图片预览








文档简介
课件48张PPT。专题4 烃的衍生物第三单元 醛 羧酸【学习目标】
1.通过对乙醛性质的探究活动,学习醛的典型化学性质。
2.知道甲醛的结构,了解甲醛在日常生活、工农业生产中的用途,以及甲醛对人体健康的危害。
3.通过对乙酸性质的探究活动,了解羧酸具有酸性的原因,认识酯化反应的特色。通过对甲酸化学性质探究活动的设计,认识甲酸的化学性质。
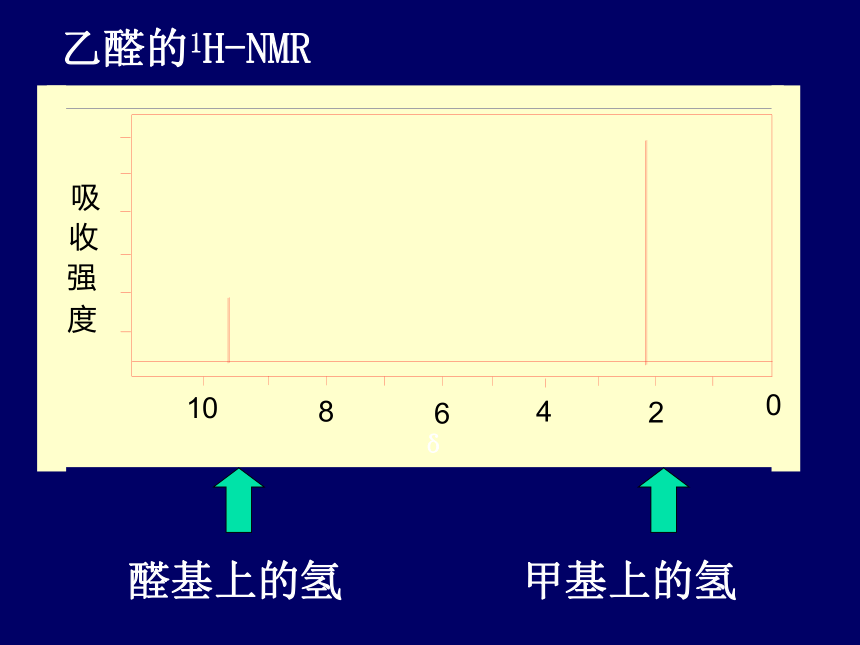
4.能初步概述重要有机化合物之间的相互转化关系。乙醛的结构:官能团:醛基醛类中具有代表性的醛-乙醛乙醛的1H-NMR(一)组成和结构:C2H4O
CH3CHO一、乙醛: 分子式:
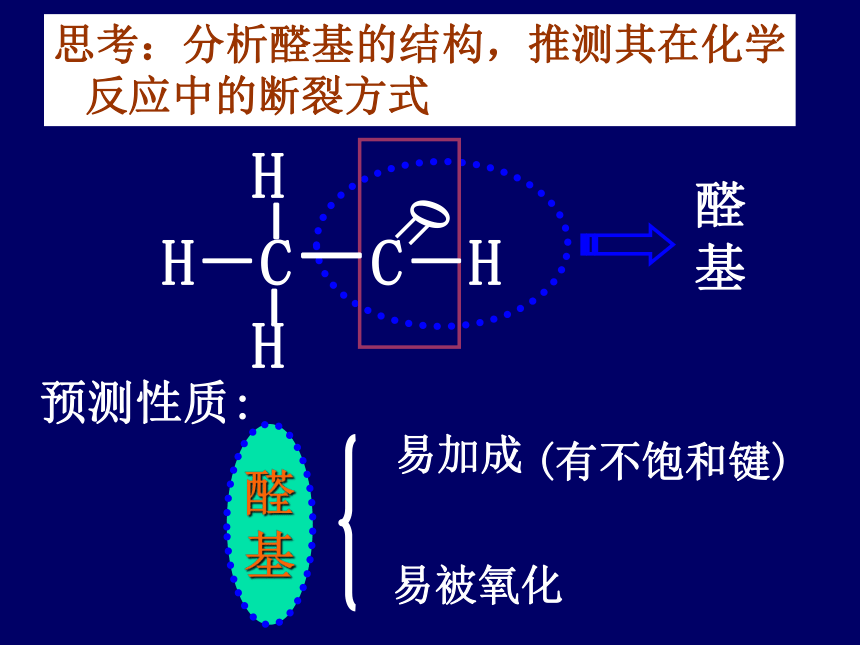
结构简式: (二)乙醛的性质1、物理性质: 无色有刺激性气味的液体,沸点20.8℃, 密度比水小,易挥发,易燃烧,能跟水、乙醇、氯仿等互溶。(有不饱和键)醛
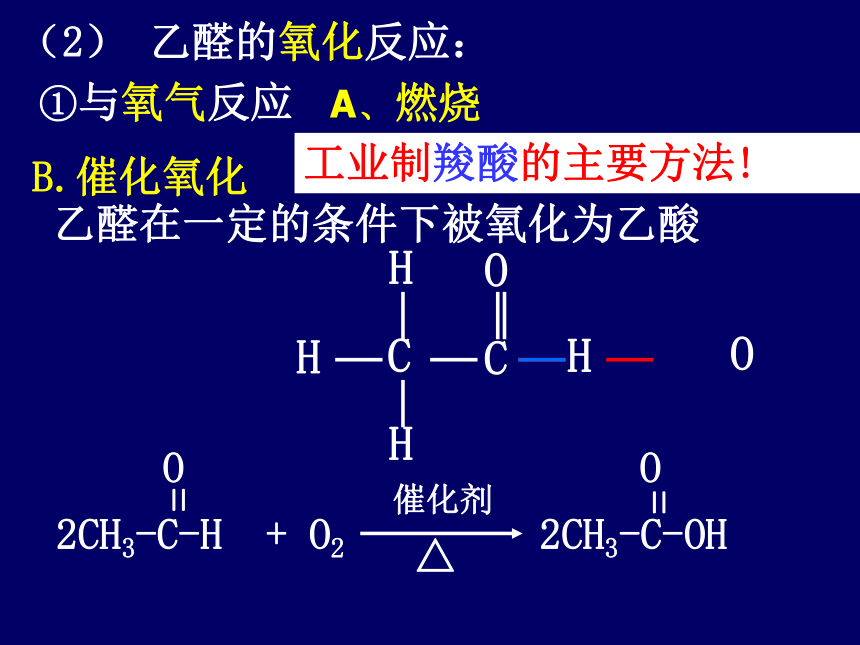
基易被氧化预测性质:思考:分析醛基的结构,推测其在化学反应中的断裂方式易加成(1) 乙醛的加成反应:2、乙醛的化学性质OCHCHHHHH分析:碳元素的化合价变化结论:加氢碳元素被还原工业制醇的主要方法!思考:有机反应中的氧化反应和还原反应
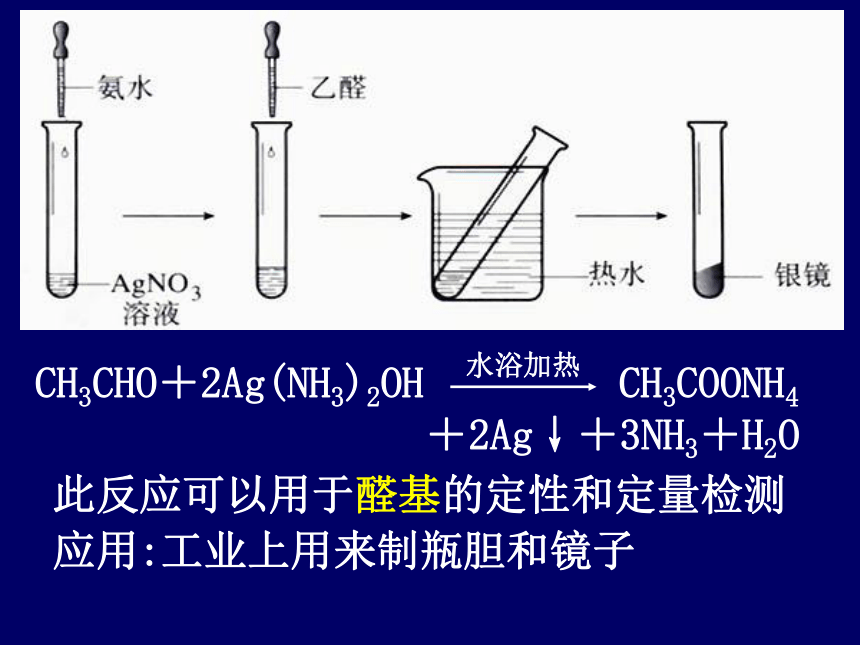
我们应该怎样判断呢?有机物得O或去H, 发生氧化反应有机物失O或加H, 发生还原反应OCHCHHHO乙醛在一定的条件下被氧化为乙酸工业制羧酸的主要方法!B.催化氧化(2) 乙醛的氧化反应:①与氧气反应 A、燃烧 A.银镜反应---与银氨溶液的反应 Ag++NH3·H2O=AgOH ↓+ NH4+
AgOH+2 NH3·H2O=[Ag(NH3)2]++OH-+2H2O
或:AgOH+2 NH3·H2O=[Ag(NH3)2]OH+2H2O银氨溶液的配制方法:取一洁净试管,加入2ml2%的AgNO3溶液,再逐滴滴入2%的稀氨水,至生成的沉淀恰好溶解。②与其它氧化剂反应 此反应可以用于醛基的定性和定量检测应用:工业上用来制瓶胆和镜子5.1mol醛基被氧化,就应有2molAg被还原3.银氨溶液现用现制,不能久置;氨水滴加至沉淀恰好溶解,不可多加,注意:1.试管要洁净,2.水浴加热时不可振荡和摇动试管否则生不成银镜4.试管内壁银镜的处理:稀硝酸清洗
B、被新制Cu(OH)2氧化新制Cu(OH)2的配制方法:2mlNaOH(50%)+4~6滴CuSO4(2%)CH3CHO+2Cu(OH)2 CH3COOH+Cu2O+2H2O砖红色加热必须过量注意:
此反应必须在碱性条件下进行应用:
此反应也用于醛基的检验和测定医学上检验病人是否患糖尿病讨论:
1.实验中观察到有黑色物质生成,试解释
2.乙醛能否使溴水或酸性KMnO4溶液褪色?
B、被新制Cu(OH)2氧化新制Cu(OH)2的配制方法:2mlNaOH(50%)+4~6滴CuSO4(2%)CH3CHO+2Cu(OH)2 CH3COOH+Cu2O+2H2O砖红色加热必须过量C、使酸性KMnO4溶液褪色醛基中碳氧双键能与H2发生加成反应醛基中碳氢键较活泼,能被氧化成羧基加成反应氧化反应乙 醛小结:乙醛的化学性质注意:和C=C双键不同的是,通
常情况下, 醛基中的C=O不能
和HX、X2、H2O发生加成反应(四)乙醛的工业制取:(1)乙醇的催化氧化
(2)乙炔水化法:(3)乙烯氧化法:(三)乙醛的用途:
是有机合成的重要原料,主要用于制取
乙酸、丁醇、乙酸乙酯二、醛类1、定义:R-CHO烃基2、分类按醛基个数分 按烃基是否饱和分 按烃基类别分 一元醛、二元醛 多元醛 饱和醛 脂肪醛芳香醛不饱和醛 醛基与烃基直接相连所得的化合物。3、饱和一元醛 :H-CHOCH3-CHOCH3CH2-CHOCH3CH2CH2-CHO甲醛 乙醛 丙醛丁醛饱和一元脂肪醛的分子式的通式:
CnH2n+1CHOCnH2nO(n≥1)三、甲醛结构式:分子式:CH2O结构简式:HCHO电子式:官能团:问题讨论:
甲醛分子中碳原子的成键方式?所有原子共面-CHO-COH(一)组成与结构室内空气污染的头号杀手 练习:下列物质分子中所有原子一定不共面的是
CH2=CH2 B.
C. D.练习:下列物质分子中所有原子一定不共面的是
CH2=CH2 B.
C. D.CH3CHOD(二)物性:(三)用途:质量分数含35%~40%的水溶液称福尔马林:杀菌、防腐制酚醛树脂、染料、香料、医药氧化 氧化 还原 CH3OH HCHO HCOOH甲醛既能被氧化又能被还原又叫蚁醛,无色,有刺激性气味的气体,易溶于水。 (四)甲醛的化学性质 1.甲醛发生银镜反应 2.酚醛树脂的制取取2.5g的苯酚与一大试管中,加入2.5mL的40%的甲醛溶液,加入少量的浓盐酸,塞上有长导管的橡皮塞,于沸水中加热问题:
1.浓盐酸作用?
2.长导管作用?
3.为什么不用温度计?
4.实验结束试管如何处理?
有机物分子之间缩去小分子(H2O、NH3等)而形成高分子化合物的反应。缩聚反应:酚醛树脂是人类合成的第一种高分子材料,至今还广泛使用,条件不同时(催化剂)可以生成线型或体型的酚醛树脂线型酚醛树脂(盐酸作催化剂)体型的酚醛树脂(氨水作催化剂)甲醛和尿素反应生成脲醛树脂,脲醛树脂可制成热固性高分子黏合剂,用于胶合板、刨花板、人造维板等木材加工。 >C=O称羰基,是酮的官能团,丙酮是最简单的酮。拓展视野酮:羰基碳原子与两个烃基相连的化合物。酮丙酮不能被银氨溶液、新制的氢氧化铜等弱氧化剂氧化,但可催化加氢生成醇饱和一元酮的分子式的通式:
CnH2nO(n≥3)1、用化学方法鉴别下列各组物质
1)溴乙烷 、乙醇 、乙醛
2)苯、甲苯、乙醇、1-己烯、甲醛、苯酚1)用新制氢氧化铜溶液2)用溴水巩固练习:醋 保 健食物中存在的酸 CH2-COOH | HO-C-COOH | CH2-COOH柠檬酸 COOH | CH-OH | CH2
|
COOH
苹果酸 COOH | CH-OH | CH -OH
|
COOH
酒石酸 COOH | CH-OH | CH3乳酸C17H35COOH硬脂酸水杨酸一、乙酸的物理性质:颜色、状态:无色液体气味:有强烈刺激性气味沸点:117.9℃ (易挥发)熔点:16.6℃(无水乙酸又称为:冰醋酸)溶解性:易溶于水、乙醇等溶剂二、乙酸的结构与分子模型分子式:结构式结构简式或C2H4O2想一想? 结 构
对化学性质的影响三、乙酸的化学性质(一) 酸性:乙酸的酸性比碳酸、苯酚强,那它是强酸吗?请你设计一个实验来比较一下盐酸与乙酸的酸性强弱。请你思考:①导电性实验: ②化学反应速率结论:探究:
设计简单一次性完成的实验装置,
验证乙酸、碳酸、苯酚溶液的酸性强弱乙酸乙酯的酯化过程 ——酯化反应的脱水方式同位素示踪法实验验证练习:请你完成下列方程式2、( 形成环)思考:酯化反应是一个可逆反应,如果要增大乙酸乙酯的产率,你有哪些方法? (1)增大反应物的浓度例:加入过量的酸或醇(2)除去反应生成的水例:采用浓硫酸(3)及时除去反应生成的乙酸乙酯例:蒸馏出乙酸乙酯乙酸乙酯的实验室
制备的注意事项1.装药品的顺序如何?
2.浓硫酸的作用是什么?
3.如何提高乙酸乙酯的产率?
4.得到的反应产物是否纯净?主要杂质有哪些?
5.饱和Na2CO3溶液有什么作用?能否用氢氧化钠溶液代替饱和碳酸钠溶液?
6.为什么导管不插入饱和Na2CO3溶液中?有无其它防倒吸的方法?催化剂,吸水剂。防止受热不匀发生倒吸乙酸乙酯制取注意事项
1. 浓硫酸的作用: 3. 导管位置高于液面的目的:① 中和乙酸;
② 溶解乙醇;
③ 降低酯的溶解度,以便使酯分层析出。2. 饱和碳酸钠溶液的作用: 缩聚反应概念:
由有机化合物分子间脱去小分子获得高分子化合物的反应
举例:
P84推测:羧基醛基推测可能发生的化学反应方程式:银镜反应
与新制Cu(OH)2
与碱反应
酯化反应羧酸概念:
分子里烃基跟羧基直接相连的有机物。
饱和一元羧酸的通式:
CnH2nO2
羧酸的分类:
分类羧基数烃基结构练习:酸牛奶中含有乳酸,结构简式为:
(1)乳酸与碳酸氢钠反应的方程式
;
(2)乳酸与钠反应的方程式________________
(3)乳酸在浓硫酸存在下二分子反应,生成物为环状时,反应方程式为_________________;
(4)乳酸发生消去反应,生成物为 ,该物质与甲醇反应,生成的有机物结构简式为 ,这一产物又可以发生加聚反应,反应方程式为 。CH3─CH─COOH
│
OH
1.通过对乙醛性质的探究活动,学习醛的典型化学性质。
2.知道甲醛的结构,了解甲醛在日常生活、工农业生产中的用途,以及甲醛对人体健康的危害。
3.通过对乙酸性质的探究活动,了解羧酸具有酸性的原因,认识酯化反应的特色。通过对甲酸化学性质探究活动的设计,认识甲酸的化学性质。
4.能初步概述重要有机化合物之间的相互转化关系。乙醛的结构:官能团:醛基醛类中具有代表性的醛-乙醛乙醛的1H-NMR(一)组成和结构:C2H4O
CH3CHO一、乙醛: 分子式:
结构简式: (二)乙醛的性质1、物理性质: 无色有刺激性气味的液体,沸点20.8℃, 密度比水小,易挥发,易燃烧,能跟水、乙醇、氯仿等互溶。(有不饱和键)醛
基易被氧化预测性质:思考:分析醛基的结构,推测其在化学反应中的断裂方式易加成(1) 乙醛的加成反应:2、乙醛的化学性质OCHCHHHHH分析:碳元素的化合价变化结论:加氢碳元素被还原工业制醇的主要方法!思考:有机反应中的氧化反应和还原反应
我们应该怎样判断呢?有机物得O或去H, 发生氧化反应有机物失O或加H, 发生还原反应OCHCHHHO乙醛在一定的条件下被氧化为乙酸工业制羧酸的主要方法!B.催化氧化(2) 乙醛的氧化反应:①与氧气反应 A、燃烧 A.银镜反应---与银氨溶液的反应 Ag++NH3·H2O=AgOH ↓+ NH4+
AgOH+2 NH3·H2O=[Ag(NH3)2]++OH-+2H2O
或:AgOH+2 NH3·H2O=[Ag(NH3)2]OH+2H2O银氨溶液的配制方法:取一洁净试管,加入2ml2%的AgNO3溶液,再逐滴滴入2%的稀氨水,至生成的沉淀恰好溶解。②与其它氧化剂反应 此反应可以用于醛基的定性和定量检测应用:工业上用来制瓶胆和镜子5.1mol醛基被氧化,就应有2molAg被还原3.银氨溶液现用现制,不能久置;氨水滴加至沉淀恰好溶解,不可多加,注意:1.试管要洁净,2.水浴加热时不可振荡和摇动试管否则生不成银镜4.试管内壁银镜的处理:稀硝酸清洗
B、被新制Cu(OH)2氧化新制Cu(OH)2的配制方法:2mlNaOH(50%)+4~6滴CuSO4(2%)CH3CHO+2Cu(OH)2 CH3COOH+Cu2O+2H2O砖红色加热必须过量注意:
此反应必须在碱性条件下进行应用:
此反应也用于醛基的检验和测定医学上检验病人是否患糖尿病讨论:
1.实验中观察到有黑色物质生成,试解释
2.乙醛能否使溴水或酸性KMnO4溶液褪色?
B、被新制Cu(OH)2氧化新制Cu(OH)2的配制方法:2mlNaOH(50%)+4~6滴CuSO4(2%)CH3CHO+2Cu(OH)2 CH3COOH+Cu2O+2H2O砖红色加热必须过量C、使酸性KMnO4溶液褪色醛基中碳氧双键能与H2发生加成反应醛基中碳氢键较活泼,能被氧化成羧基加成反应氧化反应乙 醛小结:乙醛的化学性质注意:和C=C双键不同的是,通
常情况下, 醛基中的C=O不能
和HX、X2、H2O发生加成反应(四)乙醛的工业制取:(1)乙醇的催化氧化
(2)乙炔水化法:(3)乙烯氧化法:(三)乙醛的用途:
是有机合成的重要原料,主要用于制取
乙酸、丁醇、乙酸乙酯二、醛类1、定义:R-CHO烃基2、分类按醛基个数分 按烃基是否饱和分 按烃基类别分 一元醛、二元醛 多元醛 饱和醛 脂肪醛芳香醛不饱和醛 醛基与烃基直接相连所得的化合物。3、饱和一元醛 :H-CHOCH3-CHOCH3CH2-CHOCH3CH2CH2-CHO甲醛 乙醛 丙醛丁醛饱和一元脂肪醛的分子式的通式:
CnH2n+1CHOCnH2nO(n≥1)三、甲醛结构式:分子式:CH2O结构简式:HCHO电子式:官能团:问题讨论:
甲醛分子中碳原子的成键方式?所有原子共面-CHO-COH(一)组成与结构室内空气污染的头号杀手 练习:下列物质分子中所有原子一定不共面的是
CH2=CH2 B.
C. D.练习:下列物质分子中所有原子一定不共面的是
CH2=CH2 B.
C. D.CH3CHOD(二)物性:(三)用途:质量分数含35%~40%的水溶液称福尔马林:杀菌、防腐制酚醛树脂、染料、香料、医药氧化 氧化 还原 CH3OH HCHO HCOOH甲醛既能被氧化又能被还原又叫蚁醛,无色,有刺激性气味的气体,易溶于水。 (四)甲醛的化学性质 1.甲醛发生银镜反应 2.酚醛树脂的制取取2.5g的苯酚与一大试管中,加入2.5mL的40%的甲醛溶液,加入少量的浓盐酸,塞上有长导管的橡皮塞,于沸水中加热问题:
1.浓盐酸作用?
2.长导管作用?
3.为什么不用温度计?
4.实验结束试管如何处理?
有机物分子之间缩去小分子(H2O、NH3等)而形成高分子化合物的反应。缩聚反应:酚醛树脂是人类合成的第一种高分子材料,至今还广泛使用,条件不同时(催化剂)可以生成线型或体型的酚醛树脂线型酚醛树脂(盐酸作催化剂)体型的酚醛树脂(氨水作催化剂)甲醛和尿素反应生成脲醛树脂,脲醛树脂可制成热固性高分子黏合剂,用于胶合板、刨花板、人造维板等木材加工。 >C=O称羰基,是酮的官能团,丙酮是最简单的酮。拓展视野酮:羰基碳原子与两个烃基相连的化合物。酮丙酮不能被银氨溶液、新制的氢氧化铜等弱氧化剂氧化,但可催化加氢生成醇饱和一元酮的分子式的通式:
CnH2nO(n≥3)1、用化学方法鉴别下列各组物质
1)溴乙烷 、乙醇 、乙醛
2)苯、甲苯、乙醇、1-己烯、甲醛、苯酚1)用新制氢氧化铜溶液2)用溴水巩固练习:醋 保 健食物中存在的酸 CH2-COOH | HO-C-COOH | CH2-COOH柠檬酸 COOH | CH-OH | CH2
|
COOH
苹果酸 COOH | CH-OH | CH -OH
|
COOH
酒石酸 COOH | CH-OH | CH3乳酸C17H35COOH硬脂酸水杨酸一、乙酸的物理性质:颜色、状态:无色液体气味:有强烈刺激性气味沸点:117.9℃ (易挥发)熔点:16.6℃(无水乙酸又称为:冰醋酸)溶解性:易溶于水、乙醇等溶剂二、乙酸的结构与分子模型分子式:结构式结构简式或C2H4O2想一想? 结 构
对化学性质的影响三、乙酸的化学性质(一) 酸性:乙酸的酸性比碳酸、苯酚强,那它是强酸吗?请你设计一个实验来比较一下盐酸与乙酸的酸性强弱。请你思考:①导电性实验: ②化学反应速率结论:探究:
设计简单一次性完成的实验装置,
验证乙酸、碳酸、苯酚溶液的酸性强弱乙酸乙酯的酯化过程 ——酯化反应的脱水方式同位素示踪法实验验证练习:请你完成下列方程式2、( 形成环)思考:酯化反应是一个可逆反应,如果要增大乙酸乙酯的产率,你有哪些方法? (1)增大反应物的浓度例:加入过量的酸或醇(2)除去反应生成的水例:采用浓硫酸(3)及时除去反应生成的乙酸乙酯例:蒸馏出乙酸乙酯乙酸乙酯的实验室
制备的注意事项1.装药品的顺序如何?
2.浓硫酸的作用是什么?
3.如何提高乙酸乙酯的产率?
4.得到的反应产物是否纯净?主要杂质有哪些?
5.饱和Na2CO3溶液有什么作用?能否用氢氧化钠溶液代替饱和碳酸钠溶液?
6.为什么导管不插入饱和Na2CO3溶液中?有无其它防倒吸的方法?催化剂,吸水剂。防止受热不匀发生倒吸乙酸乙酯制取注意事项
1. 浓硫酸的作用: 3. 导管位置高于液面的目的:① 中和乙酸;
② 溶解乙醇;
③ 降低酯的溶解度,以便使酯分层析出。2. 饱和碳酸钠溶液的作用: 缩聚反应概念:
由有机化合物分子间脱去小分子获得高分子化合物的反应
举例:
P84推测:羧基醛基推测可能发生的化学反应方程式:银镜反应
与新制Cu(OH)2
与碱反应
酯化反应羧酸概念:
分子里烃基跟羧基直接相连的有机物。
饱和一元羧酸的通式:
CnH2nO2
羧酸的分类:
分类羧基数烃基结构练习:酸牛奶中含有乳酸,结构简式为:
(1)乳酸与碳酸氢钠反应的方程式
;
(2)乳酸与钠反应的方程式________________
(3)乳酸在浓硫酸存在下二分子反应,生成物为环状时,反应方程式为_________________;
(4)乳酸发生消去反应,生成物为 ,该物质与甲醇反应,生成的有机物结构简式为 ,这一产物又可以发生加聚反应,反应方程式为 。CH3─CH─COOH
│
OH
