氧化还原反应(共33张PPT)
文档属性
| 名称 | 氧化还原反应(共33张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 24.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-05-04 00:00:00 | ||
图片预览








文档简介
(共33张PPT)
必修一第一章第三节 氧化还原反应
学习
目标
PART
01
PART
02
从化合价变化和电子转移的角度认识并判断氧化还原反应。
能从宏观和微观相结合的角度理解氧化还原反应与四种基本反应类型的关系;掌握双线桥、单线桥的画法。
NaCl
在实验室中可以通过哪些化学反应制得氯化钠?
任务一 电子的转移与化合价的升降
活动1讨论在实验室中可以通过哪些化学反应制得氯化钠?
实验室制取氯化钠的方法
HCl + NaOH = NaCl + H2O
2Na + Cl2 = 2NaCl
复分解
化 合
······
······
HCl + NaOH = NaCl + H2O
2Na + Cl2 = 2NaCl
复分解
化 合
活动2 宏观上看,两种方法都能得到氯化钠,但从微观角度看,两个反应还是有很大差别的,找出它们的差别。
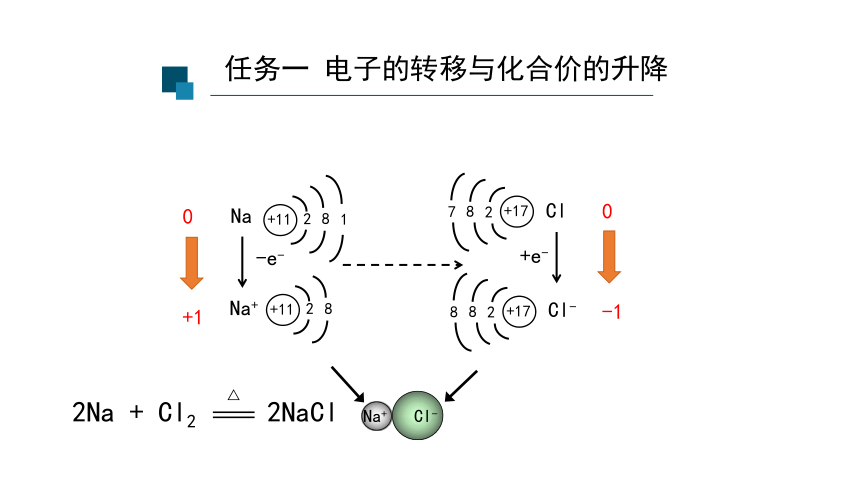
任务一 电子的转移与化合价的升降
+11
Na+ Cl-
Na
Cl
Cl-
Na+
0
+1
2
8
1
+11
2
8
+17
7
8
2
+17
8
8
2
-e-
+e-
0
-1
2Na + Cl2 2NaCl
△
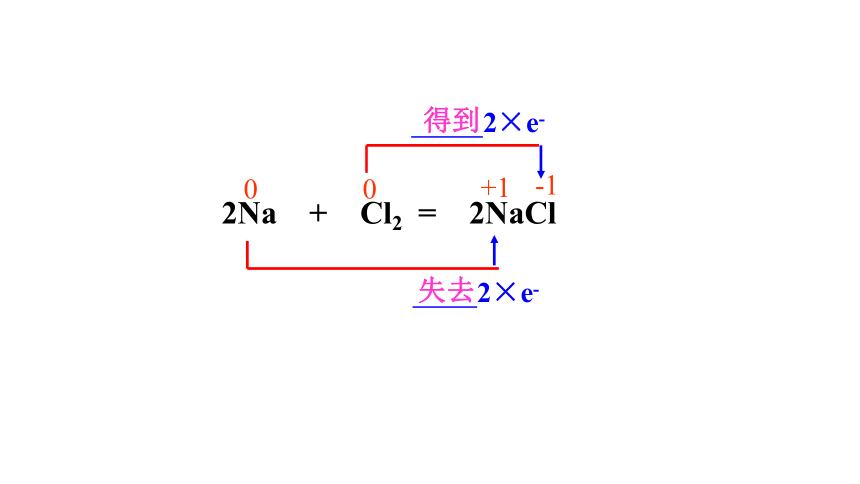
任务一 电子的转移与化合价的升降
2×e-
0
+1
0
失去
得到
2Na + Cl2 = 2NaCl
-1
2×e-
小结1 化合价升降与电子转移的关系
-4 -3 -2 -1 0 +1 +2 +3 +4 +5 +6 +7
化合价升高, 电子
化合价降低, 电子
任务一 电子的转移与化合价的升降
+1
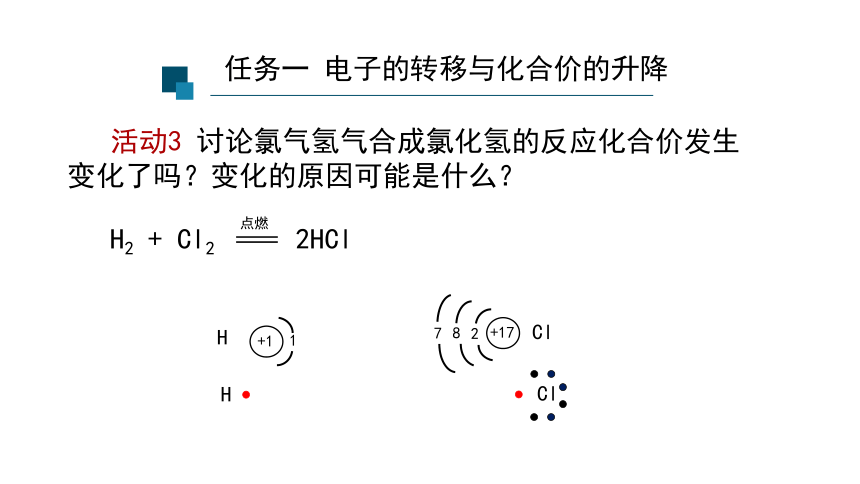
H
Cl
1
+17
7
8
2
Cl
H
H2 + Cl2 2HCl
点燃
活动3 讨论氯气氢气合成氯化氢的反应化合价发生变化了吗?变化的原因可能是什么?
任务一 电子的转移与化合价的升降
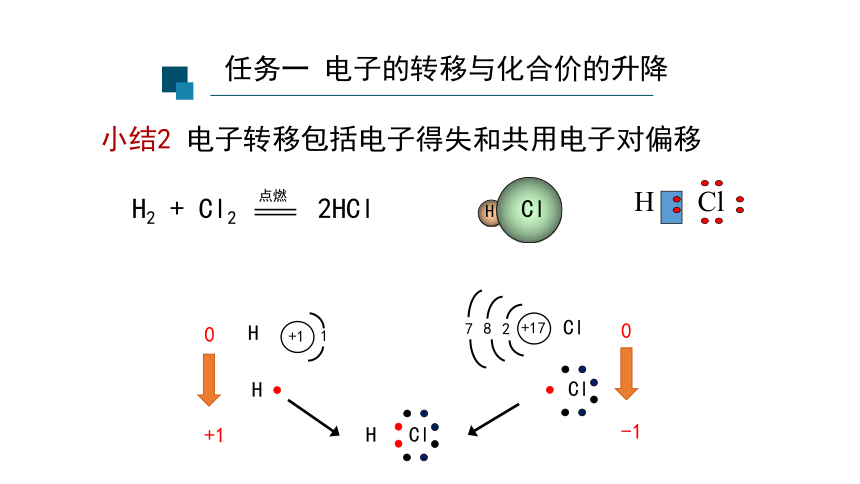
+1
H
Cl
0
+1
1
+17
7
8
2
0
-1
H Cl
H Cl
Cl
H
H2 + Cl2 2HCl
点燃
H Cl
小结2 电子转移包括电子得失和共用电子对偏移
任务一 电子的转移与化合价的升降
Zn + CuSO4 = ZnSO4 + Cu
Zn + Cu2+ Zn2+ + Cu
活动4 分析下面的反应是否有电子的转移,你的依据是什么?
任务一 电子的转移与化合价的升降
锌片
硫酸铜溶液
音乐片
活动5 利用图中装置进行锌与硫酸铜溶液反应的实验,实验现象之一是连接电路后音乐片发出声音。请你根据这一实验现象对该反应的原理做进一步思考。
铜片
任务一 电子的转移与化合价的升降
HCl + NaOH = NaCl + H2O
2Na + Cl2 = 2NaCl
复分解
化 合
活动1 对化学反应再次分类
有无电子转移
化学反应
氧化还原反应
非氧化还原反应
有
无
任务二 对化学反应的再分类
判断下列反应过程中有无化合价的改变?
(1)CaO + CO2 = CaCO3
(2)2HgO = 2Hg+ O2↑
(3)H2 + CuO = Cu + H2O
(4)CuCl2+2NaOH=Cu(OH)2↓+2NaCl
氧化还原反应
2. 氧化还原反应中有的元素的化合价可能不变。
1. 氧化还原反应中元素化合价有升有降。
小结1
氧化还原反应的重要特征是反应前后有元素的化合价变化。
任务二 对化学反应的再分类
活动2回顾初中氧化反应、还原反应的概念,思考氧化反应、还原反应能否单独发生?
任务二 对化学反应的再分类
年代 重大突破 氧化反应 还原反应
18世纪末 发现氧气 得氧的反应 失氧的反应
19世纪中 定义了 化合价 化合价升高的反应 化合价降低的反应
19世纪末 发现电子 失去电子或电子偏离的过程 得到电子或电子偏向的过程
氧化还原理论发展史
初步认识
H2 + CuO = Cu + H2O
物质得氧
物质失氧
氧化反应
还原反应
年代 重大突破 氧化反应 还原反应
18世纪末 发现氧气 得氧的反应 失氧的反应
19世纪中 定义了 化合价 化合价升高的反应 化合价降低的反应
19世纪末 发现电子 失去电子或电子偏离的过程 得到电子或电子偏向的过程
氧化还原理论发展史
初步认识
特征
H2 + CuO = Cu + H2O
物质得氧
物质失氧
氧化反应
还原反应
化合价升高
化合价降低
年代 重大突破 氧化反应 还原反应
18世纪末 发现氧气 得氧的反应 失氧的反应
19世纪中 定义了 化合价 化合价升高的反应 化合价降低的反应
19世纪末 发现电子 失去电子或电子偏离的过程 得到电子或电子偏向的过程
氧化还原理论发展史
初步认识
特征
本质
H2 + CuO = Cu + H2O
物质得氧
物质失氧
氧化反应
还原反应
化合价升高
化合价降低
得到2e-
失去2×e-
化合价降低的部分
化合价升高的部分
氧化还原反应
◎氧化反应:
◎还原反应:
还原反应
氧化反应
小结2
活动3 请你为下列反应分类,说明你的分类依据。
H2O + CaO Ca(OH)2
CaCO3 CaO + CO2 ↑
2H2O2 2H2O + O2 ↑
Fe + H2SO4 FeSO4 + H2 ↑
HCl + NaOH NaCl + H2O
2Na + Cl2 2NaCl
△
高温
MnO2
任务二 对化学反应的再分类
活动3 请你为下列反应分类,说明你的分类依据。
H2O + CaO Ca(OH)2
CaCO3 CaO + CO2 ↑
2H2O2 2H2O + O2 ↑
Fe + H2SO4 FeSO4 + H2 ↑
HCl + NaOH NaCl + H2O
2Na + Cl2 2NaCl
△
高温
MnO2
化合反应
分解反应
置换反应
复分解反应
任务二 对化学反应的再分类
活动3 请你为下列反应分类,说明你的分类依据。
H2O + CaO Ca(OH)2
CaCO3 CaO + CO2 ↑
2H2O2 2H2O + O2 ↑
Fe + H2SO4 FeSO4 + H2 ↑
HCl + NaOH NaCl + H2O
2Na + Cl2 2NaCl
△
高温
MnO2
化合反应
分解反应
置换反应
复分解反应
氧化还原反应
非氧化还原反应
任务二 对化学反应的再分类
小结3 4种基本类型的反应与氧化还原反应的关系。
任务二 对化学反应的再分类
氧化还原反应
非氧化还原反应
置换反应
复分解反应
化合反应
分解反应
任务三 巩固提升
活动1 请你对银-锌纽扣电池中涉及的反应从元素化合价的变化、电子转移、物质发生的反应等角度进行分析。
Ag2O + Zn 2Ag + ZnO
任务三 巩固提升
活动1 请你对银-锌纽扣电池中涉及的反应从元素化合价的变化、电子转移、物质发生的反应等角度进行分析。
Ag2O + Zn 2Ag + ZnO
+1 0 0 +2
化合价降低,得电子,被还原,发生还原反应
化合价升高,失电子,被氧化,发生氧化反应
总结
特征:有元素化合价升降
化学反应
氧化还原反应
本质:有电子转移
任务三 总结提升
元素化合价升高
失电子(或共用电子对偏离)
发生氧化反应
元素化合价降低
得电子(或共用电子对偏向)
发生还原反应
必修一第一章第三节 氧化还原反应
学习
目标
PART
01
PART
02
从化合价变化和电子转移的角度认识并判断氧化还原反应。
能从宏观和微观相结合的角度理解氧化还原反应与四种基本反应类型的关系;掌握双线桥、单线桥的画法。
NaCl
在实验室中可以通过哪些化学反应制得氯化钠?
任务一 电子的转移与化合价的升降
活动1讨论在实验室中可以通过哪些化学反应制得氯化钠?
实验室制取氯化钠的方法
HCl + NaOH = NaCl + H2O
2Na + Cl2 = 2NaCl
复分解
化 合
······
······
HCl + NaOH = NaCl + H2O
2Na + Cl2 = 2NaCl
复分解
化 合
活动2 宏观上看,两种方法都能得到氯化钠,但从微观角度看,两个反应还是有很大差别的,找出它们的差别。
任务一 电子的转移与化合价的升降
+11
Na+ Cl-
Na
Cl
Cl-
Na+
0
+1
2
8
1
+11
2
8
+17
7
8
2
+17
8
8
2
-e-
+e-
0
-1
2Na + Cl2 2NaCl
△
任务一 电子的转移与化合价的升降
2×e-
0
+1
0
失去
得到
2Na + Cl2 = 2NaCl
-1
2×e-
小结1 化合价升降与电子转移的关系
-4 -3 -2 -1 0 +1 +2 +3 +4 +5 +6 +7
化合价升高, 电子
化合价降低, 电子
任务一 电子的转移与化合价的升降
+1
H
Cl
1
+17
7
8
2
Cl
H
H2 + Cl2 2HCl
点燃
活动3 讨论氯气氢气合成氯化氢的反应化合价发生变化了吗?变化的原因可能是什么?
任务一 电子的转移与化合价的升降
+1
H
Cl
0
+1
1
+17
7
8
2
0
-1
H Cl
H Cl
Cl
H
H2 + Cl2 2HCl
点燃
H Cl
小结2 电子转移包括电子得失和共用电子对偏移
任务一 电子的转移与化合价的升降
Zn + CuSO4 = ZnSO4 + Cu
Zn + Cu2+ Zn2+ + Cu
活动4 分析下面的反应是否有电子的转移,你的依据是什么?
任务一 电子的转移与化合价的升降
锌片
硫酸铜溶液
音乐片
活动5 利用图中装置进行锌与硫酸铜溶液反应的实验,实验现象之一是连接电路后音乐片发出声音。请你根据这一实验现象对该反应的原理做进一步思考。
铜片
任务一 电子的转移与化合价的升降
HCl + NaOH = NaCl + H2O
2Na + Cl2 = 2NaCl
复分解
化 合
活动1 对化学反应再次分类
有无电子转移
化学反应
氧化还原反应
非氧化还原反应
有
无
任务二 对化学反应的再分类
判断下列反应过程中有无化合价的改变?
(1)CaO + CO2 = CaCO3
(2)2HgO = 2Hg+ O2↑
(3)H2 + CuO = Cu + H2O
(4)CuCl2+2NaOH=Cu(OH)2↓+2NaCl
氧化还原反应
2. 氧化还原反应中有的元素的化合价可能不变。
1. 氧化还原反应中元素化合价有升有降。
小结1
氧化还原反应的重要特征是反应前后有元素的化合价变化。
任务二 对化学反应的再分类
活动2回顾初中氧化反应、还原反应的概念,思考氧化反应、还原反应能否单独发生?
任务二 对化学反应的再分类
年代 重大突破 氧化反应 还原反应
18世纪末 发现氧气 得氧的反应 失氧的反应
19世纪中 定义了 化合价 化合价升高的反应 化合价降低的反应
19世纪末 发现电子 失去电子或电子偏离的过程 得到电子或电子偏向的过程
氧化还原理论发展史
初步认识
H2 + CuO = Cu + H2O
物质得氧
物质失氧
氧化反应
还原反应
年代 重大突破 氧化反应 还原反应
18世纪末 发现氧气 得氧的反应 失氧的反应
19世纪中 定义了 化合价 化合价升高的反应 化合价降低的反应
19世纪末 发现电子 失去电子或电子偏离的过程 得到电子或电子偏向的过程
氧化还原理论发展史
初步认识
特征
H2 + CuO = Cu + H2O
物质得氧
物质失氧
氧化反应
还原反应
化合价升高
化合价降低
年代 重大突破 氧化反应 还原反应
18世纪末 发现氧气 得氧的反应 失氧的反应
19世纪中 定义了 化合价 化合价升高的反应 化合价降低的反应
19世纪末 发现电子 失去电子或电子偏离的过程 得到电子或电子偏向的过程
氧化还原理论发展史
初步认识
特征
本质
H2 + CuO = Cu + H2O
物质得氧
物质失氧
氧化反应
还原反应
化合价升高
化合价降低
得到2e-
失去2×e-
化合价降低的部分
化合价升高的部分
氧化还原反应
◎氧化反应:
◎还原反应:
还原反应
氧化反应
小结2
活动3 请你为下列反应分类,说明你的分类依据。
H2O + CaO Ca(OH)2
CaCO3 CaO + CO2 ↑
2H2O2 2H2O + O2 ↑
Fe + H2SO4 FeSO4 + H2 ↑
HCl + NaOH NaCl + H2O
2Na + Cl2 2NaCl
△
高温
MnO2
任务二 对化学反应的再分类
活动3 请你为下列反应分类,说明你的分类依据。
H2O + CaO Ca(OH)2
CaCO3 CaO + CO2 ↑
2H2O2 2H2O + O2 ↑
Fe + H2SO4 FeSO4 + H2 ↑
HCl + NaOH NaCl + H2O
2Na + Cl2 2NaCl
△
高温
MnO2
化合反应
分解反应
置换反应
复分解反应
任务二 对化学反应的再分类
活动3 请你为下列反应分类,说明你的分类依据。
H2O + CaO Ca(OH)2
CaCO3 CaO + CO2 ↑
2H2O2 2H2O + O2 ↑
Fe + H2SO4 FeSO4 + H2 ↑
HCl + NaOH NaCl + H2O
2Na + Cl2 2NaCl
△
高温
MnO2
化合反应
分解反应
置换反应
复分解反应
氧化还原反应
非氧化还原反应
任务二 对化学反应的再分类
小结3 4种基本类型的反应与氧化还原反应的关系。
任务二 对化学反应的再分类
氧化还原反应
非氧化还原反应
置换反应
复分解反应
化合反应
分解反应
任务三 巩固提升
活动1 请你对银-锌纽扣电池中涉及的反应从元素化合价的变化、电子转移、物质发生的反应等角度进行分析。
Ag2O + Zn 2Ag + ZnO
任务三 巩固提升
活动1 请你对银-锌纽扣电池中涉及的反应从元素化合价的变化、电子转移、物质发生的反应等角度进行分析。
Ag2O + Zn 2Ag + ZnO
+1 0 0 +2
化合价降低,得电子,被还原,发生还原反应
化合价升高,失电子,被氧化,发生氧化反应
总结
特征:有元素化合价升降
化学反应
氧化还原反应
本质:有电子转移
任务三 总结提升
元素化合价升高
失电子(或共用电子对偏离)
发生氧化反应
元素化合价降低
得电子(或共用电子对偏向)
发生还原反应
