4.1 课时1醇的结构和性质 醇的重要应用 同步学案(含答案)2024-2025学年高二化学苏教版(2020)选择性必修3
文档属性
| 名称 | 4.1 课时1醇的结构和性质 醇的重要应用 同步学案(含答案)2024-2025学年高二化学苏教版(2020)选择性必修3 |
|
|
| 格式 | docx | ||
| 文件大小 | 670.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-05-06 00:00:00 | ||
图片预览




文档简介
课时1 醇的结构和性质 醇的重要应用
1. 认识醇的组成和结构特点。
2. 了解乙醇的化学性质,能从官能团角度了解醇类的其他化学性质。
3. 进一步理解醇参与反应时的各反应机理(断键方式),提高比较、分析、归纳、推理的能力。
4. 了解甲醇、乙二醇、丙三醇的结构、性质和用途,认识醇类对现代社会可持续发展的影响。
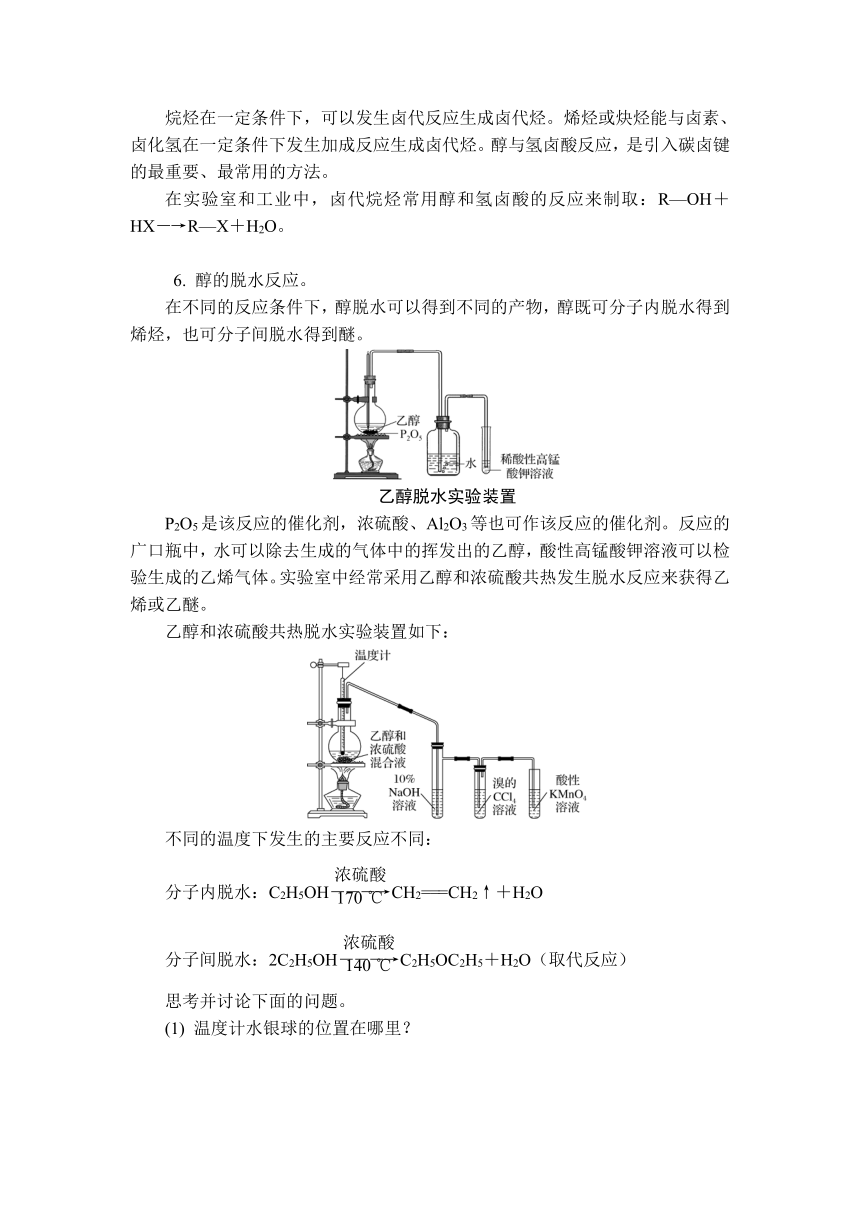
人类很早就认识了乙醇,乙醇的空间填充模型和结构式如下:
乙醇分子的空间填充模型 乙醇的结构式
1. 阅读教材第78页的内容,什么是醇?为什么要强调饱和碳?思考讨论:含羟基的物质是否一定是醇?
2. 乙醇是由乙烷中的一个氢原子被羟基取代生成,与乙烷性质差别很大,能得出什么结论?
1. 乙醇、醇与活泼金属的反应。
(1) 完成教材“基础实验”的实验1、实验2、实验3,体会教材探究乙醇中羟基氢原子的活泼性的方法,填写下表:
对比实验 反应现象 化学方程式
Na与水
Na与乙醇
Na与乙醚
结论:_____________________________________________________________。
(2) 相同物质的量的下列醇分别跟适量的钠作用,放出H2最多的是哪种?为什么?
A. 甲醇 B. 乙醇 C. 乙二醇 D. 丙三醇
2. 醇的催化氧化反应。
(1) 乙醇的催化氧化。
将铜丝放在酒精灯上烧红后(表面氧化),插入试管的乙醇溶液中,现象是 。右图标示出了乙醇中的各种化学键,讨论乙醇的催化过程中化学键的断裂情况。在不断鼓入空气的情况下,熄灭酒精灯,说明反应仍能继续进行的原因。
(2) 结合乙醇的催化氧化机理,讨论在铜或银催化下反应生成什么,写出该反应的化学方程式。
(3) 根据醇分子中羟基所连碳原子上氢原子数目的不同,可以分为伯醇、仲醇和叔醇:
伯醇:—CH2—OH
仲醇:
叔醇:
根据醇类催化氧化的反应机理,伯醇、仲醇能发生催化氧化反应,伯醇—CH2—OH可被氧化为醛,仲醇可被氧化为酮,叔醇不能发生催化氧化。
3. 醇与强氧化剂反应,乙醇可以使酸性高锰酸钾溶液和重铬酸钾溶液褪色,氧化过程如下:
CH3CH2OHCH3CHOCH3COOH
4. 醇可与羧酸发生酯化反应,反应中酸脱羟基,醇脱氢,写出乙酸与乙醇(用18O跟踪乙醇中的氧原子)反应的化学方程式。
5. 醇与氢溴酸的反应。
(1) 实验现象:________________________________
____________________,
化学方程式:_________________________________
_____________________。
(2) 加入蒸馏水、浓硫酸和溴化钠固体的目的什么?该反应可看作卤代烃水解的逆反应,浓硫酸在反应中还能起什么作用?
(3) 右侧长导管和烧杯中的水起到了什么作用?试管Ⅱ中的水起到了什么作用?
(4) 某同学设计实验检验所得的产品中是否含有溴乙烷:取试管Ⅱ中所得液体,向其中滴加硝酸银溶液,讨论该设计是否正确,为什么?
烷烃在一定条件下,可以发生卤代反应生成卤代烃。烯烃或炔烃能与卤素、卤化氢在一定条件下发生加成反应生成卤代烃。醇与氢卤酸反应,是引入碳卤键的最重要、最常用的方法。
在实验室和工业中,卤代烷烃常用醇和氢卤酸的反应来制取:R—OH+HX―→R—X+H2O。
6. 醇的脱水反应。
在不同的反应条件下,醇脱水可以得到不同的产物,醇既可分子内脱水得到烯烃,也可分子间脱水得到醚。
乙醇脱水实验装置
P2O5是该反应的催化剂,浓硫酸、Al2O3等也可作该反应的催化剂。反应的广口瓶中,水可以除去生成的气体中的挥发出的乙醇,酸性高锰酸钾溶液可以检验生成的乙烯气体。实验室中经常采用乙醇和浓硫酸共热发生脱水反应来获得乙烯或乙醚。
乙醇和浓硫酸共热脱水实验装置如下:
不同的温度下发生的主要反应不同:
分子内脱水:C2H5OHCH2===CH2↑+H2O
分子间脱水:2C2H5OHC2H5OC2H5+H2O(取代反应)
思考并讨论下面的问题。
(1) 温度计水银球的位置在哪里?
(2) 如何配制反应所需的混合液体?是否要加入沸石?
(3) 浓硫酸所起的作用是什么?
(4) 烧瓶中的液体混合物为什么会逐渐变黑?可能有哪些副反应?
(5) 生成的气体为什么要先通过NaOH溶液?
(6) 阅读教材第79页的内容,描述乙醇钠的用途和工业制取方法。
1. 醇分子间脱水反应属于取代反应,生成醚。乙醇与浓硫酸的混合液共热的温度控制在140 ℃,每两个醇分子间脱去一个水分子,反应生成的是乙醚。写出乙醇生成乙醚的化学方程式。
2. 醇分子内脱水属于消去反应:醇分子内脱去的水分子是由羟基与其所在的碳原子的邻位碳原子上的氢原子结合而成,碳碳间形成不饱和键。
结合上述消去反应机理,讨论是否所有的醇都能发生消去反应,消去反应对分子结构有什么要求?
1. 了解乙醇的应用。
2. 甲醇俗称木精或木醇,是无色透明的液体。误饮甲醇有什么危害?甲醇可用作燃料,在能源工业领域有着十分广阔的应用前景。阅读教材,了解甲醇燃料电池的原理,写出电极反应方程式。
3. 根据醇分子中的羟基数目,如何对醇进行分类?什么叫多元醇?
4. 乙二醇、丙三醇是否互为同系物?分别有什么特性和用途?硝化甘油如何生成,有什么应用?
1. (常州第二中学期中)绿色化学对化学反应提出了“原子经济性”(原子节约)的新概念及要求。理想的原子经济性反应是原料分子全部转变成所需产物,不产生副产物,实现零排放。以下反应符合绿色化学原理的是( )
A. 乙烯与O2在银催化下生成环氧乙烷
B. 乙烷与氯气制备氯乙烷
C. 以苯和乙醇为原料,在一定条件下生产乙苯
D. 乙醇和浓硫酸共热制备乙烯
2. (常州北郊高级中学期中)下列反应生成的有机物只有一种的是( )
A. CH3CH===CH2 与 HCl 加成
B. CH3CH(OH)CH3 在浓硫酸作用下发生分子内脱水
C. 1 mol CH3CH===CHCH===CHCH3 与1 mol Br2 反应
D. 1 mol CH4 与 1 mol Cl2 在光照条件下的反应
3. (常州检测)已知:实验室制备乙烯的反应为CH3CH2OH
CH2===CH2↑+H2O,生成的乙烯中混有CO2、SO2等杂质。实验小组用如图装置制备并收集乙烯(尾气处理略去),下列说法不正确的是( )
A. 配制①中混合液时,应将浓硫酸加入乙醇中
B. 应先检验装置的气密性,再加入药品、加热
C. 试剂X可选择NaOH溶液
D. ④⑤均适宜作为收集装置
4. (盐城响水中学学情分析)某有机物分子的球棍模型如图所示。下列关于该物质的说法正确的是( )
A. 能与金属钠反应生成氢气
B. 能用于萃取碘水中的单质碘
C. 能使紫色石蕊试液变红
D. 能与醋酸发生中和反应
5. (南京期末)下列物质中,属于乙醇的同系物的是( )
A. B.
C. CH2OHCH2OH D. (CH3)2CHOH
6. (镇江中学检测)人体缺乏维生素A会出现皮肤干燥、夜盲症等症状。维生素A又称视黄醇,分子结构如图所示。下列说法正确的是( )
A. 1 mol维生素A最多能与7 mol H2发生加成反应
B. 维生素A不能被氧化为醛
C. 维生素A是一种易溶于水的醇
D. 维生素A的分子式为C20H30O
7. 2021年诺贝尔生理学或医学奖表彰在“发现温度和触觉感受器——薄荷醇”领域的贡献。下列关于薄荷醇(如图所示)的说法正确的是( )
A. 可被氧化为醛
B. 可发生消去反应
C. 分子式为C10H18O
D. 其分子中存在苯环结构
8. 有机物R是一种有机消毒剂,其结构如图所示,下列说法不正确的是[已知:有机物的结构可用键线式简化表示,如丙烯醇(CH2OHCH===CH2)可表示为 ]( )
A. 有机物R的分子式为C10H18O
B. 有机物R与丙烯醇属于同系物
C. R能被酸性高锰酸钾溶液氧化
D. R能与金属钠反应生成氢气
9. 一定量的乙醇在氧气不足的情况下燃烧,得到CO、CO2和水的总质量为27.6 g,若其中水的质量为10.8 g,则CO的质量是( )
A. 4.4 g B. 2.2 g
C. 1.4 g D. 在2.2 g和4.4 g之间
10. (泰州中学阶段考试)下列有机物中,既能发生催化氧化又能发生消去反应,且消去产物中存在同分异构体的是( )
A. CH3—OH B.
C. D.
11. (淮安高中校协作体期中)乙醇(CH3CH2OH)既是生活中常见的有机物,又是重要的化工原料。
(1) 工业上可用乙烯制备乙醇,其反应的化学方程式为CH2 ===CH2+H2O
CH3CH2OH,该反应属于 (填“加成”或“取代”)反应。
(2) 官能团决定有机物的性质。乙醇中含有的官能团名称是 。
(3) 为探究乙醇的性质,某学生向试管中加入3 mL乙醇,将下端绕成螺旋状的铜丝在酒精灯火焰上灼烧至红热后,迅速插入乙醇中,可观察到铜丝表面由黑色变成红色,说明乙醇具有 性。
(4) 萃取是物质分离的一种方法。某学生拟用乙醇萃取溴水中的Br2,判断该方法是否可行: (填“是”或“否”),判断的理由是 。
12. (宿迁沭阳期中)某化学兴趣小组用图1所示装置进行探究实验,以验证产物中有乙烯生成且乙烯具有不饱和性。当温度迅速上升后,可观察到试管中溴水褪色,烧瓶中浓硫酸与乙醇的混合液体变为棕黑色。
(1) 写出该实验中生成乙烯的化学方程式: 。
(2) 甲同学认为:考虑到该混合液体反应的复杂性,溴水褪色的现象不能证明反应中有乙烯生成且乙烯具有不饱和性,其理由正确是 (填字母)。
a. 乙烯与溴水易发生取代反应
b. 使溴水褪色的反应不一定是加成反应
c. 使溴水褪色的物质不一定是乙烯
(3) 乙同学经过仔细观察试管中另一实验现象后,证明反应中有乙烯生成,请简述这种这一实验现象: 。
(4) 丙同学对上述实验装置进行了改进,在Ⅰ和Ⅱ之间增加图2装置以除去乙醇蒸气和SO2,则A中的试剂是 ,B中的试剂为 。
课时1 醇的结构和性质 醇的重要应用
【活动方案】
活动一
1. 烃分子中饱和碳原子上的氢原子被羟基取代所形成的化合物称为醇。当羟基与碳碳双键或碳碳三键相连时,容易发生异构化;例如,羟基与碳碳双键(C===C)相连时,会转变为醛或酮。含羟基的物质不一定是醇,只有羟基与饱和碳原子相连的物质才是醇。
2. 有机物的性质与官能团关系密切,乙醇的性质与羟基有很大关系。
活动二
1. (1) 反应剧烈,生成气体 2Na+2H2O===2NaOH+H2↑ 反应平缓,生成气体 2C2H5OH+2Na―→2C2H5ONa+H2↑ 无明显现象 Na与乙醚不反应 钠与羟基中的氢原子反应,与烃基中的氢原子不反应 (2) 丙三醇生成的氢气最多,因为其分子中含有3个羟基。
2. (1) 铜丝由黑色变为红色,闻到刺激性气味 反应中c、e处化学键断裂,然后在C、O之间再形成1个共价键,变为C===O。乙醇催化氧化反应是放热反应。
(2) +O2+2H2O
4. CH3CHOH+CH3COOHCH3CO18OCH2CH3+H2O
5. (1) 试管内可看到有不溶于水的油状液体生成 C2H5OH+HBrC2H5Br+H2O (2) 加入蒸馏水、浓硫酸和溴化钠固体的目的是获得氢溴酸。浓硫酸在反应中还能作吸水剂,促进反应正向进行。 (3) 右侧长导管除导气外、还使生成的产物冷凝转化液态;烧杯中的水同样起到了冷凝作用,减少生成物挥发。试管Ⅱ中的水可以溶解挥发出的乙醇,分离出生成的溴乙烷。 (4) 错误,溴乙烷不能电离出溴离子,不能直接用硝酸银溶液检验是否生成溴乙烷。
6. (1) 温度计水银球位于液面下。 (2) 将浓硫酸慢慢加入乙醇中,需要加入沸石,防止发生暴沸。 (3) 催化剂、脱水剂。 (4) 发生了副反应生成炭,反应除了不同温度下生成乙烯、乙醚外,还可能因为浓硫酸的强氧化性生成CO2、SO2等气体。 (5) 氢氧化钠溶液可以溶解挥发出的乙醇,除去副反应生成的CO2、SO2等。 (6) 乙醇与钠反应生成乙醇钠,并放出氢气,乙醇钠是有机合成中的重要试剂,它常用于医药和农药等生产中,也常用作有机合成中的强碱性催化剂。
活动三
1. 2CH3CH2OHC2H5OC2H5+H2O
2. 发生消去反应的醇分子中,连有羟基(—OH)的碳原子必须有相邻的碳原子,且此相邻的碳原子上还必须连有氢原子时,才可发生消去反应而形成不饱和键。含一个碳原子的醇(如CH3OH)无相邻碳原子,所以不能发生消去反应;与羟基(—OH)相连碳原子相邻的碳原子上没有氢原子的醇也不能发生消去反应,如:、等。
活动四
2. 甲醇有剧毒,误饮少量即会致眼睛失明甚至致人死亡。
负极:CH3OH+H2O -6e-―→CO2↑+6H+
正极:O2+4H++4e-―→2H2O
3. 根据醇分子中含有的羟基数目,可以将醇分为一元醇、二元醇、三元醇等。分子中含有两个或两个以上羟基的醇又称为多元醇。
4. 二者不是同系物,各分子中—OH数目不同,组成不相差CH2的整数倍。乙二醇是一种无色、黏稠、有甜味的液体,主要用来生产聚酯纤维,乙二醇的水溶液凝固点很低,可作汽车发动机的抗冻剂;丙三醇俗称甘油,是无色、黏稠、有甜味的液体,吸湿性强,有护肤作用,是重要的化工原料。丙三醇与硝酸发生反应生成的三硝酸甘油酯是一种烈性炸药,俗称硝化甘油,硝化甘油是一种黄色的油状透明液体,受到震动会发生爆炸;硝化甘油可用作心绞痛的缓解药物。
【课堂反馈】
1. A 乙烯与氧气在银催化作用下生成环氧乙烷,没有副产物生成,原子利用率100%,A正确;乙烷与氯气制备氯乙烷,存在副反应,反应产物除了氯乙烷外还有氯化氢和其他乙烷的取代产物等,原子没有全部利用,B错误;苯与乙醇在一定条件下生产乙苯,有副产物水生成,原子利用率不为100%,C错误;乙醇和浓硫酸混合制乙烯,有副产物水生成,原子利用率不为100%,D错误。
2. B CH3CH===CH2与HCl发生加成反应生成CH3CH2CH2Cl或CH3CHClCH3,A不符合题意;CH3CH(OH)CH3在浓硫酸作用下发生分子内脱水,生成CH3CH===CH2,B符合题意;1 mol CH3CH===CHCH===CHCH3与1 mol Br2可发生1,2 加成或1,4 加成,C不符合题意;1 mol CH4与 1 mol Cl2 在光照条件下反应生成一氯甲烷或二氯甲烷等,D不符合题意。
3. D 乙烯密度与空气非常接近,用排空气法收集会导致收集的气体不纯,④不适宜作为收集装置,D错误。
4. A 根据图中球棍模型可知该有机物是乙醇,结构简式为CH3CH2OH。羟基能与金属钠反应生成氢气,A正确;乙醇与水互溶,不能作萃取剂,B错误;乙醇中无H+,不能使紫色石蕊试液变红,C错误;乙醇与醋酸的反应是酯化反应,D错误。
5. D 苯环是不饱和烃基,不属于乙醇的同系物,A错误;邻甲基苯酚含有苯环,不属于乙醇的同系物,B错误;乙二醇含有羟基数目为2,因此不是乙醇的同系物,C错误;(CH3)2CHOH含有1个羟基,烃基为烷基,是乙醇的同系物,D正确。
6. D 维生素A分子中含有5个碳碳双键,1 mol维生素A最多能与5 mol H2发生加成反应,A错误;维生素A分子中含有“—CH2OH”,能被氧化为醛,B错误;根据醇的溶解性规律,烃基越大越难溶于水,维生素A分子中烃基较大,故维生素A不是一种易溶于水的醇,C错误。
7. B α C上只有一个H原子,无法氧化为醛,A错误;薄荷醇的两个β C上均有H原子,可发生消去反应,B正确; 薄荷醇的分子式为 C10H20O,C错误;由结构简式可知薄荷醇分子中不含苯环,D错误。
8. B 根据R的结构可知其分子式为C10H18O,A正确;R中存在环状结构,丙烯醇是链状结构,二者不属于同系物,B错误;R中含有碳碳双键,能被酸性高锰酸钾溶液氧化,C正确;R中含有羟基,能与金属钠反应生成氢气,D正确。
9. C n(H2O)==0.6 mol,由氢原子守恒得:n(C2H5OH)===0.2 mol,由碳原子守恒得:n(CO)+n(CO2)=0.2 mol×2=0.4 mol,碳的氧化物总质量为27.6 g-10.8 g=16.8 g,设CO与CO2的物质的量分别为x和y。x+y=0.4 mol,28x g/mol+44y g/mol=16.8 g(碳原子质量守恒),解得x=0.05 mol,y=0.35 mol,m(CO)=0.05 mol×28 g/mol=1.4 g。故选C。
10. D 醇能发生消去反应,说明—OH具有邻碳氢,A不符合题意;醇的消去产物中存在同分异构体,说明醇分子不对称,B不符合题意;醇能发生催化氧化,说明—OH具有同碳氢,C不符合题意。
11. (1) 加成 (2) 羟基 (3) 还原 (4) 否 乙醇与溴水互溶
12. (1) CH3CH2OHCH2===CH2↑+H2O (2) bc (3) 液体分层,下层为油状液体 (4) NaOH溶液 品红溶液(其他合理答案也可)
1. 认识醇的组成和结构特点。
2. 了解乙醇的化学性质,能从官能团角度了解醇类的其他化学性质。
3. 进一步理解醇参与反应时的各反应机理(断键方式),提高比较、分析、归纳、推理的能力。
4. 了解甲醇、乙二醇、丙三醇的结构、性质和用途,认识醇类对现代社会可持续发展的影响。
人类很早就认识了乙醇,乙醇的空间填充模型和结构式如下:
乙醇分子的空间填充模型 乙醇的结构式
1. 阅读教材第78页的内容,什么是醇?为什么要强调饱和碳?思考讨论:含羟基的物质是否一定是醇?
2. 乙醇是由乙烷中的一个氢原子被羟基取代生成,与乙烷性质差别很大,能得出什么结论?
1. 乙醇、醇与活泼金属的反应。
(1) 完成教材“基础实验”的实验1、实验2、实验3,体会教材探究乙醇中羟基氢原子的活泼性的方法,填写下表:
对比实验 反应现象 化学方程式
Na与水
Na与乙醇
Na与乙醚
结论:_____________________________________________________________。
(2) 相同物质的量的下列醇分别跟适量的钠作用,放出H2最多的是哪种?为什么?
A. 甲醇 B. 乙醇 C. 乙二醇 D. 丙三醇
2. 醇的催化氧化反应。
(1) 乙醇的催化氧化。
将铜丝放在酒精灯上烧红后(表面氧化),插入试管的乙醇溶液中,现象是 。右图标示出了乙醇中的各种化学键,讨论乙醇的催化过程中化学键的断裂情况。在不断鼓入空气的情况下,熄灭酒精灯,说明反应仍能继续进行的原因。
(2) 结合乙醇的催化氧化机理,讨论在铜或银催化下反应生成什么,写出该反应的化学方程式。
(3) 根据醇分子中羟基所连碳原子上氢原子数目的不同,可以分为伯醇、仲醇和叔醇:
伯醇:—CH2—OH
仲醇:
叔醇:
根据醇类催化氧化的反应机理,伯醇、仲醇能发生催化氧化反应,伯醇—CH2—OH可被氧化为醛,仲醇可被氧化为酮,叔醇不能发生催化氧化。
3. 醇与强氧化剂反应,乙醇可以使酸性高锰酸钾溶液和重铬酸钾溶液褪色,氧化过程如下:
CH3CH2OHCH3CHOCH3COOH
4. 醇可与羧酸发生酯化反应,反应中酸脱羟基,醇脱氢,写出乙酸与乙醇(用18O跟踪乙醇中的氧原子)反应的化学方程式。
5. 醇与氢溴酸的反应。
(1) 实验现象:________________________________
____________________,
化学方程式:_________________________________
_____________________。
(2) 加入蒸馏水、浓硫酸和溴化钠固体的目的什么?该反应可看作卤代烃水解的逆反应,浓硫酸在反应中还能起什么作用?
(3) 右侧长导管和烧杯中的水起到了什么作用?试管Ⅱ中的水起到了什么作用?
(4) 某同学设计实验检验所得的产品中是否含有溴乙烷:取试管Ⅱ中所得液体,向其中滴加硝酸银溶液,讨论该设计是否正确,为什么?
烷烃在一定条件下,可以发生卤代反应生成卤代烃。烯烃或炔烃能与卤素、卤化氢在一定条件下发生加成反应生成卤代烃。醇与氢卤酸反应,是引入碳卤键的最重要、最常用的方法。
在实验室和工业中,卤代烷烃常用醇和氢卤酸的反应来制取:R—OH+HX―→R—X+H2O。
6. 醇的脱水反应。
在不同的反应条件下,醇脱水可以得到不同的产物,醇既可分子内脱水得到烯烃,也可分子间脱水得到醚。
乙醇脱水实验装置
P2O5是该反应的催化剂,浓硫酸、Al2O3等也可作该反应的催化剂。反应的广口瓶中,水可以除去生成的气体中的挥发出的乙醇,酸性高锰酸钾溶液可以检验生成的乙烯气体。实验室中经常采用乙醇和浓硫酸共热发生脱水反应来获得乙烯或乙醚。
乙醇和浓硫酸共热脱水实验装置如下:
不同的温度下发生的主要反应不同:
分子内脱水:C2H5OHCH2===CH2↑+H2O
分子间脱水:2C2H5OHC2H5OC2H5+H2O(取代反应)
思考并讨论下面的问题。
(1) 温度计水银球的位置在哪里?
(2) 如何配制反应所需的混合液体?是否要加入沸石?
(3) 浓硫酸所起的作用是什么?
(4) 烧瓶中的液体混合物为什么会逐渐变黑?可能有哪些副反应?
(5) 生成的气体为什么要先通过NaOH溶液?
(6) 阅读教材第79页的内容,描述乙醇钠的用途和工业制取方法。
1. 醇分子间脱水反应属于取代反应,生成醚。乙醇与浓硫酸的混合液共热的温度控制在140 ℃,每两个醇分子间脱去一个水分子,反应生成的是乙醚。写出乙醇生成乙醚的化学方程式。
2. 醇分子内脱水属于消去反应:醇分子内脱去的水分子是由羟基与其所在的碳原子的邻位碳原子上的氢原子结合而成,碳碳间形成不饱和键。
结合上述消去反应机理,讨论是否所有的醇都能发生消去反应,消去反应对分子结构有什么要求?
1. 了解乙醇的应用。
2. 甲醇俗称木精或木醇,是无色透明的液体。误饮甲醇有什么危害?甲醇可用作燃料,在能源工业领域有着十分广阔的应用前景。阅读教材,了解甲醇燃料电池的原理,写出电极反应方程式。
3. 根据醇分子中的羟基数目,如何对醇进行分类?什么叫多元醇?
4. 乙二醇、丙三醇是否互为同系物?分别有什么特性和用途?硝化甘油如何生成,有什么应用?
1. (常州第二中学期中)绿色化学对化学反应提出了“原子经济性”(原子节约)的新概念及要求。理想的原子经济性反应是原料分子全部转变成所需产物,不产生副产物,实现零排放。以下反应符合绿色化学原理的是( )
A. 乙烯与O2在银催化下生成环氧乙烷
B. 乙烷与氯气制备氯乙烷
C. 以苯和乙醇为原料,在一定条件下生产乙苯
D. 乙醇和浓硫酸共热制备乙烯
2. (常州北郊高级中学期中)下列反应生成的有机物只有一种的是( )
A. CH3CH===CH2 与 HCl 加成
B. CH3CH(OH)CH3 在浓硫酸作用下发生分子内脱水
C. 1 mol CH3CH===CHCH===CHCH3 与1 mol Br2 反应
D. 1 mol CH4 与 1 mol Cl2 在光照条件下的反应
3. (常州检测)已知:实验室制备乙烯的反应为CH3CH2OH
CH2===CH2↑+H2O,生成的乙烯中混有CO2、SO2等杂质。实验小组用如图装置制备并收集乙烯(尾气处理略去),下列说法不正确的是( )
A. 配制①中混合液时,应将浓硫酸加入乙醇中
B. 应先检验装置的气密性,再加入药品、加热
C. 试剂X可选择NaOH溶液
D. ④⑤均适宜作为收集装置
4. (盐城响水中学学情分析)某有机物分子的球棍模型如图所示。下列关于该物质的说法正确的是( )
A. 能与金属钠反应生成氢气
B. 能用于萃取碘水中的单质碘
C. 能使紫色石蕊试液变红
D. 能与醋酸发生中和反应
5. (南京期末)下列物质中,属于乙醇的同系物的是( )
A. B.
C. CH2OHCH2OH D. (CH3)2CHOH
6. (镇江中学检测)人体缺乏维生素A会出现皮肤干燥、夜盲症等症状。维生素A又称视黄醇,分子结构如图所示。下列说法正确的是( )
A. 1 mol维生素A最多能与7 mol H2发生加成反应
B. 维生素A不能被氧化为醛
C. 维生素A是一种易溶于水的醇
D. 维生素A的分子式为C20H30O
7. 2021年诺贝尔生理学或医学奖表彰在“发现温度和触觉感受器——薄荷醇”领域的贡献。下列关于薄荷醇(如图所示)的说法正确的是( )
A. 可被氧化为醛
B. 可发生消去反应
C. 分子式为C10H18O
D. 其分子中存在苯环结构
8. 有机物R是一种有机消毒剂,其结构如图所示,下列说法不正确的是[已知:有机物的结构可用键线式简化表示,如丙烯醇(CH2OHCH===CH2)可表示为 ]( )
A. 有机物R的分子式为C10H18O
B. 有机物R与丙烯醇属于同系物
C. R能被酸性高锰酸钾溶液氧化
D. R能与金属钠反应生成氢气
9. 一定量的乙醇在氧气不足的情况下燃烧,得到CO、CO2和水的总质量为27.6 g,若其中水的质量为10.8 g,则CO的质量是( )
A. 4.4 g B. 2.2 g
C. 1.4 g D. 在2.2 g和4.4 g之间
10. (泰州中学阶段考试)下列有机物中,既能发生催化氧化又能发生消去反应,且消去产物中存在同分异构体的是( )
A. CH3—OH B.
C. D.
11. (淮安高中校协作体期中)乙醇(CH3CH2OH)既是生活中常见的有机物,又是重要的化工原料。
(1) 工业上可用乙烯制备乙醇,其反应的化学方程式为CH2 ===CH2+H2O
CH3CH2OH,该反应属于 (填“加成”或“取代”)反应。
(2) 官能团决定有机物的性质。乙醇中含有的官能团名称是 。
(3) 为探究乙醇的性质,某学生向试管中加入3 mL乙醇,将下端绕成螺旋状的铜丝在酒精灯火焰上灼烧至红热后,迅速插入乙醇中,可观察到铜丝表面由黑色变成红色,说明乙醇具有 性。
(4) 萃取是物质分离的一种方法。某学生拟用乙醇萃取溴水中的Br2,判断该方法是否可行: (填“是”或“否”),判断的理由是 。
12. (宿迁沭阳期中)某化学兴趣小组用图1所示装置进行探究实验,以验证产物中有乙烯生成且乙烯具有不饱和性。当温度迅速上升后,可观察到试管中溴水褪色,烧瓶中浓硫酸与乙醇的混合液体变为棕黑色。
(1) 写出该实验中生成乙烯的化学方程式: 。
(2) 甲同学认为:考虑到该混合液体反应的复杂性,溴水褪色的现象不能证明反应中有乙烯生成且乙烯具有不饱和性,其理由正确是 (填字母)。
a. 乙烯与溴水易发生取代反应
b. 使溴水褪色的反应不一定是加成反应
c. 使溴水褪色的物质不一定是乙烯
(3) 乙同学经过仔细观察试管中另一实验现象后,证明反应中有乙烯生成,请简述这种这一实验现象: 。
(4) 丙同学对上述实验装置进行了改进,在Ⅰ和Ⅱ之间增加图2装置以除去乙醇蒸气和SO2,则A中的试剂是 ,B中的试剂为 。
课时1 醇的结构和性质 醇的重要应用
【活动方案】
活动一
1. 烃分子中饱和碳原子上的氢原子被羟基取代所形成的化合物称为醇。当羟基与碳碳双键或碳碳三键相连时,容易发生异构化;例如,羟基与碳碳双键(C===C)相连时,会转变为醛或酮。含羟基的物质不一定是醇,只有羟基与饱和碳原子相连的物质才是醇。
2. 有机物的性质与官能团关系密切,乙醇的性质与羟基有很大关系。
活动二
1. (1) 反应剧烈,生成气体 2Na+2H2O===2NaOH+H2↑ 反应平缓,生成气体 2C2H5OH+2Na―→2C2H5ONa+H2↑ 无明显现象 Na与乙醚不反应 钠与羟基中的氢原子反应,与烃基中的氢原子不反应 (2) 丙三醇生成的氢气最多,因为其分子中含有3个羟基。
2. (1) 铜丝由黑色变为红色,闻到刺激性气味 反应中c、e处化学键断裂,然后在C、O之间再形成1个共价键,变为C===O。乙醇催化氧化反应是放热反应。
(2) +O2+2H2O
4. CH3CHOH+CH3COOHCH3CO18OCH2CH3+H2O
5. (1) 试管内可看到有不溶于水的油状液体生成 C2H5OH+HBrC2H5Br+H2O (2) 加入蒸馏水、浓硫酸和溴化钠固体的目的是获得氢溴酸。浓硫酸在反应中还能作吸水剂,促进反应正向进行。 (3) 右侧长导管除导气外、还使生成的产物冷凝转化液态;烧杯中的水同样起到了冷凝作用,减少生成物挥发。试管Ⅱ中的水可以溶解挥发出的乙醇,分离出生成的溴乙烷。 (4) 错误,溴乙烷不能电离出溴离子,不能直接用硝酸银溶液检验是否生成溴乙烷。
6. (1) 温度计水银球位于液面下。 (2) 将浓硫酸慢慢加入乙醇中,需要加入沸石,防止发生暴沸。 (3) 催化剂、脱水剂。 (4) 发生了副反应生成炭,反应除了不同温度下生成乙烯、乙醚外,还可能因为浓硫酸的强氧化性生成CO2、SO2等气体。 (5) 氢氧化钠溶液可以溶解挥发出的乙醇,除去副反应生成的CO2、SO2等。 (6) 乙醇与钠反应生成乙醇钠,并放出氢气,乙醇钠是有机合成中的重要试剂,它常用于医药和农药等生产中,也常用作有机合成中的强碱性催化剂。
活动三
1. 2CH3CH2OHC2H5OC2H5+H2O
2. 发生消去反应的醇分子中,连有羟基(—OH)的碳原子必须有相邻的碳原子,且此相邻的碳原子上还必须连有氢原子时,才可发生消去反应而形成不饱和键。含一个碳原子的醇(如CH3OH)无相邻碳原子,所以不能发生消去反应;与羟基(—OH)相连碳原子相邻的碳原子上没有氢原子的醇也不能发生消去反应,如:、等。
活动四
2. 甲醇有剧毒,误饮少量即会致眼睛失明甚至致人死亡。
负极:CH3OH+H2O -6e-―→CO2↑+6H+
正极:O2+4H++4e-―→2H2O
3. 根据醇分子中含有的羟基数目,可以将醇分为一元醇、二元醇、三元醇等。分子中含有两个或两个以上羟基的醇又称为多元醇。
4. 二者不是同系物,各分子中—OH数目不同,组成不相差CH2的整数倍。乙二醇是一种无色、黏稠、有甜味的液体,主要用来生产聚酯纤维,乙二醇的水溶液凝固点很低,可作汽车发动机的抗冻剂;丙三醇俗称甘油,是无色、黏稠、有甜味的液体,吸湿性强,有护肤作用,是重要的化工原料。丙三醇与硝酸发生反应生成的三硝酸甘油酯是一种烈性炸药,俗称硝化甘油,硝化甘油是一种黄色的油状透明液体,受到震动会发生爆炸;硝化甘油可用作心绞痛的缓解药物。
【课堂反馈】
1. A 乙烯与氧气在银催化作用下生成环氧乙烷,没有副产物生成,原子利用率100%,A正确;乙烷与氯气制备氯乙烷,存在副反应,反应产物除了氯乙烷外还有氯化氢和其他乙烷的取代产物等,原子没有全部利用,B错误;苯与乙醇在一定条件下生产乙苯,有副产物水生成,原子利用率不为100%,C错误;乙醇和浓硫酸混合制乙烯,有副产物水生成,原子利用率不为100%,D错误。
2. B CH3CH===CH2与HCl发生加成反应生成CH3CH2CH2Cl或CH3CHClCH3,A不符合题意;CH3CH(OH)CH3在浓硫酸作用下发生分子内脱水,生成CH3CH===CH2,B符合题意;1 mol CH3CH===CHCH===CHCH3与1 mol Br2可发生1,2 加成或1,4 加成,C不符合题意;1 mol CH4与 1 mol Cl2 在光照条件下反应生成一氯甲烷或二氯甲烷等,D不符合题意。
3. D 乙烯密度与空气非常接近,用排空气法收集会导致收集的气体不纯,④不适宜作为收集装置,D错误。
4. A 根据图中球棍模型可知该有机物是乙醇,结构简式为CH3CH2OH。羟基能与金属钠反应生成氢气,A正确;乙醇与水互溶,不能作萃取剂,B错误;乙醇中无H+,不能使紫色石蕊试液变红,C错误;乙醇与醋酸的反应是酯化反应,D错误。
5. D 苯环是不饱和烃基,不属于乙醇的同系物,A错误;邻甲基苯酚含有苯环,不属于乙醇的同系物,B错误;乙二醇含有羟基数目为2,因此不是乙醇的同系物,C错误;(CH3)2CHOH含有1个羟基,烃基为烷基,是乙醇的同系物,D正确。
6. D 维生素A分子中含有5个碳碳双键,1 mol维生素A最多能与5 mol H2发生加成反应,A错误;维生素A分子中含有“—CH2OH”,能被氧化为醛,B错误;根据醇的溶解性规律,烃基越大越难溶于水,维生素A分子中烃基较大,故维生素A不是一种易溶于水的醇,C错误。
7. B α C上只有一个H原子,无法氧化为醛,A错误;薄荷醇的两个β C上均有H原子,可发生消去反应,B正确; 薄荷醇的分子式为 C10H20O,C错误;由结构简式可知薄荷醇分子中不含苯环,D错误。
8. B 根据R的结构可知其分子式为C10H18O,A正确;R中存在环状结构,丙烯醇是链状结构,二者不属于同系物,B错误;R中含有碳碳双键,能被酸性高锰酸钾溶液氧化,C正确;R中含有羟基,能与金属钠反应生成氢气,D正确。
9. C n(H2O)==0.6 mol,由氢原子守恒得:n(C2H5OH)===0.2 mol,由碳原子守恒得:n(CO)+n(CO2)=0.2 mol×2=0.4 mol,碳的氧化物总质量为27.6 g-10.8 g=16.8 g,设CO与CO2的物质的量分别为x和y。x+y=0.4 mol,28x g/mol+44y g/mol=16.8 g(碳原子质量守恒),解得x=0.05 mol,y=0.35 mol,m(CO)=0.05 mol×28 g/mol=1.4 g。故选C。
10. D 醇能发生消去反应,说明—OH具有邻碳氢,A不符合题意;醇的消去产物中存在同分异构体,说明醇分子不对称,B不符合题意;醇能发生催化氧化,说明—OH具有同碳氢,C不符合题意。
11. (1) 加成 (2) 羟基 (3) 还原 (4) 否 乙醇与溴水互溶
12. (1) CH3CH2OHCH2===CH2↑+H2O (2) bc (3) 液体分层,下层为油状液体 (4) NaOH溶液 品红溶液(其他合理答案也可)
