元素周期律 教学设计
图片预览

文档简介
元素周期律
课时4: 镓的应用指导
(一)课时目标和评价目标
课时目标 评价目标
1.通过结合有关数据和事实认识元素最高化合价和最低化合价、原子半径等随原子序数递增而呈周期性变化的规律。 2.通过第三周期元素性质的实验探究,掌握同一周期内元素性质的变化规律与原子结构的关系,建立元素周期律认知模型。 3.应用元素周期表(律)分析和解决实际问题,了解元素周期表的结构及其应用,建构“构-位-性”模型。 4.通过科学探究过程,加深对分类法,归纳法等科学方法的认识,提高逻辑推理能力、论证能力。 1.通过微观粒子结构的视角分析解释周期性变化的规律,诊断和发展学生认识进阶水平。 2.通过第三周期元素性质差异性及变化规律的实验探究,诊断并发展学生实验能力、逻辑推理能力水平。 3.通过搭建“构-位-性”元素周期律认知模型,诊断并发展学生认知模型发展水平。 4.通过应用元素周期表、元素周期律认识陌生元素镓,分析和解决问题,诊断并发展学生问题解决能力水平。
(二)教学过程
【情境引入】5G绝配,充电必备,“氮化镓”如何撩起“镓”国梦?
镓有“电子工业脊梁”的美誉,随着手机电池容量的不断增加,大功率的快充变得越来越重要。小巧、高效、发热低,是雷军给予小米GaN充电器的评价。小米GaN充电器虽然个头比常规充电器小了近一半,但充电速度一点不含糊。
任务1: GaN中镓的化合价是多少?
问题1:除了CaN,镓还常与砷、氧、硒等非金属形成化合物,均为优质半导体材料。尝试写出它们的化学式,并判断其中镓的化合价。
问题2:随着原子序数的递增,元素的化合价呈现什么规律?
问题3:随着原子序数的递增,原子半径的大小呈现什么规律?
任务2:为什么镓的化合物常做半导体材料?
问题1:根据第三周期金属元素Na、Mg、Al原子的核外电子排布,推测性质变化规律。
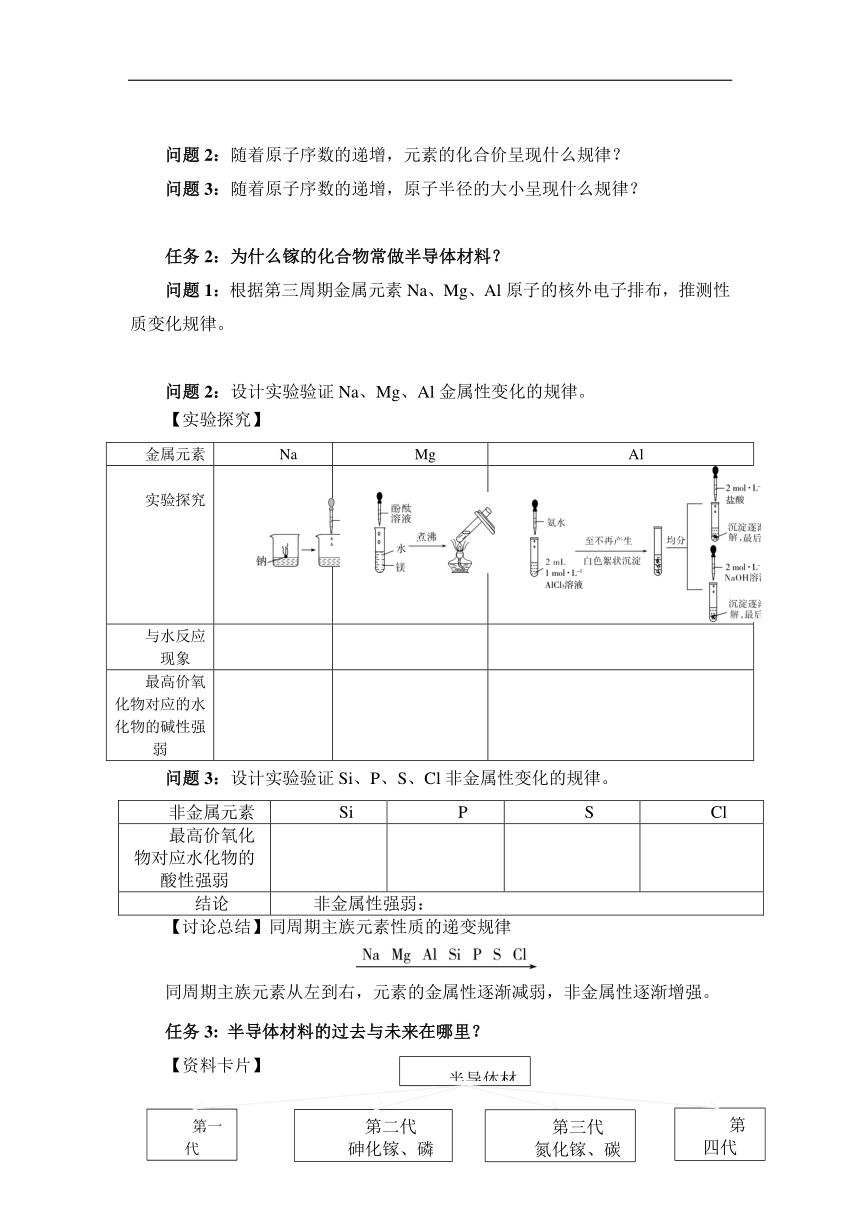
问题2:设计实验验证Na、Mg、Al金属性变化的规律。
【实验探究】
金属元素 Na Mg Al
实验探究
与水反应 现象
最高价氧化物对应的水化物的碱性强弱
问题3:设计实验验证Si、P、S、Cl非金属性变化的规律。
非金属元素 Si P S Cl
最高价氧化物对应水化物的酸性强弱
结论 非金属性强弱:
【讨论总结】同周期主族元素性质的递变规律
同周期主族元素从左到右,元素的金属性逐渐减弱,非金属性逐渐增强。
任务3: 半导体材料的过去与未来在哪里?
【资料卡片】
问题1:找一找常见的半导体材料还有哪些元素?
问题2:你还能预测哪些元素可以做半导体材料。
问题3:阅读教材,你还能发现周期表的哪些功能?
课堂选练
【基础训练】
1.元素周期表中的金属和非金属元素的分界线处用虚线表示。下列说法正确的是( )
A.元素周期表中最右上角的氦元素是得电子能力最强的元素
B.紧靠虚线两侧的元素都是两性金属元素
C.可在虚线附近寻找半导体材料(如Ge、Si等)
D.可在虚线的右上方寻找耐高温材料
2.中国科学院院士张青莲教授曾主持测定了铟(49In)、锑(51Sb)等9种元素相对原子质量的新值,被采用为国际新标准。铟与锑原子电子层数与铷(Rb)相同。下列说法不正确的是( )
A.In是第五周期第IIIA族元素
B.Sb与下一周期同族元素的原子序数差为18
C.原子半径:In>Sb
D.碱性:In(OH)33.据报道,我国科学家找到了水稻突变体“耐砷()富硒()”开关,这对提高水稻营养价值降低砷的毒性意义重大。下列说法正确的是( )
A.砷与硫属于同族元素 B.砷的简单氢化物为
C.简单氢化物的稳定性:As【能力提升】
4.2021年6月11日国家航天局公布了由“祝融号”火星车拍摄的首批科学影像图。火星气体及岩石中富含X、Y、Z、W四种元素。已知:X、Y、Z、W为原子序数递增的四种短周期元素,其中Z为金属元素,其单质与热水反应后溶液能使酚酞试液变为浅红色,X、W为同一主族元素,Y也是地球地壳中含量最高的元素,火星岩石含有ZWY3。下列判断错误的是( )
A. W位于元素周期表第三周期ⅣA族
B. X、W简单氢化物的稳定性:X>W
C. 原子半径:Z>W>Y>X
D. 火星气体中可能含有XY、XY2
5.矿物白云母是一种重要的化工原料,其化学式的氧化物形式为:K2O·3Al2O3·6SiO2·2H2O。就其组成元素完成下列填空:
(1) Al 元素在元素周期表中的位置为________________________。
(2)上述元素中(Si除外),形成的简单离子的半径由大到小的顺序为______________________(填离子符号)。
(3)简单氢化物的稳定性:H2O________SiH4(填“>”“<”或“=”)
(4)白云石所含的两种金属元素中,金属性较强的元素是________(填元素符号),写出一个能说明这一事实的化学方程式_____________________________________。
(5)已知硅酸(H2SiO3)为白色胶状沉淀。若要利用下图装置证明非金属性: C>Si,则A中加____________,B中加Na2CO3,C中加____________。
(可供选择的药品:稀硫酸、盐酸、稀硝酸、硅酸钠溶液、饱和碳酸氢钠溶液。)
课时4: 镓的应用指导
(一)课时目标和评价目标
课时目标 评价目标
1.通过结合有关数据和事实认识元素最高化合价和最低化合价、原子半径等随原子序数递增而呈周期性变化的规律。 2.通过第三周期元素性质的实验探究,掌握同一周期内元素性质的变化规律与原子结构的关系,建立元素周期律认知模型。 3.应用元素周期表(律)分析和解决实际问题,了解元素周期表的结构及其应用,建构“构-位-性”模型。 4.通过科学探究过程,加深对分类法,归纳法等科学方法的认识,提高逻辑推理能力、论证能力。 1.通过微观粒子结构的视角分析解释周期性变化的规律,诊断和发展学生认识进阶水平。 2.通过第三周期元素性质差异性及变化规律的实验探究,诊断并发展学生实验能力、逻辑推理能力水平。 3.通过搭建“构-位-性”元素周期律认知模型,诊断并发展学生认知模型发展水平。 4.通过应用元素周期表、元素周期律认识陌生元素镓,分析和解决问题,诊断并发展学生问题解决能力水平。
(二)教学过程
【情境引入】5G绝配,充电必备,“氮化镓”如何撩起“镓”国梦?
镓有“电子工业脊梁”的美誉,随着手机电池容量的不断增加,大功率的快充变得越来越重要。小巧、高效、发热低,是雷军给予小米GaN充电器的评价。小米GaN充电器虽然个头比常规充电器小了近一半,但充电速度一点不含糊。
任务1: GaN中镓的化合价是多少?
问题1:除了CaN,镓还常与砷、氧、硒等非金属形成化合物,均为优质半导体材料。尝试写出它们的化学式,并判断其中镓的化合价。
问题2:随着原子序数的递增,元素的化合价呈现什么规律?
问题3:随着原子序数的递增,原子半径的大小呈现什么规律?
任务2:为什么镓的化合物常做半导体材料?
问题1:根据第三周期金属元素Na、Mg、Al原子的核外电子排布,推测性质变化规律。
问题2:设计实验验证Na、Mg、Al金属性变化的规律。
【实验探究】
金属元素 Na Mg Al
实验探究
与水反应 现象
最高价氧化物对应的水化物的碱性强弱
问题3:设计实验验证Si、P、S、Cl非金属性变化的规律。
非金属元素 Si P S Cl
最高价氧化物对应水化物的酸性强弱
结论 非金属性强弱:
【讨论总结】同周期主族元素性质的递变规律
同周期主族元素从左到右,元素的金属性逐渐减弱,非金属性逐渐增强。
任务3: 半导体材料的过去与未来在哪里?
【资料卡片】
问题1:找一找常见的半导体材料还有哪些元素?
问题2:你还能预测哪些元素可以做半导体材料。
问题3:阅读教材,你还能发现周期表的哪些功能?
课堂选练
【基础训练】
1.元素周期表中的金属和非金属元素的分界线处用虚线表示。下列说法正确的是( )
A.元素周期表中最右上角的氦元素是得电子能力最强的元素
B.紧靠虚线两侧的元素都是两性金属元素
C.可在虚线附近寻找半导体材料(如Ge、Si等)
D.可在虚线的右上方寻找耐高温材料
2.中国科学院院士张青莲教授曾主持测定了铟(49In)、锑(51Sb)等9种元素相对原子质量的新值,被采用为国际新标准。铟与锑原子电子层数与铷(Rb)相同。下列说法不正确的是( )
A.In是第五周期第IIIA族元素
B.Sb与下一周期同族元素的原子序数差为18
C.原子半径:In>Sb
D.碱性:In(OH)3
A.砷与硫属于同族元素 B.砷的简单氢化物为
C.简单氢化物的稳定性:As
4.2021年6月11日国家航天局公布了由“祝融号”火星车拍摄的首批科学影像图。火星气体及岩石中富含X、Y、Z、W四种元素。已知:X、Y、Z、W为原子序数递增的四种短周期元素,其中Z为金属元素,其单质与热水反应后溶液能使酚酞试液变为浅红色,X、W为同一主族元素,Y也是地球地壳中含量最高的元素,火星岩石含有ZWY3。下列判断错误的是( )
A. W位于元素周期表第三周期ⅣA族
B. X、W简单氢化物的稳定性:X>W
C. 原子半径:Z>W>Y>X
D. 火星气体中可能含有XY、XY2
5.矿物白云母是一种重要的化工原料,其化学式的氧化物形式为:K2O·3Al2O3·6SiO2·2H2O。就其组成元素完成下列填空:
(1) Al 元素在元素周期表中的位置为________________________。
(2)上述元素中(Si除外),形成的简单离子的半径由大到小的顺序为______________________(填离子符号)。
(3)简单氢化物的稳定性:H2O________SiH4(填“>”“<”或“=”)
(4)白云石所含的两种金属元素中,金属性较强的元素是________(填元素符号),写出一个能说明这一事实的化学方程式_____________________________________。
(5)已知硅酸(H2SiO3)为白色胶状沉淀。若要利用下图装置证明非金属性: C>Si,则A中加____________,B中加Na2CO3,C中加____________。
(可供选择的药品:稀硫酸、盐酸、稀硝酸、硅酸钠溶液、饱和碳酸氢钠溶液。)
