4.1 课时2酚的性质及应用 (含解析) 2024-2025学年高二化学苏教版(2020)选择性必修3
文档属性
| 名称 | 4.1 课时2酚的性质及应用 (含解析) 2024-2025学年高二化学苏教版(2020)选择性必修3 |

|
|
| 格式 | docx | ||
| 文件大小 | 291.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-05-06 00:00:00 | ||
图片预览




文档简介
课时2 酚的性质及应用
1 (盐城响水中学学情分析)生活中遇到的一些问题常常涉及化学知识,下列有关叙述错误的是( )
A. 鱼虾放置时间过久,会产生难闻的腥臭气味
B. “酸可以除锈”“汽油可以去油污”都是发生了化学变化
C. 被蜂、蚁蜇咬后会感到疼痛难忍,这是因为蜂、蚁叮咬人时将甲酸注入人体,此时若能涂抹稀氨水或碳酸氢钠溶液,就可以减轻疼痛
D. 苯酚皂可用于环境消毒,医用酒精可用于皮肤消毒,其原因是它们都可以杀死细菌
2 (2025泰州中学检测)下列关于苯酚的叙述正确的是( )
A. 纯净的苯酚是粉红色晶体
B. 苯酚有毒,少量沾在皮肤上可用酒精洗去
C. 苯酚与FeCl3溶液作用生成紫色沉淀
D. 苯酚能与NaHCO3溶液反应生成CO2
3 (2025泰州阶段练习)欲除去下列物质中的少量杂质,所选除杂试剂和分离方法正确的是( )
选项 有机物(杂质) 除杂试剂 分离方法
A 乙烯(乙醇蒸气) 蒸馏水 洗气
B 乙烷(乙烯) 氢气 转化法
C 溴苯(Br2) 水 分液
D 苯(苯酚) 饱和溴水 过滤
4 (2023扬州高邮调研)化合物Z是一种抗骨质疏松药的重要中间体,可由下列反应制得。下列有关X、Y、Z的说法正确的是( )
A. X的分子式为C8H8N
B. Z可发生取代、氧化、缩聚反应
C. 可用FeCl3溶液鉴别和Z
D. Z与足量的氢气加成的产物中有3个手性碳原子
5 (盐城响水中学学情分析) 已知酸性:>H2CO3>。综合考虑反应物的转化率和原料成本等因素,将完全转变为的最佳方法是( )
A. 与稀硫酸共热后,加入足量的NaOH溶液
B. 与足量的NaOH溶液共热后,再通入足量CO2
C. 与稀硫酸共热后,加入足量的NaHCO3溶液
D. 与足量的NaOH溶液共热后,再加入适量的H2SO4溶液
6 (2024镇江学情调研)化合物Z是合成沙丁胺醇的重要中间体,其合成路线如下。下列说法错误的是( )
A. X中的官能团为羧基、酯基
B. Y一定条件下可以发生缩聚反应
C. Z与足量H2的加成产物中有5个手性碳原子
D. X与Z可用FeCl3溶液鉴别
7 下列为四种有机化合物的结构简式,均含有多个官能团。下列有关说法正确的是( )
① ② ③ ④
A. ①属于酚类,可与NaHCO3溶液反应产生CO2
B. ②属于酚类,遇FeCl3溶液显色
C. 1 mol ③最多能与1 mol Br2发生反应
D. ④属于醇类,可以发生消去反应
8 能证明苯酚具有弱酸性的方法是( )
①苯酚溶液加热变澄清
②苯酚浊液中加NaOH后,溶液变澄清,生成苯酚钠和水
③苯酚可与FeCl3反应
④在苯酚溶液中加入浓溴水产生白色沉淀
⑤苯酚几乎不能使石蕊溶液变红
⑥苯酚能与Na2CO3溶液反应生成NaHCO3
A. ⑤⑥ B. ①②⑤
C. ③④⑥ D. ③④⑤
9 (2025徐州阶段练习)下列物质间的性质差异不是由于基团之间相互影响造成的是( )
A. 甲苯能使酸性KMnO4溶液褪色而甲烷不能
B. CH3CH2Br能发生消去反应而CH3Br不能
C. 对甲基苯酚()能与NaOH溶液反应而苯甲醇不能
D. 苯酚能与溴水反应而苯不能
10 (扬州邗江中学期中)利用化合物X和Y可以制备氧杂蒽酮类化合物中间体Z。下列说法正确的是( )
A. 用NaHCO3溶液可鉴别Y和Z
B. 1 mol Y最多能与4 mol NaOH反应
C. X与足量氢气加成后的产物有3个手性碳原子
D. X、Y分子中的所有原子均可能处于同一平面
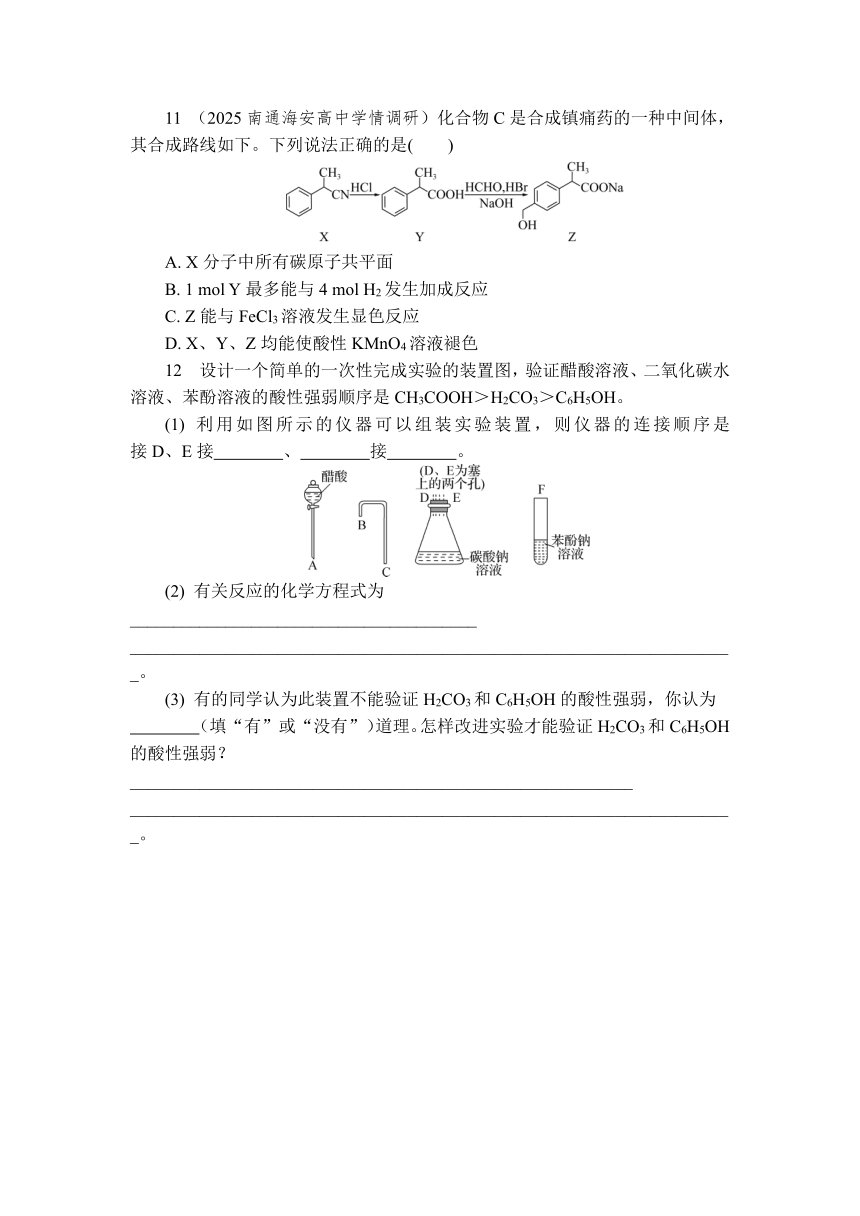
11 (2025南通海安高中学情调研)化合物C是合成镇痛药的一种中间体,其合成路线如下。下列说法正确的是( )
A. X分子中所有碳原子共平面
B. 1 mol Y最多能与4 mol H2发生加成反应
C. Z能与FeCl3溶液发生显色反应
D. X、Y、Z均能使酸性KMnO4溶液褪色
12 设计一个简单的一次性完成实验的装置图,验证醋酸溶液、二氧化碳水溶液、苯酚溶液的酸性强弱顺序是CH3COOH>H2CO3>C6H5OH。
(1) 利用如图所示的仪器可以组装实验装置,则仪器的连接顺序是 接D、E接 、 接 。
(2) 有关反应的化学方程式为________________________________________
______________________________________________________________________。
(3) 有的同学认为此装置不能验证H2CO3和C6H5OH的酸性强弱,你认为
(填“有”或“没有”)道理。怎样改进实验才能验证H2CO3和C6H5OH的酸性强弱?__________________________________________________________
______________________________________________________________________。
13 (2025泰州中学期中)酚类化合物有毒,被列为须重点控制的水污染物之一,某工厂采用下列方法处理含苯酚的废水。
Ⅰ. 回收水样中苯酚:
(1) 设备Ⅰ中进行的操作名称是 。
(2) 设备Ⅲ中发生反应的离子方程式为________________________________
______________________________________________________________________。
Ⅱ. 由苯酚和叔丁基氯[(CH3)3CCl]制取对叔丁基苯酚的流程如图:
(3) AlCl3是反应Ⅰ的催化剂,则反应Ⅰ的化学方程式为___________________
______________________________________________________________________。
(4) 测定产品中对叔丁基苯酚(摩尔质量为150 g/mol)的纯度:
步骤1:取16.00 g样品用NaOH溶液完全溶解,配成250.00 mL溶液。
步骤2:移取25.00 mL溶液加入足量HCl酸化,再加入10.00 mL 2.50 mol/L的浓溴水;充分反应后,加入足量KI溶液。
步骤3:向步骤2的溶液中逐滴加入0.50 mol/L Na2S2O3溶液,发生反应:I2+2Na2S2O3===Na2S4O6+2NaI,共消耗Na2S2O3溶液20.00 mL。
计算对叔丁基苯酚的纯度(写出计算过程)。
14 A和B两种物质的分子式都是C7H8O,它们都能跟金属钠反应放出氢气。A不溶于NaOH溶液,而B溶于NaOH溶液;B能使适量溴水褪色,并产生白色沉淀,而A不能。B苯环上的一溴代物有两种结构。
(1) 写出A和B的结构简式。
A: ,B:_______________。
(2) 写出B与NaOH溶液发生反应的化学方程式:________________________。
(3) A与金属钠反应的化学方程式为 。与足量金属钠反应生成等量H2,分别需A、B、H2O三种物质的物质的量之比为_____
_____________。
15 按以下步骤可由合成(部分试剂和反应条件已略去)。请回答下列问题。
(1) 分别写出B、D的结构简式:B 、D 。
(2) 反应①~⑦中属于消去反应的是 (填反应序号)。
(3) 不考虑反应⑥⑦,对于反应⑤,得到E的可能的结构简式为
。
(4) 写出反应④的化学方程式:________________________(注明反应条件)。
课时2 酚的性质及应用
1. B 酸除锈是酸和铁锈反应生成盐,属于化学变化,汽油去油污是利用物质的相似相溶原理,属于物理变化,B错误。
2. B 纯净的苯酚是无色晶体,苯酚暴露在空气中,氧化后变为粉红色的物质,A错误;苯酚有毒,少量沾在皮肤上可用酒精洗去,B正确;苯酚与FeCl3溶液是络合反应,生成紫色六苯酚合铁离子,不是生成沉淀,C错误;苯酚酸性比碳酸弱,不能与NaHCO3溶液反应生成CO2,D错误。
3. A 乙醇蒸气溶解在蒸馏水中,洗气后得到乙烯,A正确;反应不容易发生,且会引入杂质气体H2,B错误;Br2在溴苯中的溶解度比在水中大,用水洗涤,分液后仍不能得到纯净的溴苯,C错误;生成的2,4,6三溴苯酚会溶解在过量的苯中,不能得到纯净的苯,D错误。
4. B 键线式中端点和拐点均为C,按照C的四价结构补充H,该物质的化学式为C8H7N,A错误;Z中苯环上直接连着羟基,具有酚的性质,可以发生取代反应,酚容易被氧化,分子中含有2个酚羟基,可以发生缩聚反应,B正确;Z和中都有酚羟基,都能与FeCl3溶液发生显色反应,不可用FeCl3溶液鉴别,C错误;Z与足量的H2加成后为(标“*”碳原子为手性碳原子),共4个,D错误。
5. B 在酸性条件下部分水解生成,加入足量的NaOH溶液后生成,A错误;酯在碱性条件下完全水解,与足量的NaOH溶液共热后,水解生成,再通入足量CO2,生成, B正确;在酸性条件下部分水解生成,加入足量的NaHCO3溶液后生成,但产率较低,不是最佳方法,C错误;与足量的NaOH溶液共热后,水解生成,再加入适量H2SO4,生成,得不到所需物质,D错误。
6. C Z与足量H2的加成产物中有4个手性碳原子(标“*”碳原子):,C错误。
7. D 酚的酸性弱于碳酸,不能制备CO2,A错误;羟基没有直接连在苯环上,②不属于酚类,遇FeCl3溶液不显色,B错误;酚羟基邻、对位上的氢原子能与溴发生取代反应,故1 mol ③最多能与2 mol Br2发生反应,C错误;④分子中含有羟基,且羟基具有邻碳氢,故④属于醇类,可以发生消去反应,D正确。
8. A 苯酚溶液加热变澄清,说明温度升高苯酚的溶解度增大,与弱酸性无关,①错误;苯酚浊液中加NaOH后变澄清,生成苯酚钠和水,只能说明苯酚有酸性,不能说明酸性的强弱,②错误;苯酚与FeCl3发生显色反应,与弱酸性无关,③错误;在苯酚溶液中加入浓溴水发生取代反应生成白色2,4,6-三溴苯酚沉淀,与弱酸性无关,④错误;苯酚溶液几乎不能使石蕊溶液变红,说明苯酚溶液酸性弱,电离出的氢离子不足以使指示剂变色,⑤正确;苯酚与Na2CO3溶液反应生成NaHCO3,没有生成CO2,表明苯酚的酸性弱于碳酸的酸性,碳酸为弱酸,则苯酚有弱酸性,⑥正确;证明苯酚具有弱酸性的方法是⑤⑥,故选A。
9. B CH3Br分子中的溴原子不具有邻碳氢,不能发生消去反应,故CH3CH2Br能发生消去反应而CH3Br不能,不是由基团之间相互影响造成的,B符合题意。
10. A Y含有羧基,能与NaHCO3溶液反应放出二氧化碳气体,Z不含羧基,不能与NaHCO3溶液反应,可以用NaHCO3溶液可鉴别Y和Z,A正确;Y含有1个羧基、2个酚羟基,1 mol Y最多能与3 mol NaOH反应,B错误;X与足量氢气加成后的产物是,不含手性碳原子,C错误;Y分子中含有甲基,不可能所有原子共平面,D错误。
11. D X分子中,连接—CN的碳原子采取sp3杂化,位于四面体的中心,故X分子中所有碳原子不可能共平面,A错误;羧基中的碳氧双键不能与H2发生加成反应,B错误;Z分子中不含有酚羟基,不能与FeCl3溶液发生显色反应,C错误;X、Y、Z分子中,与苯环直接相连的第一个碳原子上均连有氢原子,故都能使酸性KMnO4溶液褪色,D正确。
12. (1) A B C F
(2) Na2CO3+2CH3COOH―→2CH3COONa+H2O+CO2↑、+H2O+CO2―→+NaHCO3
(3) 有 应在锥形瓶和试管之间加一个盛饱和NaHCO3溶液的洗气瓶,除去CO2中混有的醋酸
13. (1) 萃取、分液
(2) +CO2+H2O―→+HCO
(3)
(4) 93.75%(计算过程略)
14. (1)
(2) +NaOH―→+H2O
(3) +2Na―→+H2↑ 1∶1∶1
15. (1) (2) ②④
(3)
(4)
1 (盐城响水中学学情分析)生活中遇到的一些问题常常涉及化学知识,下列有关叙述错误的是( )
A. 鱼虾放置时间过久,会产生难闻的腥臭气味
B. “酸可以除锈”“汽油可以去油污”都是发生了化学变化
C. 被蜂、蚁蜇咬后会感到疼痛难忍,这是因为蜂、蚁叮咬人时将甲酸注入人体,此时若能涂抹稀氨水或碳酸氢钠溶液,就可以减轻疼痛
D. 苯酚皂可用于环境消毒,医用酒精可用于皮肤消毒,其原因是它们都可以杀死细菌
2 (2025泰州中学检测)下列关于苯酚的叙述正确的是( )
A. 纯净的苯酚是粉红色晶体
B. 苯酚有毒,少量沾在皮肤上可用酒精洗去
C. 苯酚与FeCl3溶液作用生成紫色沉淀
D. 苯酚能与NaHCO3溶液反应生成CO2
3 (2025泰州阶段练习)欲除去下列物质中的少量杂质,所选除杂试剂和分离方法正确的是( )
选项 有机物(杂质) 除杂试剂 分离方法
A 乙烯(乙醇蒸气) 蒸馏水 洗气
B 乙烷(乙烯) 氢气 转化法
C 溴苯(Br2) 水 分液
D 苯(苯酚) 饱和溴水 过滤
4 (2023扬州高邮调研)化合物Z是一种抗骨质疏松药的重要中间体,可由下列反应制得。下列有关X、Y、Z的说法正确的是( )
A. X的分子式为C8H8N
B. Z可发生取代、氧化、缩聚反应
C. 可用FeCl3溶液鉴别和Z
D. Z与足量的氢气加成的产物中有3个手性碳原子
5 (盐城响水中学学情分析) 已知酸性:>H2CO3>。综合考虑反应物的转化率和原料成本等因素,将完全转变为的最佳方法是( )
A. 与稀硫酸共热后,加入足量的NaOH溶液
B. 与足量的NaOH溶液共热后,再通入足量CO2
C. 与稀硫酸共热后,加入足量的NaHCO3溶液
D. 与足量的NaOH溶液共热后,再加入适量的H2SO4溶液
6 (2024镇江学情调研)化合物Z是合成沙丁胺醇的重要中间体,其合成路线如下。下列说法错误的是( )
A. X中的官能团为羧基、酯基
B. Y一定条件下可以发生缩聚反应
C. Z与足量H2的加成产物中有5个手性碳原子
D. X与Z可用FeCl3溶液鉴别
7 下列为四种有机化合物的结构简式,均含有多个官能团。下列有关说法正确的是( )
① ② ③ ④
A. ①属于酚类,可与NaHCO3溶液反应产生CO2
B. ②属于酚类,遇FeCl3溶液显色
C. 1 mol ③最多能与1 mol Br2发生反应
D. ④属于醇类,可以发生消去反应
8 能证明苯酚具有弱酸性的方法是( )
①苯酚溶液加热变澄清
②苯酚浊液中加NaOH后,溶液变澄清,生成苯酚钠和水
③苯酚可与FeCl3反应
④在苯酚溶液中加入浓溴水产生白色沉淀
⑤苯酚几乎不能使石蕊溶液变红
⑥苯酚能与Na2CO3溶液反应生成NaHCO3
A. ⑤⑥ B. ①②⑤
C. ③④⑥ D. ③④⑤
9 (2025徐州阶段练习)下列物质间的性质差异不是由于基团之间相互影响造成的是( )
A. 甲苯能使酸性KMnO4溶液褪色而甲烷不能
B. CH3CH2Br能发生消去反应而CH3Br不能
C. 对甲基苯酚()能与NaOH溶液反应而苯甲醇不能
D. 苯酚能与溴水反应而苯不能
10 (扬州邗江中学期中)利用化合物X和Y可以制备氧杂蒽酮类化合物中间体Z。下列说法正确的是( )
A. 用NaHCO3溶液可鉴别Y和Z
B. 1 mol Y最多能与4 mol NaOH反应
C. X与足量氢气加成后的产物有3个手性碳原子
D. X、Y分子中的所有原子均可能处于同一平面
11 (2025南通海安高中学情调研)化合物C是合成镇痛药的一种中间体,其合成路线如下。下列说法正确的是( )
A. X分子中所有碳原子共平面
B. 1 mol Y最多能与4 mol H2发生加成反应
C. Z能与FeCl3溶液发生显色反应
D. X、Y、Z均能使酸性KMnO4溶液褪色
12 设计一个简单的一次性完成实验的装置图,验证醋酸溶液、二氧化碳水溶液、苯酚溶液的酸性强弱顺序是CH3COOH>H2CO3>C6H5OH。
(1) 利用如图所示的仪器可以组装实验装置,则仪器的连接顺序是 接D、E接 、 接 。
(2) 有关反应的化学方程式为________________________________________
______________________________________________________________________。
(3) 有的同学认为此装置不能验证H2CO3和C6H5OH的酸性强弱,你认为
(填“有”或“没有”)道理。怎样改进实验才能验证H2CO3和C6H5OH的酸性强弱?__________________________________________________________
______________________________________________________________________。
13 (2025泰州中学期中)酚类化合物有毒,被列为须重点控制的水污染物之一,某工厂采用下列方法处理含苯酚的废水。
Ⅰ. 回收水样中苯酚:
(1) 设备Ⅰ中进行的操作名称是 。
(2) 设备Ⅲ中发生反应的离子方程式为________________________________
______________________________________________________________________。
Ⅱ. 由苯酚和叔丁基氯[(CH3)3CCl]制取对叔丁基苯酚的流程如图:
(3) AlCl3是反应Ⅰ的催化剂,则反应Ⅰ的化学方程式为___________________
______________________________________________________________________。
(4) 测定产品中对叔丁基苯酚(摩尔质量为150 g/mol)的纯度:
步骤1:取16.00 g样品用NaOH溶液完全溶解,配成250.00 mL溶液。
步骤2:移取25.00 mL溶液加入足量HCl酸化,再加入10.00 mL 2.50 mol/L的浓溴水;充分反应后,加入足量KI溶液。
步骤3:向步骤2的溶液中逐滴加入0.50 mol/L Na2S2O3溶液,发生反应:I2+2Na2S2O3===Na2S4O6+2NaI,共消耗Na2S2O3溶液20.00 mL。
计算对叔丁基苯酚的纯度(写出计算过程)。
14 A和B两种物质的分子式都是C7H8O,它们都能跟金属钠反应放出氢气。A不溶于NaOH溶液,而B溶于NaOH溶液;B能使适量溴水褪色,并产生白色沉淀,而A不能。B苯环上的一溴代物有两种结构。
(1) 写出A和B的结构简式。
A: ,B:_______________。
(2) 写出B与NaOH溶液发生反应的化学方程式:________________________。
(3) A与金属钠反应的化学方程式为 。与足量金属钠反应生成等量H2,分别需A、B、H2O三种物质的物质的量之比为_____
_____________。
15 按以下步骤可由合成(部分试剂和反应条件已略去)。请回答下列问题。
(1) 分别写出B、D的结构简式:B 、D 。
(2) 反应①~⑦中属于消去反应的是 (填反应序号)。
(3) 不考虑反应⑥⑦,对于反应⑤,得到E的可能的结构简式为
。
(4) 写出反应④的化学方程式:________________________(注明反应条件)。
课时2 酚的性质及应用
1. B 酸除锈是酸和铁锈反应生成盐,属于化学变化,汽油去油污是利用物质的相似相溶原理,属于物理变化,B错误。
2. B 纯净的苯酚是无色晶体,苯酚暴露在空气中,氧化后变为粉红色的物质,A错误;苯酚有毒,少量沾在皮肤上可用酒精洗去,B正确;苯酚与FeCl3溶液是络合反应,生成紫色六苯酚合铁离子,不是生成沉淀,C错误;苯酚酸性比碳酸弱,不能与NaHCO3溶液反应生成CO2,D错误。
3. A 乙醇蒸气溶解在蒸馏水中,洗气后得到乙烯,A正确;反应不容易发生,且会引入杂质气体H2,B错误;Br2在溴苯中的溶解度比在水中大,用水洗涤,分液后仍不能得到纯净的溴苯,C错误;生成的2,4,6三溴苯酚会溶解在过量的苯中,不能得到纯净的苯,D错误。
4. B 键线式中端点和拐点均为C,按照C的四价结构补充H,该物质的化学式为C8H7N,A错误;Z中苯环上直接连着羟基,具有酚的性质,可以发生取代反应,酚容易被氧化,分子中含有2个酚羟基,可以发生缩聚反应,B正确;Z和中都有酚羟基,都能与FeCl3溶液发生显色反应,不可用FeCl3溶液鉴别,C错误;Z与足量的H2加成后为(标“*”碳原子为手性碳原子),共4个,D错误。
5. B 在酸性条件下部分水解生成,加入足量的NaOH溶液后生成,A错误;酯在碱性条件下完全水解,与足量的NaOH溶液共热后,水解生成,再通入足量CO2,生成, B正确;在酸性条件下部分水解生成,加入足量的NaHCO3溶液后生成,但产率较低,不是最佳方法,C错误;与足量的NaOH溶液共热后,水解生成,再加入适量H2SO4,生成,得不到所需物质,D错误。
6. C Z与足量H2的加成产物中有4个手性碳原子(标“*”碳原子):,C错误。
7. D 酚的酸性弱于碳酸,不能制备CO2,A错误;羟基没有直接连在苯环上,②不属于酚类,遇FeCl3溶液不显色,B错误;酚羟基邻、对位上的氢原子能与溴发生取代反应,故1 mol ③最多能与2 mol Br2发生反应,C错误;④分子中含有羟基,且羟基具有邻碳氢,故④属于醇类,可以发生消去反应,D正确。
8. A 苯酚溶液加热变澄清,说明温度升高苯酚的溶解度增大,与弱酸性无关,①错误;苯酚浊液中加NaOH后变澄清,生成苯酚钠和水,只能说明苯酚有酸性,不能说明酸性的强弱,②错误;苯酚与FeCl3发生显色反应,与弱酸性无关,③错误;在苯酚溶液中加入浓溴水发生取代反应生成白色2,4,6-三溴苯酚沉淀,与弱酸性无关,④错误;苯酚溶液几乎不能使石蕊溶液变红,说明苯酚溶液酸性弱,电离出的氢离子不足以使指示剂变色,⑤正确;苯酚与Na2CO3溶液反应生成NaHCO3,没有生成CO2,表明苯酚的酸性弱于碳酸的酸性,碳酸为弱酸,则苯酚有弱酸性,⑥正确;证明苯酚具有弱酸性的方法是⑤⑥,故选A。
9. B CH3Br分子中的溴原子不具有邻碳氢,不能发生消去反应,故CH3CH2Br能发生消去反应而CH3Br不能,不是由基团之间相互影响造成的,B符合题意。
10. A Y含有羧基,能与NaHCO3溶液反应放出二氧化碳气体,Z不含羧基,不能与NaHCO3溶液反应,可以用NaHCO3溶液可鉴别Y和Z,A正确;Y含有1个羧基、2个酚羟基,1 mol Y最多能与3 mol NaOH反应,B错误;X与足量氢气加成后的产物是,不含手性碳原子,C错误;Y分子中含有甲基,不可能所有原子共平面,D错误。
11. D X分子中,连接—CN的碳原子采取sp3杂化,位于四面体的中心,故X分子中所有碳原子不可能共平面,A错误;羧基中的碳氧双键不能与H2发生加成反应,B错误;Z分子中不含有酚羟基,不能与FeCl3溶液发生显色反应,C错误;X、Y、Z分子中,与苯环直接相连的第一个碳原子上均连有氢原子,故都能使酸性KMnO4溶液褪色,D正确。
12. (1) A B C F
(2) Na2CO3+2CH3COOH―→2CH3COONa+H2O+CO2↑、+H2O+CO2―→+NaHCO3
(3) 有 应在锥形瓶和试管之间加一个盛饱和NaHCO3溶液的洗气瓶,除去CO2中混有的醋酸
13. (1) 萃取、分液
(2) +CO2+H2O―→+HCO
(3)
(4) 93.75%(计算过程略)
14. (1)
(2) +NaOH―→+H2O
(3) +2Na―→+H2↑ 1∶1∶1
15. (1) (2) ②④
(3)
(4)
