2025年中考化学复习专题——工艺流程题(含答案)
文档属性
| 名称 | 2025年中考化学复习专题——工艺流程题(含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 1.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-05-06 18:06:31 | ||
图片预览



文档简介
2025年中考化学复习专题——工艺流程题
1.造纸术是我国古代的四大发明之一,硫酸铝在造纸工业中常用作松香胶、蜡乳液的沉淀剂。利用铝灰(主要成分为SiO2、Fe2O3、Al2O3)制取硫酸铝晶体的主要流程如下图:
已知:①SiO2既不溶于水,也不与酸反应。②碳酸氢铵在35℃以上会开始分解,60℃时可以完全分解。请回答下列问题:
(1)酸溶池中发生反应的化学方程式为 (任写一个),生产过程中进行搅拌的目的是 。
(2)过滤器中滤渣1的成分是 。
(3)除杂室内的温度不宜过高,其原因是 。
(4)结晶池中,通常采用冷却结晶的方式得到硫酸铝晶体,说明硫酸铝的溶解度随温度的升高而 。
2.我国是世界上锌冶炼最早的国家,明代宋应星所著的《天工开物》中有关于“火法”炼锌的工艺记载是:“每炉甘石(主要成分是碳酸锌)十斤,装载入一泥罐内……然后逐层用煤炭饼(反应后生成一氧化碳)垫盛,其底铺薪,发火煅红……冷定毁罐取出……即倭铅(锌)也。”该工艺过程分解模拟如图,请结合图文信息回答问题:
(1)装入原料器之前,将炉甘石敲碎的目的是 。
(2)高温炉内,碳酸锌()在高温条件下与煤的主要成分发生反应生成和,反应的化学方程式为 。
(3)从微观角度分析冷凝器中冷凝的原理 。
(4)我国古代冶锌晚于铁和铜,分析说明其中的原因 。
(5)湿法冶金利用置换反应。向、混合液中加入粉,充分反应后过滤。若取出的滤渣滴加稀盐酸有气泡产生,则滤液中一定不含的金属阳离子是 。
3.湖北荆州盛产淡水贻贝,实验室以淡水贻贝壳(主要成分为CaCO3和少量 SiO2)为原料制备轻质碳酸钙粉末作为牙膏摩擦剂,工艺流程如下:
(1)酸浸前将贻贝壳打碎的目的是 。
(2)操作①酸浸发生反应的化学方程式是 。
(3)操作②反应的化学方程式是:。则x是 。
(4)操作④的步骤是蒸发浓缩、降温结晶、过滤、洗涤、干燥,其中过滤的目的是 。制得NH4Cl晶体在农业上可作 。
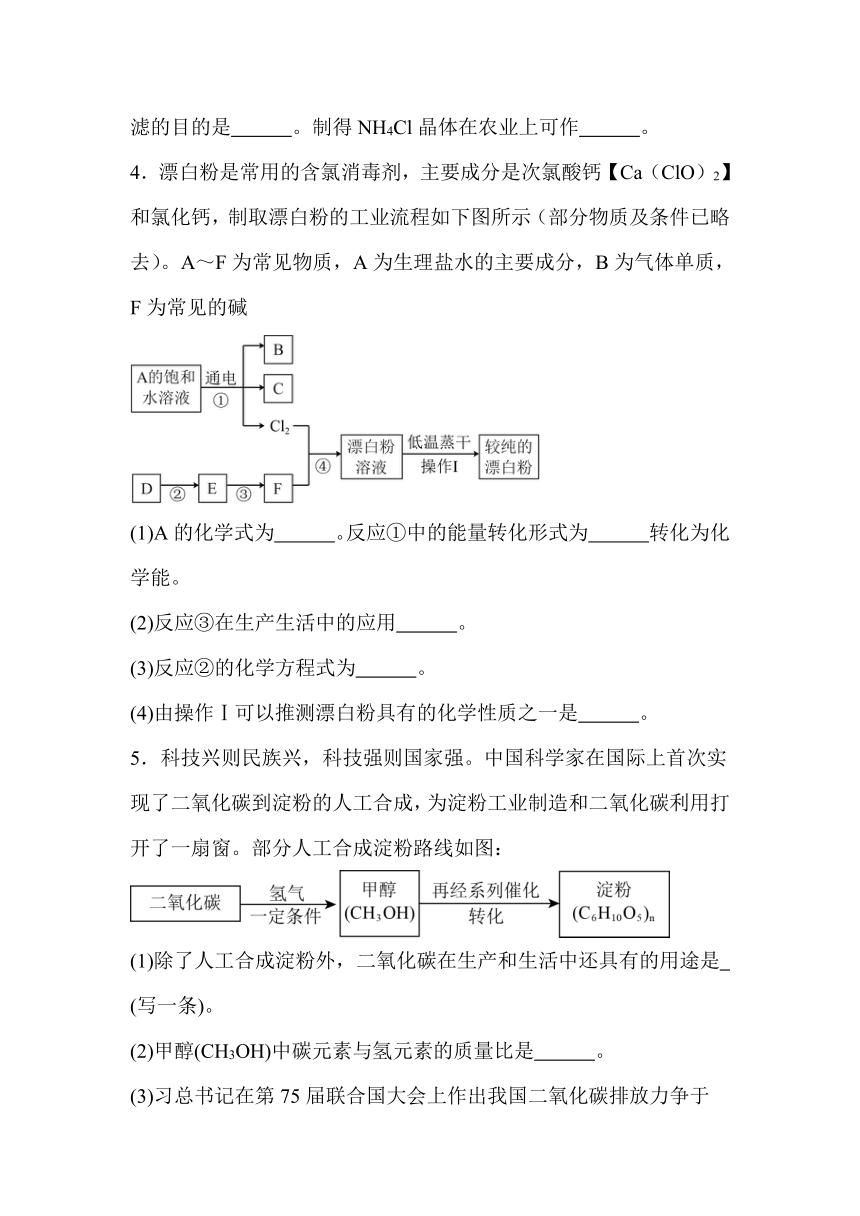
4.漂白粉是常用的含氯消毒剂,主要成分是次氯酸钙【Ca(ClO)2】和氯化钙,制取漂白粉的工业流程如下图所示(部分物质及条件已略去)。A~F为常见物质,A为生理盐水的主要成分,B为气体单质,F为常见的碱
(1)A的化学式为 。反应①中的能量转化形式为 转化为化学能。
(2)反应③在生产生活中的应用 。
(3)反应②的化学方程式为 。
(4)由操作Ⅰ可以推测漂白粉具有的化学性质之一是 。
5.科技兴则民族兴,科技强则国家强。中国科学家在国际上首次实现了二氧化碳到淀粉的人工合成,为淀粉工业制造和二氧化碳利用打开了一扇窗。部分人工合成淀粉路线如图:
(1)除了人工合成淀粉外,二氧化碳在生产和生活中还具有的用途是 (写一条)。
(2)甲醇(CH3OH)中碳元素与氢元素的质量比是 。
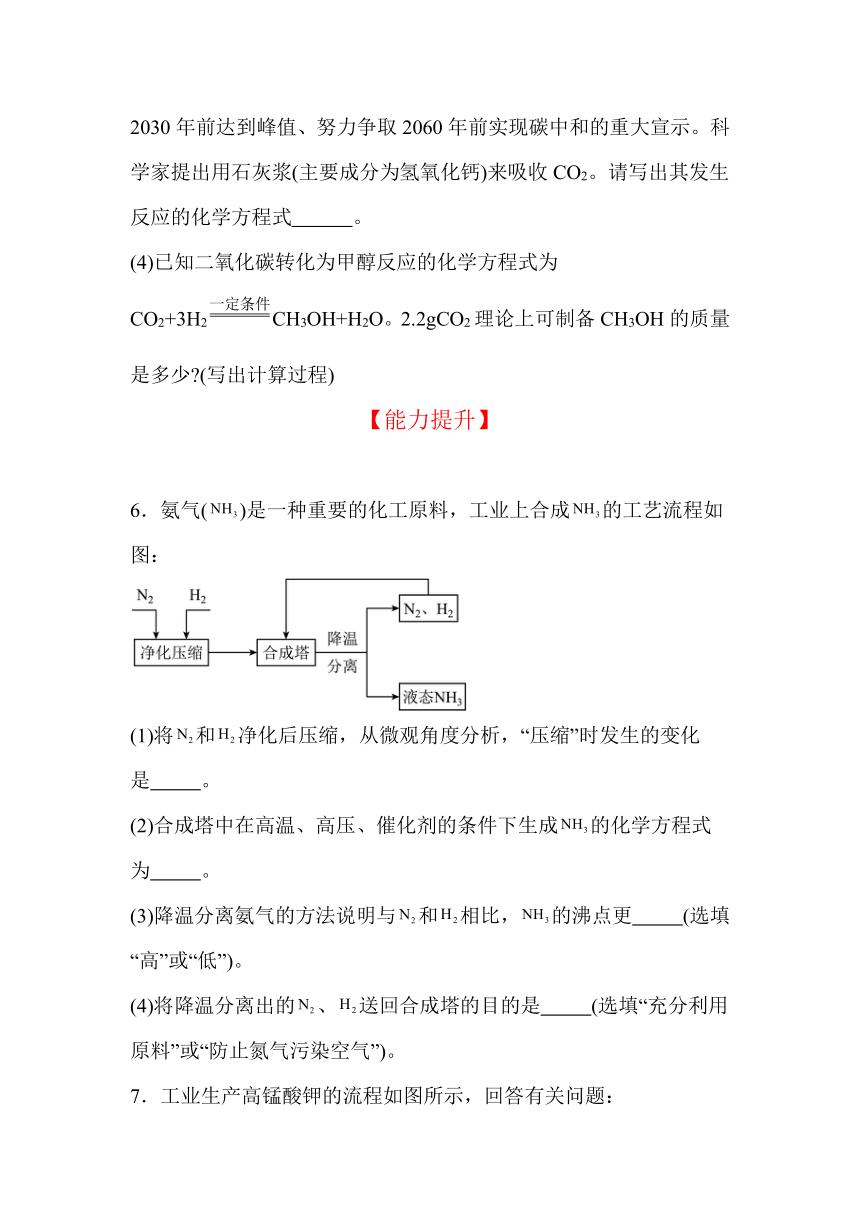
(3)习总书记在第75届联合国大会上作出我国二氧化碳排放力争于2030年前达到峰值、努力争取2060年前实现碳中和的重大宣示。科学家提出用石灰浆(主要成分为氢氧化钙)来吸收CO2。请写出其发生反应的化学方程式 。
(4)已知二氧化碳转化为甲醇反应的化学方程式为CO2+3H2CH3OH+H2O。2.2gCO2理论上可制备CH3OH的质量是多少 (写出计算过程)
【能力提升】
6.氨气()是一种重要的化工原料,工业上合成的工艺流程如图:
(1)将和净化后压缩,从微观角度分析,“压缩”时发生的变化是 。
(2)合成塔中在高温、高压、催化剂的条件下生成的化学方程式为 。
(3)降温分离氨气的方法说明与和相比,的沸点更 (选填“高”或“低”)。
(4)将降温分离出的、送回合成塔的目的是 (选填“充分利用原料”或“防止氮气污染空气”)。
7.工业生产高锰酸钾的流程如图所示,回答有关问题:
(1)Ⅰ中混合搅拌的目的是 。
(2)Ⅱ的反应物及产物如流程所示,反应前后化合价发生变化的元素有 (填元素符号);
(3)请完成Ⅲ中发生反应的化学方程式 。
(4)流程图中的物质属于氧化物的有 ,可循环利用的是 。
8.为了达到收旧利废节能减排的目的,从含有金属镁、铁、铜的粉末中,分离和提取出重要化工原料和有关金属,实验过程如下:
请回答:
(1)操作①中分离出的金属A是 。
(2)操作a中要用到玻璃棒、 、烧杯。
(3)步骤②所涉及的化学反应基本类型是 。
(4)实验步骤②中除了加入稀硫酸外,还可以选用硫酸铜溶液,请写出反应的化学方程式 。
9.海水蕴藏着丰富的海洋资源,某兴趣小组设计的综合利用海水的部分流程图如图。据图回答:
(1)海水制镁。步骤①制氢氧化镁选择向母液中加入石灰乳,而不是向海水中直接加入石灰乳,原因是 。操作的名称是 。
(2)海水晒盐。将粗盐从海水中结晶出来的方法是 。
通过步骤④除去粗盐溶液中含有的、、等杂质离子,需要依次加入过量的溶液、过量的溶液、过量的溶液,过滤除去沉淀后再加入适量的稀盐酸。其中加入适量的稀盐酸的目的是 。
(3)海水制碱。步骤⑥⑦是氨碱法制纯碱的流程,步骤⑥中需要向饱和溶液中先后通入过量的氨气、二氧化碳。其中步骤⑦中发生反应的化学方程式是 。
10.小明同学去黄山旅游时,用瓶装了一些山下的泉水,带回实验室在老师的指导下,按下列流程进行实验,制取蒸馏水。请回答下列问题。
(1)过滤过程中需要用到的玻璃仪器有烧杯、玻璃棒、 。实验室过滤后滤液仍然浑浊可能的原因有 (写一点)。
(2)电解水化学方程式 ,主要能量变化形式是 。
【拓展练习】
11.2024年4月25日,我国“神舟十八号”载人航天飞船成功发射。为保证宇航员正常的生命活动,空间站内的空气需与我们周围的空气组成相近,常常采用以下循环系统:
(1)写出步骤①发生的化学反应方程式 ,属于 (基本反应类型),
(2)甲烷()是一种常用燃料,请写出的一种微观含义 。
(3)上述循环系统给空间站补充氧气的化学反应有 (填序号)。
(4)上述循环系统中循环利用的物质是 (写化学式)。
12.从某含铜、金(Au)和镍(Ni) 废金属中回收Au并制备硫酸铜晶体(CuSO4·5H2O)的流程如下:
(1)将废旧金属研磨成粉末的目的是:
(2)X化学式为 ;
(3)操作1和2中用到的玻璃仪器有:烧杯、玻璃棒、 等;
(4)反应2的化学方程式为: 。
13.实验室以软锰矿(主要含MnO2)为原料制备MnO2的流程如图:
(1)为使软锰矿充分反应,可采取的措施有 (写一条)。
(2)“沉锰”反应为:MnSO4+2NH4HCO3MnCO3↓+(NH4)2SO4+H2O+X,X的化学式为 。
(3)实验室进行“过滤”操作需用到的玻璃仪器有 (写一种)。
(4)在空气中煅烧MnCO3会生成不同的锰氧化物,各锰的氧化物质量分数随煅烧温度的变化关系如图所示。
①温度控制在450℃的目的是 。
②加热至370℃~410℃间,二氧化锰质量分数上升的原因是 。
(5)已知金属锰能与稀硫酸反应生成+2价的锰盐溶液,写出该反应的化学方程式 。
(6)欲验证铁、铜、锰三种金属的活动性强弱为Mn>Fe>Cu,可设计的实验方案为 。
(可选择试剂:MnSO4溶液、FeSO4溶液、CuSO4溶液、Fe片、Mn片、Cu片)
14.铝镓合金是铝和镓熔合在一起的混合物,金属镓在流程中不参加化学反应。科学家研究开发出一种利用铝镓(Ga)合金制备氢气的新工艺,其流程图如下所示:
(1)物质X是 (写化学式),写出电解氧化铝的化学方程式为 。
(2)该工艺能循环使用的物质是 (写化学式)。
(3)上述过程中,涉及到的氧化物有 (写化学式)。
(4)工业上常采用电解水制取氢气,与之相比由铝镓合金制取氢气的优点是 (答1点)。
(5)生成的氢气是工业上合成氨的一种重要化工原料。氢气与氮气在催化剂表面合成氨气的微观反应过程可表示为如图2(“”表示氢原子,“”表示氮原子,“”表示催化剂)。则合成氨反应过程的正确顺序是 (填序号)。
15.民以食为天,人类主要通过食用淀粉获得能量。
(1)大米、面粉等食物中的淀粉是绿色植物通过 合成、转化形成的。
(2)2021年9月,中国科学家发表了利用CO2、H2人工合成淀粉的成果。此成果预示着人类能节约土地资源、解决粮食短缺,同时减少CO2排放,缓解 (填环境问题)等。
(3)下图为人工合成淀粉的关键步骤。
此人工合成淀粉与光合作用合成淀粉的原理 (选填“相同”、“不同”)。
(4)获得大量H2是人工合成淀粉的重要一步。下图是制氢、贮氢与释氢的一种方法。
①虚线框内制氢的总反应的基本反应类型是 反应(选填“化合”或“分解”)
答案
1.(1)/ 增大反应物的接触面积,使反应更快、更充分
(2)二氧化硅/SiO2
(3)防止温度过高导致碳酸氢铵分解
(4)增大
2.(1)增大反应物的接触面积,使反应更充分
(2)
(3)锌原子间隔变小
(4)锌的金属活动性比铁和铜强
(5)、/铜离子、银离子
3.(1)增大反应物接触面积,加快反应速率,使反应更充分
(2)五
(3)H2O
(4)将NH4Cl晶体和液体分离 氮肥
4.(1) NaCl 电能
(2)作干燥剂
(3)
(4)高温易分解
5.(1)灭火(合理即可)
(2)3∶1
(3)
(4)可制备的CH3OH的质量是1.6g。
6.(1)分子之间的间隔变小
(2)
(3)高
(4)充分利用原料
7.(1)使二氧化锰与氢氧化钾混合均匀,加快反应更充分
(2)、O
(3)
(4) 、
8.(1)铁/Fe
(2)漏斗
(3)置换反应
(4)
9.(1)蒸发浓缩后的溶液,镁离子浓度高,能提高产率和生产效率 过滤
(2)蒸发结晶 将滤液中的过量的碳酸钠和过量的氢氧化钠完全转化为氯化钠
(3)
10.(1)漏斗 滤纸破损(合理即可)
(2)电能转化为化学能
11.(1)分解反应
(2)1个甲烷分子(合理即可)
(3)①③
(4)H2O、CO2、H2、O2
12.(1)增大反应物的接触面积,使反应更快、更充分
(2)
(3)漏斗
(4)
13.(1)搅拌或将固体粉碎
(2)CO2
(3)漏斗等
(4)MnO2的质量分数最大 部分MnO、Mn2O3转化为MnO2
(5)Mn+H2SO4=MnSO4+H2↑
(6)将Fe片分别放入MnSO4溶液和CuSO4溶液中或将Mn片、Cu片分别放入FeSO4溶液中
14.(1) Al
(2)Al、Ga
(3)H2O、Al2O3
(4)节约能源(合理即可)
(5)⑤④①②③
15.(1)光合作用
(2)温室效应
(3)不同
(4)分解
1.造纸术是我国古代的四大发明之一,硫酸铝在造纸工业中常用作松香胶、蜡乳液的沉淀剂。利用铝灰(主要成分为SiO2、Fe2O3、Al2O3)制取硫酸铝晶体的主要流程如下图:
已知:①SiO2既不溶于水,也不与酸反应。②碳酸氢铵在35℃以上会开始分解,60℃时可以完全分解。请回答下列问题:
(1)酸溶池中发生反应的化学方程式为 (任写一个),生产过程中进行搅拌的目的是 。
(2)过滤器中滤渣1的成分是 。
(3)除杂室内的温度不宜过高,其原因是 。
(4)结晶池中,通常采用冷却结晶的方式得到硫酸铝晶体,说明硫酸铝的溶解度随温度的升高而 。
2.我国是世界上锌冶炼最早的国家,明代宋应星所著的《天工开物》中有关于“火法”炼锌的工艺记载是:“每炉甘石(主要成分是碳酸锌)十斤,装载入一泥罐内……然后逐层用煤炭饼(反应后生成一氧化碳)垫盛,其底铺薪,发火煅红……冷定毁罐取出……即倭铅(锌)也。”该工艺过程分解模拟如图,请结合图文信息回答问题:
(1)装入原料器之前,将炉甘石敲碎的目的是 。
(2)高温炉内,碳酸锌()在高温条件下与煤的主要成分发生反应生成和,反应的化学方程式为 。
(3)从微观角度分析冷凝器中冷凝的原理 。
(4)我国古代冶锌晚于铁和铜,分析说明其中的原因 。
(5)湿法冶金利用置换反应。向、混合液中加入粉,充分反应后过滤。若取出的滤渣滴加稀盐酸有气泡产生,则滤液中一定不含的金属阳离子是 。
3.湖北荆州盛产淡水贻贝,实验室以淡水贻贝壳(主要成分为CaCO3和少量 SiO2)为原料制备轻质碳酸钙粉末作为牙膏摩擦剂,工艺流程如下:
(1)酸浸前将贻贝壳打碎的目的是 。
(2)操作①酸浸发生反应的化学方程式是 。
(3)操作②反应的化学方程式是:。则x是 。
(4)操作④的步骤是蒸发浓缩、降温结晶、过滤、洗涤、干燥,其中过滤的目的是 。制得NH4Cl晶体在农业上可作 。
4.漂白粉是常用的含氯消毒剂,主要成分是次氯酸钙【Ca(ClO)2】和氯化钙,制取漂白粉的工业流程如下图所示(部分物质及条件已略去)。A~F为常见物质,A为生理盐水的主要成分,B为气体单质,F为常见的碱
(1)A的化学式为 。反应①中的能量转化形式为 转化为化学能。
(2)反应③在生产生活中的应用 。
(3)反应②的化学方程式为 。
(4)由操作Ⅰ可以推测漂白粉具有的化学性质之一是 。
5.科技兴则民族兴,科技强则国家强。中国科学家在国际上首次实现了二氧化碳到淀粉的人工合成,为淀粉工业制造和二氧化碳利用打开了一扇窗。部分人工合成淀粉路线如图:
(1)除了人工合成淀粉外,二氧化碳在生产和生活中还具有的用途是 (写一条)。
(2)甲醇(CH3OH)中碳元素与氢元素的质量比是 。
(3)习总书记在第75届联合国大会上作出我国二氧化碳排放力争于2030年前达到峰值、努力争取2060年前实现碳中和的重大宣示。科学家提出用石灰浆(主要成分为氢氧化钙)来吸收CO2。请写出其发生反应的化学方程式 。
(4)已知二氧化碳转化为甲醇反应的化学方程式为CO2+3H2CH3OH+H2O。2.2gCO2理论上可制备CH3OH的质量是多少 (写出计算过程)
【能力提升】
6.氨气()是一种重要的化工原料,工业上合成的工艺流程如图:
(1)将和净化后压缩,从微观角度分析,“压缩”时发生的变化是 。
(2)合成塔中在高温、高压、催化剂的条件下生成的化学方程式为 。
(3)降温分离氨气的方法说明与和相比,的沸点更 (选填“高”或“低”)。
(4)将降温分离出的、送回合成塔的目的是 (选填“充分利用原料”或“防止氮气污染空气”)。
7.工业生产高锰酸钾的流程如图所示,回答有关问题:
(1)Ⅰ中混合搅拌的目的是 。
(2)Ⅱ的反应物及产物如流程所示,反应前后化合价发生变化的元素有 (填元素符号);
(3)请完成Ⅲ中发生反应的化学方程式 。
(4)流程图中的物质属于氧化物的有 ,可循环利用的是 。
8.为了达到收旧利废节能减排的目的,从含有金属镁、铁、铜的粉末中,分离和提取出重要化工原料和有关金属,实验过程如下:
请回答:
(1)操作①中分离出的金属A是 。
(2)操作a中要用到玻璃棒、 、烧杯。
(3)步骤②所涉及的化学反应基本类型是 。
(4)实验步骤②中除了加入稀硫酸外,还可以选用硫酸铜溶液,请写出反应的化学方程式 。
9.海水蕴藏着丰富的海洋资源,某兴趣小组设计的综合利用海水的部分流程图如图。据图回答:
(1)海水制镁。步骤①制氢氧化镁选择向母液中加入石灰乳,而不是向海水中直接加入石灰乳,原因是 。操作的名称是 。
(2)海水晒盐。将粗盐从海水中结晶出来的方法是 。
通过步骤④除去粗盐溶液中含有的、、等杂质离子,需要依次加入过量的溶液、过量的溶液、过量的溶液,过滤除去沉淀后再加入适量的稀盐酸。其中加入适量的稀盐酸的目的是 。
(3)海水制碱。步骤⑥⑦是氨碱法制纯碱的流程,步骤⑥中需要向饱和溶液中先后通入过量的氨气、二氧化碳。其中步骤⑦中发生反应的化学方程式是 。
10.小明同学去黄山旅游时,用瓶装了一些山下的泉水,带回实验室在老师的指导下,按下列流程进行实验,制取蒸馏水。请回答下列问题。
(1)过滤过程中需要用到的玻璃仪器有烧杯、玻璃棒、 。实验室过滤后滤液仍然浑浊可能的原因有 (写一点)。
(2)电解水化学方程式 ,主要能量变化形式是 。
【拓展练习】
11.2024年4月25日,我国“神舟十八号”载人航天飞船成功发射。为保证宇航员正常的生命活动,空间站内的空气需与我们周围的空气组成相近,常常采用以下循环系统:
(1)写出步骤①发生的化学反应方程式 ,属于 (基本反应类型),
(2)甲烷()是一种常用燃料,请写出的一种微观含义 。
(3)上述循环系统给空间站补充氧气的化学反应有 (填序号)。
(4)上述循环系统中循环利用的物质是 (写化学式)。
12.从某含铜、金(Au)和镍(Ni) 废金属中回收Au并制备硫酸铜晶体(CuSO4·5H2O)的流程如下:
(1)将废旧金属研磨成粉末的目的是:
(2)X化学式为 ;
(3)操作1和2中用到的玻璃仪器有:烧杯、玻璃棒、 等;
(4)反应2的化学方程式为: 。
13.实验室以软锰矿(主要含MnO2)为原料制备MnO2的流程如图:
(1)为使软锰矿充分反应,可采取的措施有 (写一条)。
(2)“沉锰”反应为:MnSO4+2NH4HCO3MnCO3↓+(NH4)2SO4+H2O+X,X的化学式为 。
(3)实验室进行“过滤”操作需用到的玻璃仪器有 (写一种)。
(4)在空气中煅烧MnCO3会生成不同的锰氧化物,各锰的氧化物质量分数随煅烧温度的变化关系如图所示。
①温度控制在450℃的目的是 。
②加热至370℃~410℃间,二氧化锰质量分数上升的原因是 。
(5)已知金属锰能与稀硫酸反应生成+2价的锰盐溶液,写出该反应的化学方程式 。
(6)欲验证铁、铜、锰三种金属的活动性强弱为Mn>Fe>Cu,可设计的实验方案为 。
(可选择试剂:MnSO4溶液、FeSO4溶液、CuSO4溶液、Fe片、Mn片、Cu片)
14.铝镓合金是铝和镓熔合在一起的混合物,金属镓在流程中不参加化学反应。科学家研究开发出一种利用铝镓(Ga)合金制备氢气的新工艺,其流程图如下所示:
(1)物质X是 (写化学式),写出电解氧化铝的化学方程式为 。
(2)该工艺能循环使用的物质是 (写化学式)。
(3)上述过程中,涉及到的氧化物有 (写化学式)。
(4)工业上常采用电解水制取氢气,与之相比由铝镓合金制取氢气的优点是 (答1点)。
(5)生成的氢气是工业上合成氨的一种重要化工原料。氢气与氮气在催化剂表面合成氨气的微观反应过程可表示为如图2(“”表示氢原子,“”表示氮原子,“”表示催化剂)。则合成氨反应过程的正确顺序是 (填序号)。
15.民以食为天,人类主要通过食用淀粉获得能量。
(1)大米、面粉等食物中的淀粉是绿色植物通过 合成、转化形成的。
(2)2021年9月,中国科学家发表了利用CO2、H2人工合成淀粉的成果。此成果预示着人类能节约土地资源、解决粮食短缺,同时减少CO2排放,缓解 (填环境问题)等。
(3)下图为人工合成淀粉的关键步骤。
此人工合成淀粉与光合作用合成淀粉的原理 (选填“相同”、“不同”)。
(4)获得大量H2是人工合成淀粉的重要一步。下图是制氢、贮氢与释氢的一种方法。
①虚线框内制氢的总反应的基本反应类型是 反应(选填“化合”或“分解”)
答案
1.(1)/ 增大反应物的接触面积,使反应更快、更充分
(2)二氧化硅/SiO2
(3)防止温度过高导致碳酸氢铵分解
(4)增大
2.(1)增大反应物的接触面积,使反应更充分
(2)
(3)锌原子间隔变小
(4)锌的金属活动性比铁和铜强
(5)、/铜离子、银离子
3.(1)增大反应物接触面积,加快反应速率,使反应更充分
(2)五
(3)H2O
(4)将NH4Cl晶体和液体分离 氮肥
4.(1) NaCl 电能
(2)作干燥剂
(3)
(4)高温易分解
5.(1)灭火(合理即可)
(2)3∶1
(3)
(4)可制备的CH3OH的质量是1.6g。
6.(1)分子之间的间隔变小
(2)
(3)高
(4)充分利用原料
7.(1)使二氧化锰与氢氧化钾混合均匀,加快反应更充分
(2)、O
(3)
(4) 、
8.(1)铁/Fe
(2)漏斗
(3)置换反应
(4)
9.(1)蒸发浓缩后的溶液,镁离子浓度高,能提高产率和生产效率 过滤
(2)蒸发结晶 将滤液中的过量的碳酸钠和过量的氢氧化钠完全转化为氯化钠
(3)
10.(1)漏斗 滤纸破损(合理即可)
(2)电能转化为化学能
11.(1)分解反应
(2)1个甲烷分子(合理即可)
(3)①③
(4)H2O、CO2、H2、O2
12.(1)增大反应物的接触面积,使反应更快、更充分
(2)
(3)漏斗
(4)
13.(1)搅拌或将固体粉碎
(2)CO2
(3)漏斗等
(4)MnO2的质量分数最大 部分MnO、Mn2O3转化为MnO2
(5)Mn+H2SO4=MnSO4+H2↑
(6)将Fe片分别放入MnSO4溶液和CuSO4溶液中或将Mn片、Cu片分别放入FeSO4溶液中
14.(1) Al
(2)Al、Ga
(3)H2O、Al2O3
(4)节约能源(合理即可)
(5)⑤④①②③
15.(1)光合作用
(2)温室效应
(3)不同
(4)分解
同课章节目录
