第37练 实验仪器、装置与操作 课时作业(含解析)2026届高三化学一轮总复习
文档属性
| 名称 | 第37练 实验仪器、装置与操作 课时作业(含解析)2026届高三化学一轮总复习 | 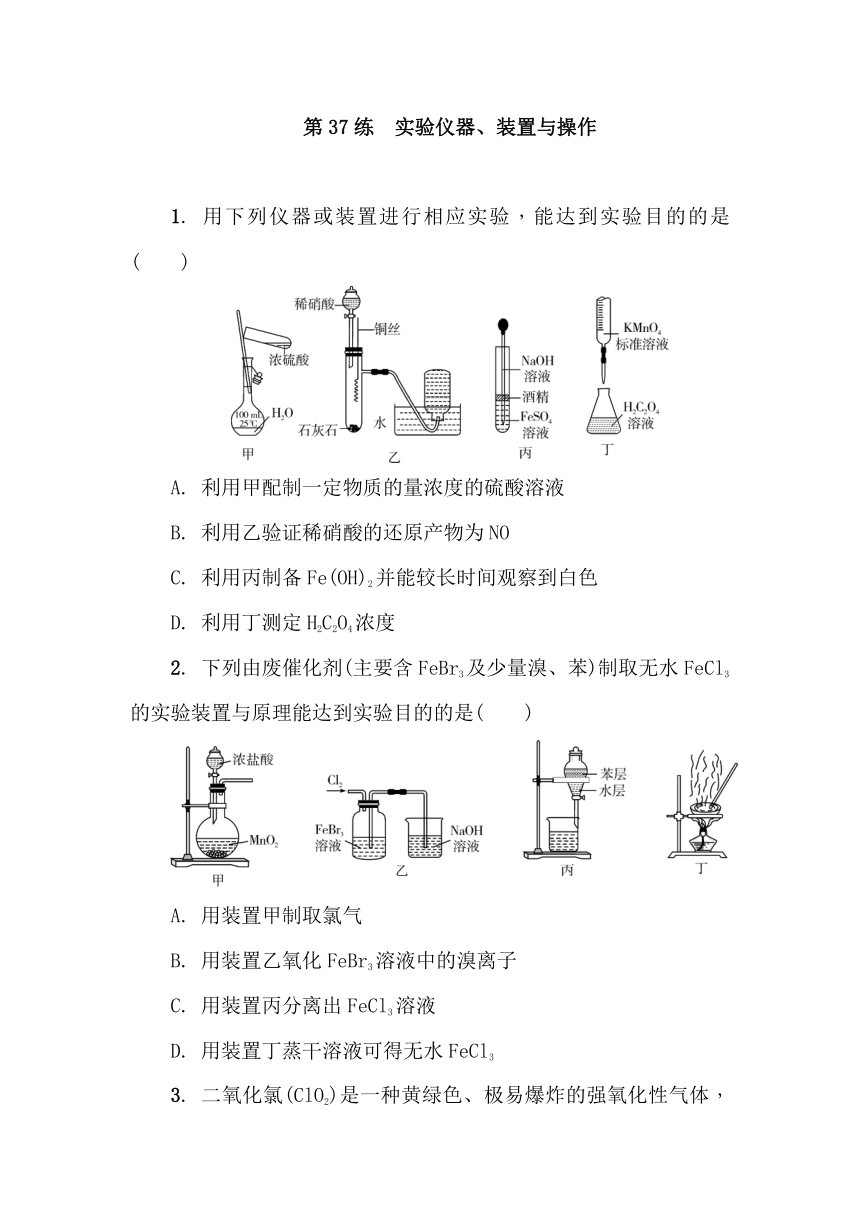 | |
| 格式 | doc | ||
| 文件大小 | 1.9MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 通用版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-05-06 21:55:20 | ||
图片预览





文档简介
第37练 实验仪器、装置与操作
1. 用下列仪器或装置进行相应实验,能达到实验目的的是( )
A. 利用甲配制一定物质的量浓度的硫酸溶液
B. 利用乙验证稀硝酸的还原产物为NO
C. 利用丙制备Fe(OH)2并能较长时间观察到白色
D. 利用丁测定H2C2O4浓度
2. 下列由废催化剂(主要含FeBr3及少量溴、苯)制取无水FeCl3的实验装置与原理能达到实验目的的是( )
A. 用装置甲制取氯气
B. 用装置乙氧化FeBr3溶液中的溴离子
C. 用装置丙分离出FeCl3溶液
D. 用装置丁蒸干溶液可得无水FeCl3
3. 二氧化氯(ClO2)是一种黄绿色、极易爆炸的强氧化性气体,易溶于水,在水中溶解度约为Cl2的5倍,其水溶液在较高温度与光照下会生成ClO和ClO。实验室制备ClO2的反应为2NaClO3+SO2+H2SO4===2ClO2+2NaHSO4。下列有关实验室制备ClO2的实验原理和装置能达到实验目的的是( )
A. B.
C. D.
4. (2024·连云港一模)实验室制备水合肼(N2H4·H2O)溶液的反应原理为NaClO+2NH3===N2H4·H2O+NaCl,N2H4·H2O能与NaClO剧烈反应。下列装置和操作能达到实验目的的是( )
A. 用装置甲制取Cl2
B. 用装置乙制备NaClO溶液
C. 用装置丙制备水合肼溶液
D. 用装置丁分离水合肼和NaCl混合溶液
5. (2025·南师附中高三下月考)下列实验装置(部分夹持装置略)正确的是( )
A. B. C. D.
6. 海水中含有丰富的碘元素,海洋中许多藻类植物具有富集碘的能力,如海带中含碘量可达0.3%~0.5%,约为海水中碘浓度的10万倍。灼烧海带提取I2时,下列实验原理与装置不能达到相应实验目的的是( )
A. 用装置甲灼烧海带 B. 用装置乙过滤得到浸出液
C. 用装置丙反应生成I2 D. 用装置丁萃取碘水中的I2
7. (2024·南京、盐城一模)实验室以CaCO3为原料,制备CO2并获得CaCl2·6H2O晶体。下列图示装置和原理能达到实验目的是( )
A. 用装置甲制取CO2 B. 用装置乙除去CO2中的HCl
C. 用装置丙干燥并收集CO2 D. 用装置丁蒸干溶液获得CaCl2·6H2O
8. (2024·南京、盐城二模)下列实验能实现的是( )
A. 装置甲左侧用于检验氯化铵受热分解出的氨气
B. 装置乙用于分离碘单质和高锰酸钾固体混合物
C. 装置丙中若a处有红色物质生成,b处变蓝,证明X一定是H2
D. 装置丁可以制取少量CO2,安全漏斗可以防止气体逸出
9. (2025·玄武高中高三下月考)实验室制备溴苯,并验证HBr生成。下列实验装置和操作能达到实验目的的是 ( )
A. 旋开装置甲中恒压滴液漏斗的活塞可使苯和溴混合液顺利滴入烧瓶中
B. 装置乙盛放NaOH溶液以除去HBr气体中混有的Br2
C. 向装置丙中滴加几滴酚酞溶液可检验HBr的生成
D. 用装置丁分离苯和溴苯
10. CuBr是常用的催化剂,受热易分解。可通过SO2+2Cu2++2Br-+2H2O===2CuBr↓+SO+4H+制备。下列实验室制备CuBr的实验装置和操作不能达到实验目的的是( )
A. 用装置甲制备SO2气体 B. 用装置乙收集SO2气体
C. 用装置丙制备CuBr D. 用装置丁吸收多余的SO2气体
11. (2025·如皋中学高三月考)下列实验装置或操作不能达到相应实验目的的是( )
A. B. C. D.
12. 向苯酚钠溶液中通CO2回收苯酚的实验原理和装置能达到实验目的的是( )
A. 用装置甲制备CO2气体
B. 用装置乙除去CO2中混有的少量HCl
C. 装置丙中发生反应生成苯酚和Na2CO3溶液
D. 从装置丁分液漏斗的下端放出苯酚层
13. (2024·苏州三模)下列制备、干燥、收集NH3,并进行喷泉实验的原理与装置能达到实验目的的是( )
A. 用装置甲制备NH3 B. 用装置乙干燥NH3
C. 用装置丙收集NH3 D. 用装置丁进行喷泉实验
14. 下列有关实验能达到相应实验目的的是( )
A. B.
C. D.
15. (2024·南京、盐城一模)下列由废铁屑制取(NH4)2Fe(SO4)2·6H2O的实验装置与操作能达到实验目的的是( )
A. 用装置甲称取一定质量的(NH4)2SO4固体
B. 用装置乙除去废铁屑表面的油污
C. 用装置丙将废铁屑充分溶解
D. 用装置丁蒸干溶液得到(NH4)2Fe(SO4)2·6H2O晶体
16. (2024·徐州四模)为模拟氨碱法制取纯碱的主要反应,设计在图所示装置。有关说法正确的是( )
A. 先从b管通入NH3再从a管通入CO2
B. 先从a管通入CO2再从b管通入NH3
C. 反应一段时间广口瓶内有晶体析出
D. c中装有碱石灰以吸收未反应的氨气
17. (2024·常州联盟学校高三上调研)下列说法正确的是( )
A. 装置甲可以用于探究铁与水蒸气反应,并点燃肥皂泡检验氢气
B. 装置乙的操作可排出盛有KMnO4溶液滴定管尖嘴内的气泡
C. 装置丙可用于实验室配制银氨溶液
D. 装置丁中若将ZnSO4溶液替换成CuSO4溶液,将无法形成原电池
第37练 实验仪器、装置与操作
1. B 解析:稀释浓硫酸时,不能在容量瓶中进行,应在烧杯内稀释,A不正确;先打开分液漏斗活塞,让稀硝酸与石灰石反应,利用产生的CO2排尽装置内的空气,再让铜丝与稀硝酸反应,可观察到气体无色,且能收集到无色气体,从而证明稀硝酸的还原产物为NO,B正确;丙装置中,酒精与水互溶,不能起到隔绝空气的作用,生成的Fe(OH)2很快被溶解的氧气氧化,不能较长时间观察到白色,C不正确;KMnO4具有强氧化性,会腐蚀橡胶,所以KMnO4标准溶液不能盛放在碱式滴定管内,D不正确。故选B。
2. C 解析:二氧化锰和浓盐酸共热制取氯气,A错误;应把氯气通到溴化铁溶液中,左边装置应长管进短管出,B错误;氯化铁溶于水不溶于苯,溴在苯中的溶解度更大,可用萃取分离,C正确;氯化铁溶液中铁离子易水解,在空气中蒸干溶液会得到氢氧化铁,得不到无水FeCl3,D错误。故选C。
3. C 解析:用浓硫酸与铜反应制备二氧化硫需要加热才能发生,选项A错误;实验室制备ClO2的反应为2NaClO3+SO2+H2SO4===2ClO2+2NaHSO4,试剂选择正确,但二氧化硫通入时导管应该长进短出,才能充分接触,否则反应很难进行,选项B错误;ClO2是一种极易爆炸的强氧化性气体,易溶于水,可用冰水吸收,选项C正确;制备过程中有毒气体直接排放到空气中会造成污染,可用装置丁处理尾气吸收,氢氧化钠能与二氧化硫、二氧化氯反应,但缺少防倒吸装置,选项D错误。故选C。
4. B 解析:浓盐酸与二氧化锰制取氯气需要加热,A装置不满足条件,A不符合题意;氯气与氢氧化钠溶液反应生成次氯酸钠、氯化钠,B装置可达到实验目的,B符合题意;氨气可被次氯酸钠氧化,反应剧烈,NaClO过量,可氧化生成的N2H4·H2O,应将NaClO注入氨水,C装置不能达到实验目的,C不符合题意;N2H4·H2O沸点较低,溶于水,应该采取蒸馏的方式提纯,蒸馏时温度计测定馏分的温度、冷凝管中冷水下进上出,D装置不能达到实验目的,D不符合题意。故选B。
5. C 解析:应该在坩埚中进行钠的燃烧实验,故A错误;氨气易溶于水,不能用排水量气法测量氨气的体积,故B错误;继续向上层清液中滴加BaCl2溶液,若不再生成白色沉淀,证明SO已沉淀完全,故C正确;向容量瓶中转移液体,应该用玻璃棒引流,故D错误。故选C。
6. D 解析:灼烧海带应在坩埚中进行,故A正确;海带灰溶于水后得到悬浊液,应用过滤的方法得到浸出液,故B正确;向用稀硫酸酸化的浸出液滴入双氧水,双氧水能将溶液中的碘离子氧化为单质碘,故C正确;碘与乙醇互溶,不能用乙醇萃取溶液中的碘,故D错误。故选D。
7. C 解析:稀硫酸与大理石反应生成微溶的硫酸钙,会覆盖在大理石表面,会阻止反应进一步发生,应该用稀盐酸与大理石反应制取CO2,A项错误;CO2和HCl都可以与碳酸钠溶液反应,应该用饱和碳酸氢钠溶液除去CO2中的HCl,B项错误;二氧化碳通入浓硫酸中干燥后,并用向上排空气法收集,C项正确;CaCl2·6H2O易失去结晶水,因此不能通过加热蒸发皿得到,可由氯化钙的热饱和溶液冷却结晶析出六水氯化钙结晶物,D项错误。故选C。
8. D 解析:左侧的五氧化二磷会吸收氯化铵分解产生的氨气,因此左侧可检测氯化氢,故A不符合题意;加热时碘升华,高锰酸钾会发生分解,因此加热法不能分离,故B不符合题意;a处有红色物质生成,说明氧化铜被还原,b处变蓝,说明气体中含有水蒸气,因此有可能X中含有水蒸气,X也可能含有乙醇、氨气、甲烷等,故C不符合题意;大理石和稀盐酸反应生成二氧化碳,安全漏斗可在左右侧形成液柱,可防止气体逸出,故D符合题意;故选D。
9. A 解析:该漏斗有一根连通反应器的管保证上下端压强一致使液体顺利滴下,A项正确;HBr和Br2均与NaOH反应,不能用NaOH除去Br2,B项错误;HBr呈酸性,不能使酚酞变色无法检验,C项错误;苯和溴苯互溶,无法分液分离,选择蒸馏进行分离,D项错误。故选A。
10. B 解析:实验室用亚硫酸钠固体和70%的硫酸制取二氧化硫,故A能达到实验目的,故A不选;二氧化硫密度比空气大,所以应用向上排空气法收集,故B不能达到实验目的,故B选;根据题给方程式,二氧化硫通入硫酸铜和NaBr的混合溶液中可制取CuBr,能达到实验目的,故C不选;SO2和NaOH溶液反应,可以用NaOH溶液吸收多余的SO2,用干燥管可以防止倒吸,能达到实验目的,故D不选。故选B。
11. B 解析:SO2通入滴有KSCN的Fe2(SO4)3溶液,SO2还原Fe3+而使溶液褪色,验证SO2还原性,A不符合题意;氯气在饱和食盐水中溶解度不大,且与饱和食盐水不反应,所以不能形成喷泉实验,故B符合题意;Cl2通入Na2S溶液发生置换反应得到S单质,证明Cl2的氧化性大于S,即说明氯比硫的非金属性强,C不符合题意;碱石灰吸收浓氨水中的水分,使平衡NH3·H2O??H2O+NH3↑正向移动,制备氨气,D不符合题意。故选B。
12. D 解析:二氧化碳从长颈漏斗逸出,甲装置不能制备二氧化碳,A错误;二氧化碳与氢氧化钠溶液反应,应选用饱和碳酸氢钠溶液,B错误;装置丙中发生反应生成苯酚和NaHCO3溶液,C错误;苯酚在水中的溶解度小,密度比水大,故可从装置丁分液漏斗的下端放出苯酚层,D正确。故选D。
13. D 解析:实验室用加热氯化铵和氢氧化钙混合物的方法制取氨气,加热时试管口应略向下倾斜,A项错误;浓硫酸能与氨气反应,不能用于干燥氨气,应使用碱石灰干燥氨气,B项错误;由于氨气密度小于空气,本装置收集氨气时导气管应“长进短出”,C项错误;氨气极易溶于水,用装置丁可以进行喷泉实验,D项正确。故选D。
14. C 解析:浓盐酸与MnO2的反应需要加热,故A错误;氨气的密度比空气的密度小,应选用向下排空气法收集,故B错误;蒸馏时温度计测定馏分的温度,冷却水下进上出,图中操作合理,故C正确;乙酸乙酯能与NaOH溶液反应,小试管中应为饱和Na2CO3溶液,故D错误。故选C。
15. B 解析:装置甲中,物品与砝码的位置颠倒,使用游码时称取的(NH4)2SO4固体的质量偏低,A不能达到实验目的;Na2CO3溶液呈碱性,能促进油脂水解,从而去除物品表面的油污,所以可用装置乙除去废铁屑表面的油污,B能达到实验目的;浓硫酸具有强氧化性,能使铁表面发生钝化,所以不能用装置丙将废铁屑充分溶解,C不能达到实验目的;(NH4)2Fe(SO4)2·6H2O晶体受热易失去结晶水,不能用蒸干溶液的方法制取,所以用装置丁蒸干溶液得不到(NH4)2Fe(SO4)2·6H2O晶体,D不能达到实验目的。故选B。
16. C 解析:不能直接将氨气通入水中,会引起倒吸,A错误;先从a管通入氨气,再从B管通入CO2,B错误;NaHCO3的溶解度随温度降低而增大,所以反应一段时间后广口瓶内有NaHCO3晶体析出,C正确;碱石灰能干燥氨气,但不能吸收未反应的氨气,D错误。
17. A 解析:湿棉花受热产生水蒸气,高温下Fe与水蒸气反应生成氢气,氢气具有可燃性,点燃肥皂泡检验氢气,A正确;高锰酸钾溶液具有强氧化性,会腐蚀橡胶管,所以高锰酸钾溶液应盛放在酸式滴定管中,不能盛放在碱式滴定管中,B错误;实验室配制银氨溶液时应该把氨水逐滴滴入硝酸银溶液中,C错误;装置丁中若将ZnSO4溶液替换成CuSO4溶液,仍然可以形成原电池,锌是负极,铜是正极,D错误。故选A。
1. 用下列仪器或装置进行相应实验,能达到实验目的的是( )
A. 利用甲配制一定物质的量浓度的硫酸溶液
B. 利用乙验证稀硝酸的还原产物为NO
C. 利用丙制备Fe(OH)2并能较长时间观察到白色
D. 利用丁测定H2C2O4浓度
2. 下列由废催化剂(主要含FeBr3及少量溴、苯)制取无水FeCl3的实验装置与原理能达到实验目的的是( )
A. 用装置甲制取氯气
B. 用装置乙氧化FeBr3溶液中的溴离子
C. 用装置丙分离出FeCl3溶液
D. 用装置丁蒸干溶液可得无水FeCl3
3. 二氧化氯(ClO2)是一种黄绿色、极易爆炸的强氧化性气体,易溶于水,在水中溶解度约为Cl2的5倍,其水溶液在较高温度与光照下会生成ClO和ClO。实验室制备ClO2的反应为2NaClO3+SO2+H2SO4===2ClO2+2NaHSO4。下列有关实验室制备ClO2的实验原理和装置能达到实验目的的是( )
A. B.
C. D.
4. (2024·连云港一模)实验室制备水合肼(N2H4·H2O)溶液的反应原理为NaClO+2NH3===N2H4·H2O+NaCl,N2H4·H2O能与NaClO剧烈反应。下列装置和操作能达到实验目的的是( )
A. 用装置甲制取Cl2
B. 用装置乙制备NaClO溶液
C. 用装置丙制备水合肼溶液
D. 用装置丁分离水合肼和NaCl混合溶液
5. (2025·南师附中高三下月考)下列实验装置(部分夹持装置略)正确的是( )
A. B. C. D.
6. 海水中含有丰富的碘元素,海洋中许多藻类植物具有富集碘的能力,如海带中含碘量可达0.3%~0.5%,约为海水中碘浓度的10万倍。灼烧海带提取I2时,下列实验原理与装置不能达到相应实验目的的是( )
A. 用装置甲灼烧海带 B. 用装置乙过滤得到浸出液
C. 用装置丙反应生成I2 D. 用装置丁萃取碘水中的I2
7. (2024·南京、盐城一模)实验室以CaCO3为原料,制备CO2并获得CaCl2·6H2O晶体。下列图示装置和原理能达到实验目的是( )
A. 用装置甲制取CO2 B. 用装置乙除去CO2中的HCl
C. 用装置丙干燥并收集CO2 D. 用装置丁蒸干溶液获得CaCl2·6H2O
8. (2024·南京、盐城二模)下列实验能实现的是( )
A. 装置甲左侧用于检验氯化铵受热分解出的氨气
B. 装置乙用于分离碘单质和高锰酸钾固体混合物
C. 装置丙中若a处有红色物质生成,b处变蓝,证明X一定是H2
D. 装置丁可以制取少量CO2,安全漏斗可以防止气体逸出
9. (2025·玄武高中高三下月考)实验室制备溴苯,并验证HBr生成。下列实验装置和操作能达到实验目的的是 ( )
A. 旋开装置甲中恒压滴液漏斗的活塞可使苯和溴混合液顺利滴入烧瓶中
B. 装置乙盛放NaOH溶液以除去HBr气体中混有的Br2
C. 向装置丙中滴加几滴酚酞溶液可检验HBr的生成
D. 用装置丁分离苯和溴苯
10. CuBr是常用的催化剂,受热易分解。可通过SO2+2Cu2++2Br-+2H2O===2CuBr↓+SO+4H+制备。下列实验室制备CuBr的实验装置和操作不能达到实验目的的是( )
A. 用装置甲制备SO2气体 B. 用装置乙收集SO2气体
C. 用装置丙制备CuBr D. 用装置丁吸收多余的SO2气体
11. (2025·如皋中学高三月考)下列实验装置或操作不能达到相应实验目的的是( )
A. B. C. D.
12. 向苯酚钠溶液中通CO2回收苯酚的实验原理和装置能达到实验目的的是( )
A. 用装置甲制备CO2气体
B. 用装置乙除去CO2中混有的少量HCl
C. 装置丙中发生反应生成苯酚和Na2CO3溶液
D. 从装置丁分液漏斗的下端放出苯酚层
13. (2024·苏州三模)下列制备、干燥、收集NH3,并进行喷泉实验的原理与装置能达到实验目的的是( )
A. 用装置甲制备NH3 B. 用装置乙干燥NH3
C. 用装置丙收集NH3 D. 用装置丁进行喷泉实验
14. 下列有关实验能达到相应实验目的的是( )
A. B.
C. D.
15. (2024·南京、盐城一模)下列由废铁屑制取(NH4)2Fe(SO4)2·6H2O的实验装置与操作能达到实验目的的是( )
A. 用装置甲称取一定质量的(NH4)2SO4固体
B. 用装置乙除去废铁屑表面的油污
C. 用装置丙将废铁屑充分溶解
D. 用装置丁蒸干溶液得到(NH4)2Fe(SO4)2·6H2O晶体
16. (2024·徐州四模)为模拟氨碱法制取纯碱的主要反应,设计在图所示装置。有关说法正确的是( )
A. 先从b管通入NH3再从a管通入CO2
B. 先从a管通入CO2再从b管通入NH3
C. 反应一段时间广口瓶内有晶体析出
D. c中装有碱石灰以吸收未反应的氨气
17. (2024·常州联盟学校高三上调研)下列说法正确的是( )
A. 装置甲可以用于探究铁与水蒸气反应,并点燃肥皂泡检验氢气
B. 装置乙的操作可排出盛有KMnO4溶液滴定管尖嘴内的气泡
C. 装置丙可用于实验室配制银氨溶液
D. 装置丁中若将ZnSO4溶液替换成CuSO4溶液,将无法形成原电池
第37练 实验仪器、装置与操作
1. B 解析:稀释浓硫酸时,不能在容量瓶中进行,应在烧杯内稀释,A不正确;先打开分液漏斗活塞,让稀硝酸与石灰石反应,利用产生的CO2排尽装置内的空气,再让铜丝与稀硝酸反应,可观察到气体无色,且能收集到无色气体,从而证明稀硝酸的还原产物为NO,B正确;丙装置中,酒精与水互溶,不能起到隔绝空气的作用,生成的Fe(OH)2很快被溶解的氧气氧化,不能较长时间观察到白色,C不正确;KMnO4具有强氧化性,会腐蚀橡胶,所以KMnO4标准溶液不能盛放在碱式滴定管内,D不正确。故选B。
2. C 解析:二氧化锰和浓盐酸共热制取氯气,A错误;应把氯气通到溴化铁溶液中,左边装置应长管进短管出,B错误;氯化铁溶于水不溶于苯,溴在苯中的溶解度更大,可用萃取分离,C正确;氯化铁溶液中铁离子易水解,在空气中蒸干溶液会得到氢氧化铁,得不到无水FeCl3,D错误。故选C。
3. C 解析:用浓硫酸与铜反应制备二氧化硫需要加热才能发生,选项A错误;实验室制备ClO2的反应为2NaClO3+SO2+H2SO4===2ClO2+2NaHSO4,试剂选择正确,但二氧化硫通入时导管应该长进短出,才能充分接触,否则反应很难进行,选项B错误;ClO2是一种极易爆炸的强氧化性气体,易溶于水,可用冰水吸收,选项C正确;制备过程中有毒气体直接排放到空气中会造成污染,可用装置丁处理尾气吸收,氢氧化钠能与二氧化硫、二氧化氯反应,但缺少防倒吸装置,选项D错误。故选C。
4. B 解析:浓盐酸与二氧化锰制取氯气需要加热,A装置不满足条件,A不符合题意;氯气与氢氧化钠溶液反应生成次氯酸钠、氯化钠,B装置可达到实验目的,B符合题意;氨气可被次氯酸钠氧化,反应剧烈,NaClO过量,可氧化生成的N2H4·H2O,应将NaClO注入氨水,C装置不能达到实验目的,C不符合题意;N2H4·H2O沸点较低,溶于水,应该采取蒸馏的方式提纯,蒸馏时温度计测定馏分的温度、冷凝管中冷水下进上出,D装置不能达到实验目的,D不符合题意。故选B。
5. C 解析:应该在坩埚中进行钠的燃烧实验,故A错误;氨气易溶于水,不能用排水量气法测量氨气的体积,故B错误;继续向上层清液中滴加BaCl2溶液,若不再生成白色沉淀,证明SO已沉淀完全,故C正确;向容量瓶中转移液体,应该用玻璃棒引流,故D错误。故选C。
6. D 解析:灼烧海带应在坩埚中进行,故A正确;海带灰溶于水后得到悬浊液,应用过滤的方法得到浸出液,故B正确;向用稀硫酸酸化的浸出液滴入双氧水,双氧水能将溶液中的碘离子氧化为单质碘,故C正确;碘与乙醇互溶,不能用乙醇萃取溶液中的碘,故D错误。故选D。
7. C 解析:稀硫酸与大理石反应生成微溶的硫酸钙,会覆盖在大理石表面,会阻止反应进一步发生,应该用稀盐酸与大理石反应制取CO2,A项错误;CO2和HCl都可以与碳酸钠溶液反应,应该用饱和碳酸氢钠溶液除去CO2中的HCl,B项错误;二氧化碳通入浓硫酸中干燥后,并用向上排空气法收集,C项正确;CaCl2·6H2O易失去结晶水,因此不能通过加热蒸发皿得到,可由氯化钙的热饱和溶液冷却结晶析出六水氯化钙结晶物,D项错误。故选C。
8. D 解析:左侧的五氧化二磷会吸收氯化铵分解产生的氨气,因此左侧可检测氯化氢,故A不符合题意;加热时碘升华,高锰酸钾会发生分解,因此加热法不能分离,故B不符合题意;a处有红色物质生成,说明氧化铜被还原,b处变蓝,说明气体中含有水蒸气,因此有可能X中含有水蒸气,X也可能含有乙醇、氨气、甲烷等,故C不符合题意;大理石和稀盐酸反应生成二氧化碳,安全漏斗可在左右侧形成液柱,可防止气体逸出,故D符合题意;故选D。
9. A 解析:该漏斗有一根连通反应器的管保证上下端压强一致使液体顺利滴下,A项正确;HBr和Br2均与NaOH反应,不能用NaOH除去Br2,B项错误;HBr呈酸性,不能使酚酞变色无法检验,C项错误;苯和溴苯互溶,无法分液分离,选择蒸馏进行分离,D项错误。故选A。
10. B 解析:实验室用亚硫酸钠固体和70%的硫酸制取二氧化硫,故A能达到实验目的,故A不选;二氧化硫密度比空气大,所以应用向上排空气法收集,故B不能达到实验目的,故B选;根据题给方程式,二氧化硫通入硫酸铜和NaBr的混合溶液中可制取CuBr,能达到实验目的,故C不选;SO2和NaOH溶液反应,可以用NaOH溶液吸收多余的SO2,用干燥管可以防止倒吸,能达到实验目的,故D不选。故选B。
11. B 解析:SO2通入滴有KSCN的Fe2(SO4)3溶液,SO2还原Fe3+而使溶液褪色,验证SO2还原性,A不符合题意;氯气在饱和食盐水中溶解度不大,且与饱和食盐水不反应,所以不能形成喷泉实验,故B符合题意;Cl2通入Na2S溶液发生置换反应得到S单质,证明Cl2的氧化性大于S,即说明氯比硫的非金属性强,C不符合题意;碱石灰吸收浓氨水中的水分,使平衡NH3·H2O??H2O+NH3↑正向移动,制备氨气,D不符合题意。故选B。
12. D 解析:二氧化碳从长颈漏斗逸出,甲装置不能制备二氧化碳,A错误;二氧化碳与氢氧化钠溶液反应,应选用饱和碳酸氢钠溶液,B错误;装置丙中发生反应生成苯酚和NaHCO3溶液,C错误;苯酚在水中的溶解度小,密度比水大,故可从装置丁分液漏斗的下端放出苯酚层,D正确。故选D。
13. D 解析:实验室用加热氯化铵和氢氧化钙混合物的方法制取氨气,加热时试管口应略向下倾斜,A项错误;浓硫酸能与氨气反应,不能用于干燥氨气,应使用碱石灰干燥氨气,B项错误;由于氨气密度小于空气,本装置收集氨气时导气管应“长进短出”,C项错误;氨气极易溶于水,用装置丁可以进行喷泉实验,D项正确。故选D。
14. C 解析:浓盐酸与MnO2的反应需要加热,故A错误;氨气的密度比空气的密度小,应选用向下排空气法收集,故B错误;蒸馏时温度计测定馏分的温度,冷却水下进上出,图中操作合理,故C正确;乙酸乙酯能与NaOH溶液反应,小试管中应为饱和Na2CO3溶液,故D错误。故选C。
15. B 解析:装置甲中,物品与砝码的位置颠倒,使用游码时称取的(NH4)2SO4固体的质量偏低,A不能达到实验目的;Na2CO3溶液呈碱性,能促进油脂水解,从而去除物品表面的油污,所以可用装置乙除去废铁屑表面的油污,B能达到实验目的;浓硫酸具有强氧化性,能使铁表面发生钝化,所以不能用装置丙将废铁屑充分溶解,C不能达到实验目的;(NH4)2Fe(SO4)2·6H2O晶体受热易失去结晶水,不能用蒸干溶液的方法制取,所以用装置丁蒸干溶液得不到(NH4)2Fe(SO4)2·6H2O晶体,D不能达到实验目的。故选B。
16. C 解析:不能直接将氨气通入水中,会引起倒吸,A错误;先从a管通入氨气,再从B管通入CO2,B错误;NaHCO3的溶解度随温度降低而增大,所以反应一段时间后广口瓶内有NaHCO3晶体析出,C正确;碱石灰能干燥氨气,但不能吸收未反应的氨气,D错误。
17. A 解析:湿棉花受热产生水蒸气,高温下Fe与水蒸气反应生成氢气,氢气具有可燃性,点燃肥皂泡检验氢气,A正确;高锰酸钾溶液具有强氧化性,会腐蚀橡胶管,所以高锰酸钾溶液应盛放在酸式滴定管中,不能盛放在碱式滴定管中,B错误;实验室配制银氨溶液时应该把氨水逐滴滴入硝酸银溶液中,C错误;装置丁中若将ZnSO4溶液替换成CuSO4溶液,仍然可以形成原电池,锌是负极,铜是正极,D错误。故选A。
同课章节目录
