6.3 课题2化学电源燃料电池 练习(含答案) 2024-2025学年高一化学苏教版(2019)必修2
文档属性
| 名称 | 6.3 课题2化学电源燃料电池 练习(含答案) 2024-2025学年高一化学苏教版(2019)必修2 |
|
|
| 格式 | docx | ||
| 文件大小 | 368.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-05-08 00:00:00 | ||
图片预览


文档简介
课题2 化学电源 燃料电池
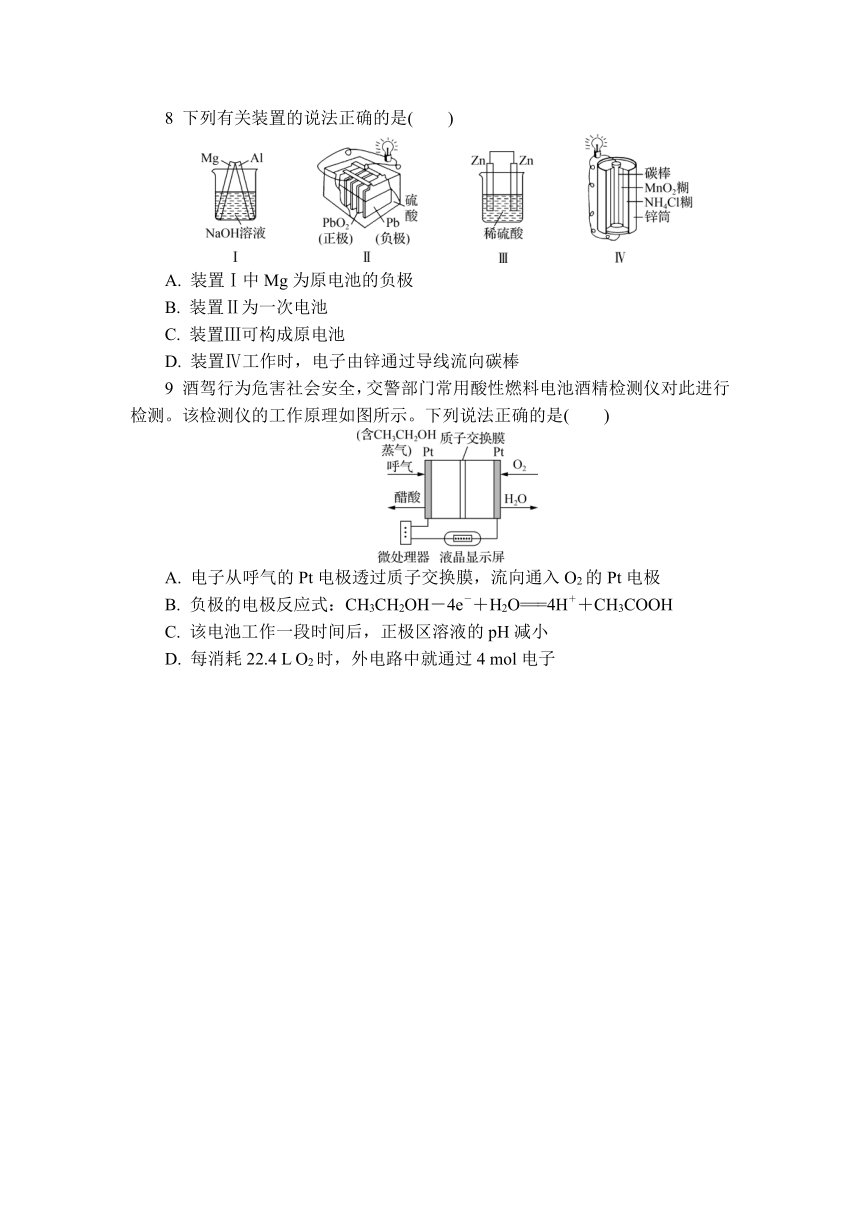
1 下列有关电池的叙述不正确的是( )
A. 水果电池是方便实用的家用电池
B. 铅蓄电池是一种常用的二次电池
C. 氢氧燃料电池是一种高效、无污染的发电装置
D. 锌锰干电池工作一段时间后,锌外壳逐渐变薄
2 下列关于原电池的叙述不正确的是( )
A. 原电池中失去电子的电极为正极
B. 原电池的负极发生氧化反应
C. 原电池是将氧化还原反应产生的化学能转化为电能的一种装置
D. 原电池中,电子由负极经导线流向正极
3 (2023南京协同体七校期中联考)普通水泥在固化过程中其自由水分子减少并形成碱性溶液。根据这一物理、化学特点,科学家发明了电动势法测水泥的初凝时间。此法的原理如图所示,反应的总方程式为2Cu+Ag2O===Cu2O+2Ag。下列有关说法正确的是( )
A. 负极反应式为Ag2O+2e-+H2O===2Ag+2OH-
B. 测量原理示意图中,电子从Ag2O/Ag电极经导线流向Cu电极
C. 电池工作时,OH-向Cu电极移动
D. 电池工作时,OH-浓度增大
4 (2024河北邯郸期末)LiO2电池比能量高,在汽车、航天等领域具有良好的应用前景,电池结构如图所示。下列关于该电池的说法正确的是( )
A. 金属锂为正极,光催化电极为负极
B. 电解质1和电解质2都不能是水溶液
C. 放电时,Li+经离子交换膜由右侧移动到左侧
D. 电池每消耗标准状况下22.4 L O2时,电路中转移4 mol电子
5 (2023扬州邗江区期中)我国科研人员研制出一种LiN2电池,电池反应为6Li+N2===2Li3N,其放电过程为原电池工作原理,电池结构如图所示。下列说法正确的是( )
A. 该装置实现了电能向化学能的转化
B. N2发生还原反应
C. a极反应式为Li+e-===Li+
D. 电池工作时,电子从a电极经导线流向b电极,再从b电极经电解质溶液流向a电极
6 (2024宿迁期末)AlMnO电池原理如图所示,总反应为Al+MnO+2H2O===[Al(OH)4]-+MnO2。下列说法正确的是( )
A. 多孔Ni作负极
B. Al电极反应式为Al-3e-+4OH-===[Al(OH)4]-
C. 电池工作时,K+向负极区移动
D. 正极反应式为MnO+3e-+4H+===MnO2+2H2O
7 (2024盐城期末)负载有Pt和Ag的活性炭,可选择性去除Cl-实现废酸的纯化,其工作原理如图。下列说法正确的是( )
A. Ag作原电池正极
B. 电流由Ag经活性炭流向Pt
C. 每消耗标准状况下11.2 L O2,最多去除2 mol Cl-
D. Pt表面发生的反应:O2+2H2O+4e-===4OH-
8 下列有关装置的说法正确的是( )
A. 装置Ⅰ中Mg为原电池的负极
B. 装置Ⅱ为一次电池
C. 装置Ⅲ可构成原电池
D. 装置Ⅳ工作时,电子由锌通过导线流向碳棒
9 酒驾行为危害社会安全,交警部门常用酸性燃料电池酒精检测仪对此进行检测。该检测仪的工作原理如图所示。下列说法正确的是( )
A. 电子从呼气的Pt电极透过质子交换膜,流向通入O2的Pt电极
B. 负极的电极反应式:CH3CH2OH-4e-+H2O===4H++CH3COOH
C. 该电池工作一段时间后,正极区溶液的pH减小
D. 每消耗22.4 L O2时,外电路中就通过4 mol电子
10 CO2还原为甲醇(CH3OH)是人工合成淀粉的第一步。CO2催化加氢主要反应为CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=-49.4 kJ/mol。
(1) H2O分子用电子式表示为________。反应中每生成0.5 mol甲醇,转移电子的物质的量是________mol。
(2) 一定条件下,该反应过程中的能量变化情况如图所示,其中E2-E1=________kJ/mol。
(3) T1 ℃下,向一容积为3 L的恒容密闭容器中加入一定量的CO2和H2,在催化剂存在时发生反应:
CO2(g)+3H2(g) CH3OH(g)+H2O(g),测得不同时间(t)各物质的物质的量如表所示。
t/min n(CO2)/mol n(H2)/mol n(CH3OH)/mol n(H2O)/mol
0 2.00 6.00 0 0
t1 1.65 a 0.35 0.35
t2 b 3.60 0.80 0.80
t3 b 3.60 0.80 0.80
①0~t1 min内,用H2浓度变化表示该反应的化学反应速率为________mol/(L·min)。
②下列有关上述反应的说法正确的是______(填字母)。
A. CH3OH中的化学键是共价键
B. 消耗3 mol H2(g)的同时生成1 mol H2O(g),此时该反应达到化学平衡状态
C. 0~t1 min内反应放出的热量小于t1~t2 min内放出的热量
(4) 甲醇(CH3OH)燃料电池的电极采用膜电极,该电极由催化剂层和质子交换膜构成,其中质子交换膜能传导H+,同时作为隔膜防止两极的物质相互反应。该电池的工作原理如图所示。
①该电池的负极是________(填“电极a”或“电极b”)。
②工作时,电极b的电极反应式是____________________________。
(5) 以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。
①A为生物燃料电池的________(填“正”或“负”)极。
②正极反应式为______________________________,负极反应式为_________
________________________________________________________。
③放电过程中,H+由________(填“正”或“负”,下同)极区向________极区迁移。
④在电池反应中,每消耗1 mol氧气,理论上能生成标准状况下CO2气体________L。
⑤该电池________(填“能”或“不能”)在高温下工作。
课题2 化学电源 燃料电池
1. A 水果电池产生的电流非常微弱且不能连续长时间放电,不能作为家用电池,A错误。
2. A 原电池中,负极失电子,正极得电子,A错误。
3. C 反应的总方程式为2Cu+Ag2O===Cu2O+2Ag,Cu作负极,发生氧化反应,电极反应式为2Cu-2e-+2OH-===Cu2O+H2O,Ag2O/Ag作正极,发生还原反应,电极反应式为Ag2O+2e-+H2O===2Ag+2OH-,A错误;Cu作负极,Ag2O/Ag作正极,电子由Cu电极经导线流向Ag2O/Ag电极, B错误;电池工作时,阴离子移向负极,则OH-向Cu电极移动,C正确;反应的总方程式为2Cu+Ag2O===Cu2O+2Ag,电池工作时,OH-浓度不变,D错误。
4. B 金属锂为负极,光催化电极为正极,A错误;Li、Li2O2均能与H2O反应,故电解质1和电解质2都不能是水溶液,B正确;放电时,阳离子向正极移动,故阳离子(Li+)经离子交换膜由左侧移动到右侧,C错误;正极反应式为O2+2Li++2e-===Li2O2,电池每消耗标准状况下22.4 L(即1 mol)O2时,电路中转移2 mol电子,D错误。
5. B 该装置放电过程为原电池工作原理,则该装置实现了化学能向电能的转化,A错误;电池反应为6Li+N2===2Li3N,氮的化合价降低,则N2发生还原反应,B正确;a极为负极,其电极反应式为Li-e-===Li+,C错误;电池工作时,电子从a电极经导线流向b电极,电子只在导线中移动,不能在溶液中移动,D错误。
6. B 由总反应知,Al元素的化合价升高,失去电子,Al作负极,多孔Ni作正极,A错误;电池工作时,阳离子向正极区移动,故K+向正极区移动,C错误;正极区溶液显碱性,应该用OH-平衡电荷,正极反应式为MnO+3e-+2H2O===MnO2+4OH-,D错误。
7. C O2在Pt表面得电子,则Ag发生失电子的反应,Ag作原电池的负极,A错误;电子由Ag经活性炭流向Pt,则电流由Pt经活性炭流向Ag,B错误;每消耗标准状况下11.2 L(即0.5 mol)O2,转移2 mol电子,需要消耗2 mol Ag,则生成2 mol Ag+,最多可去除2 mol Cl-,C正确;由题干信息“实现废酸的纯化”知,溶液显酸性,故产物不能是OH-,D错误。
8. D Al能够与NaOH溶液反应,而Mg不能反应,所以装置Ⅰ中Mg为原电池的正极,Al为原电池的负极,A错误。装置Ⅱ为铅蓄电池,可充电也可放电,为二次电池,B错误。装置Ⅲ中2个电极都是Zn,没有活动性不同的电极,因此不可构成原电池,C错误。由于电极活动性Zn比C强,所以Zn为负极,碳棒为正极,故装置Ⅳ工作时,电子由负极锌通过导线流向正极碳棒,D正确。
9. B 电子从呼气的Pt电极经导线流向通入氧气的Pt电极,不能通过质子交换膜移动,A错误;呼气通入的Pt电极为原电池的负极,呼出的乙醇在负极失去电子发生氧化反应生成乙酸,B正确;通入氧气的Pt电极为正极,酸性条件下,正极反应式为O2+4e-+4H+===2H2O,放电时消耗氢离子,则正极区溶液的pH增大,C错误;没有说明是否为标准状况,无法计算消耗22.4 L氧气的物质的量和外电路中电子转移的物质的量,D错误。
10. (1) 3
(2) 49.4
(3) ① ②AC
(4) ①电极a ②O2+4e-+4H+===2H2O
(5) ①正 ②O2+4H++4e-===2H2O
C6H12O6+6H2O-24e-===6CO2↑+24H+
③负 正 ④22.4 ⑤不能
1 下列有关电池的叙述不正确的是( )
A. 水果电池是方便实用的家用电池
B. 铅蓄电池是一种常用的二次电池
C. 氢氧燃料电池是一种高效、无污染的发电装置
D. 锌锰干电池工作一段时间后,锌外壳逐渐变薄
2 下列关于原电池的叙述不正确的是( )
A. 原电池中失去电子的电极为正极
B. 原电池的负极发生氧化反应
C. 原电池是将氧化还原反应产生的化学能转化为电能的一种装置
D. 原电池中,电子由负极经导线流向正极
3 (2023南京协同体七校期中联考)普通水泥在固化过程中其自由水分子减少并形成碱性溶液。根据这一物理、化学特点,科学家发明了电动势法测水泥的初凝时间。此法的原理如图所示,反应的总方程式为2Cu+Ag2O===Cu2O+2Ag。下列有关说法正确的是( )
A. 负极反应式为Ag2O+2e-+H2O===2Ag+2OH-
B. 测量原理示意图中,电子从Ag2O/Ag电极经导线流向Cu电极
C. 电池工作时,OH-向Cu电极移动
D. 电池工作时,OH-浓度增大
4 (2024河北邯郸期末)LiO2电池比能量高,在汽车、航天等领域具有良好的应用前景,电池结构如图所示。下列关于该电池的说法正确的是( )
A. 金属锂为正极,光催化电极为负极
B. 电解质1和电解质2都不能是水溶液
C. 放电时,Li+经离子交换膜由右侧移动到左侧
D. 电池每消耗标准状况下22.4 L O2时,电路中转移4 mol电子
5 (2023扬州邗江区期中)我国科研人员研制出一种LiN2电池,电池反应为6Li+N2===2Li3N,其放电过程为原电池工作原理,电池结构如图所示。下列说法正确的是( )
A. 该装置实现了电能向化学能的转化
B. N2发生还原反应
C. a极反应式为Li+e-===Li+
D. 电池工作时,电子从a电极经导线流向b电极,再从b电极经电解质溶液流向a电极
6 (2024宿迁期末)AlMnO电池原理如图所示,总反应为Al+MnO+2H2O===[Al(OH)4]-+MnO2。下列说法正确的是( )
A. 多孔Ni作负极
B. Al电极反应式为Al-3e-+4OH-===[Al(OH)4]-
C. 电池工作时,K+向负极区移动
D. 正极反应式为MnO+3e-+4H+===MnO2+2H2O
7 (2024盐城期末)负载有Pt和Ag的活性炭,可选择性去除Cl-实现废酸的纯化,其工作原理如图。下列说法正确的是( )
A. Ag作原电池正极
B. 电流由Ag经活性炭流向Pt
C. 每消耗标准状况下11.2 L O2,最多去除2 mol Cl-
D. Pt表面发生的反应:O2+2H2O+4e-===4OH-
8 下列有关装置的说法正确的是( )
A. 装置Ⅰ中Mg为原电池的负极
B. 装置Ⅱ为一次电池
C. 装置Ⅲ可构成原电池
D. 装置Ⅳ工作时,电子由锌通过导线流向碳棒
9 酒驾行为危害社会安全,交警部门常用酸性燃料电池酒精检测仪对此进行检测。该检测仪的工作原理如图所示。下列说法正确的是( )
A. 电子从呼气的Pt电极透过质子交换膜,流向通入O2的Pt电极
B. 负极的电极反应式:CH3CH2OH-4e-+H2O===4H++CH3COOH
C. 该电池工作一段时间后,正极区溶液的pH减小
D. 每消耗22.4 L O2时,外电路中就通过4 mol电子
10 CO2还原为甲醇(CH3OH)是人工合成淀粉的第一步。CO2催化加氢主要反应为CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH=-49.4 kJ/mol。
(1) H2O分子用电子式表示为________。反应中每生成0.5 mol甲醇,转移电子的物质的量是________mol。
(2) 一定条件下,该反应过程中的能量变化情况如图所示,其中E2-E1=________kJ/mol。
(3) T1 ℃下,向一容积为3 L的恒容密闭容器中加入一定量的CO2和H2,在催化剂存在时发生反应:
CO2(g)+3H2(g) CH3OH(g)+H2O(g),测得不同时间(t)各物质的物质的量如表所示。
t/min n(CO2)/mol n(H2)/mol n(CH3OH)/mol n(H2O)/mol
0 2.00 6.00 0 0
t1 1.65 a 0.35 0.35
t2 b 3.60 0.80 0.80
t3 b 3.60 0.80 0.80
①0~t1 min内,用H2浓度变化表示该反应的化学反应速率为________mol/(L·min)。
②下列有关上述反应的说法正确的是______(填字母)。
A. CH3OH中的化学键是共价键
B. 消耗3 mol H2(g)的同时生成1 mol H2O(g),此时该反应达到化学平衡状态
C. 0~t1 min内反应放出的热量小于t1~t2 min内放出的热量
(4) 甲醇(CH3OH)燃料电池的电极采用膜电极,该电极由催化剂层和质子交换膜构成,其中质子交换膜能传导H+,同时作为隔膜防止两极的物质相互反应。该电池的工作原理如图所示。
①该电池的负极是________(填“电极a”或“电极b”)。
②工作时,电极b的电极反应式是____________________________。
(5) 以葡萄糖为燃料的微生物燃料电池结构示意图如图所示。
①A为生物燃料电池的________(填“正”或“负”)极。
②正极反应式为______________________________,负极反应式为_________
________________________________________________________。
③放电过程中,H+由________(填“正”或“负”,下同)极区向________极区迁移。
④在电池反应中,每消耗1 mol氧气,理论上能生成标准状况下CO2气体________L。
⑤该电池________(填“能”或“不能”)在高温下工作。
课题2 化学电源 燃料电池
1. A 水果电池产生的电流非常微弱且不能连续长时间放电,不能作为家用电池,A错误。
2. A 原电池中,负极失电子,正极得电子,A错误。
3. C 反应的总方程式为2Cu+Ag2O===Cu2O+2Ag,Cu作负极,发生氧化反应,电极反应式为2Cu-2e-+2OH-===Cu2O+H2O,Ag2O/Ag作正极,发生还原反应,电极反应式为Ag2O+2e-+H2O===2Ag+2OH-,A错误;Cu作负极,Ag2O/Ag作正极,电子由Cu电极经导线流向Ag2O/Ag电极, B错误;电池工作时,阴离子移向负极,则OH-向Cu电极移动,C正确;反应的总方程式为2Cu+Ag2O===Cu2O+2Ag,电池工作时,OH-浓度不变,D错误。
4. B 金属锂为负极,光催化电极为正极,A错误;Li、Li2O2均能与H2O反应,故电解质1和电解质2都不能是水溶液,B正确;放电时,阳离子向正极移动,故阳离子(Li+)经离子交换膜由左侧移动到右侧,C错误;正极反应式为O2+2Li++2e-===Li2O2,电池每消耗标准状况下22.4 L(即1 mol)O2时,电路中转移2 mol电子,D错误。
5. B 该装置放电过程为原电池工作原理,则该装置实现了化学能向电能的转化,A错误;电池反应为6Li+N2===2Li3N,氮的化合价降低,则N2发生还原反应,B正确;a极为负极,其电极反应式为Li-e-===Li+,C错误;电池工作时,电子从a电极经导线流向b电极,电子只在导线中移动,不能在溶液中移动,D错误。
6. B 由总反应知,Al元素的化合价升高,失去电子,Al作负极,多孔Ni作正极,A错误;电池工作时,阳离子向正极区移动,故K+向正极区移动,C错误;正极区溶液显碱性,应该用OH-平衡电荷,正极反应式为MnO+3e-+2H2O===MnO2+4OH-,D错误。
7. C O2在Pt表面得电子,则Ag发生失电子的反应,Ag作原电池的负极,A错误;电子由Ag经活性炭流向Pt,则电流由Pt经活性炭流向Ag,B错误;每消耗标准状况下11.2 L(即0.5 mol)O2,转移2 mol电子,需要消耗2 mol Ag,则生成2 mol Ag+,最多可去除2 mol Cl-,C正确;由题干信息“实现废酸的纯化”知,溶液显酸性,故产物不能是OH-,D错误。
8. D Al能够与NaOH溶液反应,而Mg不能反应,所以装置Ⅰ中Mg为原电池的正极,Al为原电池的负极,A错误。装置Ⅱ为铅蓄电池,可充电也可放电,为二次电池,B错误。装置Ⅲ中2个电极都是Zn,没有活动性不同的电极,因此不可构成原电池,C错误。由于电极活动性Zn比C强,所以Zn为负极,碳棒为正极,故装置Ⅳ工作时,电子由负极锌通过导线流向正极碳棒,D正确。
9. B 电子从呼气的Pt电极经导线流向通入氧气的Pt电极,不能通过质子交换膜移动,A错误;呼气通入的Pt电极为原电池的负极,呼出的乙醇在负极失去电子发生氧化反应生成乙酸,B正确;通入氧气的Pt电极为正极,酸性条件下,正极反应式为O2+4e-+4H+===2H2O,放电时消耗氢离子,则正极区溶液的pH增大,C错误;没有说明是否为标准状况,无法计算消耗22.4 L氧气的物质的量和外电路中电子转移的物质的量,D错误。
10. (1) 3
(2) 49.4
(3) ① ②AC
(4) ①电极a ②O2+4e-+4H+===2H2O
(5) ①正 ②O2+4H++4e-===2H2O
C6H12O6+6H2O-24e-===6CO2↑+24H+
③负 正 ④22.4 ⑤不能
