7.1 氮的固定 练习(含答案) 2024-2025学年高一化学苏教版(2019)必修2
文档属性
| 名称 | 7.1 氮的固定 练习(含答案) 2024-2025学年高一化学苏教版(2019)必修2 |

|
|
| 格式 | docx | ||
| 文件大小 | 706.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-05-08 00:00:00 | ||
图片预览


文档简介
第一单元 氮的固定
1 (2023宿迁泗阳实验高级中学质量调研)下图中能实现人工固氮的是( )
A. 闪电 B. 合成氨车间
C. 豆科植物根瘤菌 D. 绿色植物光合作用
2 (2024常州联盟校月考)下列关于NO和NO2的说法正确的是( )
A. NO2能与水反应生成硝酸,故NO2是酸性氧化物
B. 除去NO2中混有的NO,可将混合气通入水中
C. NO与NO2互为同素异形体
D. 3NO2+H2O===2HNO3+NO中氧化剂与还原剂物质的量之比为1∶2
3 (2023淮安马坝中学期中)下列有关氮气的说法错误的是( )
A. 镁在空气中燃烧除生成氧化镁外还生成氮化镁
B. 雷电时发生的固氮属于高能固氮
C. 氮气既可作氧化剂又可作还原剂
D. 1 mol N2可与3 mol H2完全反应生成2 mol NH3
4 (2023南通通州调研一)下列关于氮氧化物的形成、吸收等说法正确的是( )
A. 汽车尾气中含氮氧化物,主要来源于烃类燃料
B. 用石灰乳吸收NO和NO2,增加气体流速可提高氮氧化物的吸收率
C. 收集NO2气体时采用排水法,可提高NO2气体的纯度
D. 用尿素[CO(NH2)2]可将NO2转化为N2,是利用了CO(NH2)2的还原性
5 (2023盐城阜宁期中)科学家研究出了一种在酸性介质中利用电解原理进行电化学固氮的方法,反应机理如图所示,氨气在催化剂电极表面产生。下列说法正确的是( )
A. 该过程中存在H+发生氧化反应转化为H原子
B. 在该过程中,氮气分子中N≡N断裂产生N原子
C. 在催化剂作用下,N2与H原子反应可能生成N2H4和NH3两种产物
D. 与传统工业合成氨法比较,电化学固氮法会消耗大量电能,没有研究价值
6 (2024苏州期末)常温下,用H2处理烟气中NO的转化过程如图所示。下列说法正确的是( )
A. 步骤Ⅰ反应的离子方程式为Ce4++H2===Ce3++2H+
B. 该转化过程中NO被氧化
C. 步骤Ⅱ中每消耗1 mol NO,转移2×6.02×1023电子
D. 反应过程中,混合溶液内Ce3+和Ce4+的总数减少
7 (2023扬州中学月考)从化学的视角深刻理解氮循环,合理使用含氮化合物,科学处理大气和水圈中的氮元素,保障地球生态安全,是化学学科的重要研究内容和责任。煤燃烧时,烟气中NO含量随温度和氧气含量的变化如图所示。下列说法不正确的是( )
A. 燃煤过程中发生了氮的固定
B. 燃煤温度越高NOx污染越重
C. 含氧量越高越容易生成NO
D. 煤燃烧不影响自然界氮循环
8 (2024扬州期末)氮氧化物(NO、NO2)是当前环境保护研究的热点课题。
(1) 氮氧化物大量排放对环境造成的影响有__________________________(写出一点)。
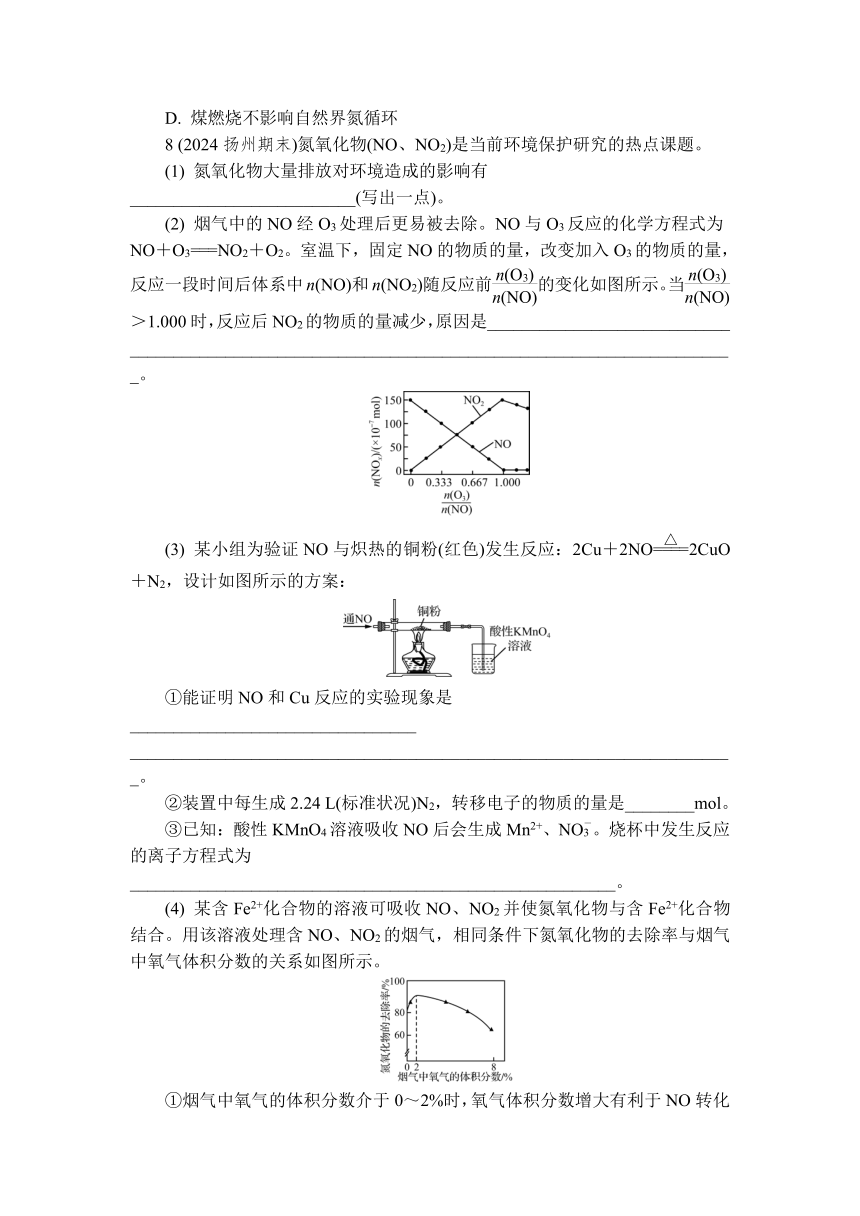
(2) 烟气中的NO经O3处理后更易被去除。NO与O3反应的化学方程式为NO+O3===NO2+O2。室温下,固定NO的物质的量,改变加入O3的物质的量,反应一段时间后体系中n(NO)和n(NO2)随反应前的变化如图所示。当>1.000时,反应后NO2的物质的量减少,原因是____________________________
______________________________________________________________________。
(3) 某小组为验证NO与炽热的铜粉(红色)发生反应:2Cu+2NO2CuO+N2,设计如图所示的方案:
①能证明NO和Cu反应的实验现象是_________________________________
______________________________________________________________________。
②装置中每生成2.24 L(标准状况)N2,转移电子的物质的量是________mol。
③已知:酸性KMnO4溶液吸收NO后会生成Mn2+、NO。烧杯中发生反应的离子方程式为________________________________________________________。
(4) 某含Fe2+化合物的溶液可吸收NO、NO2并使氮氧化物与含Fe2+化合物结合。用该溶液处理含NO、NO2的烟气,相同条件下氮氧化物的去除率与烟气中氧气体积分数的关系如图所示。
①烟气中氧气的体积分数介于0~2%时,氧气体积分数增大有利于NO转化为NO2,该反应的化学方程式为__________________________。与NO相比,NO2更易被溶液吸收去除,原因是___________________________________________。
②烟气中氧气的体积分数介于2%~8%时,随着O2体积分数的上升,氮氧化物去除率减小,原因是___________________________________________________
______________________________________________________________________。
9 (2023苏州黄埭中学期中节选)工业或机动车尾气中的NOx会造成环境问题,可用多种方法脱除。
(1) 碱液吸收:石灰乳可吸收硝酸工业的尾气(含NO、NO2),获得副产品Ca(NO2)2。
①等物质的量NO与NO2被Ca(OH)2吸收,反应的化学方程式为___________
_____________________________________________________________。
②采用气-液逆流接触吸收(尾气从塔底进入,石灰乳从塔顶喷淋),其目的是____________________________________________________________________。
③该工艺需控制NO和NO2的物质的量之比接近1∶1,若n(NO)∶n(NO2)
<1∶1,则会导致____________________;若n(NO)∶n(NO2)>1∶1,则会导致____________________________________。
④生产中需保持弱碱性,在酸性溶液中Ca(NO2)2会发生分解,产物之一是NO,该反应的离子方程式为________________________________。
(2) 还原法:尿素水溶液热解产生的氨气发生催化反应可去除尾气中的NOx。NH3与NO2转化生成 N2的反应中,当生成1 mol N2时,转移的电子数为__________mol。
第一单元 氮的固定
1. B 闪电过程中引发氮气和氧气生成NO,属于自然固氮,A错误;合成氨过程是将氮气和氢气在高温、高压、催化剂条件下转化为氨气,属于人工固氮,B正确;豆科植物根瘤菌能将氮气转化为硝酸根离子等化合态氮,属于生物固氮,C错误;绿色植物光合作用不能实现氮的固定,D错误。
2. D NO2能与水反应生成硝酸和NO,有NO生成,NO2不是酸性氧化物,A错误;NO2能与水反应生成硝酸和NO,NO和水不反应,混合气通入水中不能除去NO2中混有的NO,B错误;同素异形体是同种元素组成的不同单质,C错误;3NO2+H2O===2HNO3+NO中降价的N原子与升价的N原子的个数比为1∶2,所以氧化剂与还原剂物质的量之比为1∶2,D正确。
3. D 镁既能和氧气反应生成氧化镁,又能和氮气反应生成氮化镁,所以镁在空气中燃烧除生成氧化镁外还生成氮化镁,A正确;N2和O2在放电条件下可以反应生成NO,属于高能固氮,B正确;氮气中N元素的化合价为0,既可以升高为+2、+3、+4、+5,又可以降低为-3,所以氮气既可作氧化剂又可作还原剂,C正确;N2+3H22NH3是可逆反应,1 mol N2与3 mol H2不能完全反应,生成的NH3的物质的量小于2 mol,D错误。
4. D 汽车尾气中含氮氧化物,主要由空气中的氮气和氧气在气缸中高温条件下化合生成,A错误;用石灰乳吸收NO和NO2生成亚硝酸钙,减慢气体流速可增加氮氧化物与石灰乳的接触时间,提高氮氧化物的吸收率,B错误;NO2能和水反应生成硝酸和NO,因此不能采用排水法收集NO2,C错误;用CO(NH2)2将NO2转化为N2,该过程中NO2为氧化剂,则CO(NH2)2为还原剂,D正确。
5. C H+转化为H原子,H元素的化合价降低,发生还原反应,A错误;N2转化为NH3时,不存在单独的N原子,B错误;在反应过程存在N2H4和NH3,C正确;与传统工业合成氨法比较,电化学固氮法不需要高温高压,条件比较温和,具有研究价值,D错误。
6. C 步骤Ⅰ反应的离子方程式为2Ce4++H2===2Ce3++2H+,A错误;总反应为2H2+2NON2+2H2O,转移4e-,NO被还原,每消耗1 mol NO,转移 2 mol e-,B错误,C正确;Ce3+是催化剂,Ce4+是中间产物,总数恒定,D错误。
7. D 燃煤过程中发生了N2到NO的反应,为氮的固定,A正确;由图可知,温度越高,烟气中NO浓度越高,污染越重,B正确;由图可知,含氧量越高,烟气中NO浓度越高,越容易生成NO,C正确;煤燃烧时使N2转化为NO,污染环境,影响了氮循环,D错误。
8. (1) (硝酸型)酸雨;光化学烟雾;破坏臭氧层等(答案合理即可)
(2) O3将NO2氧化为更高价态氮氧化物
(3) ①玻璃管中粉末由红色变为黑色 ②0.4
③3MnO+5NO+4H+===3Mn2++2H2O+5NO
(4) ①2NO+O2===2NO2 NO2在溶液中的溶解度更大 ②O2将Fe2+氧化
9. (1) ①NO+NO2+Ca(OH)2===Ca(NO2)2+H2O
②有利于尾气中NO、NO2与石灰乳的充分接触,从而提高吸收效率
③产品中含有Ca(NO3)2 NO会随尾气排放污染空气
④3NO+2H+===NO+2NO↑+H2O
(2)
1 (2023宿迁泗阳实验高级中学质量调研)下图中能实现人工固氮的是( )
A. 闪电 B. 合成氨车间
C. 豆科植物根瘤菌 D. 绿色植物光合作用
2 (2024常州联盟校月考)下列关于NO和NO2的说法正确的是( )
A. NO2能与水反应生成硝酸,故NO2是酸性氧化物
B. 除去NO2中混有的NO,可将混合气通入水中
C. NO与NO2互为同素异形体
D. 3NO2+H2O===2HNO3+NO中氧化剂与还原剂物质的量之比为1∶2
3 (2023淮安马坝中学期中)下列有关氮气的说法错误的是( )
A. 镁在空气中燃烧除生成氧化镁外还生成氮化镁
B. 雷电时发生的固氮属于高能固氮
C. 氮气既可作氧化剂又可作还原剂
D. 1 mol N2可与3 mol H2完全反应生成2 mol NH3
4 (2023南通通州调研一)下列关于氮氧化物的形成、吸收等说法正确的是( )
A. 汽车尾气中含氮氧化物,主要来源于烃类燃料
B. 用石灰乳吸收NO和NO2,增加气体流速可提高氮氧化物的吸收率
C. 收集NO2气体时采用排水法,可提高NO2气体的纯度
D. 用尿素[CO(NH2)2]可将NO2转化为N2,是利用了CO(NH2)2的还原性
5 (2023盐城阜宁期中)科学家研究出了一种在酸性介质中利用电解原理进行电化学固氮的方法,反应机理如图所示,氨气在催化剂电极表面产生。下列说法正确的是( )
A. 该过程中存在H+发生氧化反应转化为H原子
B. 在该过程中,氮气分子中N≡N断裂产生N原子
C. 在催化剂作用下,N2与H原子反应可能生成N2H4和NH3两种产物
D. 与传统工业合成氨法比较,电化学固氮法会消耗大量电能,没有研究价值
6 (2024苏州期末)常温下,用H2处理烟气中NO的转化过程如图所示。下列说法正确的是( )
A. 步骤Ⅰ反应的离子方程式为Ce4++H2===Ce3++2H+
B. 该转化过程中NO被氧化
C. 步骤Ⅱ中每消耗1 mol NO,转移2×6.02×1023电子
D. 反应过程中,混合溶液内Ce3+和Ce4+的总数减少
7 (2023扬州中学月考)从化学的视角深刻理解氮循环,合理使用含氮化合物,科学处理大气和水圈中的氮元素,保障地球生态安全,是化学学科的重要研究内容和责任。煤燃烧时,烟气中NO含量随温度和氧气含量的变化如图所示。下列说法不正确的是( )
A. 燃煤过程中发生了氮的固定
B. 燃煤温度越高NOx污染越重
C. 含氧量越高越容易生成NO
D. 煤燃烧不影响自然界氮循环
8 (2024扬州期末)氮氧化物(NO、NO2)是当前环境保护研究的热点课题。
(1) 氮氧化物大量排放对环境造成的影响有__________________________(写出一点)。
(2) 烟气中的NO经O3处理后更易被去除。NO与O3反应的化学方程式为NO+O3===NO2+O2。室温下,固定NO的物质的量,改变加入O3的物质的量,反应一段时间后体系中n(NO)和n(NO2)随反应前的变化如图所示。当>1.000时,反应后NO2的物质的量减少,原因是____________________________
______________________________________________________________________。
(3) 某小组为验证NO与炽热的铜粉(红色)发生反应:2Cu+2NO2CuO+N2,设计如图所示的方案:
①能证明NO和Cu反应的实验现象是_________________________________
______________________________________________________________________。
②装置中每生成2.24 L(标准状况)N2,转移电子的物质的量是________mol。
③已知:酸性KMnO4溶液吸收NO后会生成Mn2+、NO。烧杯中发生反应的离子方程式为________________________________________________________。
(4) 某含Fe2+化合物的溶液可吸收NO、NO2并使氮氧化物与含Fe2+化合物结合。用该溶液处理含NO、NO2的烟气,相同条件下氮氧化物的去除率与烟气中氧气体积分数的关系如图所示。
①烟气中氧气的体积分数介于0~2%时,氧气体积分数增大有利于NO转化为NO2,该反应的化学方程式为__________________________。与NO相比,NO2更易被溶液吸收去除,原因是___________________________________________。
②烟气中氧气的体积分数介于2%~8%时,随着O2体积分数的上升,氮氧化物去除率减小,原因是___________________________________________________
______________________________________________________________________。
9 (2023苏州黄埭中学期中节选)工业或机动车尾气中的NOx会造成环境问题,可用多种方法脱除。
(1) 碱液吸收:石灰乳可吸收硝酸工业的尾气(含NO、NO2),获得副产品Ca(NO2)2。
①等物质的量NO与NO2被Ca(OH)2吸收,反应的化学方程式为___________
_____________________________________________________________。
②采用气-液逆流接触吸收(尾气从塔底进入,石灰乳从塔顶喷淋),其目的是____________________________________________________________________。
③该工艺需控制NO和NO2的物质的量之比接近1∶1,若n(NO)∶n(NO2)
<1∶1,则会导致____________________;若n(NO)∶n(NO2)>1∶1,则会导致____________________________________。
④生产中需保持弱碱性,在酸性溶液中Ca(NO2)2会发生分解,产物之一是NO,该反应的离子方程式为________________________________。
(2) 还原法:尿素水溶液热解产生的氨气发生催化反应可去除尾气中的NOx。NH3与NO2转化生成 N2的反应中,当生成1 mol N2时,转移的电子数为__________mol。
第一单元 氮的固定
1. B 闪电过程中引发氮气和氧气生成NO,属于自然固氮,A错误;合成氨过程是将氮气和氢气在高温、高压、催化剂条件下转化为氨气,属于人工固氮,B正确;豆科植物根瘤菌能将氮气转化为硝酸根离子等化合态氮,属于生物固氮,C错误;绿色植物光合作用不能实现氮的固定,D错误。
2. D NO2能与水反应生成硝酸和NO,有NO生成,NO2不是酸性氧化物,A错误;NO2能与水反应生成硝酸和NO,NO和水不反应,混合气通入水中不能除去NO2中混有的NO,B错误;同素异形体是同种元素组成的不同单质,C错误;3NO2+H2O===2HNO3+NO中降价的N原子与升价的N原子的个数比为1∶2,所以氧化剂与还原剂物质的量之比为1∶2,D正确。
3. D 镁既能和氧气反应生成氧化镁,又能和氮气反应生成氮化镁,所以镁在空气中燃烧除生成氧化镁外还生成氮化镁,A正确;N2和O2在放电条件下可以反应生成NO,属于高能固氮,B正确;氮气中N元素的化合价为0,既可以升高为+2、+3、+4、+5,又可以降低为-3,所以氮气既可作氧化剂又可作还原剂,C正确;N2+3H22NH3是可逆反应,1 mol N2与3 mol H2不能完全反应,生成的NH3的物质的量小于2 mol,D错误。
4. D 汽车尾气中含氮氧化物,主要由空气中的氮气和氧气在气缸中高温条件下化合生成,A错误;用石灰乳吸收NO和NO2生成亚硝酸钙,减慢气体流速可增加氮氧化物与石灰乳的接触时间,提高氮氧化物的吸收率,B错误;NO2能和水反应生成硝酸和NO,因此不能采用排水法收集NO2,C错误;用CO(NH2)2将NO2转化为N2,该过程中NO2为氧化剂,则CO(NH2)2为还原剂,D正确。
5. C H+转化为H原子,H元素的化合价降低,发生还原反应,A错误;N2转化为NH3时,不存在单独的N原子,B错误;在反应过程存在N2H4和NH3,C正确;与传统工业合成氨法比较,电化学固氮法不需要高温高压,条件比较温和,具有研究价值,D错误。
6. C 步骤Ⅰ反应的离子方程式为2Ce4++H2===2Ce3++2H+,A错误;总反应为2H2+2NON2+2H2O,转移4e-,NO被还原,每消耗1 mol NO,转移 2 mol e-,B错误,C正确;Ce3+是催化剂,Ce4+是中间产物,总数恒定,D错误。
7. D 燃煤过程中发生了N2到NO的反应,为氮的固定,A正确;由图可知,温度越高,烟气中NO浓度越高,污染越重,B正确;由图可知,含氧量越高,烟气中NO浓度越高,越容易生成NO,C正确;煤燃烧时使N2转化为NO,污染环境,影响了氮循环,D错误。
8. (1) (硝酸型)酸雨;光化学烟雾;破坏臭氧层等(答案合理即可)
(2) O3将NO2氧化为更高价态氮氧化物
(3) ①玻璃管中粉末由红色变为黑色 ②0.4
③3MnO+5NO+4H+===3Mn2++2H2O+5NO
(4) ①2NO+O2===2NO2 NO2在溶液中的溶解度更大 ②O2将Fe2+氧化
9. (1) ①NO+NO2+Ca(OH)2===Ca(NO2)2+H2O
②有利于尾气中NO、NO2与石灰乳的充分接触,从而提高吸收效率
③产品中含有Ca(NO3)2 NO会随尾气排放污染空气
④3NO+2H+===NO+2NO↑+H2O
(2)
