广东省珠海市第二中学2025届高三下学期4月考前冲刺试题 化学(PDF版,含答案)
文档属性
| 名称 | 广东省珠海市第二中学2025届高三下学期4月考前冲刺试题 化学(PDF版,含答案) |

|
|
| 格式 | |||
| 文件大小 | 3.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-05-09 15:16:49 | ||
图片预览


文档简介
珠海市第 中学 2025届 三年级考前冲刺卷(化学学科)
满分 1 00分,考试 时 75分钟
注意事项:
1 .答卷前,考 务必 字迹钢笔或签字笔将 的姓名、考 号、考场号和座位号填写在答题
卡上。将条形码横贴在答题卡右上 “ 条形码粘贴处” 。
2.作答选择题时,选出每 题答案后, 2B铅笔把答题卡上对应题 选项的答案信息点涂 ;
如需改动, 橡 擦 净后,再选涂其他答案,答案不能答在试卷上。
3. 选择题必须 字迹钢笔或签字笔作答,答案必须写在答题卡各题 指定区域内相应位置上:
如需改动,先划掉原来的答案,然后再写上新的答案,不准使 铅笔和涂改液。不按以上要求作答
的答案 效。
可能 到的相对原 质量:H-1 C-1 2 N-1 4 O-1 6 Na-23 Al-27 Si-28 Mn-55 Cu-64
、选择题:本题共 1 6 题,共 44分。第 1 ~ 1 0 题,每 题 2分;第 1 1 ~ 1 6 题,每 题 4
分。在每 题给出的四个选项中,只有 项是符合题 要求的。
1 . 世界 明史上,中华 化是世界上唯 从未间断的 明,始终显示出顽强的 命 和 穷的魅 。
下列 物主要由硅酸盐材料制成的是
A.东 汉 铜 奔 B.唐代“ 鎏 舞 C.秦“ 兵 俑” D.仅 49g的 汉“ 直
“ 踏 燕” 衔杯纹银壶” 裾素纱禅 ”
2. 化学和 活、科技、社会发展息息相关。下列说法正确的是
A. 太阳能电池使 的材料是半导体,其主要成分是 SiO2
B. “ 深海 号” 船海 浸泡区镶上铝基是利 了牺牲阳极的 属防腐原理
C. 巴黎奥运会场馆使 的“ 碲化镉” 光伏发电系统将化学能转化为电能
D. “ 三元催化器” 将汽 尾 中 NO 和 CO转化为 N2和 CO2,有利于实现碳
中和
3. 化学处处呈现美。下列说法正确的是
A. 环 烷呈现对称美,分 中六个碳原 连接呈环,呈平 正六边形结构
B. S8分 呈现“ 皇冠” 结构,分 中的硫原 通过共价键结合,S8属于共价晶体
C. 霓虹灯发出五颜六 的光,该过程属于化学变化
D. 锌 在 AgNO3溶液中 成“ 银树” ,反应中锌被氧化
试卷第 1 ,共 1 0
4. 下列有关物质结构和性质的说法,正确的是
A. NO3 与 SO32 的中 原 杂化轨道类型均为 sp2杂化
B. O2和 O3都是单质,在 H2O 中溶解度 乎 样
C. 可燃冰(CH4 8H2O)中甲烷分 与 分 之间没有氢键
D. 分 晶体都存在分 间作 和共价键
5. 勤劳致富,越努 越幸福。下列项 与所述的化学知识没有关联的是
选
产活动 化学原理
项
A 冬季来临时, 灰浆涂抹树 灰浆可以减少植物光合作
B 新会陈 年份越陈, 越浓郁 味的来源之 柠檬烯具有果 味道
C 碳酸氢铵可 作饼 的膨松剂 碳酸氢铵中和酸且受热易分解产 体
D 煮 浆点 制作 腐 胶体聚沉
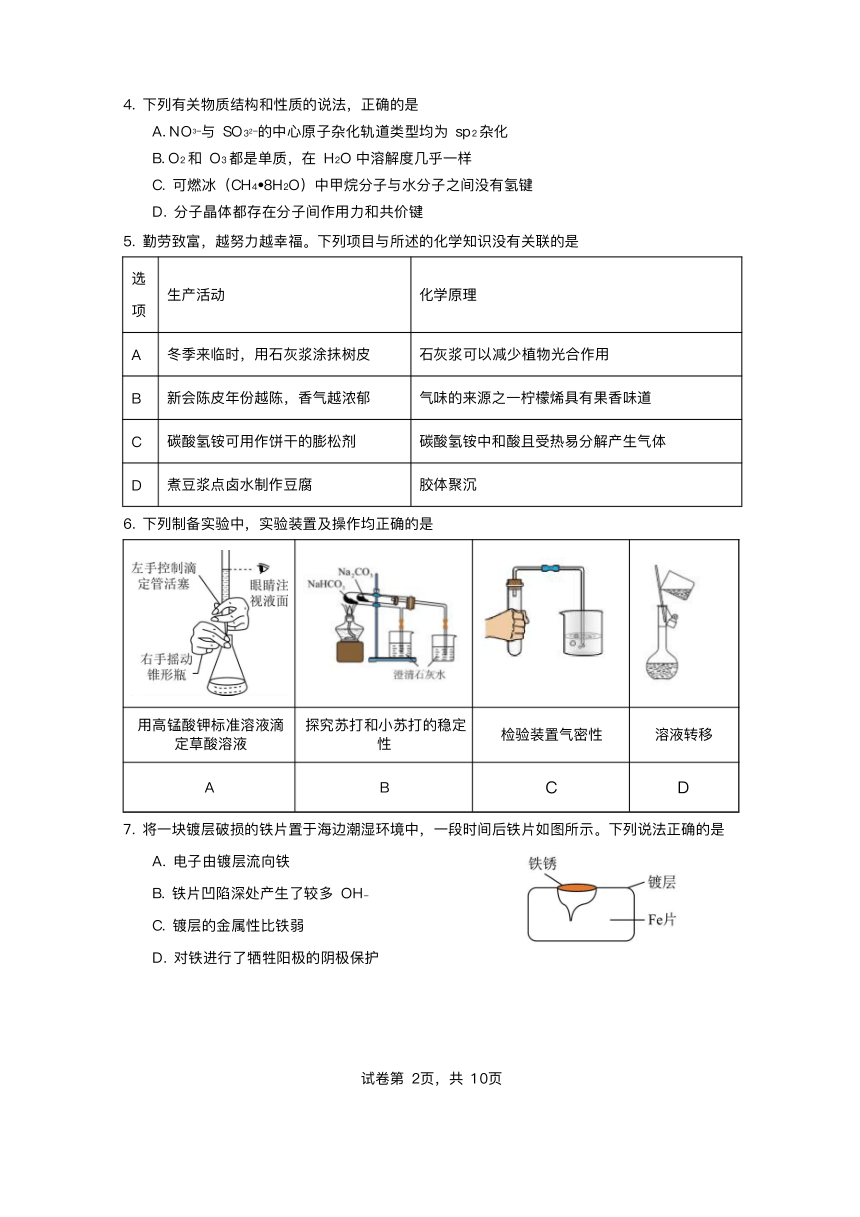
6. 下列制备实验中,实验装置及操作均正确的是
锰酸钾标准溶液滴 探究苏打和 苏打的稳定
检验装置 密性 溶液转移
定草酸溶液 性
A B C D
7. 将 块镀层破损的铁 置于海边潮湿环境中, 段时间后铁 如图所示。下列说法正确的是
A. 电 由镀层流向铁
B. 铁 凹陷深处产 了较多 OH-
C. 镀层的 属性 铁弱
D. 对铁进 了牺牲阳极的阴极保护
试卷第 2 ,共 1 0
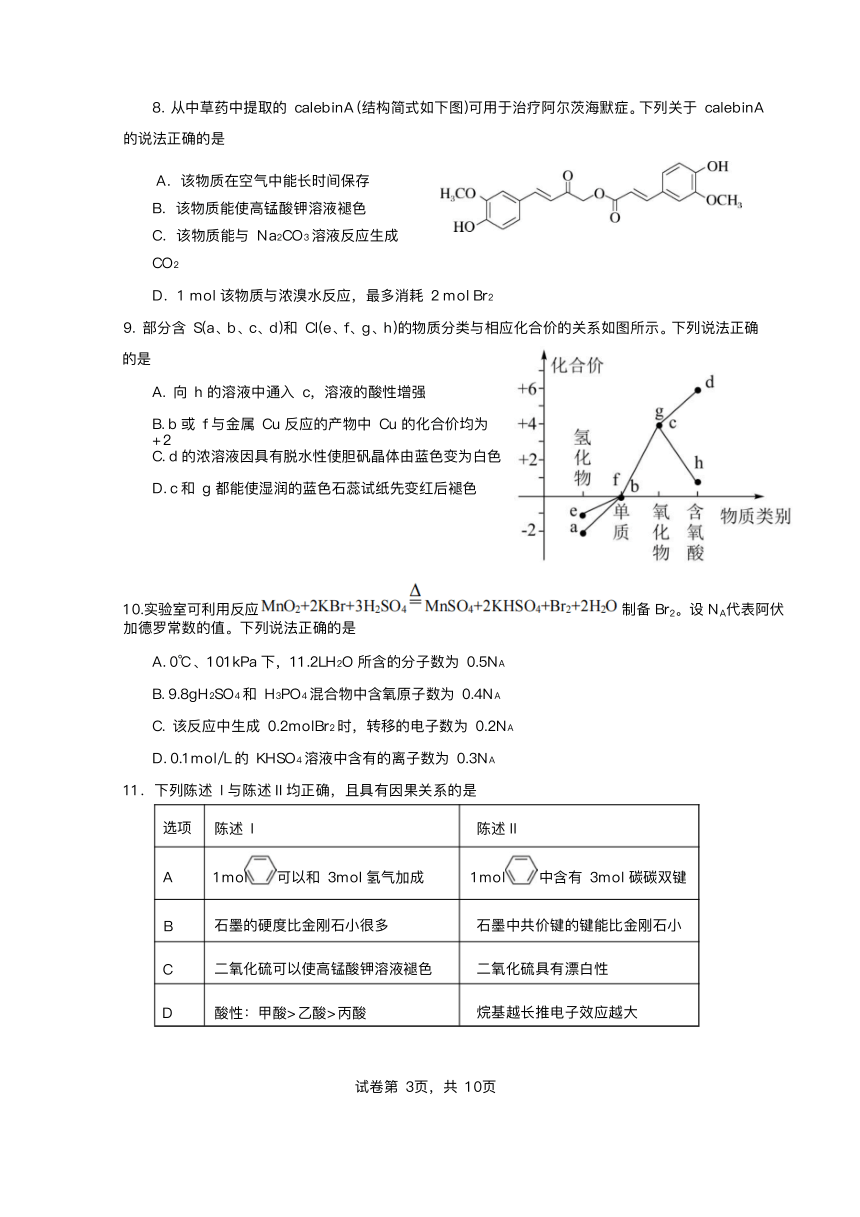
8.从中草药中提取的 calebinA (结构简式如下图)可 于治疗阿尔茨海默症。下列关于 calebinA
的说法正确的是
A.该物质在空 中能 时间保存
B.该物质能使 锰酸钾溶液褪
C.该物质能与 Na2CO3溶液反应 成
CO2
D.1 mol该物质与浓溴 反应,最多消耗 2 mol Br2
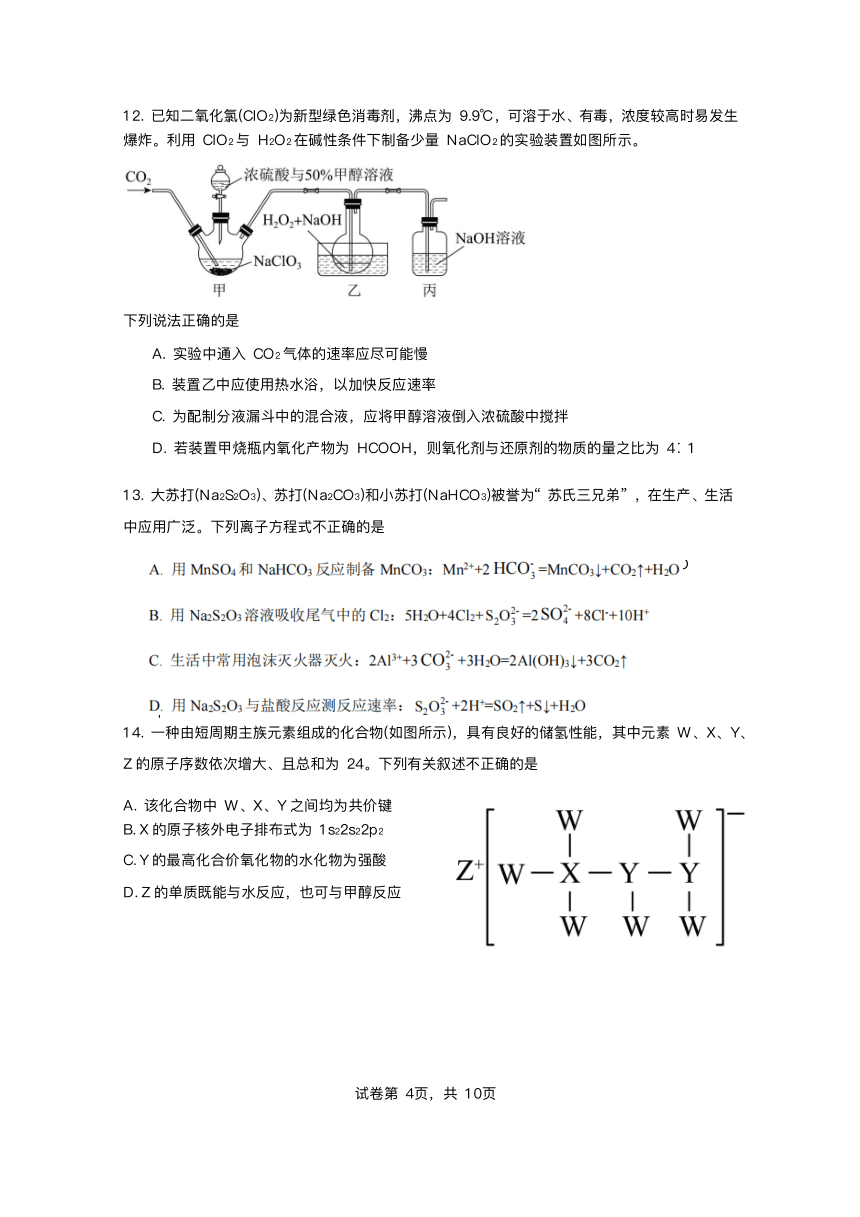
9. 部分含 S(a、b、c、d)和 Cl(e、f、g、h)的物质分类与相应化合价的关系如图所示。下列说法正确
的是
A. 向 h 的溶液中通 c,溶液的酸性增强
B. b或 f与 属 Cu 反应的产物中 Cu 的化合价均为
+2
C. d的浓溶液因具有脱 性使胆矾晶体由蓝 变为
D. c和 g 都能使湿润的蓝 蕊试纸先变红后褪
1 0.实验室可利 反应 制备 Br2。设 NA代表阿伏
加德罗常数的值。下列说法正确的是
A. 0℃、1 01 kPa下,1 1 .2LH2O 所含的分 数为 0.5NA
B. 9.8gH2SO4和 H3PO4混合物中含氧原 数为 0.4NA
C. 该反应中 成 0.2molBr2时,转移的电 数为 0.2NA
D. 0.1mol/L的 KHSO4溶液中含有的离 数为 0.3NA
1 1.下列陈述 I 与陈述Ⅱ均正确,且具有因果关系的是
选项 陈述 I 陈述Ⅱ
A 1mol 可以和 3mol氢 加成 1mol 中含有 3mol碳碳双键
B 墨的硬度 刚 很多 墨中共价键的键能 刚
C 氧化硫可以使 锰酸钾溶液褪 氧化硫具有漂 性
D 酸性:甲酸> 酸>丙酸 烷基越 推电 效应越
试卷第 3 ,共 1 0
1 2. 已知 氧化氯(ClO2)为新型绿 消毒剂,沸点为 9.9℃,可溶于 、有毒,浓度较 时易发
爆炸。利 ClO2与 H2O2在碱性条件下制备少量 NaClO2的实验装置如图所示。
下列说法正确的是
A. 实验中通 CO2 体的速率应尽可能慢
B. 装置 中应使 热 浴,以加快反应速率
C. 为配制分液漏 中的混合液,应将甲醇溶液倒 浓硫酸中搅拌
D. 若装置甲烧瓶内氧化产物为 HCOOH,则氧化剂与还原剂的物质的量之 为 4∶ 1
1 3. 苏打(Na2S2O3)、苏打(Na2CO3)和 苏打(NaHCO3)被誉为“ 苏 三兄弟” ,在 产、 活
中应 泛。下列离 程式不正确的是
-
A. MnSO4和 NaHCO3反应制备 MnCO3: HCO =MnCO3↓+CO2↑+H2O
3
Mn2++2
2- 2-
B. Na2S2O3溶液吸收尾 中的 Cl2: S O3 = SO +8Cl-+1 0H+
5H2O+4Cl2+ 2
2-
C. 活中常 泡沫灭 器灭 : CO3 +3H2O=2Al(OH)3↓+3CO2↑
2Al3++3
2-
D. Na2S2O3与盐酸反应测反应速 S O3 +2H+=SO2↑+S↓+H2O
率:
1 4. 种由短周期主族元素组成的化合物(如图所示),具有良好的储氢性能,其中元素 W、X、Y、
Z的原 序数依次增 、且总和为 24。下列有关叙述不正确的是
A. 该化合物中 W、X、Y之间均为共价键
B. X的原 核外电 排布式为 1 s22s22p2
C. Y的最 化合价氧化物的 化物为强酸
D. Z的单质既能与 反应,也可与甲醇反应
试卷第 4 ,共 1 0
1 5. 甲酸(HCOOH)可在纳 级 Pd 表 分解为活性 H2和 CO2,经下列历程实现 NO 3 的催化
还原。
已知 Fe(Ⅱ)、Fe(Ⅲ)表示 Fe3O4中 价铁和三价铁。下列说法不正确的是
A. 产中将催化剂处理成纳 级颗粒可增 甲酸分解的速率
B.在整个历程中,每 1 molH2可还原 2molNO 3
C.HCOOH 分解时,只有极性共价键发 了断裂
D.反应历程中 成的 H+可调节体系 pH,有增强 NO 3 氧化性的作
1 6. 某新型钠离 次电池(如图) 溶解了 NaPF6的 甲氧基 烷作电解质溶液。放电时嵌
PbSe中的 Na变成 Na+后脱嵌。下列说法错误的是
A. 外电路通过 1mol电 时,理论上两电极质量变化的差值为 23g
B. 充电时,阳极电极反应为: V4 x3 4 3
e
C.放电 段时间后,电解质溶液中的 Na+浓度基本保持不
变
D.D. 电解质溶液不能 NaPF6的 溶液替换
试卷第 5 ,共 1 0
、 选择题:本题共 4 题,共 56分。
1 7. 苯酚能与 Fe3+形成[Fe(C6H5O)6]3-的紫 配合物,该过程属于可逆反应。某 组同学探究铁
离 与苯酚的反应。
(1)配制1 00mL0.1mol /L苯酚溶液,需要 到的玻璃仪器有:烧杯、玻璃棒、胶头滴管和_______。
(2)探究铁盐种类和 pH 对苯酚与 Fe3+显 反应的影响。查阅资
料:i.Na+对苯酚与 Fe3+的显 反应 影响;
ii. 组同学得出猜想 H+对 Fe3+与苯酚的显 反应有抑制作 ,从化学平衡 度解释其原因
___________________________________________________________________________________。iii.
[Fe(C6H5O)6]3-对特定波 光的吸收程度( 吸光度 A 表示)与[Fe(C6H5O)6]3-浓度在 定范围内成
正 。
提出猜想:猜想 1:Cl-对苯酚与 Fe3+的显 反应有影响
2-
猜想 SO 对苯酚与 Fe3+的显 反应有影响
4
2:
进 实验:常温下, 盐酸调节 pH,配制得到 pH 分别为 a和 b的 0.1mol/LFeCl3溶液(a>b);
硫酸调节 pH,配制得到 pH 分别为 a和 b 的 0.05mol/LFe2(SO4)3溶液。取 4 试管各加
5ml 0.1 mol/L苯酚溶液,按实验 1 ~ 4分别再加 0.1mL含 Fe3+的试剂,显 1 0min 后 紫
外-可 分光光度计测定该溶液的吸光度(本实验条件下,pH 改变对 Fe3+ 解程度的影响可忽略)。
含 Fe3+的试剂
序 吸光
0.1mol/LFeCl3 0.05mol/LFe2(SO4)3
号 度
溶液 溶液
1 pH=a / A1
2 pH=b / A2
3 / pH=a A3
4 / pH=b A4
结果讨论:实验结果为 A2 A3 A4
A1
①根据实验结果, 组同学认为此结果不 以证明猜想“ H+对 Fe3+与苯酚的显 反应有抑制作 ”
成 的理由是_______________________________________________________________________。
试卷第 6 ,共 1 0
②为进 步验证猜想, 组同学设计了实验 5和 6,补充下表中试剂 M 为_______________。
含 Fe 的试剂
序 再加 的 吸光
0.1mol /LFeCl 溶
号 0.05mol/LF S3 2 4 溶3 试剂 度
e O
液 液
5 / pH =a NaCl固体 A5
6 pH =a / 试剂 M A6
2-
③根据实验 1 ~ 6的结果, 组同学得出猜想 1 不成 ,猜想 2成 , SO 对苯酚与 Fe3+的显
且
反应起抑制作 ,得出此结论的实验依据是:A3 A A1 A6(填“ >”、“ <”或“ =”。)
(3)通过以上实验结论分析:与苯酚相 ,对羟基苯甲酸与 FeCl3溶液发 显 反应_______。 (填
“ 更容易” 或“ 更难” )
(4)实验室中常 某些配合物的性质进 物质的检验,请举 例 并说明现象_______。
1 8. 业上利 钨矿(其主要成分是 FeWO4、MnWO4,还含有少量 SiO2和 Al2O3)制备钨的
艺流程如下图所示:
已知:①上述流程中,钨的化合价只在最后 步发 改变;②常温下钨酸难溶于 。回答下列问题:
(1)已知元素钨与铬同族,钨在元素周期表中的位置是第六周期第______族,其位于元素周期表
________区。
(2)提 钨矿“ 焙烧” 效率的措施有__________(任写 条),FeWO4在“ 焙烧” 过程中发 反
应的化学 程式为__________________________________________________。
(3)“ 滤渣” 的主要成分是______(填化学式)。
试卷第 7 ,共 1 0
(4)钨酸钙(CaWO4)和氢氧化钙都是微溶电解质。某温度下 Ca(OH)2和 CaWO4的饱和溶液中,
pc(Ca2+)与 pc(阴离 )的关系如图所示,已知:pc(离 )=-lgc(离 )。该温度下将 Na2WO4溶液
加 灰乳中得到 量钨酸钙,发 反应的离 程式为__________________________________,该反
应的平衡常数 K=_______________。
(5)合 具有 属单质更优越的性能,Cu-Mn-Al合 为磁性形状记忆合 材料之 ,其晶胞
结构如图所示(已知:Mn 原 和 Al原 位于 Cu 原 所构成的 个 正 体的体 )。
①若 A 原 的坐标参数为(0,0,0),则 B原 的坐标参数为_______________。
②已知该合 晶体的密度为 pg·cm-3,则最近的两个 Al原 间的距离为____________________pm(列
出计算式,阿伏加德罗常数的值 NA表示)。
1 9. 酸性 CuCl2溶液主要组成为 HCl与 CuCl2 (HCl与 CuCl2会络合为 H2CuCl4),其具有溶铜速率
快、稳定、易控制及易再 等优点,常应 于印刷线路板(PCB)的刻蚀。刻蚀原理为 Cu(s)+
H2CuCl4(aq)→H2CuCl3(aq)+ CuCl(s),CuCl(s)+2HCl(aq)→H2CuCl3(aq)
(1)CuCl中基态亚铜离 的价层电 轨道表示式为_______________________。
2-
(2)CuCl2溶液中存在平衡: [Cu(H2O)4]2+(蓝 )+4Cl- 2O H 0,下列说法4
不正确的是___________(填序号)。
A. 加 滴AgNO 溶液,平衡逆向移动3
B. 加热溶液,溶液由蓝绿 变为 绿 ,平衡常数 K增
2-
C. 加 稀释,c([Cu(H2O)4]2+):c(CuCl 4 )的 值会减
D. 加 少量 NaCl固体,平衡正向移动, Cl -转化率增
试卷第 8 ,共 1 0
(3)盐酸的浓度会影响刻蚀速率,CuCl2浓度相同,盐酸浓度分别为 1 .5mol/L、2.5mol/L、
3.0mol/L时,c(H2CuCl3)随时间的变化曲线如图所示,中间速率变缓慢的可能原因是
______________________。c(HCl)= 1 .5mol/L时,在 0~ 1 .5min 内,H2CuCl3的平均 成速率为
___________________________。
(4)Cu2+能形成多种配合物。铜氨溶液具有显著的抗菌作 。往 0.2 mol/L CuSO4溶液中通 氨 ,
测得 Cu2+ 和铜氨各级配合物的物质的量分数 Xn与平衡体系的 p[NH3](NH3浓度的负对数)
的关系如图所示。
①曲线 4代表的含铜微粒为________________。
②b点的纵坐标为_______________。
③结合图像信息,计算反应 Cu(OH)2 +4NH3 [Cu(NH3)4]2+ + 2OH 的平衡常数 K。
(已知 Cu(OH)2的 Ksp = 2.2×1 0-20,写出计算过程)
试卷第 9 ,共 1 0
20. 化合物 V是 种重要的免疫增强剂, 业上可以进 如下路线的合成:
(1)化合物Ⅰ的名称为__________。
(2)化合物Ⅱ中含氧官能团的名称是______________。化合物Ⅱ的某种同分异构体,在核磁共振氢
谱图上只有 4组峰,能够发 银镜反应,且苯环上的 氯代物有 3种,其结构简式为______________。(3)
关于上述示意图中的相关物质及转化,下列说法正确的有__________。
A. 化合物Ⅴ中存在 3个 性碳原
B. 由化合物Ⅰ到Ⅱ的转化中,有π键的断裂与形成
C. 由化合物Ⅱ到Ⅲ以及由Ⅳ到Ⅴ的转化过程,反应类型相同
D. 化合物Ⅴ中 N 原 的杂化 式为 sp2杂化
(4)对化合物Ⅴ,分析预测其可能的化学性质,完成下表。
序号 反应试剂、条件 反应形成的新结构 反应类型
① ______________ ______________
② ______________ ______________________ 催化氧化反应
(5)由化合物Ⅲ到Ⅳ的转化中, 成 种副产物,其分 式 C H NO ,请写出其结构简式为1 2 1 3 8
为
__________________________。
(6)以 1,2- 溴 烷 CH N 为有机原料,合成 。基于你设计的合成
和
路线,回答下列问题:
①第 步反应的化学 程式为_____________________________________________(注明反应条件)。
②第 步的产物与CH NO 反应的物质的量之 为__________。
3 2
③最后 步的反应条件是__________________。
试卷第 1 0 ,共 1 0
珠海市第 中学 2025届 三年级考前冲刺卷(化学学科)
参考答案
、选择题(本题共 16 题,第 1~10 题,每 题 2分;第 11~16 题,每 题 4分,共 44
分。)
题 1 2 3 4 5 6 7 8
选项 C B D C A C C B
题 9 10 11 12 13 14 15 16
选项 A B D D C B B A
、 选择题
17.(14分,每空 2分)
(1)100mL容量瓶
(2)铁离 与苯酚的显 时,存在反应 Fe3++6C6H5OH [Fe(C6H5O)6]3 +6H+,氢离 浓度增 ,
平衡逆向移动,[Fe(C6H5O)6]3 的浓度减 ,溶液颜 变浅。
①氯离 或硫酸根对苯酚与铁离 的显 反应也有影响 ②硫酸钠 ③>
(3)更难 (4)Fe3+的检验:在溶液中加 滴 KSCN溶液,溶液变为红
18. (14分,除标注外每空 2分)
(1)ⅥB(1分) d(1分)
温
(2)将 钨矿粉碎、搅拌、空 逆通等(1分) 4FeWO4+O2+4Na2C 4Na2WO4+2Fe2O3+4C
O O
(3)H2SiO3和 Al(OH)3
(4)
3 3 2 840 10(5)① (1 分) ② 3 N 102
3 A
19.(14分,除标注外每空 2分)
(1) (1 分) (2)CD
(3)反应 成的固体 CuCl覆盖了铜,阻碍反应进 , 成 H2CuCl3的速率较 0.2mol·L-1·min-1
慢
(4)①[Cu(NH3)3]2+ ②0.14
三答案 第 1 共 2
c[Cu(NH 2�]
③根据题 信息,Cu2++NH3= [Cu(NH3)]2+ K 1 ) ,�
c ( 2 3)
1
a点时 c(Cu2+)=c[Cu(NH3)2+] K 1 =104.1,
, (c NH3 )
代 曲线后 交点可计算得到 [Cu(NH3)]2+ +NH3= [Cu(NH3)2]2+ K2=103.5
[Cu(NH3)2]2+ +NH3 K3=102.9
[Cu(NH ) ]
[Cu(NH3)3]2+ +NH3 K3=102.1
[Cu(NH ) ]
Cu(OH)2+4NH3 [Cu(NH3)4]2++2OH
[c (NH ) 2� ] 2( OH�)
所以,K 3 4Cu c4 ( N 3 )
H
=104.1×103.5×102.9×102.1×2.2×10-20= 2.2×10-7.4 (3分)
(评分细则:写出 K的表达式 1 分,分析出 K1等数据 1 分,答案 1
分)20. (14分,除标注外每空 2分)
(1)苯甲醛(1分)
(2)硝基(1分)
(3)BC
(4)①浓硫酸、加热 消去反应(1分,两个空格 1分,都对给 1分, 对 错不给分)
②O 、Cu、加热2 (1 分,两个空格 1分,都对给 1分, 对 错不给分)
(5)
(6) ①BrCH CH Br�2NaO HOCH CH2 2 � ②1: 2(1 分) ③浓硫
H H O2 OH2 2
酸、加热(1分)
三答案 第 2 共 2
学 科 ( 北 京 ) 股 份 有 限 公 司
满分 1 00分,考试 时 75分钟
注意事项:
1 .答卷前,考 务必 字迹钢笔或签字笔将 的姓名、考 号、考场号和座位号填写在答题
卡上。将条形码横贴在答题卡右上 “ 条形码粘贴处” 。
2.作答选择题时,选出每 题答案后, 2B铅笔把答题卡上对应题 选项的答案信息点涂 ;
如需改动, 橡 擦 净后,再选涂其他答案,答案不能答在试卷上。
3. 选择题必须 字迹钢笔或签字笔作答,答案必须写在答题卡各题 指定区域内相应位置上:
如需改动,先划掉原来的答案,然后再写上新的答案,不准使 铅笔和涂改液。不按以上要求作答
的答案 效。
可能 到的相对原 质量:H-1 C-1 2 N-1 4 O-1 6 Na-23 Al-27 Si-28 Mn-55 Cu-64
、选择题:本题共 1 6 题,共 44分。第 1 ~ 1 0 题,每 题 2分;第 1 1 ~ 1 6 题,每 题 4
分。在每 题给出的四个选项中,只有 项是符合题 要求的。
1 . 世界 明史上,中华 化是世界上唯 从未间断的 明,始终显示出顽强的 命 和 穷的魅 。
下列 物主要由硅酸盐材料制成的是
A.东 汉 铜 奔 B.唐代“ 鎏 舞 C.秦“ 兵 俑” D.仅 49g的 汉“ 直
“ 踏 燕” 衔杯纹银壶” 裾素纱禅 ”
2. 化学和 活、科技、社会发展息息相关。下列说法正确的是
A. 太阳能电池使 的材料是半导体,其主要成分是 SiO2
B. “ 深海 号” 船海 浸泡区镶上铝基是利 了牺牲阳极的 属防腐原理
C. 巴黎奥运会场馆使 的“ 碲化镉” 光伏发电系统将化学能转化为电能
D. “ 三元催化器” 将汽 尾 中 NO 和 CO转化为 N2和 CO2,有利于实现碳
中和
3. 化学处处呈现美。下列说法正确的是
A. 环 烷呈现对称美,分 中六个碳原 连接呈环,呈平 正六边形结构
B. S8分 呈现“ 皇冠” 结构,分 中的硫原 通过共价键结合,S8属于共价晶体
C. 霓虹灯发出五颜六 的光,该过程属于化学变化
D. 锌 在 AgNO3溶液中 成“ 银树” ,反应中锌被氧化
试卷第 1 ,共 1 0
4. 下列有关物质结构和性质的说法,正确的是
A. NO3 与 SO32 的中 原 杂化轨道类型均为 sp2杂化
B. O2和 O3都是单质,在 H2O 中溶解度 乎 样
C. 可燃冰(CH4 8H2O)中甲烷分 与 分 之间没有氢键
D. 分 晶体都存在分 间作 和共价键
5. 勤劳致富,越努 越幸福。下列项 与所述的化学知识没有关联的是
选
产活动 化学原理
项
A 冬季来临时, 灰浆涂抹树 灰浆可以减少植物光合作
B 新会陈 年份越陈, 越浓郁 味的来源之 柠檬烯具有果 味道
C 碳酸氢铵可 作饼 的膨松剂 碳酸氢铵中和酸且受热易分解产 体
D 煮 浆点 制作 腐 胶体聚沉
6. 下列制备实验中,实验装置及操作均正确的是
锰酸钾标准溶液滴 探究苏打和 苏打的稳定
检验装置 密性 溶液转移
定草酸溶液 性
A B C D
7. 将 块镀层破损的铁 置于海边潮湿环境中, 段时间后铁 如图所示。下列说法正确的是
A. 电 由镀层流向铁
B. 铁 凹陷深处产 了较多 OH-
C. 镀层的 属性 铁弱
D. 对铁进 了牺牲阳极的阴极保护
试卷第 2 ,共 1 0
8.从中草药中提取的 calebinA (结构简式如下图)可 于治疗阿尔茨海默症。下列关于 calebinA
的说法正确的是
A.该物质在空 中能 时间保存
B.该物质能使 锰酸钾溶液褪
C.该物质能与 Na2CO3溶液反应 成
CO2
D.1 mol该物质与浓溴 反应,最多消耗 2 mol Br2
9. 部分含 S(a、b、c、d)和 Cl(e、f、g、h)的物质分类与相应化合价的关系如图所示。下列说法正确
的是
A. 向 h 的溶液中通 c,溶液的酸性增强
B. b或 f与 属 Cu 反应的产物中 Cu 的化合价均为
+2
C. d的浓溶液因具有脱 性使胆矾晶体由蓝 变为
D. c和 g 都能使湿润的蓝 蕊试纸先变红后褪
1 0.实验室可利 反应 制备 Br2。设 NA代表阿伏
加德罗常数的值。下列说法正确的是
A. 0℃、1 01 kPa下,1 1 .2LH2O 所含的分 数为 0.5NA
B. 9.8gH2SO4和 H3PO4混合物中含氧原 数为 0.4NA
C. 该反应中 成 0.2molBr2时,转移的电 数为 0.2NA
D. 0.1mol/L的 KHSO4溶液中含有的离 数为 0.3NA
1 1.下列陈述 I 与陈述Ⅱ均正确,且具有因果关系的是
选项 陈述 I 陈述Ⅱ
A 1mol 可以和 3mol氢 加成 1mol 中含有 3mol碳碳双键
B 墨的硬度 刚 很多 墨中共价键的键能 刚
C 氧化硫可以使 锰酸钾溶液褪 氧化硫具有漂 性
D 酸性:甲酸> 酸>丙酸 烷基越 推电 效应越
试卷第 3 ,共 1 0
1 2. 已知 氧化氯(ClO2)为新型绿 消毒剂,沸点为 9.9℃,可溶于 、有毒,浓度较 时易发
爆炸。利 ClO2与 H2O2在碱性条件下制备少量 NaClO2的实验装置如图所示。
下列说法正确的是
A. 实验中通 CO2 体的速率应尽可能慢
B. 装置 中应使 热 浴,以加快反应速率
C. 为配制分液漏 中的混合液,应将甲醇溶液倒 浓硫酸中搅拌
D. 若装置甲烧瓶内氧化产物为 HCOOH,则氧化剂与还原剂的物质的量之 为 4∶ 1
1 3. 苏打(Na2S2O3)、苏打(Na2CO3)和 苏打(NaHCO3)被誉为“ 苏 三兄弟” ,在 产、 活
中应 泛。下列离 程式不正确的是
-
A. MnSO4和 NaHCO3反应制备 MnCO3: HCO =MnCO3↓+CO2↑+H2O
3
Mn2++2
2- 2-
B. Na2S2O3溶液吸收尾 中的 Cl2: S O3 = SO +8Cl-+1 0H+
5H2O+4Cl2+ 2
2-
C. 活中常 泡沫灭 器灭 : CO3 +3H2O=2Al(OH)3↓+3CO2↑
2Al3++3
2-
D. Na2S2O3与盐酸反应测反应速 S O3 +2H+=SO2↑+S↓+H2O
率:
1 4. 种由短周期主族元素组成的化合物(如图所示),具有良好的储氢性能,其中元素 W、X、Y、
Z的原 序数依次增 、且总和为 24。下列有关叙述不正确的是
A. 该化合物中 W、X、Y之间均为共价键
B. X的原 核外电 排布式为 1 s22s22p2
C. Y的最 化合价氧化物的 化物为强酸
D. Z的单质既能与 反应,也可与甲醇反应
试卷第 4 ,共 1 0
1 5. 甲酸(HCOOH)可在纳 级 Pd 表 分解为活性 H2和 CO2,经下列历程实现 NO 3 的催化
还原。
已知 Fe(Ⅱ)、Fe(Ⅲ)表示 Fe3O4中 价铁和三价铁。下列说法不正确的是
A. 产中将催化剂处理成纳 级颗粒可增 甲酸分解的速率
B.在整个历程中,每 1 molH2可还原 2molNO 3
C.HCOOH 分解时,只有极性共价键发 了断裂
D.反应历程中 成的 H+可调节体系 pH,有增强 NO 3 氧化性的作
1 6. 某新型钠离 次电池(如图) 溶解了 NaPF6的 甲氧基 烷作电解质溶液。放电时嵌
PbSe中的 Na变成 Na+后脱嵌。下列说法错误的是
A. 外电路通过 1mol电 时,理论上两电极质量变化的差值为 23g
B. 充电时,阳极电极反应为: V4 x3 4 3
e
C.放电 段时间后,电解质溶液中的 Na+浓度基本保持不
变
D.D. 电解质溶液不能 NaPF6的 溶液替换
试卷第 5 ,共 1 0
、 选择题:本题共 4 题,共 56分。
1 7. 苯酚能与 Fe3+形成[Fe(C6H5O)6]3-的紫 配合物,该过程属于可逆反应。某 组同学探究铁
离 与苯酚的反应。
(1)配制1 00mL0.1mol /L苯酚溶液,需要 到的玻璃仪器有:烧杯、玻璃棒、胶头滴管和_______。
(2)探究铁盐种类和 pH 对苯酚与 Fe3+显 反应的影响。查阅资
料:i.Na+对苯酚与 Fe3+的显 反应 影响;
ii. 组同学得出猜想 H+对 Fe3+与苯酚的显 反应有抑制作 ,从化学平衡 度解释其原因
___________________________________________________________________________________。iii.
[Fe(C6H5O)6]3-对特定波 光的吸收程度( 吸光度 A 表示)与[Fe(C6H5O)6]3-浓度在 定范围内成
正 。
提出猜想:猜想 1:Cl-对苯酚与 Fe3+的显 反应有影响
2-
猜想 SO 对苯酚与 Fe3+的显 反应有影响
4
2:
进 实验:常温下, 盐酸调节 pH,配制得到 pH 分别为 a和 b的 0.1mol/LFeCl3溶液(a>b);
硫酸调节 pH,配制得到 pH 分别为 a和 b 的 0.05mol/LFe2(SO4)3溶液。取 4 试管各加
5ml 0.1 mol/L苯酚溶液,按实验 1 ~ 4分别再加 0.1mL含 Fe3+的试剂,显 1 0min 后 紫
外-可 分光光度计测定该溶液的吸光度(本实验条件下,pH 改变对 Fe3+ 解程度的影响可忽略)。
含 Fe3+的试剂
序 吸光
0.1mol/LFeCl3 0.05mol/LFe2(SO4)3
号 度
溶液 溶液
1 pH=a / A1
2 pH=b / A2
3 / pH=a A3
4 / pH=b A4
结果讨论:实验结果为 A2 A3 A4
A1
①根据实验结果, 组同学认为此结果不 以证明猜想“ H+对 Fe3+与苯酚的显 反应有抑制作 ”
成 的理由是_______________________________________________________________________。
试卷第 6 ,共 1 0
②为进 步验证猜想, 组同学设计了实验 5和 6,补充下表中试剂 M 为_______________。
含 Fe 的试剂
序 再加 的 吸光
0.1mol /LFeCl 溶
号 0.05mol/LF S3 2 4 溶3 试剂 度
e O
液 液
5 / pH =a NaCl固体 A5
6 pH =a / 试剂 M A6
2-
③根据实验 1 ~ 6的结果, 组同学得出猜想 1 不成 ,猜想 2成 , SO 对苯酚与 Fe3+的显
且
反应起抑制作 ,得出此结论的实验依据是:A3 A A1 A6(填“ >”、“ <”或“ =”。)
(3)通过以上实验结论分析:与苯酚相 ,对羟基苯甲酸与 FeCl3溶液发 显 反应_______。 (填
“ 更容易” 或“ 更难” )
(4)实验室中常 某些配合物的性质进 物质的检验,请举 例 并说明现象_______。
1 8. 业上利 钨矿(其主要成分是 FeWO4、MnWO4,还含有少量 SiO2和 Al2O3)制备钨的
艺流程如下图所示:
已知:①上述流程中,钨的化合价只在最后 步发 改变;②常温下钨酸难溶于 。回答下列问题:
(1)已知元素钨与铬同族,钨在元素周期表中的位置是第六周期第______族,其位于元素周期表
________区。
(2)提 钨矿“ 焙烧” 效率的措施有__________(任写 条),FeWO4在“ 焙烧” 过程中发 反
应的化学 程式为__________________________________________________。
(3)“ 滤渣” 的主要成分是______(填化学式)。
试卷第 7 ,共 1 0
(4)钨酸钙(CaWO4)和氢氧化钙都是微溶电解质。某温度下 Ca(OH)2和 CaWO4的饱和溶液中,
pc(Ca2+)与 pc(阴离 )的关系如图所示,已知:pc(离 )=-lgc(离 )。该温度下将 Na2WO4溶液
加 灰乳中得到 量钨酸钙,发 反应的离 程式为__________________________________,该反
应的平衡常数 K=_______________。
(5)合 具有 属单质更优越的性能,Cu-Mn-Al合 为磁性形状记忆合 材料之 ,其晶胞
结构如图所示(已知:Mn 原 和 Al原 位于 Cu 原 所构成的 个 正 体的体 )。
①若 A 原 的坐标参数为(0,0,0),则 B原 的坐标参数为_______________。
②已知该合 晶体的密度为 pg·cm-3,则最近的两个 Al原 间的距离为____________________pm(列
出计算式,阿伏加德罗常数的值 NA表示)。
1 9. 酸性 CuCl2溶液主要组成为 HCl与 CuCl2 (HCl与 CuCl2会络合为 H2CuCl4),其具有溶铜速率
快、稳定、易控制及易再 等优点,常应 于印刷线路板(PCB)的刻蚀。刻蚀原理为 Cu(s)+
H2CuCl4(aq)→H2CuCl3(aq)+ CuCl(s),CuCl(s)+2HCl(aq)→H2CuCl3(aq)
(1)CuCl中基态亚铜离 的价层电 轨道表示式为_______________________。
2-
(2)CuCl2溶液中存在平衡: [Cu(H2O)4]2+(蓝 )+4Cl- 2O H 0,下列说法4
不正确的是___________(填序号)。
A. 加 滴AgNO 溶液,平衡逆向移动3
B. 加热溶液,溶液由蓝绿 变为 绿 ,平衡常数 K增
2-
C. 加 稀释,c([Cu(H2O)4]2+):c(CuCl 4 )的 值会减
D. 加 少量 NaCl固体,平衡正向移动, Cl -转化率增
试卷第 8 ,共 1 0
(3)盐酸的浓度会影响刻蚀速率,CuCl2浓度相同,盐酸浓度分别为 1 .5mol/L、2.5mol/L、
3.0mol/L时,c(H2CuCl3)随时间的变化曲线如图所示,中间速率变缓慢的可能原因是
______________________。c(HCl)= 1 .5mol/L时,在 0~ 1 .5min 内,H2CuCl3的平均 成速率为
___________________________。
(4)Cu2+能形成多种配合物。铜氨溶液具有显著的抗菌作 。往 0.2 mol/L CuSO4溶液中通 氨 ,
测得 Cu2+ 和铜氨各级配合物的物质的量分数 Xn与平衡体系的 p[NH3](NH3浓度的负对数)
的关系如图所示。
①曲线 4代表的含铜微粒为________________。
②b点的纵坐标为_______________。
③结合图像信息,计算反应 Cu(OH)2 +4NH3 [Cu(NH3)4]2+ + 2OH 的平衡常数 K。
(已知 Cu(OH)2的 Ksp = 2.2×1 0-20,写出计算过程)
试卷第 9 ,共 1 0
20. 化合物 V是 种重要的免疫增强剂, 业上可以进 如下路线的合成:
(1)化合物Ⅰ的名称为__________。
(2)化合物Ⅱ中含氧官能团的名称是______________。化合物Ⅱ的某种同分异构体,在核磁共振氢
谱图上只有 4组峰,能够发 银镜反应,且苯环上的 氯代物有 3种,其结构简式为______________。(3)
关于上述示意图中的相关物质及转化,下列说法正确的有__________。
A. 化合物Ⅴ中存在 3个 性碳原
B. 由化合物Ⅰ到Ⅱ的转化中,有π键的断裂与形成
C. 由化合物Ⅱ到Ⅲ以及由Ⅳ到Ⅴ的转化过程,反应类型相同
D. 化合物Ⅴ中 N 原 的杂化 式为 sp2杂化
(4)对化合物Ⅴ,分析预测其可能的化学性质,完成下表。
序号 反应试剂、条件 反应形成的新结构 反应类型
① ______________ ______________
② ______________ ______________________ 催化氧化反应
(5)由化合物Ⅲ到Ⅳ的转化中, 成 种副产物,其分 式 C H NO ,请写出其结构简式为1 2 1 3 8
为
__________________________。
(6)以 1,2- 溴 烷 CH N 为有机原料,合成 。基于你设计的合成
和
路线,回答下列问题:
①第 步反应的化学 程式为_____________________________________________(注明反应条件)。
②第 步的产物与CH NO 反应的物质的量之 为__________。
3 2
③最后 步的反应条件是__________________。
试卷第 1 0 ,共 1 0
珠海市第 中学 2025届 三年级考前冲刺卷(化学学科)
参考答案
、选择题(本题共 16 题,第 1~10 题,每 题 2分;第 11~16 题,每 题 4分,共 44
分。)
题 1 2 3 4 5 6 7 8
选项 C B D C A C C B
题 9 10 11 12 13 14 15 16
选项 A B D D C B B A
、 选择题
17.(14分,每空 2分)
(1)100mL容量瓶
(2)铁离 与苯酚的显 时,存在反应 Fe3++6C6H5OH [Fe(C6H5O)6]3 +6H+,氢离 浓度增 ,
平衡逆向移动,[Fe(C6H5O)6]3 的浓度减 ,溶液颜 变浅。
①氯离 或硫酸根对苯酚与铁离 的显 反应也有影响 ②硫酸钠 ③>
(3)更难 (4)Fe3+的检验:在溶液中加 滴 KSCN溶液,溶液变为红
18. (14分,除标注外每空 2分)
(1)ⅥB(1分) d(1分)
温
(2)将 钨矿粉碎、搅拌、空 逆通等(1分) 4FeWO4+O2+4Na2C 4Na2WO4+2Fe2O3+4C
O O
(3)H2SiO3和 Al(OH)3
(4)
3 3 2 840 10(5)① (1 分) ② 3 N 102
3 A
19.(14分,除标注外每空 2分)
(1) (1 分) (2)CD
(3)反应 成的固体 CuCl覆盖了铜,阻碍反应进 , 成 H2CuCl3的速率较 0.2mol·L-1·min-1
慢
(4)①[Cu(NH3)3]2+ ②0.14
三答案 第 1 共 2
c[Cu(NH 2�]
③根据题 信息,Cu2++NH3= [Cu(NH3)]2+ K 1 ) ,�
c ( 2 3)
1
a点时 c(Cu2+)=c[Cu(NH3)2+] K 1 =104.1,
, (c NH3 )
代 曲线后 交点可计算得到 [Cu(NH3)]2+ +NH3= [Cu(NH3)2]2+ K2=103.5
[Cu(NH3)2]2+ +NH3 K3=102.9
[Cu(NH ) ]
[Cu(NH3)3]2+ +NH3 K3=102.1
[Cu(NH ) ]
Cu(OH)2+4NH3 [Cu(NH3)4]2++2OH
[c (NH ) 2� ] 2( OH�)
所以,K 3 4Cu c4 ( N 3 )
H
=104.1×103.5×102.9×102.1×2.2×10-20= 2.2×10-7.4 (3分)
(评分细则:写出 K的表达式 1 分,分析出 K1等数据 1 分,答案 1
分)20. (14分,除标注外每空 2分)
(1)苯甲醛(1分)
(2)硝基(1分)
(3)BC
(4)①浓硫酸、加热 消去反应(1分,两个空格 1分,都对给 1分, 对 错不给分)
②O 、Cu、加热2 (1 分,两个空格 1分,都对给 1分, 对 错不给分)
(5)
(6) ①BrCH CH Br�2NaO HOCH CH2 2 � ②1: 2(1 分) ③浓硫
H H O2 OH2 2
酸、加热(1分)
三答案 第 2 共 2
学 科 ( 北 京 ) 股 份 有 限 公 司
同课章节目录
