3.4 课题1羧酸酯 学案(含答案) 2024-2025学年高二化学人教版(2019)选择性必修3
文档属性
| 名称 | 3.4 课题1羧酸酯 学案(含答案) 2024-2025学年高二化学人教版(2019)选择性必修3 |
|
|
| 格式 | docx | ||
| 文件大小 | 337.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-05-10 00:00:00 | ||
图片预览




文档简介
课题1 羧酸 酯
1. 认识羧酸、酯的典型代表物的组成、结构特点和性质。
2. 探究酯化反应的机理。了解如何用酯化反应制取高分子材料。
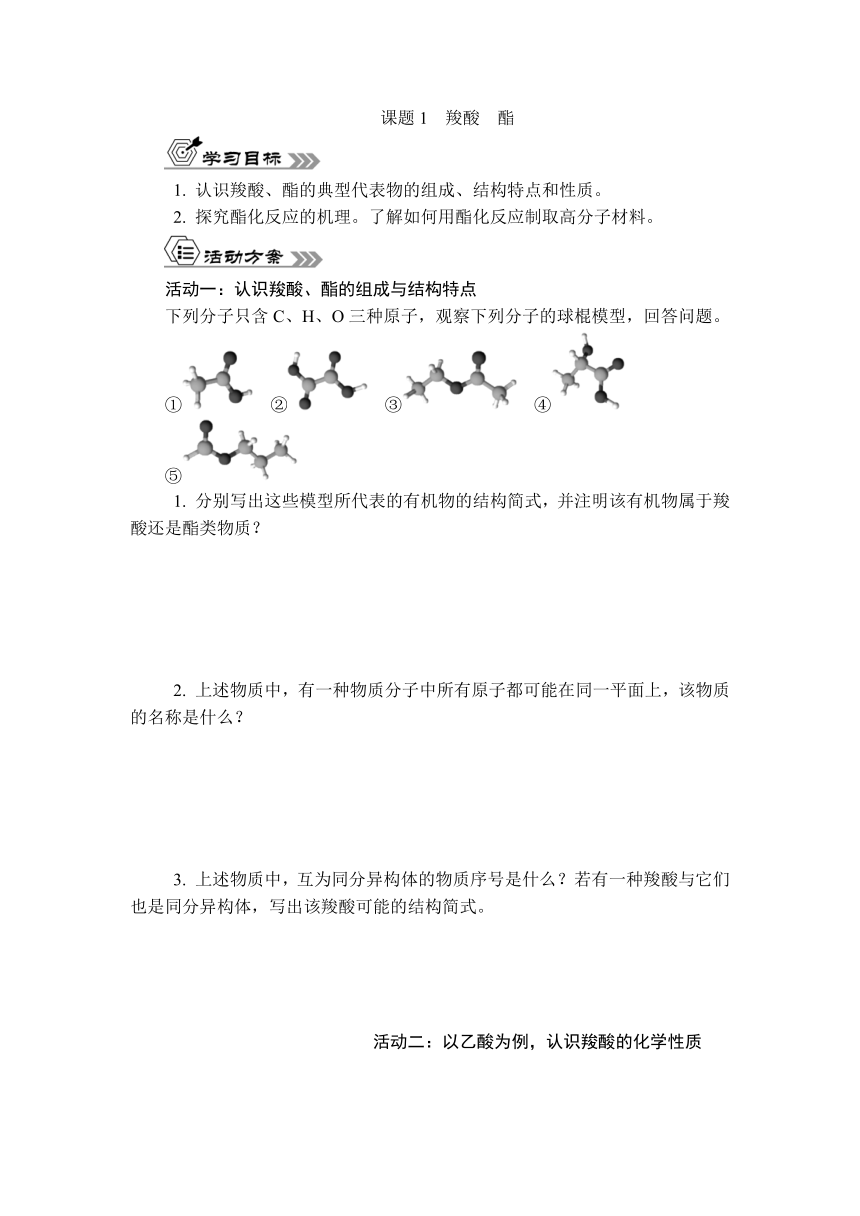
下列分子只含C、H、O三种原子,观察下列分子的球棍模型,回答问题。
① ② ③ ④ ⑤
1. 分别写出这些模型所代表的有机物的结构简式,并注明该有机物属于羧酸还是酯类物质?
2. 上述物质中,有一种物质分子中所有原子都可能在同一平面上,该物质的名称是什么?
3. 上述物质中,互为同分异构体的物质序号是什么?若有一种羧酸与它们也是同分异构体,写出该羧酸可能的结构简式。
1. 回忆并在下表中写出体现乙酸化学性质的化学方程式(若属于离子反应则写离子方程式)。
性质 实例 化学方程式(或离子方程式)
酸性 与金属钠反应
与氢氧化钠反应
与氧化镁反应
与可溶性碳酸盐反应
与碳酸氢盐反应
酯化反应 与乙醇反应
2. 对乙酸和乙醇发生酯化反应的机理提出可能的猜想。化学中常用同位素原子来研究反应的机理,如果乙醇中的氧原子是18O,则如何确定反应的机理?
3. 仿照乙酸的化学性质,写出下列各组物质发生酯化反应的化学方程式(注明反应条件)。
(1) 丙酸与乙醇:____________________________________________。
(2) 乙二酸与过量乙醇:____________________________________________。
(3) 过量冰醋酸与乙二醇:___________________________________________。
(4) 乙二酸与乙二醇反应。
①生成环状化合物:____________________________________________。
②生成高分子化合物:____________________________________________。
(5) 一定条件下乳酸()的反应。
①生成环状化合物:_________________________________________________。
②生成高分子化合物:_______________________________________________。
4. 甲酸除了具有酸性,还可能具有哪些化学性质?请从分子结构的角度进行分析。
1. 探讨乙酸乙酯在不同条件下的水解速率。
实验探究:在3支相同的试管内,分别加入2 mL稀硫酸、氢氧化钠溶液、蒸馏水,再分别加入0.5 mL的乙酸乙酯,一起放入同一水浴中加热,数分钟后取出,观察实验现象。
(1) 将实验现象和你所得出的结论填写到下表中。
水解条件 实验现象 实验结论
①酸性
②碱性
③中性
(2) 为什么酸和碱能加快化学反应速率?为什么酯在碱性条件下水解可以进行到底?
(3) 分别写出乙酸乙酯在酸性条件和碱性条件下发生反应的化学方程式。
2. 模仿乙酸乙酯的水解反应,书写下列反应的化学方程式(注明反应条件)。
(1) 甲酸乙酯与氢氧化钠溶液反应。
(2) 阿司匹林()与氢氧化钠溶液反应。
1. 从结构上看,下列物质既具有羧酸的性质,又具有醛的性质的是( )
A. 甲醛 B. 乙醛 C. 甲酸 D. 乙酸
2. 苹果中含有戊酸戊酯[CH3(CH2)3COO(CH2)4CH3],菠萝中含有丁酸乙酯[CH3(CH2)2COOCH2CH3],香蕉中含有乙酸异戊酯[CH3COOCH2CH2CH(CH3)2]。下列说法不正确的是( )
A. 都难溶于水、易溶于有机溶剂 B. 都具有芳香气味,密度都比水小
C. 三种酯互为同分异构体 D. 三种酯互为同系物
3. 将 1 mol 乙醇(其中的氧用 18O 标记)在浓硫酸存在的条件下与足量乙酸充分反应。下列叙述不正确的是( )
A. 生成的乙酸乙酯中含有18O B. 生成的水分子中含有18O
C. 反应后有乙醇剩余 D. 不可能生成 90 g 乙酸乙酯
4. 下列对有机物的叙述不正确的是( )
A. 常温下,能与NaHCO3溶液反应放出CO2气体
B. 能发生碱性水解,1 mol该有机物完全反应需要消耗8 mol NaOH
C. 与稀硫酸共热时,生成两种有机物
D. 该有机物的分子式为C14H10O9
5. 实验室用如图所示装置制取乙酸乙酯。
(1) 加热前,试管中加入几粒碎瓷片的作用是____________。浓硫酸的作用是________________,加快反应速率;同时作______________,有利于平衡向酯化反应方向移动。饱和Na2CO3溶液的作用是____________________________________和_____
____________________;导气管不能插入饱和Na2CO3溶液中的原因是____________________。
(2) 实验生成的乙酸乙酯的密度比水的__________(填“大”或“小”),有________气味;若实验中温度过高,温度达170 ℃,副产物中主要有机物是________________(填名称)。
(3) 在试管中配制实验所需的乙醇、乙酸和浓硫酸的混合液时,可先加入3 mL乙醇,然后___________________________________________________________。
6. 某有机物A能与NaOH溶液反应,其分子中含有苯环,相对分子质量为136,其中含碳的质量分数为70.6%,氢的质量分数为5.9%,其余为氧。
(1) A的分子式是____________。
(2) 若A能与NaHCO3溶液反应放出CO2气体,其结构有________种。
(3) 若A与NaOH溶液在加热时才能反应,且1 mol A消耗1 mol NaOH,则A的结构简式可能是____________________。
(4) 若A与NaOH溶液在加热时才能反应,且1 mol A消耗2 mol NaOH,则符合条件的A的结构可能有________种,其中能发生银镜反应的有________种,不能发生银镜反应的物质的结构简式是____________________________。
课题1 羧酸 酯
【活动方案】
活动一:1. ①CH3COOH(羧酸)
②(羧酸)
③(酯)
④CH3CHOHCOOH(羧酸)
⑤HCOOCH2CH2CH3(酯)
2. 乙二酸
3. ③⑤互为同分异构体。CH3CH2CH2COOH、
活动二:1. 酸性:2CH3COOH+2Na―→2CH3COO-+H2↑+2Na+
CH3COOH+OH-―→CH3COO-+H2O
2CH3COOH+MgO―→2CH3COO-+Mg2++H2O
2CH3COOH+CO―→2CH3COO-+CO2↑+H2O
CH3COOH+HCO―→CH3COO-+CO2↑+H2O
酯化反应:CH3COOH+HOCH2CH3CH3COOCH2CH3+H2O
2. 乙酸和乙醇发生酯化反应时,有两种可能机理:机理1是乙酸中羧基脱去羟基,乙醇脱去羟基氢;机理2是乙酸中羧基脱去氢,乙醇脱去羟基。当乙醇中的氧原子是18O时,若18O在生成的乙酸乙酯中,则为机理1,若18O在生成的水中,则为机理2。
3. (1) CH3CH2COOH+CH3CH2OHCH3CH2COOCH2CH3+H2O
(2) +2CH3CH2OH+2H2O
(3) 2CH3COOH++2H2O
(4) ①++2H2O
②n+n+(2n-1)H2O
(5) ①
②
4.
甲酸分子中既有羧基的结构(上图中圆圈),又有醛基的结构(上图中方框),这使得甲酸既表现出羧酸的性质,又表现出醛的性质。
活动三:1. (1) ①试管中乙酸乙酯部分消失 ②试管中乙酸乙酯几乎全部消失 ③试管中乙酸乙酯基本没变 实验结论:乙酸乙酯在碱性条件下水解速率最快,在蒸馏水中水解速率最慢
(2) 酸、碱对酯的水解均有催化作用。碱可以中和酯水解生成的羧酸,使平衡正向移动。
(3) CH3COOCH2CH3+H2OCH3COOH+HOCH2CH3
CH3COOCH2CH3+NaOHCH3COONa+HOCH2CH3
2. (1) HCOOCH2CH3+NaOHHCOONa+HOCH2CH3
(2) +3NaOH+CH3COONa+2H2O
【课堂反馈】
1. C 2. C 3. B 4. C
5. (1) 防止暴沸 作催化剂 吸水剂 除去酯中混有的乙酸和乙醇 降低酯在水中的溶解度,易于分层 防止倒吸 (2) 小 果香 乙烯
(3) 边振荡试管边慢慢加入2 mL浓硫酸和2 mL乙酸
6. (1) C8H8O2 (2) 4
(3) 、
(4) 4 3
1. 认识羧酸、酯的典型代表物的组成、结构特点和性质。
2. 探究酯化反应的机理。了解如何用酯化反应制取高分子材料。
下列分子只含C、H、O三种原子,观察下列分子的球棍模型,回答问题。
① ② ③ ④ ⑤
1. 分别写出这些模型所代表的有机物的结构简式,并注明该有机物属于羧酸还是酯类物质?
2. 上述物质中,有一种物质分子中所有原子都可能在同一平面上,该物质的名称是什么?
3. 上述物质中,互为同分异构体的物质序号是什么?若有一种羧酸与它们也是同分异构体,写出该羧酸可能的结构简式。
1. 回忆并在下表中写出体现乙酸化学性质的化学方程式(若属于离子反应则写离子方程式)。
性质 实例 化学方程式(或离子方程式)
酸性 与金属钠反应
与氢氧化钠反应
与氧化镁反应
与可溶性碳酸盐反应
与碳酸氢盐反应
酯化反应 与乙醇反应
2. 对乙酸和乙醇发生酯化反应的机理提出可能的猜想。化学中常用同位素原子来研究反应的机理,如果乙醇中的氧原子是18O,则如何确定反应的机理?
3. 仿照乙酸的化学性质,写出下列各组物质发生酯化反应的化学方程式(注明反应条件)。
(1) 丙酸与乙醇:____________________________________________。
(2) 乙二酸与过量乙醇:____________________________________________。
(3) 过量冰醋酸与乙二醇:___________________________________________。
(4) 乙二酸与乙二醇反应。
①生成环状化合物:____________________________________________。
②生成高分子化合物:____________________________________________。
(5) 一定条件下乳酸()的反应。
①生成环状化合物:_________________________________________________。
②生成高分子化合物:_______________________________________________。
4. 甲酸除了具有酸性,还可能具有哪些化学性质?请从分子结构的角度进行分析。
1. 探讨乙酸乙酯在不同条件下的水解速率。
实验探究:在3支相同的试管内,分别加入2 mL稀硫酸、氢氧化钠溶液、蒸馏水,再分别加入0.5 mL的乙酸乙酯,一起放入同一水浴中加热,数分钟后取出,观察实验现象。
(1) 将实验现象和你所得出的结论填写到下表中。
水解条件 实验现象 实验结论
①酸性
②碱性
③中性
(2) 为什么酸和碱能加快化学反应速率?为什么酯在碱性条件下水解可以进行到底?
(3) 分别写出乙酸乙酯在酸性条件和碱性条件下发生反应的化学方程式。
2. 模仿乙酸乙酯的水解反应,书写下列反应的化学方程式(注明反应条件)。
(1) 甲酸乙酯与氢氧化钠溶液反应。
(2) 阿司匹林()与氢氧化钠溶液反应。
1. 从结构上看,下列物质既具有羧酸的性质,又具有醛的性质的是( )
A. 甲醛 B. 乙醛 C. 甲酸 D. 乙酸
2. 苹果中含有戊酸戊酯[CH3(CH2)3COO(CH2)4CH3],菠萝中含有丁酸乙酯[CH3(CH2)2COOCH2CH3],香蕉中含有乙酸异戊酯[CH3COOCH2CH2CH(CH3)2]。下列说法不正确的是( )
A. 都难溶于水、易溶于有机溶剂 B. 都具有芳香气味,密度都比水小
C. 三种酯互为同分异构体 D. 三种酯互为同系物
3. 将 1 mol 乙醇(其中的氧用 18O 标记)在浓硫酸存在的条件下与足量乙酸充分反应。下列叙述不正确的是( )
A. 生成的乙酸乙酯中含有18O B. 生成的水分子中含有18O
C. 反应后有乙醇剩余 D. 不可能生成 90 g 乙酸乙酯
4. 下列对有机物的叙述不正确的是( )
A. 常温下,能与NaHCO3溶液反应放出CO2气体
B. 能发生碱性水解,1 mol该有机物完全反应需要消耗8 mol NaOH
C. 与稀硫酸共热时,生成两种有机物
D. 该有机物的分子式为C14H10O9
5. 实验室用如图所示装置制取乙酸乙酯。
(1) 加热前,试管中加入几粒碎瓷片的作用是____________。浓硫酸的作用是________________,加快反应速率;同时作______________,有利于平衡向酯化反应方向移动。饱和Na2CO3溶液的作用是____________________________________和_____
____________________;导气管不能插入饱和Na2CO3溶液中的原因是____________________。
(2) 实验生成的乙酸乙酯的密度比水的__________(填“大”或“小”),有________气味;若实验中温度过高,温度达170 ℃,副产物中主要有机物是________________(填名称)。
(3) 在试管中配制实验所需的乙醇、乙酸和浓硫酸的混合液时,可先加入3 mL乙醇,然后___________________________________________________________。
6. 某有机物A能与NaOH溶液反应,其分子中含有苯环,相对分子质量为136,其中含碳的质量分数为70.6%,氢的质量分数为5.9%,其余为氧。
(1) A的分子式是____________。
(2) 若A能与NaHCO3溶液反应放出CO2气体,其结构有________种。
(3) 若A与NaOH溶液在加热时才能反应,且1 mol A消耗1 mol NaOH,则A的结构简式可能是____________________。
(4) 若A与NaOH溶液在加热时才能反应,且1 mol A消耗2 mol NaOH,则符合条件的A的结构可能有________种,其中能发生银镜反应的有________种,不能发生银镜反应的物质的结构简式是____________________________。
课题1 羧酸 酯
【活动方案】
活动一:1. ①CH3COOH(羧酸)
②(羧酸)
③(酯)
④CH3CHOHCOOH(羧酸)
⑤HCOOCH2CH2CH3(酯)
2. 乙二酸
3. ③⑤互为同分异构体。CH3CH2CH2COOH、
活动二:1. 酸性:2CH3COOH+2Na―→2CH3COO-+H2↑+2Na+
CH3COOH+OH-―→CH3COO-+H2O
2CH3COOH+MgO―→2CH3COO-+Mg2++H2O
2CH3COOH+CO―→2CH3COO-+CO2↑+H2O
CH3COOH+HCO―→CH3COO-+CO2↑+H2O
酯化反应:CH3COOH+HOCH2CH3CH3COOCH2CH3+H2O
2. 乙酸和乙醇发生酯化反应时,有两种可能机理:机理1是乙酸中羧基脱去羟基,乙醇脱去羟基氢;机理2是乙酸中羧基脱去氢,乙醇脱去羟基。当乙醇中的氧原子是18O时,若18O在生成的乙酸乙酯中,则为机理1,若18O在生成的水中,则为机理2。
3. (1) CH3CH2COOH+CH3CH2OHCH3CH2COOCH2CH3+H2O
(2) +2CH3CH2OH+2H2O
(3) 2CH3COOH++2H2O
(4) ①++2H2O
②n+n+(2n-1)H2O
(5) ①
②
4.
甲酸分子中既有羧基的结构(上图中圆圈),又有醛基的结构(上图中方框),这使得甲酸既表现出羧酸的性质,又表现出醛的性质。
活动三:1. (1) ①试管中乙酸乙酯部分消失 ②试管中乙酸乙酯几乎全部消失 ③试管中乙酸乙酯基本没变 实验结论:乙酸乙酯在碱性条件下水解速率最快,在蒸馏水中水解速率最慢
(2) 酸、碱对酯的水解均有催化作用。碱可以中和酯水解生成的羧酸,使平衡正向移动。
(3) CH3COOCH2CH3+H2OCH3COOH+HOCH2CH3
CH3COOCH2CH3+NaOHCH3COONa+HOCH2CH3
2. (1) HCOOCH2CH3+NaOHHCOONa+HOCH2CH3
(2) +3NaOH+CH3COONa+2H2O
【课堂反馈】
1. C 2. C 3. B 4. C
5. (1) 防止暴沸 作催化剂 吸水剂 除去酯中混有的乙酸和乙醇 降低酯在水中的溶解度,易于分层 防止倒吸 (2) 小 果香 乙烯
(3) 边振荡试管边慢慢加入2 mL浓硫酸和2 mL乙酸
6. (1) C8H8O2 (2) 4
(3) 、
(4) 4 3
