4.2 课题1 氨基酸和多肽 学案(含答案) 2024-2025学年高二化学人教版(2019)选择性必修3
文档属性
| 名称 | 4.2 课题1 氨基酸和多肽 学案(含答案) 2024-2025学年高二化学人教版(2019)选择性必修3 |

|
|
| 格式 | docx | ||
| 文件大小 | 168.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2025-05-10 00:00:00 | ||
图片预览


文档简介
课题1 氨基酸和多肽
1. 知道常见的氨基酸。
2. 了解氨基酸的两性、成肽反应;认识人工合成多肽的意义。
3. 了解氨基酸、蛋白质与人体健康的关系。
阅读下列材料,回答问题。
氨基酸是生物体内构成蛋白质分子的基本单位,与生命活动有着密切的关系。组成人体内的氨基酸有21种,但有8种氨基酸(色氨酸、苏氨酸、蛋氨酸、缬氨酸、赖氨酸、亮氨酸、异亮氨酸和苯丙氨酸)在人体不能合成,必须通过食物供给,称为必需氨基酸。
氨基酸在人体内通过新陈代谢可以发挥下列作用:①合成组织蛋白质;②变成酸、激素等物质;③转变成碳水化合物和脂肪;④氧化成二氧化碳、水及尿素。人体缺乏某种氨基酸,会影响抗体代谢的正常进行和导致疾病。如:胱氨酸缺乏会引起胰岛素减少,血糖升高。
如何保证人体必需氨基酸的摄取?
1. 分析下列几种人体氨基酸的结构,回答下列问题。
甘氨酸 苯丙氨酸 蛋氨酸
丙氨酸 谷氨酸 苏氨酸
(1) 归纳氨基酸的组成元素有哪些?氨基酸分子中共同含有的官能团有哪些?
(2) 氨基酸所具有的共同结构是什么?最简单的氨基酸的名称是什么?
(3) 上述氨基酸中,不含有手性碳原子的氨基酸的名称是什么,含有手性碳原子最多的氨基酸的名称是什么?
2. 查阅相关资料,归纳氨基酸的一些共同的物理性质。
1. 探究氨基酸的两性。
(1) 根据氨基酸中含有的官能团,写出甘氨酸与盐酸及NaOH溶液反应的化学方程式。
(2) 根据氨基酸的两性,结合晶体结构的知识解释氨基酸熔点较高的原因。
2. 阅读下列材料,回答问题。
羧基与氨基可以发生类似酯化反应那样的脱水反应,形成肽键(酰胺键)。组成肽的氨基酸单元称为氨基酸残基。二肽分子中含2个氨基酸残基,三肽分子中则含3个氨基酸残基。通常把有氨基的一端叫N端,写在左边;有羧基的一端叫C端, 链状二肽的结构
写在右边(如右图所示)。多个氨基酸结合成多肽时,能够形成的异构体的种类十分繁多,如:10种氨基酸形成的十肽理论上将超过1010种,20种氨基酸形成的十肽理论上将超过1013种。一般把相对分子质量在10 000以上的,并具有一定空间结构的多肽称为蛋白质。
(1) 写出两个丙氨酸分子反应生成二肽的化学方程式,并指出反应的类型。
(2) 甘氨酸和丙氨酸的混合物在一定条件下可以发生反应生成链状二肽,试写出生成的所有二肽的结构简式。
(3) 十肽中肽键的数目是多少?你认为多肽具有的主要化学性质有哪些?
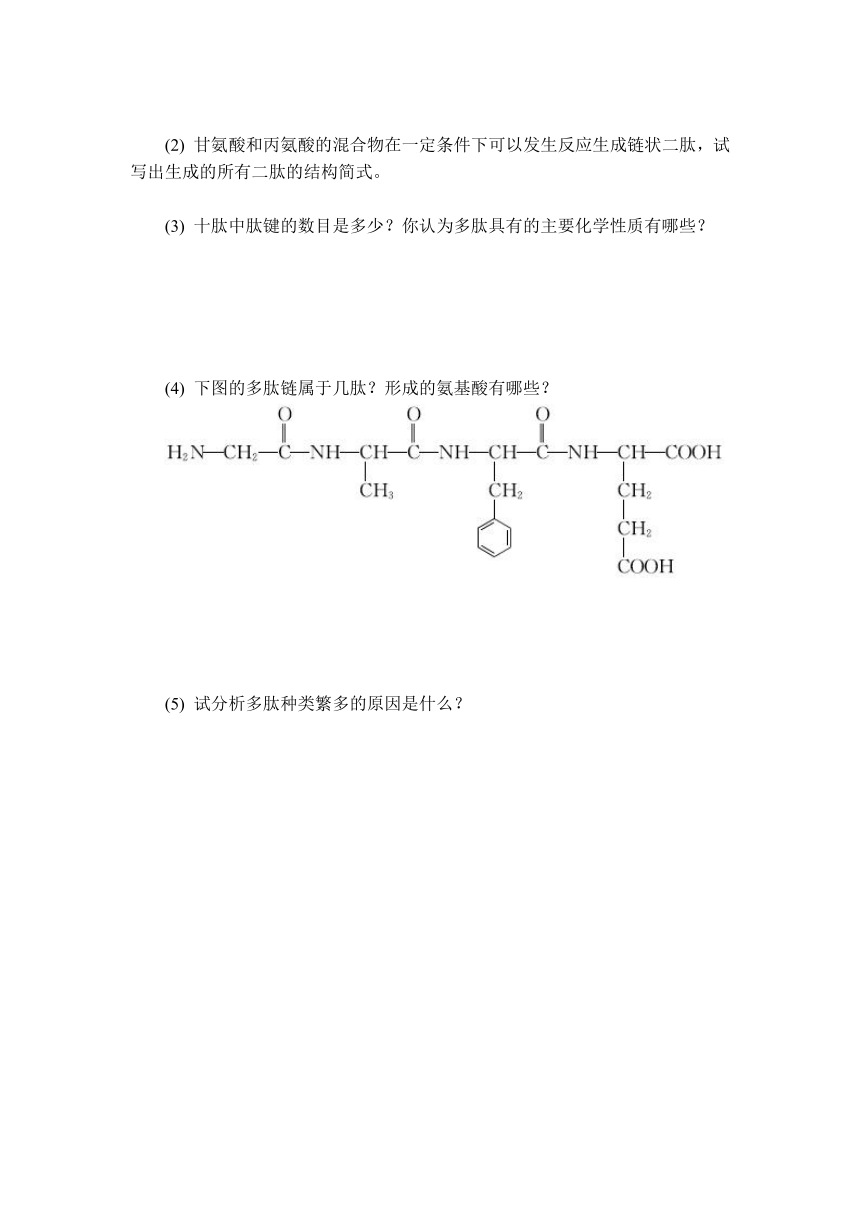
(4) 下图的多肽链属于几肽?形成的氨基酸有哪些?
(5) 试分析多肽种类繁多的原因是什么?
1. L-多巴是一种有机物,它可用于帕金森综合征的治疗,其结构简式如下图所示。这种药物的研制是基于获得2000年诺贝尔生理学或医学奖和获得2001年诺贝尔化学奖的研究成果。下列关于L多巴酸碱性的叙述不正确的是( )
A. 能溶于烧碱溶液 B. 遇FeCl3溶液显紫色
C. 能与浓溴水发生反应 D. 不能与强酸溶液反应
2. α 氨基丙酸与α 氨基苯丙酸混合物脱水成肽,能形成二肽的种类共有( )
A. 1种 B. 2种 C. 3种 D. 4种
3. 有些年轻人喜欢染发,染发时一般要用到一种着色剂——对苯二胺,它是一种有毒的化学药品,有致癌性,会对染发者的身体带来伤害,其分子结构如下图所示。下列有关对苯二胺的说法不正确的是( )
A. 对苯二胺分子中有与NH3相似的结构存在
B. 对苯二胺分子中所有原子都可能共平面
C. 每1 mol对苯二胺能和2 mol HCl 发生反应
D. 由对二硝基苯制取对苯二胺的反应为还原反应
4. 下列物质中,既能与盐酸反应,又能与NaOH溶液反应的是( )
①NaHCO3 ② (NH4)2CO3 ③Al(OH)3 ④NH4Cl ⑤H2NCH2COOH
⑥CH3COOH
A. ①②③ B. ①②④⑤ C. ⑤⑥ D. ①②③⑤
5. 某有机物分子中含有C、N、H、O四种元素,下图为该有机物的球棍模型。
(1)该有机物的化学式为________________,结构简式为_________________
__________________________________。
(2)该有机物可能发生的化学反应有____________(填序号)。
①水解反应 ②加聚反应 ③取代反应 ④消去反应 ⑤酯化反应
(3)写出该有机物在NaOH溶液中发生水解反应的化学方程式:____________
______________________________________。
6. 现有一种“多肽”,其分子式是C55H70O19N10,彻底水解后只得到下列四种氨基酸。
(1) 该多肽是________肽。
(2) 该多肽水解后有________个谷氨酸。
(3) 该多肽水解后有________个苯丙氨酸。
课题1 氨基酸和多肽
【活动方案】
活动一:合理饮食、摄入富含蛋白质的食物。
活动二:1. (1) 组成元素主要有C、H、O、N、S等;结构中共同含有的官能团:羧基、氨基。
(2) 甘氨酸 (3) 甘氨酸 苏氨酸
2. 无色晶体、熔点较高,除少数外,一般能溶于水,而难溶于乙醇、乙醚等有机溶剂。
活动三:1. (1) +HCl―→
+NaOH―→H2O+
(2) 氨基酸分子中的氨基和羧基相互作用,使氨基酸成为带有正电荷和负电荷的两性离子,离子间通过静电作用形成内盐,从而使得熔点升高。
2. (1) ―→H2O+
取代反应
(2)
(3) 9 既能与酸反应,也能与碱反应
(4) 四肽 CH2—NH2—COOH
(5) 形成多肽的氨基酸的种类不同;氨基酸的排列方式多样。
【课堂反馈】
1. D 2. D 3. B 4. D
5. (1) C5H11O2N HOCH2CH2NHCOCH2CH3
(2) ①③④⑤
(3) HOCH2CH2NHCOCH2CH3+NaOH―→HOCH2CH2NH2+CH3CH2COONa
6. (1) 十 (2) 4 (3) 3
1. 知道常见的氨基酸。
2. 了解氨基酸的两性、成肽反应;认识人工合成多肽的意义。
3. 了解氨基酸、蛋白质与人体健康的关系。
阅读下列材料,回答问题。
氨基酸是生物体内构成蛋白质分子的基本单位,与生命活动有着密切的关系。组成人体内的氨基酸有21种,但有8种氨基酸(色氨酸、苏氨酸、蛋氨酸、缬氨酸、赖氨酸、亮氨酸、异亮氨酸和苯丙氨酸)在人体不能合成,必须通过食物供给,称为必需氨基酸。
氨基酸在人体内通过新陈代谢可以发挥下列作用:①合成组织蛋白质;②变成酸、激素等物质;③转变成碳水化合物和脂肪;④氧化成二氧化碳、水及尿素。人体缺乏某种氨基酸,会影响抗体代谢的正常进行和导致疾病。如:胱氨酸缺乏会引起胰岛素减少,血糖升高。
如何保证人体必需氨基酸的摄取?
1. 分析下列几种人体氨基酸的结构,回答下列问题。
甘氨酸 苯丙氨酸 蛋氨酸
丙氨酸 谷氨酸 苏氨酸
(1) 归纳氨基酸的组成元素有哪些?氨基酸分子中共同含有的官能团有哪些?
(2) 氨基酸所具有的共同结构是什么?最简单的氨基酸的名称是什么?
(3) 上述氨基酸中,不含有手性碳原子的氨基酸的名称是什么,含有手性碳原子最多的氨基酸的名称是什么?
2. 查阅相关资料,归纳氨基酸的一些共同的物理性质。
1. 探究氨基酸的两性。
(1) 根据氨基酸中含有的官能团,写出甘氨酸与盐酸及NaOH溶液反应的化学方程式。
(2) 根据氨基酸的两性,结合晶体结构的知识解释氨基酸熔点较高的原因。
2. 阅读下列材料,回答问题。
羧基与氨基可以发生类似酯化反应那样的脱水反应,形成肽键(酰胺键)。组成肽的氨基酸单元称为氨基酸残基。二肽分子中含2个氨基酸残基,三肽分子中则含3个氨基酸残基。通常把有氨基的一端叫N端,写在左边;有羧基的一端叫C端, 链状二肽的结构
写在右边(如右图所示)。多个氨基酸结合成多肽时,能够形成的异构体的种类十分繁多,如:10种氨基酸形成的十肽理论上将超过1010种,20种氨基酸形成的十肽理论上将超过1013种。一般把相对分子质量在10 000以上的,并具有一定空间结构的多肽称为蛋白质。
(1) 写出两个丙氨酸分子反应生成二肽的化学方程式,并指出反应的类型。
(2) 甘氨酸和丙氨酸的混合物在一定条件下可以发生反应生成链状二肽,试写出生成的所有二肽的结构简式。
(3) 十肽中肽键的数目是多少?你认为多肽具有的主要化学性质有哪些?
(4) 下图的多肽链属于几肽?形成的氨基酸有哪些?
(5) 试分析多肽种类繁多的原因是什么?
1. L-多巴是一种有机物,它可用于帕金森综合征的治疗,其结构简式如下图所示。这种药物的研制是基于获得2000年诺贝尔生理学或医学奖和获得2001年诺贝尔化学奖的研究成果。下列关于L多巴酸碱性的叙述不正确的是( )
A. 能溶于烧碱溶液 B. 遇FeCl3溶液显紫色
C. 能与浓溴水发生反应 D. 不能与强酸溶液反应
2. α 氨基丙酸与α 氨基苯丙酸混合物脱水成肽,能形成二肽的种类共有( )
A. 1种 B. 2种 C. 3种 D. 4种
3. 有些年轻人喜欢染发,染发时一般要用到一种着色剂——对苯二胺,它是一种有毒的化学药品,有致癌性,会对染发者的身体带来伤害,其分子结构如下图所示。下列有关对苯二胺的说法不正确的是( )
A. 对苯二胺分子中有与NH3相似的结构存在
B. 对苯二胺分子中所有原子都可能共平面
C. 每1 mol对苯二胺能和2 mol HCl 发生反应
D. 由对二硝基苯制取对苯二胺的反应为还原反应
4. 下列物质中,既能与盐酸反应,又能与NaOH溶液反应的是( )
①NaHCO3 ② (NH4)2CO3 ③Al(OH)3 ④NH4Cl ⑤H2NCH2COOH
⑥CH3COOH
A. ①②③ B. ①②④⑤ C. ⑤⑥ D. ①②③⑤
5. 某有机物分子中含有C、N、H、O四种元素,下图为该有机物的球棍模型。
(1)该有机物的化学式为________________,结构简式为_________________
__________________________________。
(2)该有机物可能发生的化学反应有____________(填序号)。
①水解反应 ②加聚反应 ③取代反应 ④消去反应 ⑤酯化反应
(3)写出该有机物在NaOH溶液中发生水解反应的化学方程式:____________
______________________________________。
6. 现有一种“多肽”,其分子式是C55H70O19N10,彻底水解后只得到下列四种氨基酸。
(1) 该多肽是________肽。
(2) 该多肽水解后有________个谷氨酸。
(3) 该多肽水解后有________个苯丙氨酸。
课题1 氨基酸和多肽
【活动方案】
活动一:合理饮食、摄入富含蛋白质的食物。
活动二:1. (1) 组成元素主要有C、H、O、N、S等;结构中共同含有的官能团:羧基、氨基。
(2) 甘氨酸 (3) 甘氨酸 苏氨酸
2. 无色晶体、熔点较高,除少数外,一般能溶于水,而难溶于乙醇、乙醚等有机溶剂。
活动三:1. (1) +HCl―→
+NaOH―→H2O+
(2) 氨基酸分子中的氨基和羧基相互作用,使氨基酸成为带有正电荷和负电荷的两性离子,离子间通过静电作用形成内盐,从而使得熔点升高。
2. (1) ―→H2O+
取代反应
(2)
(3) 9 既能与酸反应,也能与碱反应
(4) 四肽 CH2—NH2—COOH
(5) 形成多肽的氨基酸的种类不同;氨基酸的排列方式多样。
【课堂反馈】
1. D 2. D 3. B 4. D
5. (1) C5H11O2N HOCH2CH2NHCOCH2CH3
(2) ①③④⑤
(3) HOCH2CH2NHCOCH2CH3+NaOH―→HOCH2CH2NH2+CH3CH2COONa
6. (1) 十 (2) 4 (3) 3
